白细胞介素4降低脐带间充质干细胞对造血干细胞分化潜能的维持能力
2019-05-18郭冬阳卢艳岳影星杨舟鑫
郭冬阳 卢艳 岳影星 杨舟鑫
目前的研究表明,间充质干细胞(mesenchymal stem cells,MSC)可以从多种组织,如骨髓、脂肪、脐带、羊膜、绒毛膜和牙髓等中分离得到。MSC可以向骨、脂肪、软骨、肌腱和肌肉等中胚层来源的组织细胞分化[1],因而在再生医学和组织修复中可能具有良好的应用前景。目前对于骨髓MSC的研究比较全面和深入,而对脐带MSC(umbilical cord mesenchymal stem cells,UC-MSC)的研究相对少一些。由于UC-MSC来源限制少,并且增殖能力强于骨髓MSC,因此对其的研究也越来越多[2]。
MSC增殖、分化、迁移和免疫调节功能会受到内环境中多种因素的调节,很多免疫相关细胞因子如γ-干扰素、肿瘤坏死因子-α、白细胞介素1β和白细胞介素27等均具有调控MSC的能力[3-6]。白细胞介素4(interleukin-4,IL-4)可以调控T细胞、B细胞和巨噬细胞等多种免疫细胞,参与体液免疫。目前对于IL-4调控MSC各种生物学特性的研究并不多。使用IL-4处理UC-MSC后,可以检测到UC-MSC增殖能力的下降以及CD106 表达的上升;加入IL-4诱导的UC-MSC条件培养基可以促进脐血CD34+造血干细胞的分化,其作用可能与IL-4诱导UC-MSC的IL-6分泌有关[7-8]。
MSC一方面促进造血干细胞分化,另一方面在维持造血干细胞分化潜能方面也有作用。为研究IL-4对MSC维持造血干细胞分化潜能的调节作用,本研究向UC-MSC和脐血造血干细胞共培养体系中加入IL-4,然后研究其中造血干细胞数目及分化潜能的变化。
材料与方法
一、主要试剂及仪器
DF12和IMDM干粉培养基、胰蛋白酶、2-巯基乙醇均为美国Gibico公司产品;胎牛血清、健马血清购自美国Thermo scientif i c公司;CD34阳性分选试剂盒、MethoCult H4435培养基为加拿大Stemcell technologies公司产品;藻红蛋白偶联的CD11b、CD14、CD15,异硫氰酸荧光素偶联的CD34抗体以及同型对照抗体均为美国BD公司产品;白介素4细胞因子购买于Peprotech公司。倒置相差显微镜以及成像系统购买于日本Olympus公司;流式细胞仪购买于美国BD公司产品。
二、主要实验方法
1. UC-MSC培养:在获得知情同意的情况下,收集足月妊娠的脐带。用缓冲液冲洗脐带后,剪碎脐带之后用胶原酶和胰酶各消化30 min。用滤网过滤消化的产物从而去掉没有消化完全的组织块。将悬液离心后弃去上清液,加入含10%胎牛血清、100 U/ml青/链霉素的DF12培养基重悬细胞沉淀,加入到细胞培养瓶中,放在37 ℃培养箱中培养。在细胞生长到接近融合时,按照1 : 3的比例进行传代扩增。
2.脐带血CD34+细胞分离:获得知情同意的情况下,收集足月妊娠的脐血标本。使用密度梯度离心的方法,分离脐血中的单个核细胞,并用PBS缓冲液清洗1遍。根据说明书的要求,使用CD34阳性分选试剂盒在磁珠分选器上分选出其中CD34+细胞。用含15%胎牛血清、15%健马血清、100 U/ ml青(链)霉素的IMDM培养基重悬细胞备用。
3. UC-MSC与脐血CD34+细胞共培养:UC- MSC支持造血干细胞的体系参考文献[2]。将培养的UC-MSC用丝裂霉素处理后,消化细胞,用DF12完全培养基把UC-MSC重悬。依照2×104个/ 孔把UC-MSC加入到24孔板。贴壁4 h后,更换为IMDM完全培养基,并加入2×104个CD34+细胞。置于37 ℃孵箱培养,培养7 d后更换一半培养基,在第14天收集细胞。对照组UC-MSC和CD34+细胞共培养组;IL-4组在加入CD34+的同时加入含终浓度20 ng/ml的IL-4的IMDM完全培养基,培养7 d后更换的培养基也为含终浓度20 ng/ml的IL-4的IMDM完全培养基。
4.共培养后细胞集落培养:轻轻晃动孔板后,收集未与MSC黏附的悬浮细胞,取3×103的细胞与半固体培养基充分混合,加入到6孔板中,于37 ℃细胞孵箱中培养。在14 d后通过倒置显微镜计数其中≥50个细胞集落形成单位。
5.流式细胞术检测收集细胞:对照组和IL-4组的细胞分别使用CD34或CD11b,CD14,CD15抗体标记后15 min,用PBS清洗一遍后,用0.4 ml PBS重悬细胞,在流式细胞仪上检测。
三、统计学分析方法
使用GraphPad Prism5.0软件进行统计学分析,共培养体系中的细胞数量、共培养体系中细胞在半固体培养基中形成的集落形成单位数量和总细胞数。以x± s表示,对照组与IL-4组间细胞数量和集落形成单位的差异比较采用两独立样本t检验,以P< 0.05为差异有统计学意义。
结 果
一、IL-4对UC-MSC与造血干细胞共培养体系细胞数量的调节作用
UC-MSC与造血干细胞共培养组与造血干细胞单独培养组相比,细胞数量有很大的增加。加入IL-4(20ng/ml)后,镜下可以观察到共培养细胞数量较对照组有明显下降(图1)。收集细胞计数发现,IL-4组的细胞数量(1.31±0.05)×105个/孔与对照组(2.80±0.28)×105个/孔相比显著下降(t=7.31,P< 0.05,图 2)。
二、IL-4处理对共培养体系中CD34+细胞比例的影响
用流式细胞仪分析IL-4组和造血干细胞单独培养组共培养后的细胞中表达CD34的细胞的比例,对照组细胞CD34+细胞比例为6.21%,而IL-4组下降为2.50%,CD34+的造血干细胞比例有明显的下降(图3)。
三、 IL-4处理后共培养体系中细胞集落形成能力的变化
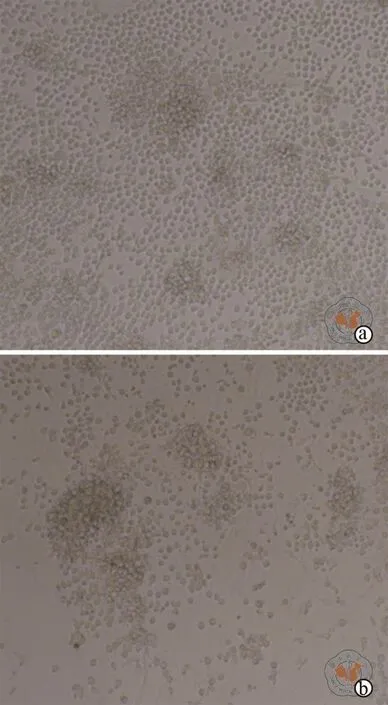
图1 IL-4处理后UC-MSC与造血干细胞共培养体系细胞状态

图2 IL-4处理后UC-MSC与造血干细胞共培养体系细胞数量的影响
取共培养得到的细胞,在半固体培养基培养14 天后,倒置显微镜下观察集落形成单位。两组中形成的集落形成单位包括CFU-G(粒系集落形成单位)、CFU-M(巨噬系集落形成单位)、CFU-GM(粒-巨噬集落形成单位)、BFU-E(红系爆式集落形成单位)、CFU-GEMM(粒红单巨核集落形成单位)。其中。BFU-E和CFU-GEMM比例较少,主要以CFU-GM、CFU-G和CFU-M为主。如表1所示,细胞形成CFU-M的能力(9.33±1.53)个/孔较对照组(17.67±0.58)个 /孔有明显下降(t= 8.84,P<0.001;形成 CFU-GM 的能力(15.67±3.22)个/孔较对照组(29.33±4.04)个/孔有明显下降(t=4.58,P< 0.05);形成总集落形成单位的能力(39.33±9.07)个/孔较对照组(62.67±6.66)个/孔也有下降(t=3.59,P<0.05),但 CFU-G 形成能力没有明显变化 [对照组:(13.33±3.22)个/孔;IL-4组(12.33±2.52)个/孔,t=0.42,P=0.69]。把分化得到的细胞进行计数,发现IL-4组得到的细胞分化出的细胞总数(3.67±1.71)×105个 / 孔与对照组(9.50±3.13)×105个/孔相比也明显下降(t= 2.83,P< 0.05)。
表1 IL-4处理后共培养体系中细胞集落形成能力的变化(± s)

表1 IL-4处理后共培养体系中细胞集落形成能力的变化(± s)
分组 样本数 BFU-E CFU-G CFU-M CFU-GM CFU- GEMM 总集落形成单位 总细胞数(×105)对照组 31.00±1.0013.33±3.2217.67±0.5829.33±4.041.33±1.5362.67±6.669.50±3.13 IL-4 组 31.00±1.7312.33±2.529.33±1.5315.67±3.221.00±1.0039.33±9.073.67±1.71 t 值 0.000.428.844.580.323.592.83 P 值 0.990.69 < 0.01 < 0.050.77 < 0.05 < 0.05
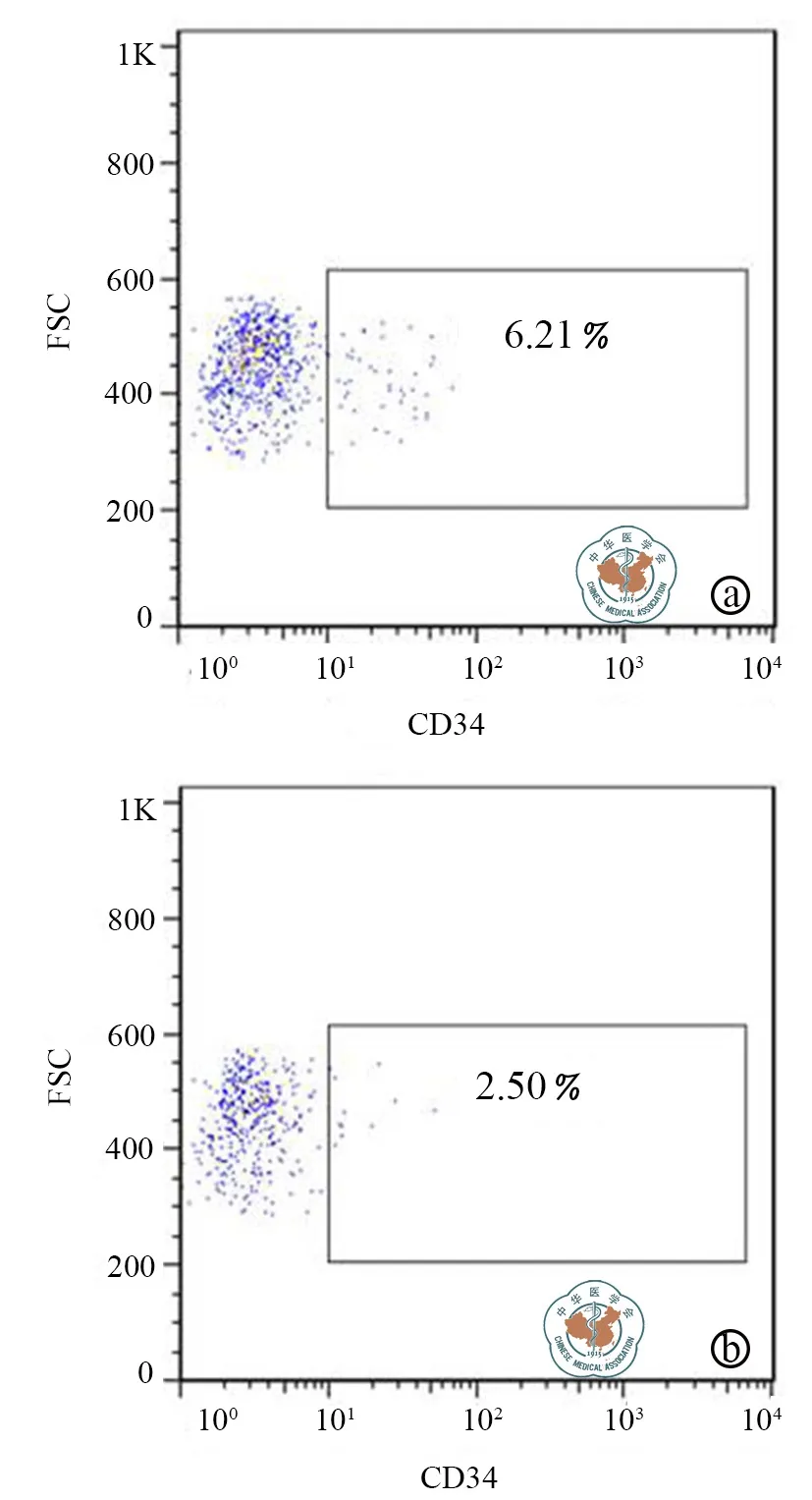
图3 IL-4处理对共培养体系中CD34+细胞比例的影响
四、 IL-4处理后共培养体系中细胞分化成巨噬细胞能力的变化
收集分化得到的细胞,其中CD11b+、CD14+和CD15+的细胞比例通过流式细胞术进行分析。如图 4,IL-4组共培养后细胞分化成CD14+细胞的能力下降,而分化成的CD15+细胞比例上升。CD11b表达在髓系细胞上,巨噬细胞表达CD14,粒细胞表达CD15。因此,这一结果与集落形成实验一样,表明IL-4组的细胞分化成巨噬细胞的能力下降。
讨 论
本研究在UC-MSC和造血干细胞的共培养体系中加入IL-4处理后,研究了IL-4对这一体系中造血干细胞分化潜能的影响。观察到细胞数量减少以及CD34+细胞比例下降。这些细胞分化成的CFU-M和CFU-GM下降,分化成的细胞中CD14+细胞比例也下降,提示其分化成巨噬细胞的能力下降。IL-4组分化成的细胞中CD15+细胞比例有上升;但CFU-G没有变化,CFU-GM下降,因此这些细胞分化粒细胞能力并没有上升,只是由于巨噬细胞分化能力下降而导致的粒细胞比例相对上升。这些结果均说明加入IL-4后MSC对造血干细胞的维持能力下降。
课题组的另一项研究表明,IL-4处理的UC- MSC培养上清可以促进造血干细胞的分化,形成更多集落形成单位[7]。而在本研究,IL-4降低了UC-MSC对造血干细胞的维持作用。这可能是由于IL-4通过促进UC-MSC分泌IL-6等细胞因子或直接作用于造血干细胞,使造血干细胞由能维持自身分化能力的不对称分裂转变为向下游细胞分化,造成造血干细胞的消耗。这两组实验采取了不一样的体系,在本研究中使用的是共培养的体系,不同于单纯使用上清的诱导分化体系。此外,本研究中IL-4一共持续处理了14 d,对UC-MSC的作用强度要远强于使用培养上清体系,IL-4的作用强度在MSC调控造血相关性质过程中可能有重要的调节作用。

图4 IL-4处理对共培养体系中细胞分化成CD11b+、CD14+和CD15+细胞能力的影响
其他免疫相关细胞因子也可以调节造血干细胞。I型辅助T细胞分泌的IFN-γ可以破坏小鼠动物模型中的造血干细胞,造成骨髓衰竭[9]。而IL-1β诱导的UC-MSC上清具有促进CFU-G和CFU- GM的能力[10]。目前,MSC被认为可被用于移植物抗宿主病和一些自身免疫性疾病的治疗,并有相关临床研究已经表明MSC的治疗效果[11-12]。这主要是由于MSC具有免疫调节功能,在细胞因子等的调控下MSC可以释放前列腺素E2等免疫调节因子从而抑制过激的炎症反应[13]。但在免疫系统激活的状态下,也会引起UC-MSC造血相关基因表达的改变,从而影响体内造血过程。因此,在使用UC-MSC治疗免疫相关疾病时需要考虑炎症反应是否也会影响造血干细胞的功能。
总之,IL-4可以降低UC-MSC对造血干细胞的维持能力,尤其会降低向巨噬细胞的分化潜能。这一研究提示在Ⅱ型辅助T细胞相关体液免疫疾病中使用MSC治疗时,也需要兼顾机体造血相关功能。
