乙二醇辅助聚乙烯醇制备花状氧化铈探索
2019-05-10幸康虔尹艳红万诗琴郑换琴刘鹏飞
幸康虔, 尹艳红,2, 万诗琴, 郑换琴, 刘鹏飞
(1.江西理工大学材料科学与工程学院,江西 赣州 341000;2.崇义章源钨业股份有限公司,江西 赣州 341000)
近年来,氧化铈(CeO2)在环境和能源等相关领域起着至关重要作用,引起了研究者的广泛关注[1-3].立方结构CeO2具有独特的物理和化学特性,如高机械强度、阳离子导电性、氧储存能力等,在高温陶瓷、催化剂、燃料电池、太阳能电池和抛光材料等方面得到了广泛应用[4-6].特殊形貌的纳米CeO2,相比于块体CeO2,其氧化还原反应和氧气输送等特性得到很大改善.因此,基于CeO2的优异性能和潜在的应用领域,合成形貌可控的CeO2受到越来越多的关注[7-9].
目前制备CeO2的常用方法是液相法,主要包括溶胶凝胶法、沉淀法、水热合成法、水解法等[10-11].溶胶凝胶法是以无机盐或金属有机醇盐为原料,在均相溶液中进行水解缩聚反应,溶胶逐渐变成凝胶,将凝胶干燥、焙烧,得到纳米粉体.该制备方法能够增加多组元体系的均匀性,反应易于控制,常常用于制备比表面积很大的凝胶和粉末.沉淀法是在液相中发生化学反应,生成不溶于溶剂的前驱体,前驱体经过干燥、焙烧,得到纳米金属氧化物.该制备方法因为原料成本低、工艺简单、操作简便、对设备要求低,可用于制备多种纳米氧化物,适合合成单一或者复合氧化物纳米微粒[12-17].
在前期研究基础上[18-22],针对公司不规则产品进行形貌尺寸改进,在酸性环境下,采用水作为溶剂,或水和乙二醇共同作为溶剂,聚乙烯醇(PVA)作为分散剂,利用沉淀法二次析出前驱体,对其产物CeO2的形貌尺寸进行调控.
1实 验
1.1 CeO2的制备
1)配制 Ce(NO3)3溶液、PVA 溶液、(NH4)2C2O4溶液
配制硝酸铈(Ce(NO3)3)溶液:称取 7 g CeO2,置于烧杯中,再加入20 mL浓HNO3、10 mL双氧水和10 mL去离子水,搅拌并加热到80℃,待溶液变成无色澄清溶液时,停止搅拌和加热,冷却至室温.
配制PVA溶液:称取0.4 g PVA固体,置于烧杯中,再加入100 mL去离子水,120℃油浴加热,使PVA彻底溶解,冷却至室温.
配制草酸铵((NH4)2C2O4)溶液:称取 0.9g(NH4)2C2O4固体颗粒,置于烧杯中,再加入100 mL去离子水作为溶剂,溶解后得到(NH4)2C2O4溶液,记为 A1.若加入50 mL去离子水和50 mL乙二醇作为溶剂,溶解后得到(NH4)2C2O4溶液,记为 A2.
2)Ce2(C2O4)3前驱体制备及煅烧
将上述的Ce(NO3)3溶液与PVA溶液混合,分别将 A1、A2溶液滴加到 Ce(NO3)3与 PVA 混合液中,过滤沉淀物,100 ℃干燥 2 h,得到 Ce2(C2O4)3,分别记为 B1、B2,经 600 ℃煅烧,得到产物,分别记为 C1、C2.
1.2 样品的表征及电化学性能分析
通过X射线衍射仪(XRD)、扫描电子显微镜(SEM)和能谱对样品组成、形貌和成分进行表征.通过BT-9300ST激光粒度仪对散射角测量,估算产物粒度分布,测试范围达到 0.1~1 000 μm.
1.3 样品的光降解甲基橙实验
将0.05g样品加入到60mL甲基橙水溶液(0.01g/L)中,为保持溶液的均匀性,溶液一直处于被磁性搅拌器搅拌状态,先在暗处搅拌30 min,之后在模拟日光照射下,每隔30 min取一次混合溶液,在3 000 r/min转速的离心机中离心5 min,取上清液用于甲基橙降解实验.
2 结果与讨论
2.1 原料的形貌分析
原料CeO2由某公司提供,为了进一步了解其形貌,对其进行了SEM测试,具体结果如图1所示.
由图 1(a)和图 1(b)可知,CeO2呈无规则形态,尺寸在2~10 μm之间,团聚严重,这种形貌尺寸不利于其性能的有效发挥.因此,为了扩大其应用范围,需要将不规则形貌变成规则形貌,并减少其尺寸.通常可以通过以下方法调控其形貌尺寸,一方面,在化学反应过程中添加分散剂或模板,进而调节其前驱体的形核及生长方向;另一方面,通过高温反应去除分散剂或模板,从而在控制CeO2尺寸的同时控制其形貌.
2.2 产物的组成与形貌分析
对所得前驱体进行600℃煅烧,除去有机物,得到最终产物,利用XRD对其进行物相分析,具体结果如图2所示.

图1 原料CeO2的SEM像Fig.1 SEM image of raw material of CeO2
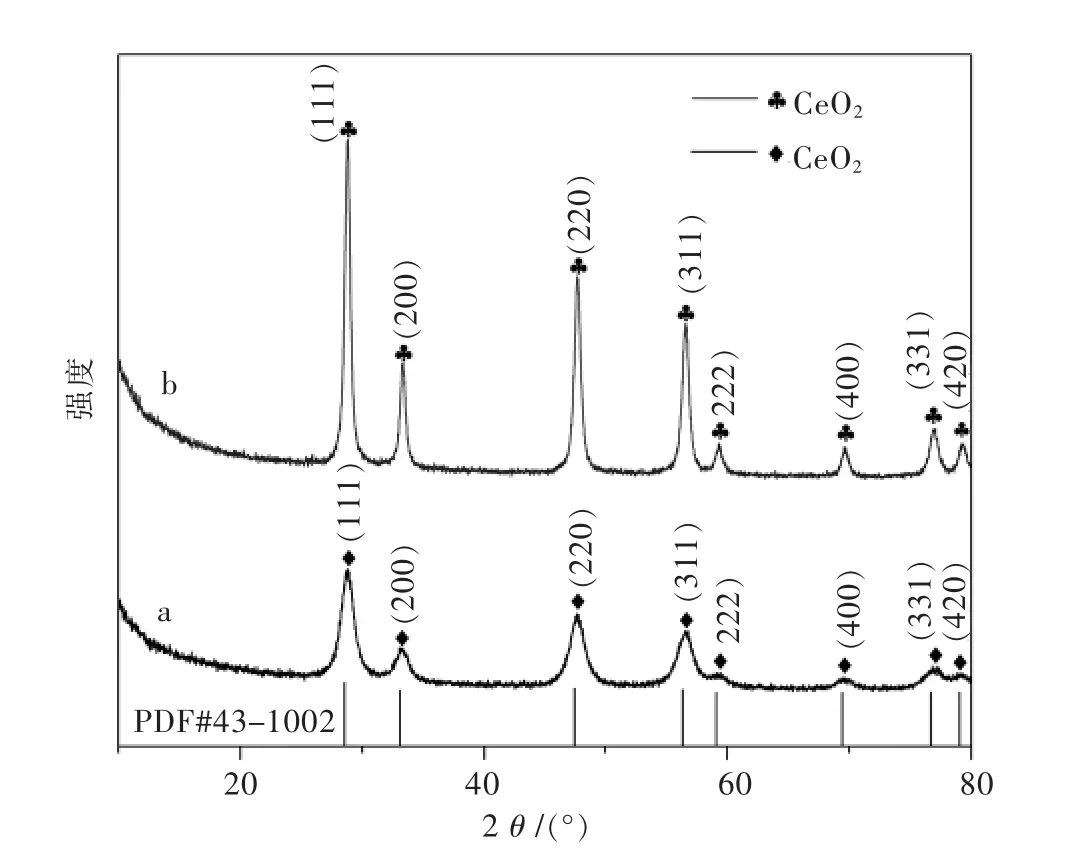
图 2 煅烧产物 C1(a)和 C2(b)的 XRDFig.2 XRD of calcination products C1(a) and C2(b)
图2中曲线a和b表明,以水为溶剂或水和乙二醇共同作为溶剂所得煅烧产物的衍射峰都在2θ为28.55°、33.08°、47.49°、56.34°、59.39°、69.63°、76.94°、79.31°处分别对应晶面 (111)、(200)、(220)、(311)、(222)、(400)、(331) 和(420).通过对照 JCPDS 粉末衍射卡PDF#43-1002,与立方晶系CeO2的标准衍射峰一致,所以2种产物都是立方相CeO2.除了CeO2的特征峰,没有出现其他峰,表明产物CeO2中不含其他杂质.图2(b)中的衍射峰强度高于图2(a)中的衍射峰,说明以水和乙二醇共同作为溶剂制备的Ce2(C2O4)3/PVA 前驱体,经过煅烧后所得 CeO2,晶体发育更好.
对以水为溶剂制备的CeO2进行形貌和成分分析,具体结果见图 3.如图 3(a)~图 3(c),CeO2分布不均匀,呈碎片状,尺寸为500 nm~5μm左右.大部分呈片状长方形结构,长度和宽度尺寸约3~10 μm和1~2 μm,厚度约100 nm.CeO2的尺寸分布不均匀,且形貌不规则,团聚较为严重.这有可能是水的流动性较大,在前驱体形核与生长过程中,使得Ce2(C2O4)3不能均匀依附于聚合物PVA表面,形成的前驱体Ce2(C2O4)3/PVA经煅烧,除去PVA后,所得产物CeO2呈不均匀分布.由图3(d)中的EDS可知,产物主要由Ce和O元素组成,Ce和O的原子比大约为1∶2,说明产物为 CeO2.
图 4(a)~图 4(c)是水和乙二醇共同作为溶剂所得 CeO2的SEM 像.由图 4(a)可知,多数 CeO2以团簇形式存在,少部分呈条状存在.对图4(a)进一步放大,得到图4(b),部分CeO2团簇体呈花束状插层形式,直径大约 2~5 μm,部分 CeO2以长条状 CeO2形式存在,形貌较规则,长度大约4 μm,宽度大约1.5 μm.对图 4(b) 中的花束进一步放大,得到图 4(c),可知,花束状CeO2由长条状CeO2堆叠而成,长条状CeO2厚度约100 nm,长条状CeO2堆积成花束状结构.图4(d)是对图2(c)中局部区域进行EDS分析,可知产物主要由Ce和O组成,Ce和O的原子比约为 1∶2.
2.3 花状CeO2的形成机理
花状CeO2的形成机理有以下2种可能:一种是在水和乙二醇的混合体系下,因为乙二醇的黏度相较于水更大,所以在乙二醇的作用下将易碎的小片前驱体黏合在一起,形成小的花状前驱体,如图5(a)所示.另一种是PVA的分散作用促使棒状前驱体开裂,如开花一般,形成花状前驱体,如图5(b)所示.花状前驱体经过煅烧形成花状CeO2.
前驱体制备过程中,Ce(NO3)3与(NH4)2C2O4发生反应,生成 Ce2(C2O4)3沉淀,见方程式(1),由于乙二醇含有羟基具有亲水性,可以与PVA水溶液混溶,组成油/水微反应器,在反应体系中具有调节前驱体Ce2(C2O4)3生长方向的作用,此外,乙二醇的黏度更大,可以使体系具有一定的黏度行为,有利于发挥PVA对前驱体的分散作用.前驱体中含有的有机物PVA,经600℃煅烧,分解成水蒸气和CO2,见方程式(2),前驱体Ce2(C2O4)3分解产生 CeO2,见方程式(3),反应方程式如下:

图 3 煅烧产物 C1的 SEM (a~c) 和 EDS(d)Fig.3 SEM (a~c) and EDS (d) of calcination product of C1
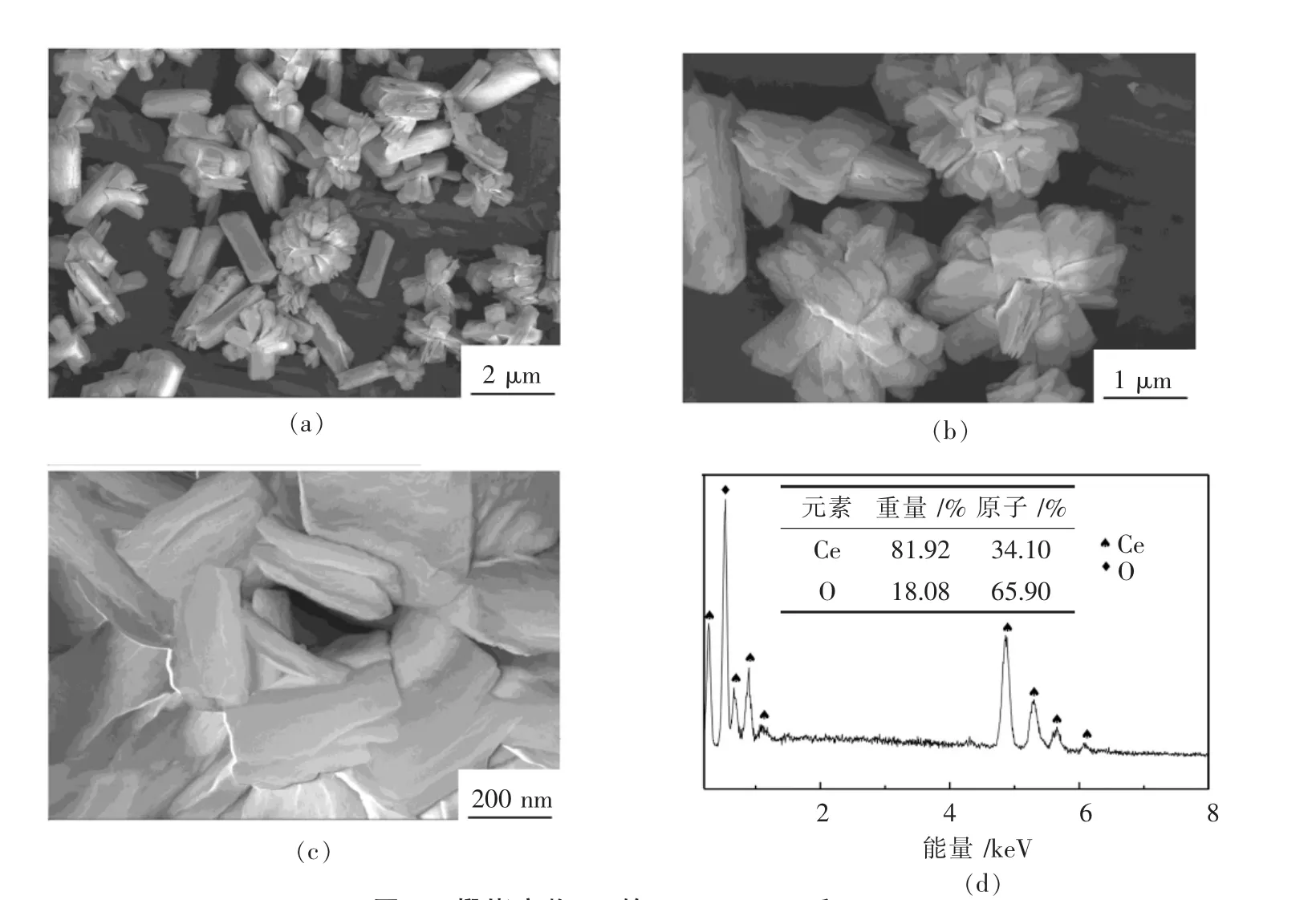
图 4 煅烧产物 C2的 SEM (a~c) 和 EDS (d)Fig.4 SEM images(a~c) and EDS (d) of calcination product of C2


2.4 产物的光催化性能及比表面积
室温下,通过模拟日光照射对甲基橙进行光降解,3种CeO2的光催化降解结果如图6(a)所示.从图6中数据可以得知,光催化降解甲基橙1 h时,花状CeO2降解率为72.68%,而片状CeO2和公司原料降解率分别为59.78%和56.40%,花状CeO2降解率远高于其他2个样品.从图6中数据可知,花状CeO2具有较高的光催化性能,因此在光催化应用方面,花状CeO2有着很高的应用价值.对样品的比表面积进行测试(图 6(b)),结果显示,花状 CeO2的比表面积(21.45 m2/g)比片状 CeO2(14.9 m2/g)和原料(1.84 m2/g)更高,所以花状CeO2能够更加快速地吸收并降解甲基橙染料.

图5 花状CeO2前驱体可能的2种生长机理图解说明Fig.5 Graphical explanation of the possible growth mechanism of flowered-like CeO2

图6 片状C1、花状C2和公司原料的光催化性能和比表面积Fig.6 Photocatalytic properties and specific surface area of C1with sheetlike structure,C2with flower-like structure and raw material
3结 论
1)在水体系中,PVA可以促使铈前驱体生成片状易碎的CeO2.
2)在水和乙二醇的混合体系中,因形成类似水/油体系,增加了黏度,使PVA合成的小片状前驱体黏合,而大片棒状前驱体则裂开,形成花状.
3)乙二醇辅助 PVA 调节前驱体 Ce2(C2O4)3,有利于其按一定方向生长,乙二醇的黏稠性会加固Ce2(C2O4)3与 PVA 的结合效果.
4)花状规则形貌的CeO2具有高比表面积特性,在光催化过程可以快速吸附色素,加快光催化反应进程.
