急性脑梗死合并应激性上消化道出血的危险因素
2019-05-08刘菁菁刘文宏贺茂林
刘菁菁 刘文宏 贺茂林
急性脑梗死是一类严重危及患者生存质量的疾病,消化道出血是其内科并发症之一,可延长住院时间,阻碍康复,甚至导致死亡。近年来,有关急性脑梗死合并上消化道出血危险因素的研究很多,但多为回顾性研究,观点不统一。目前认为危险因素主要包括:高龄、既往合并症、消化道疾病史[1]、脑梗死病情严重程度、梗死面积[2]、梗死部位[3]、服用非甾体类抗炎药 (non-steroid anti-inflammatory drug,NSAID)、抗凝治疗等[4]。应激性上消化道出血是由于急性脑梗死严重的生理应激反应引起胃或食管黏膜损伤[5]。本文通过前瞻性的研究设计寻找急性脑梗死引发应激性上消化道出血的独立危险因素,从而为临床防治提供更充实的证据。
1 对象与方法
本研究采用前瞻性队列研究方法,所有实验设计符合人体试验委员会制定的伦理学标准,所有患者入组前均签署知情同意书。
1.1 研究对象纳入2016年1月至2017年6月北京世纪坛医院神经内科住院的急性脑梗死患者350例,其中合并上消化道出血33例(9.4%),未合并上消化道出血317例 (90.6%)。全组男231例,女 119 例,年龄(66.75±13.47)岁。入组标准:①符合1995年中华医学会全国第4次脑血管病学术会议制定的急性脑梗死诊断标准[6];②上消化道出血临床表现为呕吐物为咖啡色或胃管内抽出咖啡色液体,且胃内容物潜血阳性,和/或大便呈柏油样且大便潜血强阳性[7]。排除标准:①急性脑梗死发病前即发生上消化道出血;②既往有上消化道溃疡、肿瘤、出血史;③既往有食管胃底静脉曲张、肝硬化病史;④入院时距急性脑梗死发病时间大于72 h;⑤住院时间短于7 d或长于21 d。
1.2 研究方法记录所有患者的一般情况(年龄、性别)、既往史(高血压、糖尿病、心脏病、吸烟、卒中、残障程度)、入院时血压、神经功能损伤程度、脑梗死分型、单/双侧梗死,NSAID用药史、入院后是否给予预防性抑制胃酸保护胃粘膜治疗、抗凝、抗血小板聚集和溶栓治疗。其中,既往残障程度按改良 Rankin 量表(modified Rankin scale,mRS)分为>2分组和≤2分组,按入院时血压是否≥140/90 mmHg分为血压升高组和血压正常组,入院后神经功能损伤程度用美国国立卫生研究院卒中量表(National Institute of Health Stroke Scale,NIHSS)及格拉斯哥昏迷评分(Glasgow coma scale,GCS)表示,脑梗死分型使用牛津郡社区卒中研究分型(Oxfordshire Community Stroke Project,OCSP) 及TOAST(Trial of ORG 10172 in acute stroke treatment)分型。在比较预防性抑制胃酸保护胃黏膜治疗、抗凝、抗血小板聚集和溶栓治疗的影响时,去除了16例入院时即发生上消化道出血者。
1.3 统计学方法采用SPSS 19.0进行统计分析。计量资料经K-S检验后为非正态分布,采用中位数(最小值,最大值)表示,相互比较采用非参数检验 (Mann-Whitney U检验)。计数资料采用例数(发生率)表示,相互比较采用Pearson卡方检验或Fisher确切概率法。采用偏相关分析明确排除NIHSS影响后与上消化道出血有关的危险因素。采用多因素logistic回归分析(向前条件法)确定独立危险因素。检验水准α=0.05,均采用双侧检验。
2 结果
2.1 一般资料上消化道出血组在年龄、性别、既往高血压、糖尿病、吸烟、卒中史、mRS、NSAID用药史、是否进行预防性抑制胃酸保护胃粘膜治疗、抗血小板治疗和抗凝治疗上与未发生上消化道出血组(对照组)没有统计学差异(P>0.05)。但上消化道出血组患者入院时NIHSS明显高于对照组,GCS明显低于对照组。在有心脏病史、入院时血压升高、OCSP分型中的完全前循环梗死(total anterior circulation infarct,TACI)和后循环梗死(posterior circulation infarction,POCI)及 TOAST 分型中的心源性脑栓塞、双侧梗死、接受过溶栓治疗的患者中上消化道出血的发生率均明显升高,OCSP分型中的腔隙性梗死 (lacunar infarction,LACI)和TOAST分型中的小动脉闭塞的患者中上消化道出血发生率明显降低。差异均有统计学意义,P<0.05。详见表 1。
2.2 采用偏相关分析去除NIHSS对其他危险因素的影响去除神经功能损伤严重程度(NIHSS)的影响后,仅POCI、双侧梗死仍与上消化道出血存在相关性(P<0.05)。 详见表 2。
2.3 采用多因素logistic回归分析寻找独立危险因素将NIHSS、是否为POCI、双侧梗死纳入多因素logistic回归方程,发现只有高NIHSS、双侧梗死为急性脑梗死患者合并上消化道出血的独立危险因素。详见表3。拟合方程:logit(上消化道出血)=-5.281+0.228NIHSS+2.246双侧梗死。
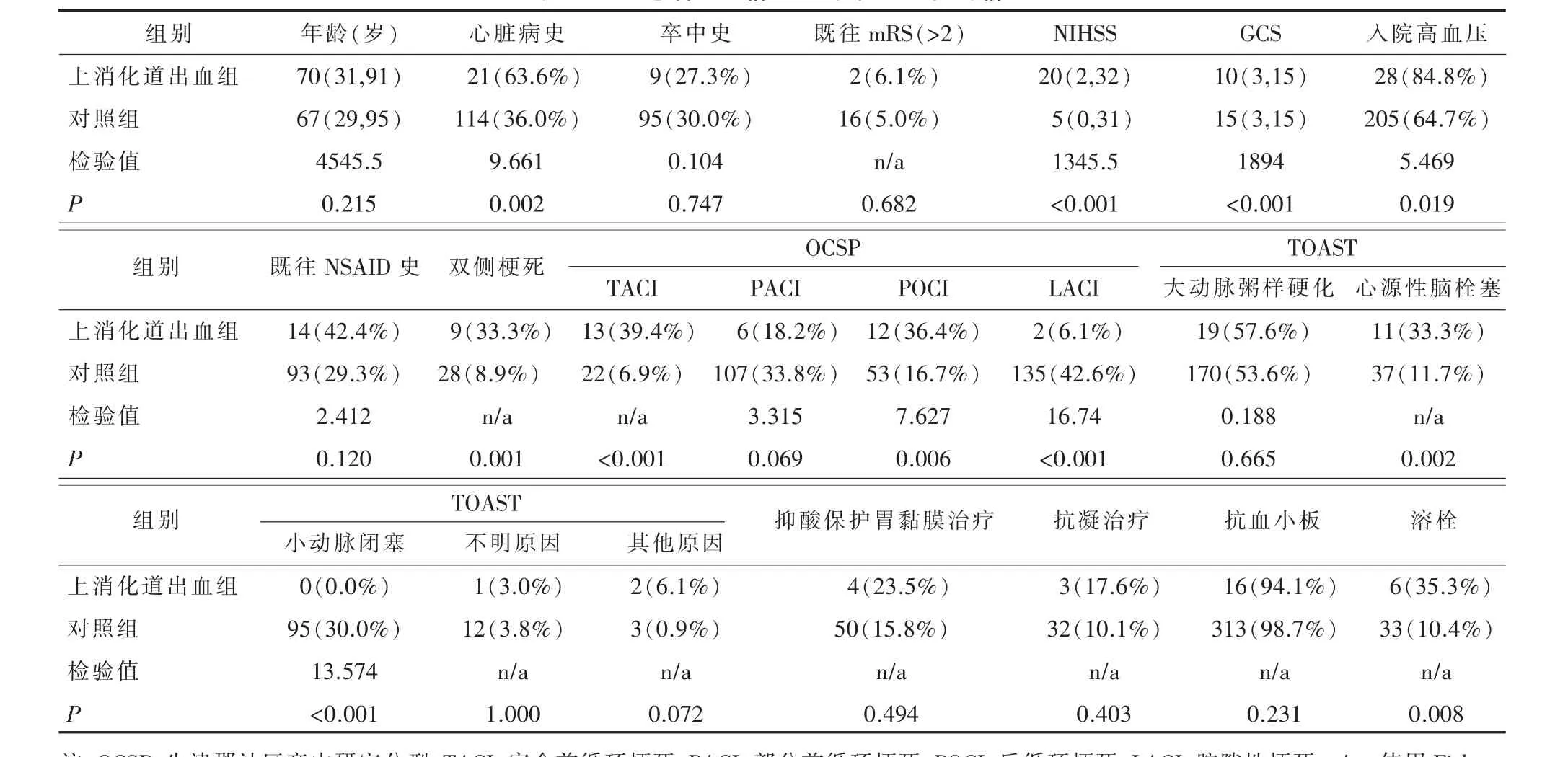
表1 两组患者一般情况、既往史和入院时情况
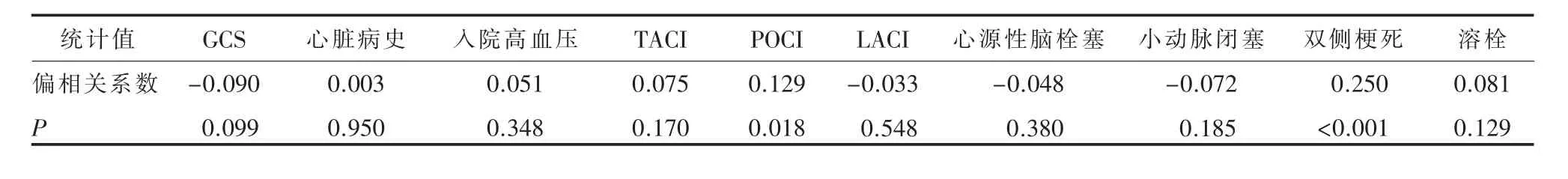
表2 急性脑梗死上消化道出血危险因素的偏相关分析(去除NIHSS影响)
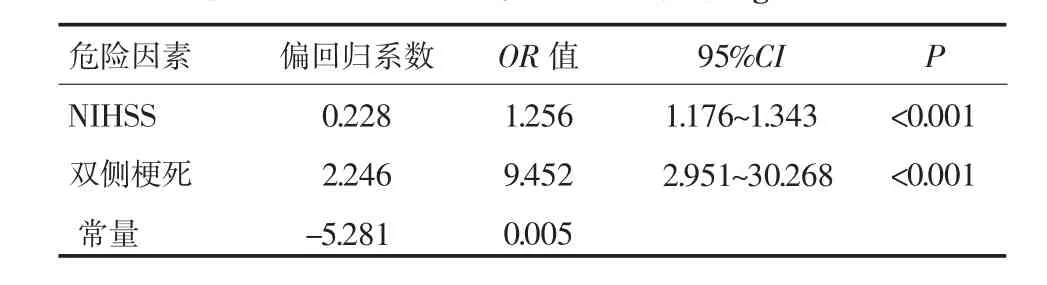
表3 急性脑梗死上消化道出血危险因素的logistic回归分析
3 讨论
本研究中上消化道出血在急性脑梗死患者中发生率为9.4%,远高于国外报道的1.5%[1]~5.2%[8]。但在我国学者的研究中,这一比例明显升高,在7.8%[9]~13.5%[7],与本研究中的发病率相近。这提示不同种族急性脑梗死合并上消化道出血的发生率或许不同,而上消化道出血由于某种原因在国人急性脑梗死患者中更易发生[9]。
既往研究发现,脑梗死损害越严重合并上消化道出血可能性越大[7,10]。本研究中入院时神经功能损伤程度与是否发生上消化道出血密切相关,高NIHSS、低GCS的患者更容易发生上消化道出血。尤其高NIHSS更是急性脑梗死合并应激性上消化道出血的独立危险因素。患者的NIHSS每增加1分,其发生上消化道出血的概率增加25.6%。这是由于严重的脑梗死会引发严重而持久的应激,致使自主神经调节功能紊乱,刺激胃蛋白酶及胃酸释放增多,损害胃黏膜屏障后出现糜烂或溃疡,形成上消化道出血[11]。
本研究发现,除了脑梗死严重程度之外,双侧梗死也是应激性上消化道出血的独立危险因素。双侧梗死患者合并应激性上消化道出血是单侧梗死的近9.5倍。这在既往的研究中鲜有人提出[12]。可能是由于脑缺血会引起中枢神经系统和胃肠系统轴的破坏会引起胃排空障碍及胃肠道粘膜营养障碍,从而使胃肠道出血风险增加[13]。近年来功能影像学的进步发现了胃肠道的皮层和延髓控制是多灶双侧性的[13]。故此双侧的脑组织损伤相较单侧对中枢-胃肠道系统轴的破坏性更大,也更易诱发应激性上消化道出血。
由于急性脑梗死应激性上消化道出血的发病率相对较低,在本研究中可能存在一定统计偏差,对急性脑梗死发生上消化道出血的预测逊于未发生者。尚需在今后的研究中扩大样本量,进行多中心研究加以验证。
为此,我们应当对入院时高NIHSS及双侧梗死者给予足够重视,预防上消化道出血的发生,减少对预后的影响。
