液相色谱串联质谱检测牙鲆鱼中的小清蛋白过敏原
2019-05-07葛敏敏王建华林洪
葛敏敏,王建华,林洪
1(中国海洋大学 食品科学与工程学院,山东 青岛, 266003)2(青岛海关检验检疫技术中心,山东 青岛,266002)
小清蛋白(parvalbumin,PV)是水产品中的主要过敏原,在真骨鱼类中广泛存在,其对温度、pH和变性剂都较为稳定,因此很多加工过的鱼类产品仍具有致敏性。鱼类肌肉中小清蛋白的含量范围为 0~1.5 mmol /L[1],牙鲆的PV有3个亚基,本文只研究其中1个亚基G9I585(uniprot中PV编号),对其进行定性定量分析。
“bottom up”[2]的蛋白质组学分析方法,其一般过程为:首先利用酶将目标蛋白质切成小分子质量的肽段,然后通过液相色谱串联质谱(high performance liquid chromatography tandem mass spectrometry,HPLC-MS/MS)对肽段进行检测。HPLC-MS/MS分析方法的建立最好每个蛋白质选 2~3 个特征肽段,以获得更好的特异性[3],一般选用胰蛋白酶对蛋白质进行酶解,产生的肽羧基末端通常为精氨酸或赖氨酸,经ESI源离子化后主要产生带有2个正电荷的离子,二级质谱碎裂时产生的子离子一般为Y型离子带有1个正电荷[4]。目前“bottom up”方法逐渐应用于牛奶[5]、鸡蛋、鱼类[6]、甲壳贝类动物[7]、坚果[8]、小麦、花生[9]等主要致敏原的检测,相比于传统方法酶联免疫吸附测定(ELISA)[10]、聚合酶链式反应(PCR)[11],LC-MS / MS方法具有准确、灵敏、快速的特点,因此LC-MS/MS将作为一种重要的过敏原检测方法。
在真骨鱼类PV的检测方面,蔡秋凤等[12-13]分别采用ELISA和Western-blotting 方法对不同加工方式的鲢鱼的PV的含量变化进行分析,CARRERA等[6]利用LC-MS/MS方法对真骨鱼的PV进行定性分析,但没有进行定量检测。
本实验利用高分辨质谱进行特征肽段的筛选,选择ALTDAETK、LFLQNFAFSASAR和SDFIEEDELK作为牙鲆PV的特征肽段,并对蛋白质提取液体和酶解过程的吲哚-3-乙酸(indole-3-acetic, IAA)浓度、酶用量、酶解时间进行了优化,建立了以ALTDAETK作为定量肽段,LFLQNFAFSASAR和SDFIEEDELK作为定性肽段的牙鲆PV检测的LC-MS / MS方法,可以实现对牙鲆中PV的精确定量。采用LC-MS/MS方法对牙鲆中PV的定量分析及对牙鲆PV的前处理优化过程未见文献报道。
1 材料与方法
1.1 材料与试剂
牙鲆、大菱鲆购自山东青岛。
LTDAETK(摩尔质量:847.9 g/mol,简称ALT)、SDFIEEDELK(摩尔质量:1 224.3 g/mol,简称SDF)、LFLQNFAFSASAR(摩尔质量:1 253.4 g/mol,简称LFL)、SDFIEEDELK(摩尔质量:605.8 g/mol,简称sdf)、重组PV(摩尔质量:11 645.0 g/mol),委托上海Sangon Biotech公司合成(纯度>95%);测序级胰蛋白酶,瑞士Roche公司;二硫苏糖醇,北京Solarbio公司;吲哚-3-乙酸,北京Solarbio公司;Rapigest SF,美国Waters公司;Tris(分析纯),北京Scientan公司;甘氨酸(分析纯),北京Solarbio公司;EDTANa4(分析纯),天津Kermel公司;乙腈(色谱纯),德国Merck公司;甲酸(色谱纯),德国Fluka公司。
1.2 仪器与设备
1200/6430液相色谱-三重四级杆串联质谱仪,美国Agilent公司;UPLC-Q-Exactive Focus MS超高效液相色谱四级杆静电场轨道阱质谱联用仪,美国Thermo Scientific公司;BEH-C18色谱柱,美国Waters公司;HS501水平振荡器,德国IKA公司;CR21G高速冷冻离心机,日本HITACHI公司;调速形迷你离心机,上海Sangon Biotech公司;Mill-Q超纯水装置,美国Millipore公司;HH-1水浴锅,国华电器有限公司。
1.3 方法
1.3.1 重组PV的酶解
前处理:取10 μL重组PV水溶液(8 μg/mL),加入90 μL Rapigest SF(0.1%,体积分数),加入30 μL IAA(浓度5 mol/L) 溶液,40 ℃避光水浴30 min; 加入20 μL胰蛋白酶溶液(质量浓度0.1 mg/mL),加入水使酶解液体积达到198 μL,酶解14 h,加入2 μL甲酸终止酶解,12 000 r/min离心30 min后,取上清;进UPLC-Q-Exactive Focus MS检测。
1.3.2 样品前处理条件优化
提取:新鲜牙鲆取肌肉打碎,取1 g(精确至0.01 g)样品,加入 10 mL蛋白质提取液3 (0.1 mol/L Tris,0.5 mmol/L 甘氨酸),水平振荡30 min,12 000 r/min离心30 min后,取上清;上清液于100 ℃水浴锅中加热5 min,12 000 r/min离心30 min取上清。
酶解:取10 μL上清液,加入90 μL Rapigest SF(质量浓度1 mg/mL),按酶/蛋白质质量比为2∶5加入胰蛋白酶溶液(0.1 mg/mL),加入水使酶解液体积达到198 μL,酶解12 h,加入2 μL甲酸终止酶解,12 000 r/min离心30 min后, 取上清;待LC-MS/MS上样分析。
1.3.3 UPLC-Q-Exactive Focus MS条件
色谱条件色谱柱:EC-C18色谱柱(100 mm×3 mm, 1.7 μm);柱温:35 ℃;进样量:5 μL;流动相A:含1%(体积分数)甲酸的水溶液;流动相B:含1%(体积分数)甲酸的乙腈溶液;梯度洗脱程序:0~15 min,97%~70%A;15~18 min,70%~100%A;18~22 min, 0%A;22~22.1 min,0%~97%A;22.1~25 min,97%A;流速0.3 mL/min。
质谱条件:带有加热器的电子喷雾电离源(HESI),辅助气体加热器温度:300 ℃;毛细管电压:3 500 V; 毛细管温度为320 ℃;正模式的电喷雾电压设置为3 500 V;扫描模式:Full MS+ddMS2正离子模式数据非依赖型扫描,其中Full MS的分辨率为70 000, 扫描范围为400~1 400m/z,DD-MS2确认模式分辨率17 500,四极杆的碰撞能量介于10~30 eV。
使用MaxQuent软件[14]进行数据处理,牙鲆PV的氨基酸序列用作Fasta文件。
1.3.4 LC-MS/MS方法的建立
色谱条件色谱柱:BEH-C18色谱柱(100 mm×2.1 mm, 2.7 μm);柱温:35 ℃;进样量:10 μL;流动相A:含1%(体积分数)甲酸的水溶液;流动相B:含1%(体积分数)甲酸的乙腈溶液;梯度洗脱程序:0~13 min,97%~70%A;13~18 min,70%~40% A;18~19 min, 40%~0% A;19~21 min, 0% A;21~22 min, 0%~97% A;22~24 min, 97% A。流速0.2 mL/min。
质谱条件离子源:电子喷雾电离源(ESI);毛细管电压:3 500 V;雾化气压力:275.9 kPa;干燥气温度:300 ℃;干燥气流速:12.0 L/min(氮气);采集模式:多反应监测(MRM)模式。
2 结果与分析
2.1 特征肽段的选择
重组PV酶解液经高分辨质谱检测,其数据经MaxQuent软件处理,从而得到酶解肽段的响应及得分(表1)。
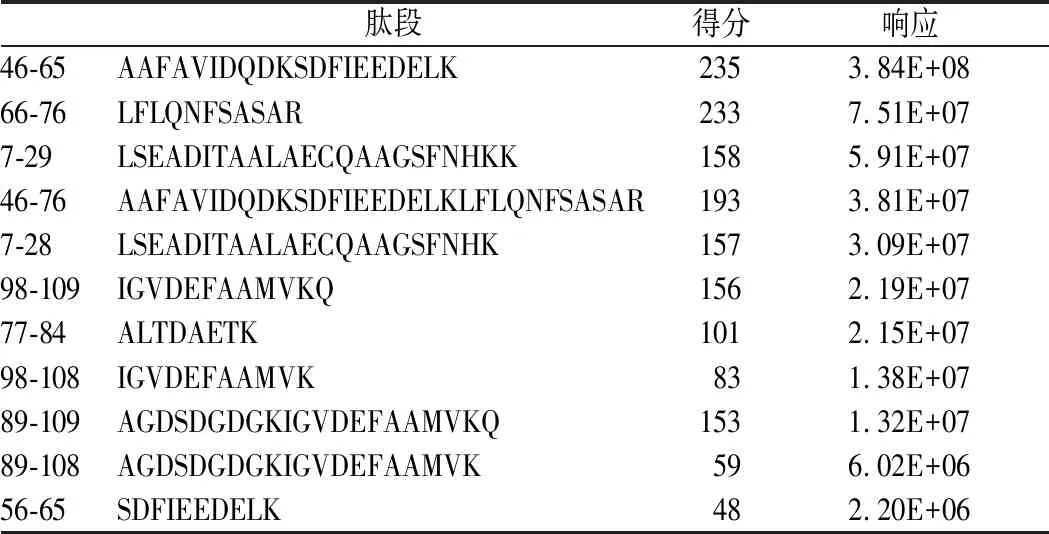
表1 重组PV的酶解肽段的响应及得分Table 1 Intension and scorre of enzymolysis peptides of recombination PV
根据肽段稳定性和质谱检测的要求,特征肽不应含有易氧化氨基酸半胱氨酸(C)和蛋氨酸(M)且长度在8到18个氨基酸[15], LFLQNFSASAR、ALTDAETK、 SDFIEEDELK满足要求,因此选择这3个肽段作为特征肽段。CARRER等[6]将LFLQNFSASAR等19种作为鉴定真骨鱼的肽段,没有将ALTDAETK、 SDFIEEDELK作为鉴定真骨鱼的肽段。为了确定肽段的独特性,3个特征肽段在UniProtKB 数据库中进行序列对比,结果显示SDFIEEDELK为牙鲆特有肽段,而LFLQNFSASAR和ALTDAETK两个肽段在三文鱼、鲤鱼、鳕鱼、鲈鱼等多种真骨鱼中含有。用LC-MS/MS方法对三文鱼和鲤鱼肌肉样品进行检测,没有SDFIEEDELK检出,LFLQNFSASAR和ALTDAETK均有检出,与数据库检索结果一致。
2.2 前处理方法优化
首先对提取液方法进行优化,以提取液所提取的总蛋白质浓度进行比较分析;其次在重组PV的酶解方法(见1.3.1)基础上对IAA浓度、酶用量、酶解时间4个酶解条件依次进行单因素水平的优化,以肽段在仪器上的相对响应进行比较分析。
2.2.1 蛋白质提取液的优化
在WU等[16]的牙鲆PV提取液1的基础上进行提取液的优化,优化的3种蛋白质提取液分别为:蛋白质提取液1:Tris(0.1 mol/L),甘氨酸(0.5 mmol/L),DTT(1 mmol/L);蛋白质提取液2:Tris(0.1 mol/L),甘氨酸(0.5 mmol/L),DTT(1 mmol/L),EDTA(5 mmol/L);蛋白质提取液3:Tris(0.1 mol/L),甘氨酸(0.5 mmol/L)。
提取液1、2、3所提取的总蛋白质质量浓度分别为1.49 mg/mL、1.18 mg/mL、0.94 mg/mL(蛋白质质量浓度由BCA方法测得)。由图1可以看出,ALT、LFL两个肽段的相对响应为提取液3>提取液2>提取液1,对于SDF肽段来说提取液3>提取液1>提取液2。
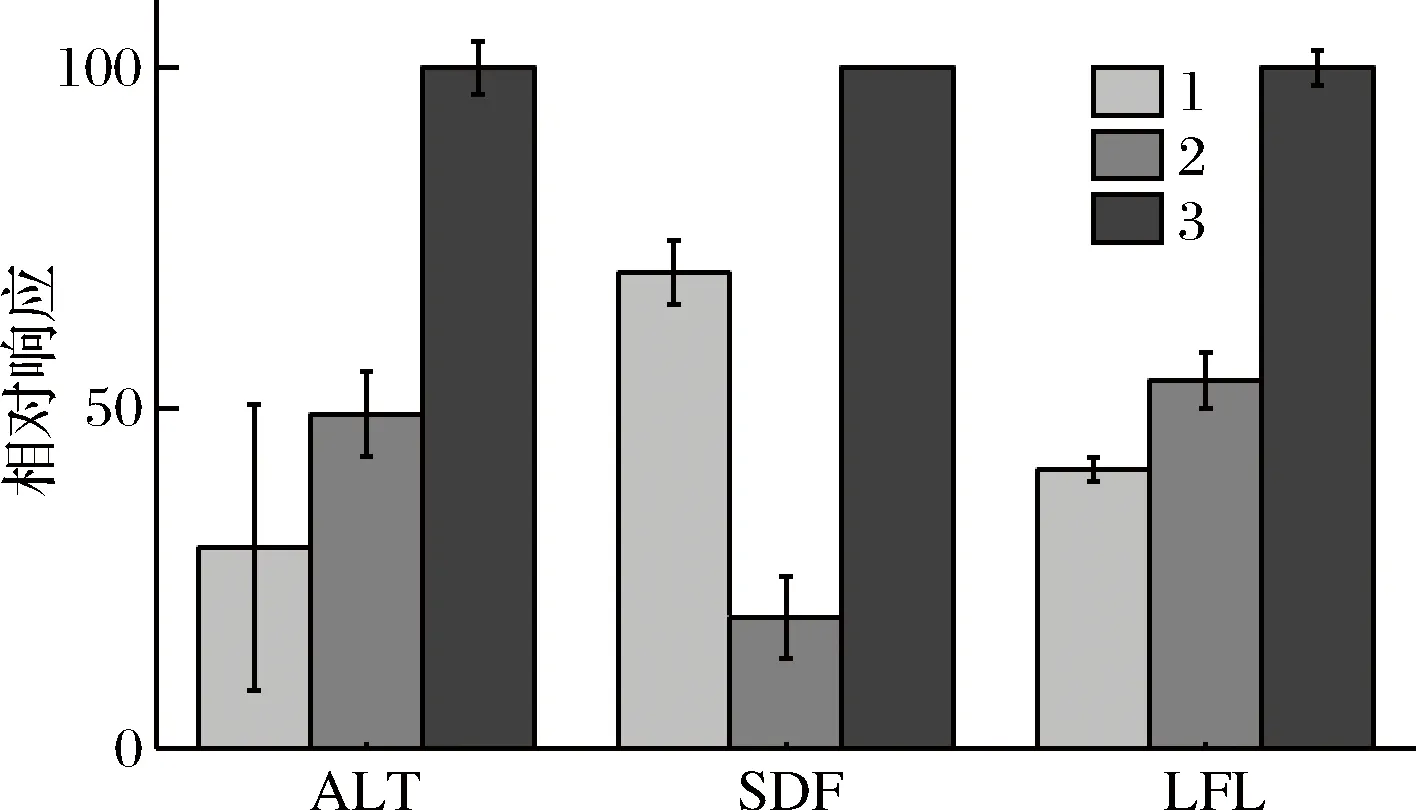
图1 提取液优化Fig.1 Optimization of extraction liquid
提取液中的DTT作为一种还原剂,可以避免蛋白质中半胱氨酸之间形成分子内或分子间的二硫键,阻止蛋白高分子聚合物的形成提高提取效率[3],但是在酶解过程中DTT也会对酶作用,抑制酶的活性导致酶解效率降低,从而质谱响应降低,因此经不含DTT的提取液3提取的样品响应最高;从提取液1和提取液2比较来看,EDTA对蛋白提取效率没有提高作用。综合考虑选择提取液3。
2.2.2 IAA浓度的优化
进行IAA(5 mmol/mL)用量的优化,IAA优化的3个水平分别为添加0、15、30 μL,其结果如图2所示,对于ALT、SDF肽段来说0 μL>15 μL>30 μL,对于LFL来说30 μL>0 μL>15 μL。肽段与IAA烷基化过程中发生的非特异性化学修饰有关[18],这将改变标肽的质量,而肽的质量发生变化将导致该肽不能被MRM方法检出,因此测得的肽产率将低于实际产率;再者作为烷基化试剂的IAA可能对酶存在一定的抑制作用从而导致酶解程度下降,综合考虑,选择酶解过程不添加IAA。

图2 IAA优化提取液优化Fig.2 Optimization of IAA
2.2.3 酶用量优化
PV是一种钙结合蛋白,具有由约30 个氨基酸残基组成的螺旋-环-螺旋蛋白模体的EF手图像,每个EF手图像(模体)结合1个Ca2+,为小清蛋白提供了更加稳定的结构[1],PV具有较高的酶解稳定性,因此本实验设计的5个水平的酶/蛋白质(质量比)高于一般的酶/蛋白质(1∶100~1∶10)[17],酶/蛋白质(质量比)分别为1∶10、1∶5、2∶5、3∶5、4∶5(提取液蛋白质浓度通过BCA方法侧得)。酶用量优化结果如图3所示,ALT与SDF肽段相对响应随酶/蛋白质的增加而增强,但ALT肽段相对响应变化较为缓慢,SDF变化较大,而LFL肽段相对响应随酶/蛋白质(质量比)增加大致呈降低趋势。
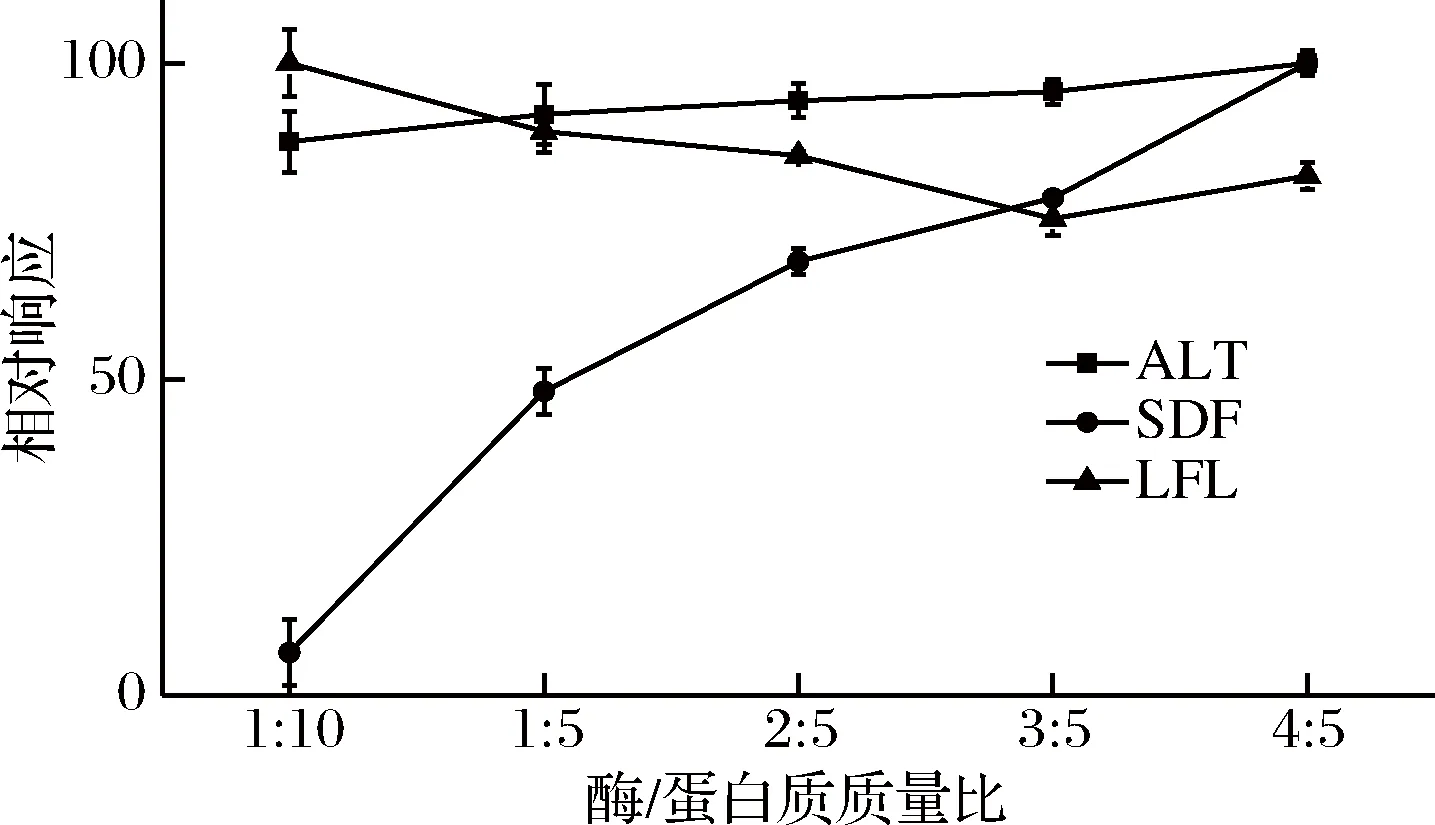
图3 酶/蛋白质质量比的优化Fig.3 Optimization of the ratio of enzyme and protein
不同的肽段由于其所在二级结构、自身性质及酶浓度不同,其酶解效率有所差异,酶/蛋白质(质量比)为1∶10~4∶5,ALT肽段的酶解得量比较稳定,改变酶的浓度对酶解效果影响不大,可能已经达到较高程度的酶解;SDF肽段的酶解得量随酶/蛋白质的增大而增大,说明此肽段还未达到完全或较高程度的酶解;LFL肽段可能由于酶解产物抑制或酶错切造成其响应随酶浓度增加而逐渐降低,综合考虑以酶解得量比较稳定的ALT肽段作为定量肽段,以SDF、LFL肽段为定性肽段,酶/蛋白质为2∶5。
2.2.4 酶解时间优化
分别选择4、6、8、10、12、14 h六个酶解时间进行酶解时间的优化,如图4所示,ALT、SDF、LFL三个肽段酶解12 h后达到平台期,因此酶解时间12 h为最优,酶解时间优化图如图4所示。
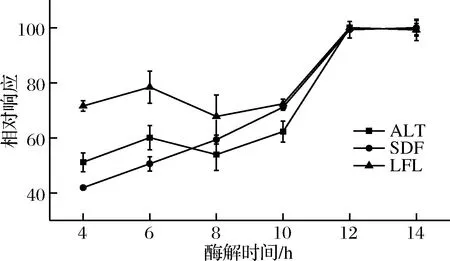
图4 酶解时间优化Fig.4 Optimization ofenzymolysis time
2.2.5 酶解效率
蛋白质的定量依赖于该蛋白质消化成的用作定量的目标肽段,而对于蛋白质的绝对定量方法的准确性取决于用作定量的目标肽段的酶解程度,若该目标肽段没有达到完全酶解则会损害方法的准确性[18],以优化的牙鲆样品的最优酶解条件(酶/蛋白质为2∶5,酶解时间12 h),对1 000 mg/mL、500 mg/L、200 mg/L 三个质量浓度水平的重组PV进行酶解,以ALT肽段作为定量肽段,以SDF与LFL肽段为定性肽段, ALT肽段酶解效率在104%~106%,满足检测要求。
2.3 LC-MS/MS方法质谱参数优化
LFL定性离子对与CARRERA等[6]一致,其他肽段质谱参数没有文献报道,为了获得最佳的质谱采集参数,对ALT、SDF、LFL、sdf四个合成肽段的前体离子、产物离子、碎裂电压、碰撞能量等进行优化,优化结果见表2。
2.4 线性关系与定量限
以ALT肽段为定量肽段,SDF、LFL肽段为定性肽段,建立PV的检测方法,在0.005~100 000 mg/L 9个点质量浓度,ALT质谱响应与内标sdf响应之比(y)与ALT浓度与内标sdf浓度之比(x) 的线性关系为y= 1.221 1x+0.013 3(R2>0.999)。小清蛋白定量限为2.74 mg/kg。
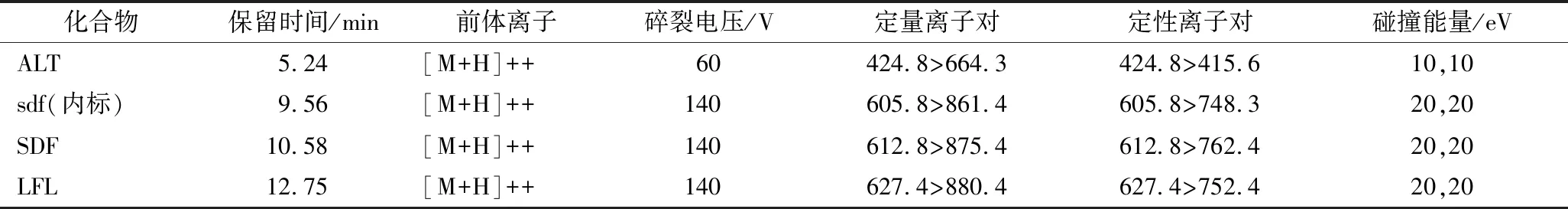
表2 小清蛋白的酶解3个肽段的保留时间和质谱参数Table 2 Retention time and mass spectrometric parameters of three peptides
2.3.3 添加回收
大菱鲆与牙鲆是同属于鲆科的真骨鱼类,经已经建立的LC-MS/MS方法检测,大菱鲆中不含SDFIEEDELK、LFLQNFSASAR和ALTDAETK肽段。为了验证牙鲆中PV含量检测方法的准确性,选择与牙鲆相近的物种大菱鲆为空白基质,以重组PV为标准品进行添加回收实验,3个添加水平的平均回收率在95%~102%,满足检测要求,相对标准偏差3%~6%。
2.4 实际样品检测
采用大菱鲆为空白基质配制标准曲线对牙鲆进行检测,检测结果为ALT肽段含量为0.85 mg/g,小清蛋白含量为11.72 mg/g。
3 结论
本实验建立了以Tris(浓度0.1 mol/L)、甘氨酸(浓度0.5 mmol/L) 为提取液,酶解过程中酶/蛋白质(质量比)为2∶5,酶解时间为12 h的牙鲆中PV的前处理方法;以ALTDAETK为定量肽段,SDFIEEDELK、SDFIEEDELK为定性肽段的牙鲆PV的HPLC-MS/MS检测方法,首次实现了用LC-MS/MS方法对牙鲆中主要过敏原PV的精确定量检测。
