肠系膜上动脉栓塞的外科诊治:18例报告
2019-05-05余超何磊丁丁彭浩
余超,何磊,丁丁,彭浩
作者单位:安徽医科大学第三附属医院(合肥市第一人民医院)胃肠外科,安徽 合肥 230061
肠系膜上动脉栓塞是外科较为少见的急腹症,该病早期临床症状缺乏特异性表现,误诊率高,而一旦未能及时诊治,死亡率极高。为提高对该疾病的早期诊断及治疗水平,笔者对18例肠系膜上动脉栓塞的病人进行回顾性分析。
1 临床资料
1.1 一般资料本组18例病人选自2011年1月至2017年6月安徽医科大学第三附属医院(合肥市第一人民医院),男11例,女7例;年龄范围为58~84岁,中位年龄70岁,年龄(70.2±7.6)岁。自发病至明确诊断时间范围为6~65 h,平均23 h。本研究符合《世界医学协会赫尔辛基宣言》相关要求。病人对所受治疗知情同意。
1.2 病史特点18例中15例有房颤病史,7例既往有风湿性心脏病病史,6例有冠心病史,8例有高血压、高血脂病史;2例曾有过下肢动脉栓塞病史,9例有脑血管病病史,1例伴有主动脉夹层(图1)。
1.3 临床表现所有病人均有剧烈腹痛,部分病人即使使用强镇痛药如哌替啶、吗啡,仍然效果不佳,10例伴有恶心呕吐,12例伴腹胀,便血6例,体格检查9例有明显腹部压痛、反跳痛及腹肌紧张。5例肠鸣音活跃,13例肠鸣音减弱或消失。7例诊断性腹穿抽出血性液体。
1.4 检查方法(1)实验室检查:本组18例病人中,16例病人有白细胞升高,17例有中性粒细胞百分比升高。10例有凝血功能异常,包括凝血酶原时间、活化部分凝血活酶时间延长以及D-二聚体升高等。4例病人出现肝肾功能不全。(2)影像学检查:本研究中16例病人行腹部CT平扫检查,其中11例行腹部增强CT或CT血管成像(CTA)检查,10例发现肠管扩张,9例出现腹盆腔积液,1例出现少见的门静脉积气(图2)。本研究中11例病人经过增强CT或CTA确诊,7例通过术中探查确诊,术前确诊率61%。
1.5 治疗方法(1)非手术治疗,4例病人,方法主要包括抗感染、低分子肝素抗凝治疗,扩容、纠正内稳态紊乱、肠内及肠外营养支持等。(2)手术治疗,14例病人,方法为①术前处理:确诊病人给予低分子肝素抗凝,罂粟碱扩血管治疗,维持体内内稳态平衡,并积极抗感染治疗,因该病预后差,死亡率高,积极与家属沟通,如合并严重的基础病,应迅速与相关科室会诊讨论,尽早手术。②手术方式:手术治疗方式主要为肠系膜上动脉切开取栓(图3)及坏死肠管切除。先探查肠系膜上动脉,了解栓塞部位,后行切开取栓,取栓后根据肠管血运及肠蠕动情况,决定肠切除的范围。③术后处理方法:术后给予正规的抗感染、抗凝、扩血管治疗,并监测凝血功能。
2 治疗结果
4例病人行非手术治疗,其中1例因晚期肿瘤伴转移,家属拒绝手术,另外3例因病人高龄(均大于80岁),合并较多基础疾病,一般情况差,病人家属拒绝手术。手术残留小肠肠管长度少于150 cm定义为广泛肠切除,如残留小肠大于150 cm定义为局部肠切除。在发病12 h内手术的有6例,6例中无广泛肠切除病人;术后均恢复良好出院。超过12 h手术的有8例,其中5例有广泛肠切除,最严重的1例自屈氏韧带下方约15 cm处至横结肠中段全部坏死,行坏死小肠加右半结肠切除,术后2 d死亡。9例病人行一期肠切除吻合,其中1例广泛肠切除病人术后出现吻合口漏,二次手术后因感染性休克死亡。5例行肠造口术,其中2例病人因肠管活性难以判断,行疑似坏死肠管造瘘观察,1例术后24 h行二次手术再次切除坏死肠管后造瘘,顺利出院。术后短肠综合征病人有2例。
3 讨论
肠系膜上动脉栓塞诊治最关键在于早诊断早治疗,一旦出现误诊,或没有及时处理,常常造成严重的后果[1-2]。要做到早期诊断,则需要对该病早期的临床表现有充分的认识。肠系膜上动脉栓塞的栓子主要来源于心脏,因此,多数病人合并心血管系统疾病,尤其是房颤,杨冬山等[3]报道指出,肠系膜上动脉栓塞的病人,84%合并有房颤,本组研究18例病人中,有15例房颤病人,房颤发生率很高。因此在病史上应该询问病人有无合并心脏疾病,尤其是房颤病史。在早期的症状体征上应特别注意症状体征分离的病人,即腹痛症状明显,而腹部早期无明显的压痛及腹膜炎体征,当疾病进展,发生肠坏死时,则会出现腹膜炎体征。Bergan等[4]1975年提出了诊断肠系膜上动脉栓塞的三联征,包括突发上腹或脐周持续性剧烈疼痛,而无相应的腹部体征;房颤及器质性心脏病;胃肠排空症状(恶心、呕吐、腹泻,肠鸣音早期亢进等)。所以对于房颤病人,突发剧烈的原因不明的腹痛,有症状体征分离的,要首先考虑到本病的可能。该病的实验室检查并无明显特异性[5],可以表现为白细胞升高、凝血功能改变、D-二聚体升高等,一定程度上可以反映病人的病情严重程度。如果腹腔穿刺抽出不凝血,常提示有肠坏死。
影像学检查是肠系膜动脉栓塞确诊的主要方法,包括增强CT扫描、CTA及选择性肠系膜上动脉血管造影,肠系膜上动脉闭塞或充盈缺损是本病最直接、最可靠的依据。选择性肠系膜上动脉造影可以清楚的显示栓塞的部位,侧支循环的情况,但是该检查为有创检查,更重要的是可能会因为检查费时,对于病情时间较长和有肠坏死的病人可能造成不利影响;而腹部增强CT及血管CTA特异度和灵敏度都较高,不仅能清楚显示肠系膜血管情况,还能和其他急腹症相鉴别,在该病的诊断上更具价值,本组病人主要依靠增强CT或CTA确诊。龚晓虹等[6]认为CT检查安全、快速、准确,是诊断急性肠系膜上动脉栓塞的首选检查方法。
门静脉积气是一种较少见的影像学表现,最常发生于急性肠系膜缺血性疾病中,也可以发生于肠道炎性疾病、移植物抗宿主病等。本研究中有1例病人出现了罕见的门静脉积气,门静脉积气发生原因主要包括[7-8]:肠黏膜发生破坏性改变,消化道内压力增高,产气杆菌感染,主要机制常为肠黏膜损伤,肠屏障功能障碍,气体进入丰富的黏膜下静脉血管丛,经肠系膜静脉到达门静脉系统。门静脉和肠系膜上静脉积气可同时存在。门静脉积气需要与胆管疾病相鉴别,由于胆汁的流向是向肝门方向,胆管积气的气体常常位于肝门部区域,一般不会进入肝脏包膜下2 cm区域。而门静脉的血流方向是离开肝门方向,积气常分布于肝脏的边缘部位。CT平扫可以清楚区别门静脉内积气和胆管内积气,而增强扫描更能明确气体是在增强的门静脉系统内,还是在增强的门静脉旁的胆管内。有研究表明,门静脉积气与肠缺血或者肠坏死密切相关,一旦出现门静脉积气,常常提示预后不佳[9],本研究中一例门静脉积气病人,术前有腹膜炎体征,术中探查广泛小肠坏死,术后死亡。
肠系膜上动脉栓塞病人非手术治疗死亡率极高[10],本研究4例病人行保守治疗,均死亡,因此,一旦诊断明确,不建议行保守治疗。手术是首选的治疗方案,开腹动脉取栓或部分小肠切除术是目前广泛应用的治疗方法。该病病人大多高龄,心功能差或者基础疾病多,麻醉和手术风险大,在手术时机的把握上,一旦确诊,应尽早尽快积极手术治疗,避免因手术和麻醉犹豫不决导致广泛小肠坏死引起严重后果。外科治疗的主要目的是切除坏死的小肠,去除栓子避免栓塞进一步发展导致更广泛的肠坏死。术中注意:原则上应该先切开肠系膜上动脉取栓,取栓成功后,再根据缺血肠管的血运恢复情况决定肠管的切除范围。如果术中发现坏死小肠肠管不多,可以扩大切除坏死肠管的范围,切除坏死小肠上下15 cm肠管,确保残留小肠活性,以免术后发生吻合口瘘,同时切除栓塞部分的肠系膜。如果术中发现坏死肠管较多,则应遵循损伤控制外科的理念[11],对于较广泛的可疑小肠坏死,可根据肠管颜色、肠蠕动情况、小肠切缘出血情况等判断肠管活性,对可疑小肠行肠造口,注意观察造口肠管的颜色和血运,24~36 h后再决定是否再次剖腹行坏死小肠切除。因为有二次手术的可能,应积极与家属沟通,交代病情,此为计划内再手术,取得家属理解。病人术后给予低分子肝素抗凝、待进食后给予口服华法林抗凝治疗,注意监测凝血功能。有研究表明,肠缺血耐受时间为6~12 h[12],一旦缺血超过12 h,小肠极易发生缺血坏死,随着缺血时间延长,肠坏死的范围也越大,死亡率越高。本研究中在发病12 h内手术的病人均恢复良好出院,而超过12 h的病人有5例广泛肠切除,2例死亡。因此及时诊断,早期手术治疗是提高病人预后的重要因素。
肠系膜上动脉栓塞术后并发症主要包括感染性休克,心、肾功能不全,呼吸衰竭及多脏器功能衰竭,吻合口瘘、吻合口出血及短肠综合征等。术前应积极扩容,纠正酸碱失衡及水电解质紊乱,防治急性肾功能衰竭,积极治疗基础疾病如心脏病等,应用抗凝和扩张血管药物,预防缺血的进一步发展。胃肠减压、营养支持、预防性应用抗生素。术后抗凝治疗,密切检测凝血功能及血流动力学,维持内环境的稳定。恰当而充分的围手术期处理是提高治愈率的重要环节。
随着我国人口的老龄化和心血管疾病的增加,肠系膜上动脉栓塞的发病率也有所上升,由于该病容易误诊,死亡率高,外科医生应提高该病的认识,如果能够早期诊断,及早治疗,是可以明显改善病人的预后的。
(本文图1~3见插图5-5)

图1 肠系膜上动脉栓塞合并主动脉夹层
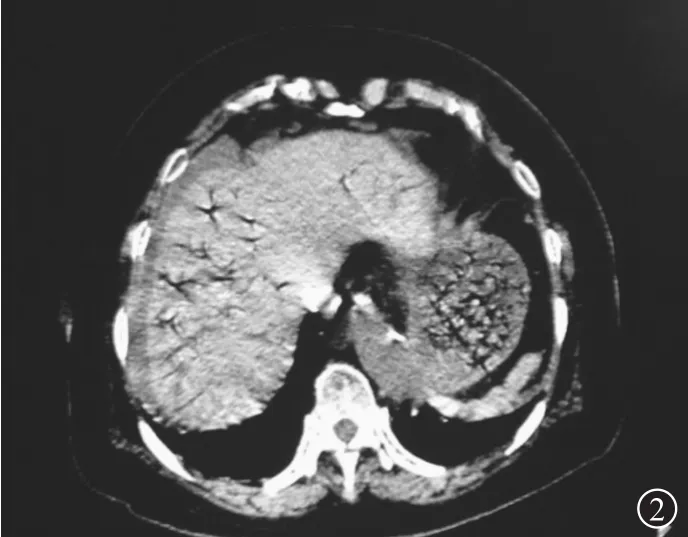
图2 肠系膜上动脉栓塞病人门静脉积气

图3 肠系膜上动脉栓塞病人肠系膜上动脉切开取栓
