经皮冠状动脉介入治疗术中应用生物可吸收支架的安全性和有效性的系统评价
2019-04-26梁宇博林欣车千秋孙润民王琼英马俊丽胡浩常鹏张春余静白锋
梁宇博,林欣,车千秋,孙润民,王琼英,马俊丽,胡浩,常鹏,张春,余静,白锋
经皮冠状动脉介入治疗(PCI)已成为目前冠心病国际共识的主要治疗方式[1,2]。然而,冠状动脉(冠脉)内金属支架的永久存留,会影响冠脉的舒张和收缩功能,且存在延迟内皮化、内皮表型改变、慢性炎症、新生动脉粥样硬化、支架断裂等风险及不良影响,最终可能增加长期不良心血管事件的发生风险[3-9]。近年来,生物可吸收支架(BVS)以其独特的设计理念和良好的应用前景,被称为是继经皮冠状动脉腔内成形术(PTCA)、裸金属支架(MS)、药物洗脱支架(DES)之后,经皮冠脉治疗的第四次革命[10]。生物可吸收支架能够在一定时间内提供不弱于金属支架的支撑作用,同时其携载的抗增殖药物能有效抑制新生内膜增生,最终支架骨架能在一段时间内完全降解[11],达到血管“功能性修复”的目的。
这项新技术自问世即获得了心血管介入医师和广大冠状动脉粥样硬化性心脏病(冠心病)患者的极大关注。美国雅培公司研发的ABSORB BVS为例,早期的队列研究与注册研究已初步证实了其治疗简单冠脉病变的可行性、安全性及有效性。该支架与目前临床应用最广泛的药物涂层支架——依维莫司洗脱支架(EES)开展了多项随机对照研究、观察性研究,随着两种支架治疗冠心病患者的长期临床随访结果陆续公布[12-17],以及雅培公司宣布BRS退市,广大心血管介入医师对生物可吸收支架以及这项技术在冠心病患者中的应用信心有所下降。但由于目前各项关于BVS的研究在样本量、随访时间等多个方面存在不同,且因随访时间较短而导致临床终点事件发生率相对较低,因此统计学把握度可能不足,难以检测到两组支架在独立临床事件上的统计学差异。本研究旨在检索国内外最新的临床随机对照研究,通过Meta分析对比BVS和DES治疗冠心病患者的安全性及临床疗效,更加客观的反应生物可吸收支架及技术在冠心病患者应用中的安全性和有效性,以期进一步指导临床研究和应用。
1 资料与方法
1.1 纳入及排除标准
1.1.1 纳入标准①包括有心肌缺血证据,经经皮冠脉介入术(PCI)治疗原生冠脉病变的患者的随机对照研究;②有明确的基线资料,包含以下临床终点指标:全因死亡,心源性死亡、心肌梗死(MI)、靶血管心肌梗死(TV-MI)、靶病变血运重建(TLR)、靶血管血运重建(TVR)及支架内血栓。
1.1.2 排除标准①评判、综述类文章,单纯报道BVS与EES,非随机对照的文章;②无结局指标或原始数据不充分及未找到原文的文献;③纳入急性心肌梗死(包括酶学尚未恢复正常的MI)、心力衰竭(EF%<30%)等非研究人群的研究;④同一研究人群重复发表的文献;
1.2 文献检索策略计算机检索数据库包括PubMed、Embase、Embase、Web of science及Cochrane Database。检索时间设定为2008-01至2017-09。英文检索词包括:percutaneous coronary intervention、bioresorbable vascular scaffold、everolimus eluting stent、Randomized Controlled Trial;中文检索词包括“生物可吸收支架”、“生物可吸收血管支架”、“药物洗脱支架”、“经皮冠状动脉介入治疗”。检索方式为采用主题词与自由词相结合的方式检索。
1.3 文献筛选及质量评价根据预先设计的文献检索策略进行检索,获得符合检索要求的文献113篇,去除重复文献9篇,阅读题目与摘要后,排除非临床研究、单臂研究、病案报道、综述、Meta分析等共56篇,仔细查阅全文,排除低质量研究48篇,排除研究方向不符的RCT文献2篇,最终纳入7篇RCT文献。文献的质量评价由2名研究者独立完成,当有分歧时,与第3名研究员讨论决定。根据改良的Jadad量表评价纳入文献的质量,主要依据为以下几方面:①随机序列产生;②分配隐藏;③是否对研究者和受试者施盲;④研究结局盲法评价;⑤结局数据的完整性;⑥选择性报告研究结果;⑦其他偏倚。
1.4 数据提取文献的检索和选择以及数据的提取均由2位研究者分别独立完成,按照纳入排除标准筛选文献,并进行数据的提取,如果有分歧通过讨论确定或由第3位研究者确定。
1.5 效应指标
1.5.1 安全性指标对生物可吸收血管支架的安全性的评价指标为全因死亡率、心源性死亡率、心肌梗死率、支架内血栓发生率。心源性死亡指不能确定直接死亡原因为非心源性的一切死亡。心肌梗死定义为由于心肌缺血导致心肌细胞死亡,心肌梗死标准为:血清心肌标志物(主要是肌钙蛋白)升高(至少超过99%参考值上限),并至少伴有以下一项临床指标:①缺血症状;②新发生的缺血性ECG改变[新的ST-T改变或左束支传导阻滞(LBBB)];③ECG示病理性Q波形成;④影像学证据显示有新的心肌活性丧失或新发的局部室壁运动异常;⑤冠脉造影或尸检证实冠脉内有血栓。支架内血栓分为确定的支架内血栓(有相应的临床表现加造影或病理学证据)、极可能的支架内血栓(缺乏造影或病理证据,主要指术后30 d内难以解释的死亡或任何时间的靶血管心肌梗死)和可能的支架内血栓(30 d后发生的无法解释的死亡)[18]。
1.5.2 有效性指标有效性指标包括靶病变血运重建率、靶血管血运重建率及各项复合终点发生率,包括靶血管失败率、靶病变失败率、面向设备的主要心血管不良事件发生率、面向患者的复合终点发生率、面向设备的复合终点发生率等。其中TLR为因靶病变(植入支架近远端5 mm以内的血管段)再狭窄或其他并发症而引起再次行PCI或冠脉搭桥术;TVR定义为因靶血管(植入支架的整条冠脉及其分支)任何一段再狭窄或其他并发症而引起再次行PCI或冠脉搭桥术;TVF是指患者心因死亡、心肌梗死或有临床指征的TVR的复合结局;靶病变失败,又称为面向设备的复合终点(DOCE),是指患者心因死亡、靶血管心肌梗死或有临床指征的靶病变血运重建(TLR)的复合结局。面向设备的主要心血管不良事件是指患者心因死亡、心肌梗死或有临床指征的靶血管血运重建的复合结局;面向患者的复合终点是指患者全因死亡、心肌梗死或所有血运重建的复合结局[18]。
1.6 统计分析 异质性检验使用I2值,I2值显示了纳入研究间由于异质性而导致的研究间差异占总体差异的百分比。当I2<50%表示异质性可能不重要,I2在50%~75%为显著异质性,I2在75%~100%表示有很大异质性。以P<0.05为差异有统计学意义。纳入的6项研究异质性检验结果均I2<50%,P>0.05,异质性不明显,采用固定效应模型进行分析。采用Cochrane协作网提供的Review Manager 5.3软件进行统计分析,定量综合数据资料。采用固定效应模型计算比值比(OR)和95%置信区间(CI)。
2 结果
2.1 纳入研究质量分析和基线特征本文纳入7篇RCT文献,纳入的研究均为高质量随机对照研究(Jadad评分均>4分),实验均为单盲,采用随机序列,有明确的隐藏和退出记录。共5546例患者,其中BVS组3241例,EES组2309例。主要包含患有原发性冠脉疾病需要行PCI治疗的患者,两组患者基线特征相似,平均年龄62.5±10.1岁,男性比70.7%~87.5%,吸烟比例21.7%~49.5%;入选患者中,高血压患者63.7%、糖尿病患者平均占比24.3%;入组患者中急性心肌梗死19.4%、稳定型心绞痛患者50.7%、不稳定型心绞痛23.58%。冠状动脉病变共6406处,以LAD病变为主,占总病变44.74%;其次为RCA病变,占总病变31.1%。文献筛选流程见图1,纳入各研究的基线特征及病变特征见表1、2,文献质量偏倚评价见图2。
2.2 BVS与EES结局事件对比其中直接观察指标包括:全因死亡,心源性死亡、MI、靶血管心肌梗死(TV-MI)、TLR、TVR及支架内血栓(表2)。就数据分析可见,应用BVS与应用EES相比,短时间内在安全性和有效性方面并无明显差异。在1年内随访中,除靶血管心肌梗死率两组差异有统计学意义外(OR=1.57,95%CI:1.06~2.31,P=0.02),各项终点指标(心肌梗死、支架内血栓、所有血运重建、靶血管血运重建等)均无明显差异。而在2~3年随访中,各项临床终点,如心肌梗死、靶血管心肌梗死、支架内血栓等发生率差异日益明显,如BVS组2~3年随访中心肌梗死发生率为7.86%,高于EES组(4.89%)、靶血管心肌梗死发生率为6.49%,高于EES组(3.53%)、TVR发生率为9.42%,高于EES组(7.02%)、支架内血栓发生率为2.58%,显著高于EES组(0.68%)。以上差异均有统计学意义。
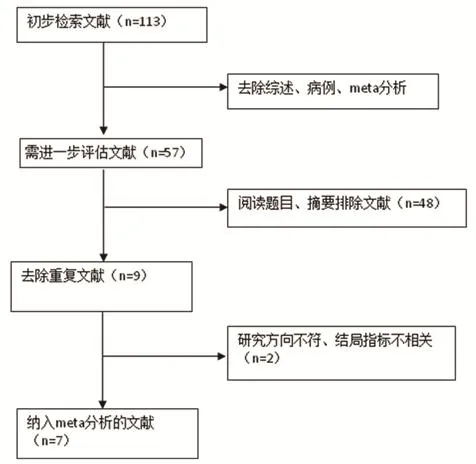
图1 文献筛选流程图
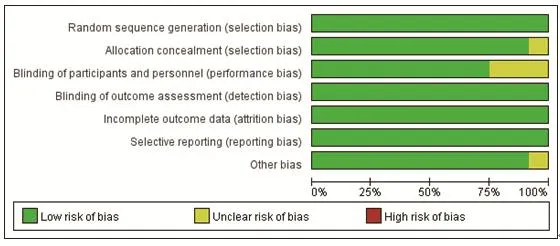
图2 文献偏倚风险图
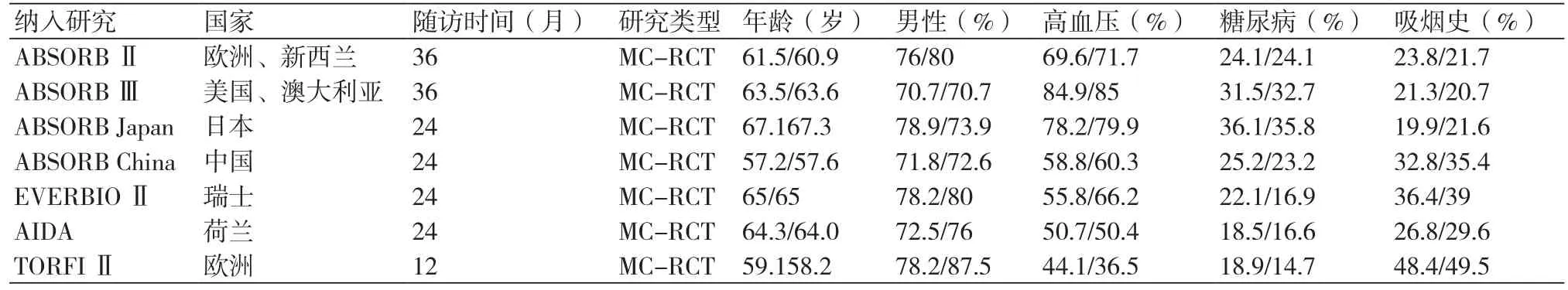
表1 患者基线特征
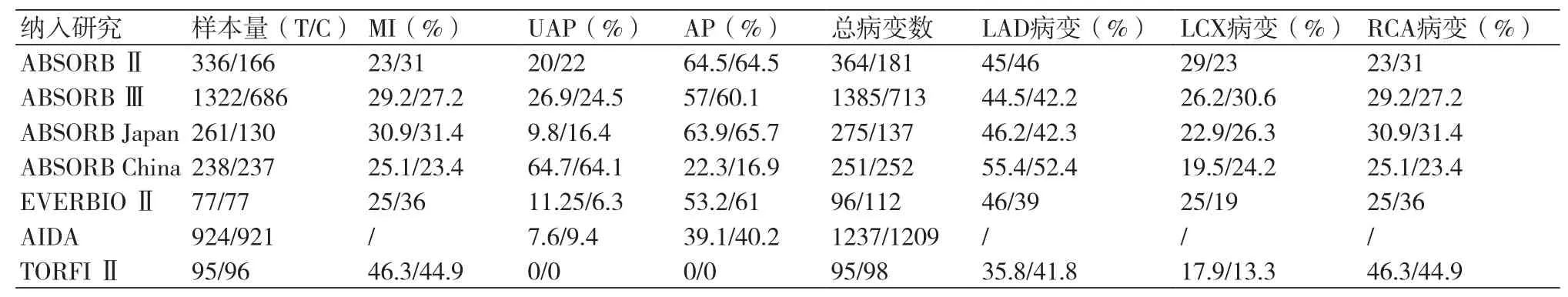
表2 患者病变特征
2.3 复合终点对比复合终点包括:面向支架的MACE,包括心源性死亡、心肌梗死及缺血驱动的靶病变血运重建。POCE包括全因死亡、心肌梗塞和所有血运重建。DOCE即靶病变失败(TLF),包括心源性死亡、TLR及TV-MI、TVF(表5-6)。
2.3.1 MACE应用BVS较EES明显增加了患者MACE事件发生率。对应用两种支架的患者进行随访,1年内BVS组MACE发生率为7.33%(171/2333)、EES组为5.72%(80/1398),差异无统计学意义(P=0.09);2~3年随访中BVS组支架内血栓发生率为14.68%(461/3143),高于EES组(235/2208,10.64%),差异有统计学意义(OR=1.37,95%CI:1.15~1.63,P=0.0003)(图3)。
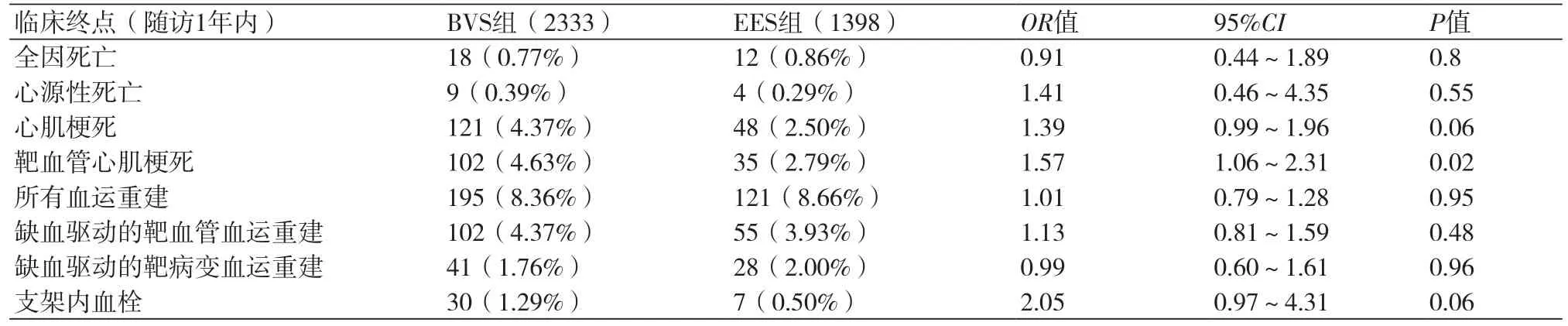
表3 患者结局时间对比(1年随访)(n,%)
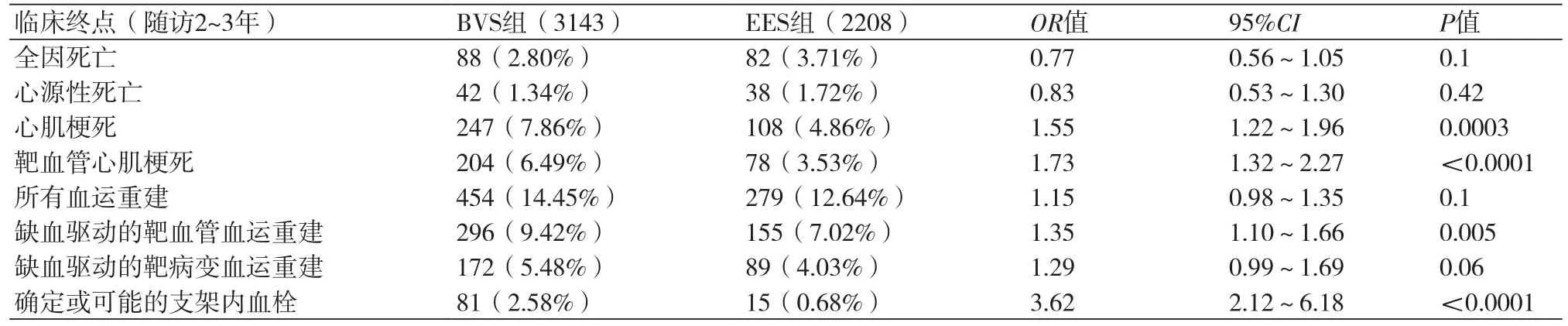
表4 患者结局事件对比:2~3年随访(n,%)
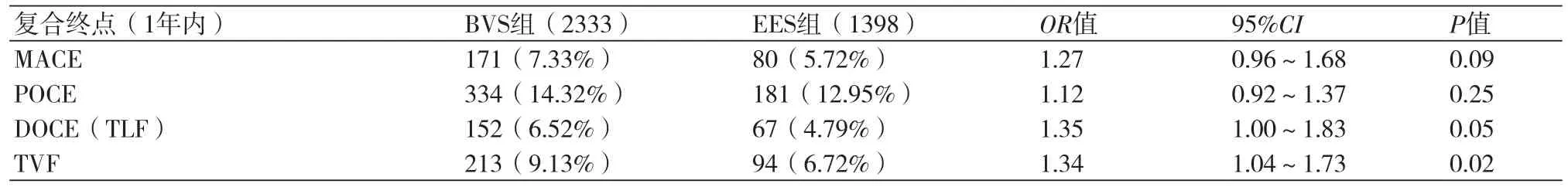
表5 患者复合终点事件对比(1年随访)(n,%)

表6 患者复合终点事件对比(2~3年随访)(n,%)
2.3.2 POCE应用BVS较应用EES增加了患者术后POCE事件发生率。对应用两种支架的患者进行随访,1年内BVS组POCE发生率为14.32%(334/2333)、EES组为18.95%(181/1398),差异无统计学意义(P=0.25);2~3年随访中BVS组POCE发生率为25.12%(789/3143)、EES组为21.24%(469/2208),BVS组POCE发生率高于EES组,差异有统计学意义(OR=1.21,95%CI:1.06~1.38,P=0.005)(图4)。
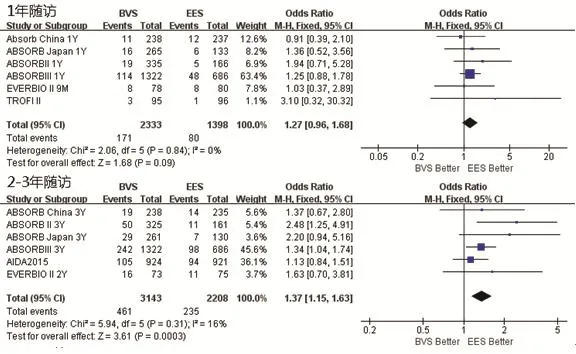
图3 比较植入BVS与植入EES患者MACE事件发生率的Met分析
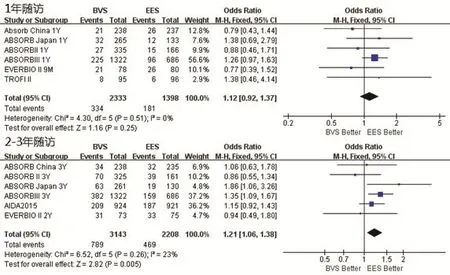
图4 比较植入BVS与植入EES患者POCE事件发生率的Meta分析
2.3.3 DOCE应用BVS较EES增加了患者POCE事件发生率。对应用两种支架的患者进行随访,1年内BVS组DOCE发生率为6.52%(152/2333),EES组为4.79%(67/1398),差异无统计学意义(P=0.05);2~3年随访中,BVS组DOCE发生率为13.31%(418/3143),高于EES组(205/2208,9.28%),差异有统计学意义(OR=1.41,95%CI:1.18~1.69,P=0.0002)(图5)。
2.3.4 TVF应用BVS较EES增加了患者TVF发生率。对应用两种支架的患者进行随访,1年内BVS组TVF发生率为9.13%(213/2333),高于EES组(94/1398,6.72%),差异有统计学意义(P=0.02);2~3年随访中,BVS组TVF发生率为17.26%(542/3143),EES组为12.27%(271/2208),BVS组TVF发生率高于EES组,差异有统计学意义(OR=1.44,95%CI:1.23~1.69,P<0.00001)(图6)。
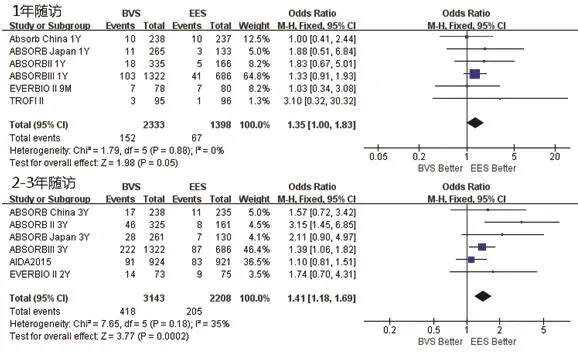
图5 比较植入BVS与植入EES患者DOCE事件发生率的Meta分析

图6 比较植入BVS与植入EES患者TVF事件发生率的Meta分析
2.4 异质性分析上述各终点均未发现研究间存在异质性(I2<50%,P>0.1),故本Mata分析均采用固定效应模型。剔除任一研究均未对总体结局产生统计学改变。
3 讨论
在PCI领域,随着技术的革新,PTCA、MS、DES的应用,冠心病介入治疗的疗效逐步上升,尤其是随着新一代药物洗脱支架应用于临床,支架内血栓等事件明显有所减少。然而,金属支架在冠状动脉内的长期存留,仍然存在包括且不限于血管几何结构与运动功能的受损、晚期支架贴壁不良、晚期/极晚期支架内血栓、新生动脉粥样硬化及支架再狭窄等问题[13]。因此,旨在短期内为血管提供支撑力,然后完全消失,解除支架对血管的束缚,恢复血管的生理特性的BVS被视为经皮冠状动脉治疗的第四次革命,一经推出即获得了心血管介入医师及广大冠心病患者的广泛关注。在ABSORB Ⅱ、ABSORB JAPAN、ABSORB CHINA和 ABSORB Ⅲ系列随机对照研究[12-14]中,分别以临床和造影终点作为主要观察指标,对比PCI中置入BVS和EES,实现了非劣效性结果。但是这些单个研究的设计样本量较小,随访时间短,在临床终点上尚难以获得令人信服的结论。在之前的研究中,临床结果都是BVS降解完成之前得到的,因为BVS的主要收益应该来自于其完全降解之后,故短期内BVS只要不明显劣于DES,在支架完全降解后,患者的晚期收益可能会更加明显。但随着大量随机对照研究的加入和随访时间的延长,实验结果越来越向不利于BVS的方向发展。为了明确比较BVS与EES的安全性和有效性,我们再次综合高质量的随机对照研究,以最新的数据证实了在2~3年的随访中,BVS的安全性和有效性并不优于EES。
在本项研究中,我们纳入7项随机对照研究,共5546例接受PCI治疗的患者,其中3241例植入BVS,2305例植入EES。经数据合并分析,对于接受PCI治疗的冠脉疾病患者,在术后1年内,BVS组在全因死亡率、心源性死亡率、心肌梗死率、支架内血栓发生率差异均无统计学意义,在TVF及靶血管心肌梗死发生率高于EES组,MACE、POCE等复合终点率差异亦无统计学意义。而在术后2~3年内,BVS组心肌梗死率、靶血管心梗率、支架内血栓发生率明显升高,靶血管血运重建率、各项复合终点的发生率均明显高于EES组,故认为BVS在安全性和有效性上尚劣于EES。
在2016年,LANCET上就有一项荟萃分析[19]表明,与EES相比,BVS有着更高的支架内血栓的风险且与时间有一定关系,术后30 d内支架内血栓发生率较高;而在一项包含147项研究的Meta分析[20]中,BRS支架内血栓发生率显著高于目前的DES,但在1年后从1.0%降至0.5%。同时间的多项研究及随访均倾向于BVS对EES的非劣效性。但BVS的完全降解至少需要3年[21],在支架完全降解后其收益应当更加明显,而在本项研究中,BVS组2~3年随访与1年随访相比,心肌梗死率由4.37%上升至7.86%,血栓发生率从1.29%上升至2.58%,各复合终点事件发生率明显升高。这可能与患者的入选标准不同、基线资料不完全相同、手术医师判断和操作不同有关,但更提示现行的BVS尚存在一些问题。
目前BVS的局限性可能体现在以下几个方面:①支架厚度及强度:目前BVS支架成分大多是聚合物或可降解金属(如聚乳酸支架、可降解镁支架),而可降解材料的机械性能与钴铬合金或不锈钢等材料相比尚有一定距离。如聚乳酸的抗张力强度是50~70 MPa,而钴铬合金及不锈钢则为1449 MPa和668 MPa;破裂临界时的伸长率聚乳酸为2%~6%,而钴铬合金或不锈钢为40%[22]。弹性模量与径向支撑力密切相关,为了达到与钴铬合金相同的支撑力,聚合物支架不得不牺牲厚度换取强度。目前常见BVS厚度约150~200 μm,钴铬合金支架厚度为80 μm。因此其通过性能较金属支架明显降低,这会严重限制其在复杂及严重扭曲、钙化病变中的应用。②可视性及操作性:聚合物在X射线下不显影,只有存在于支架两端的不透光的铂金显影,导致术者操作定位困难且不易判断支架贴壁情况,以致造成支架贴壁不良,且容易存在金属标记物脱落问题。植入BVS时不仅需要充分的球囊预扩张作为准备、更高压力的后扩张来确保支架完全释放,通常还需血管内超声和光学相干断层成像等影像学技术作为辅助手段来确认释放的完全程度和排除支架边缘的血管内皮损伤和支架贴壁不良[23]。而后扩张压力过大时,甚至可导致BVS本身结构的破坏[24]。③血管直径:在一项包含ABSORB Ⅲ实验[25]中,血管直径≥2.5 mm,两组靶病变失败率之比为7.8%:6.1%,非劣效性P<0.007;而当血管直径<2.5 mm时,BVS植入后靶病变失败率则高达19%。从该试验结果可以看出,对于在较小的病变血管,植入BVS的靶病变失败率及直接内血栓发生率明显高于较大的血管。④对于分支血管的影响。在ABSORB EXTEND试验中[26],对植入BRS的435例患者(共1209个分支病变)及植入依维莫司药物洗脱支架(Xience支架,Abbott,美国)的237例患者(包含682个分支)的回顾性血管造影进行评估,研究表明,植入BRS的患者分支闭塞发生趋势更高(BVS 6.0%vs. XIENCE 4.1%,P=0.09),发生分支闭塞的患者存在更高的心梗发生率(6.5vs. 0.5%,P<0.01)。而Xience只存在参考血管直径≤0.5 mm的小分支闭塞的风险(10.5%vs. 3.9%,P=0.03)。据此可见,BVS从机械性质到操作方法,均与传统EES有很大区别,机械的套用EES支架的手术方法和经验可能反而增加患者的风险。
总的来说,BVS作为一种新型血管支架装置,因其可完全降解性而承担了较小的对血管形态结构及血流动力学的影响、有助于病变血管的“生理恢复”、对其他治疗及检查影响小等诸多期望。然而随着研究的深入和随访的进行,越来越多的证据证明目前BVS的安全性与有效性不优于目前主流的新一代DES。其适用的患者类型、置入的策略及其与DES的临床疗效比较仍有待更多研究与更长期的随访予以验证。BVS虽然是一项前途远大的革命性技术,但目前还仍存在很多不足之处。要取代传统DES支架,BVS尚需大幅的改进和研究,不断提升其性能与安全性。
