例析物质的定量分析
2019-04-25浙江俞真蓉
浙江 俞真蓉
1.前言
定量分析在科学研究中的重要性是不言而喻的。在化学研究中,我们不仅需要知道化学物质的组成元素、组成成分,而且需要知道某物质组成元素或成分的含量,这就需要用定量分析的方法来测定。
物质的定量分析一般过程如下:取样→试样溶解→干扰组分的分离→测定方法的选择及数据测定→数据分析处理及结果的表示。
在生产和科研中只有准确、可靠的分析结果才具有实际应用价值,否则将导致生产或科研方面产生重大损失、资源严重浪费等不良后果。因此,物质的定量分析是新高考化学实验的热点和难点,考查学生对所学知识进行分析、类推、计算化学问题的能力,物质的定量分析同时渗透化学反应原理方面知识。它充分体现“源于教材又不拘泥于教材”的命题指导思想,在一定程度上考查学生的创新思维能力,有利于高校选拔人才。本文总结了五种常考物质的定量分析题型,并提出相应的解题模板,帮助学生提高此考点的解题能力。
2.解题模板
“物质的定量分析”选题背景与实际问题紧密结合,把物质的性质、实验操作与化学计算有机融合,突出了化学计算的本质,体现化学学科对计算的要求,基于教学实践并结合“物质的定量分析”涉及的相关化学知识和原理,总结出如下解题模板:
第一步,分析题给实验情境,明确实验反应原理,写出相关化学方程式(或离子方程式)并配平(可能只有一个反应,也可能是多个相关反应);第二步,分析已知物和所求物之间存在的定量关系(可能是直接关系,也可能是间接关系);第三步,代入题给数据,进行定量计算,得出结论。
3.分类例析
考向1:滴定法
酸碱中和滴定是高中化学重要的定量实验,既是学习的重点和难点,又是高考化学的热点。由“酸碱中和滴定”拓展、延伸,演变的滴定类型有:氧化还原滴定、电势滴定、配位(络合)滴定、沉淀滴定,还有返滴定法和双指示剂滴定法等。
【案例1】(2016·天津·节选)水中溶氧量(DO)是衡量水体自净能力的一个指标,通常用每升水中溶解氧分子的质量表示,单位mg/L,我国《地表水环境质量标准》规定,生活饮用水源的DO不能低于5 mg/L。某化学小组同学设计了下列装置(夹持装置略),测定某河水的DO。

1.测定原理:


2.测定步骤:
a.安装装置,检验气密性,充N2排尽空气后,停止充N2。
b.向烧瓶中加入200 mL水样。
c.向烧瓶中依次迅速加入1 mL MnSO4无氧溶液(过量)、2 mL碱性KI无氧溶液(过量),开启搅拌器,至反应①完全。
d.搅拌并向烧瓶中加入2 mL硫酸无氧溶液至反应②完全,溶液为中性或弱酸性。
e.从烧瓶中取出40.00 mL溶液,以淀粉作指示剂,用0.010 00 mol·L-1Na2S2O3溶液进行滴定,记录数据。
f.……
g.处理数据(忽略氧气从水样中的逸出量和加入试剂后水样体积的变化)。
回答下列问题:
若某次滴定消耗Na2S2O3溶液4.50 mL,水样的DO=________mg/L(保留一位小数)。作为饮用水源,此次测得DO是否达标:________(填“是”或“否”)。
【答案】9.0;是

【案例2】(2016·浙江·29节选)无水MgBr2可用作催化剂。实验室采用镁屑与液溴为原料制备无水MgBr2,装置如图:
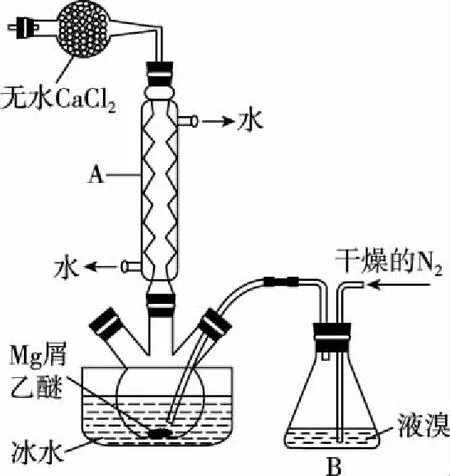

测定时,先称取0.250 0 g无水MgBr2产品,溶解后,用0.050 0 mol·L-1的EDTA标准溶液滴定至终点,消耗EDTA标准溶液26.50 mL,则测得无水MgBr2产品的纯度是________(以质量分数表示)。
【答案】97.52%

考向2:重量法
热重分析法,即物质在一定温度作用下,随温度的升高,会产生相应的变化,如水分蒸发、失去结晶水、小分子易挥发物的逸出、物质的分解氧化等,然后利用差量法计算某一成分质量。
【案例3】(2017·全国卷Ⅲ·26节选)绿矾是含有一定量结晶水的硫酸亚铁,在工农业生产中具有重要的用途。某化学兴趣小组对绿矾的一些性质进行探究。回答下列问题:
为测定绿矾中结晶水含量,将石英玻璃管(带两端开关K1和K2)(设为装置A)称重,记为m1g。将样品装入石英玻璃管中,再次将装置A称重,记为m2g。按如图所示连接好装置进行实验。
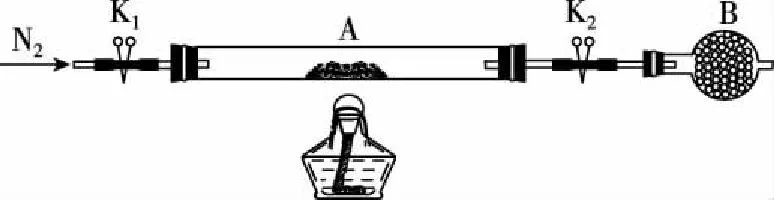
实验过程:打开K1和K2,缓缓通入N2→点燃酒精灯,加热→熄灭酒精灯→关闭K1和K2→冷却至室温→称量,按上述操作步骤,直至A恒重,记为m3g。
根据实验记录,计算绿矾化学式中结晶水数目x=________(列式表示)。


考向3:沉淀法
沉淀法,即利用沉淀反应使待测组分以微溶化合物的形式沉淀出来,再使之转化为称量形式称量,从而计算其纯度。
【案例4】(2016·浙江金华模拟·节选)某校化学兴趣小组的同学开展测定Na2SO3和NaCl的固体混合物中Na2SO3的质量分数实验,操作流程如下:
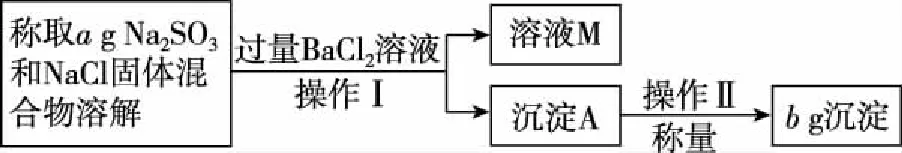
根据操作流程中的数据计算Na2SO3的质量分数:________。


考向4:气体法
气体法,即通过反应产生气体的体积或质量来计算某一成分的物质的量或质量,从而得到物质的纯度。
【案例5】为了测定已部分变质的过氧化钠样品的纯度,设计如图所示的实验装置,图中Q为弹性良好的气球,称取一定量的样品放入其中,按如图所示的装置安装好仪器,打开分液漏斗的活塞,将稀硫酸滴入气球中。

实验结束时,量筒Ⅰ中有xmL水,量筒Ⅱ中收集到ymL气体,则过氧化钠的纯度是________(用含x、y的式子表示,上述体积均已折算成标准状况)。


考向5:分光光度法
在分光光度计中,将不同波长的光连续地照射到一定浓度的样品溶液时,便可得到与不同波长相对应的吸收强度。如以波长(λ)为横坐标,吸收强度(A)为纵坐标,就可绘出该物质的吸收光谱曲线。利用该曲线进行物质定性、定量的分析方法,称为分光光度法。
用紫外光源测定无色物质的方法,称为紫外分光光度法;用可见光光源测定有色物质的方法,称为可见光光度法。它们与比色法一样,都以Lambert-Bee定律为基础。


准确称取0.315 0 g无水Cu(NO3)2,用蒸馏水溶解并定容至100 mL,准确移取该溶液10.00 mL,加过量NH3·H2O,再用蒸馏水定容至100 mL,测得溶液吸光度A=0.620,则无水Cu(NO3)2产品的纯度是________(以质量分数表示)。
【答案】92.51%

3.思考
从上述案例可以看出,虽然物质的定量分析类型较多,实验涉及的原理不尽相同,但总的解题策略是不变的,即在定性实验的基础上研究量的关系,根据实验反应原理和记录的数据,通过分析、计算、推理等确定有关样品含量。
