避雨栽培对“桂葡6号”葡萄酒花色苷组成及含量的影响
2019-04-09谢太理周咏梅谢林君黄小云吴代东
余 欢,谢太理,张 劲,周咏梅,谢林君,黄小云,吴代东,成 果
(广西壮族自治区农业科学院葡萄与葡萄酒研究所,广西 南宁 530007)
【研究意义】避雨栽培是广西鲜食与酿酒葡萄的主要栽培模式,不仅可以有效防控葡萄病害,降低葡萄病害用药30 %以上[1-2],还可对决定葡萄果实及葡萄酒颜色的花色苷类物质及其它指标产生影响。“桂葡6号”是经驯化筛选出的丰产、抗病性好的红色酿酒葡萄品种,源于广西地区收集的野生资源,2015年经审定后命名,是广西本土酿酒品种之一[3]。因此,探讨避雨栽培对“桂葡6号”葡萄酒花色苷的影响,对挖掘广西本地葡萄品种资源,提升特色酿酒葡萄品质至关重要。【前人研究进展】花色苷(Anthocyanins)是葡萄果实及葡萄酒中重要的类黄酮物质,决定着葡萄果实及葡萄酒的色度色调,其组成由葡萄品种的基因型决定[4-6]。而相同品种葡萄及葡萄酒中花色苷的组成及含量受到栽培模式、气候等因素的影响[7]。国内外关于避雨栽培对酿酒葡萄果实及葡萄酒品质影响的研究结论存在差异。Li等[8]发现简易避雨栽培下‘赤霞珠’的花色苷含量显著增加,但花色苷的组成没有发生变化。李舒婷等[9]研究发现‘赤霞珠’避雨栽培有助于缓解气候变化对果皮中花色苷等类黄酮物质积累的影响,有利于稳定果实的类黄酮代谢。王敏等[10]研究发现,避雨栽培的‘赤霞珠’酿造的葡萄酒在口感、色泽等方面明显优于露天栽培。也有研究发现避雨栽培降低了‘赤霞珠’及其葡萄酒的花青素含量[11-13],迟明等[14]发现避雨栽培可以增加‘赤霞珠’葡萄果实还原糖、总酚和单宁的含量,但降低了果实总花色素含量。【本研究切入点】目前国内外有关避雨栽培对酿酒葡萄及葡萄酒花色苷影响的研究主要集中于欧亚种,本研究团队前期进行了“桂葡6号”果实及葡萄酒花色苷组分特征的相关研究,但关于在避雨栽培模式下 “桂葡6号”葡萄酒花色苷的研究尚未开展[15-16]。现对避雨与露天栽培“桂葡6号”葡萄酒的花色苷组成与含量进行分析,有利于进一步完善“桂葡6号”推广技术,为指导生产提供理论依据。【拟解决的关键问题】以避雨栽培的“桂葡6号”酒样为试验对象,与露天栽培进行对比,通过液相色谱等检测方法分析不同瓶储期的花色苷含量等指标,为提高“桂葡6号”酿酒品质提供理论依据。
1 材料与方法
1.1 试验地点及材料
试验地点:广西壮族自治区农业科学院明阳双季葡萄示范园(22°50′59′′ N, 108°14′35′′ E)。试验葡萄为:7年生“桂葡6号”(Vitissp.)。果园土质为黄壤土,南北行向,株行距1.6 m×3.0 m,单臂60度“V”形篱架栽培,树势中等,滴灌和管理水平良好,田间土肥水管理和病虫害防治等同常规[17]。2017年从葡萄萌芽开始进行覆盖避雨棚膜与不覆膜2种处理,于同年7月果实达到技术成熟度(糖酸比≥20)时进行人工采收。
试验材料:二甲花翠素-3-O-葡萄糖苷标准品(美国Sigma-Aldrich公司);甲醇、甲酸和乙腈(均为色谱级,美国Fisher公司);Lalvin 71B活性干酵母(法国Lallemand公司)。
1.2 仪器与设备
UV-1801紫外分光光度计(北京瑞利分析仪器公司);5804R低温冷冻离心机(德国Eppendorf公司);岛津LC-20AD高效液相色谱(日本岛津公司)。
1.3 试验方法
1.3.1 发酵试验 参照成果等[15]的方法。除梗破碎后入罐,每个品种3 罐(20 L/罐)作3次重复。随后每罐按照20 g/t和30 mg/L的剂量分别加入果胶酶和H2SO3(在葡萄醪中加糖,预设葡萄酒乙醇体积分数为12.5 %)。放置在15 ℃恒温冷库中,24 h后按照200 mg/L剂量加入Lalvin 71B活性干酵母。酒精发酵过程控制在25 ℃直到残糖小于4 g/L。每天进行压帽,测定温度和比重。酒精发酵结束后避雨栽培和露天栽培的3次重复酒样取样,置于-20 ℃保存待测化学指标;乙醇发酵结束后,避雨栽培和露天栽培的3次重复酒样分别装瓶放置在15 ℃保存,瓶储1、3、6和9月后分别取样,-20 ℃保存待测花色苷及色度色调。
1.3.2 化学指标测定 参照国标《中华人民共和国国家标准—葡萄酒》(GB 15037-2006)分析测定葡萄酒中pH值、残糖、滴定酸、挥发酸、酒精度、总酚等基本化学指标。
1.3.3 色度色调测定 CIELab法测定酒样色度色调。CIELab参数(L、a、b和C)利用1 mm光程条件下440、530和600 nm酒样吸光度计算[32]。
1.3.4 花色苷类物质检测 参照文献[18]方法测定。采用岛津LC-20AD高效液相色谱对提取产物进行检测。系统检测包括电喷雾离子源和离子阱质谱检测器。HPLC条件:Zorbax Eclipse SB C18色谱柱(250 mm×4.6 mm,5 μm);流动相A:含2 %甲酸-6 %乙腈溶液,流动相B:含2 %甲酸-54 %乙腈溶液。洗脱程序:1~18 min,10 %~25 % B;18~20 min,25 % B;20~30 min,25 %~40 % B;30~35 min,40 %~70 % B;35~40 min,70 %~100 % B。流速1.0 mL/min;柱温50 ℃;检测波长525 nm;进样量30 μl。MS条件:电喷雾离子源,正离子模式;雾化器压力35 psi;干燥气流速12 L/min;干燥气温度300 ℃;质量扫描范围m/z 100~1500。酒样经过过滤后,用0.45 μm滤膜过滤直接进样,每个样品重复进样3次。
1.3.5 花色苷类物质定性与定量分析 花色苷定性工作对照中国农业大学葡萄酒研究中心建立的“葡萄与葡萄酒花色苷HPLC-UV-MS指纹谱库”完成[18]。建立5~500 mg/L,9个水平、3个重复的二甲花翠素-3-O-葡萄糖苷标准曲线,相关系数在0.999以上,其他花色苷以相当于二甲花翠素-3-O-葡萄糖苷的含量计。
1.3.6 统计分析 使用SPSS 20.0(IBM公司)进行单因素方差分析(多组间比较采用 One-Way ANOVA 法,两组间比较采用独立样本t检验P<0.05),使用Microsoft Excel 2010 进行数据处理及绘图。

图1 避雨和露天栽培下“桂葡6号”葡萄酒的CIELab参数Fig.1 CIELab color parameters of ‘Guipu 6’ wines under the rain-shelter and open-field cultivation
2 结果与分析
2.1 对葡萄酒化学指标的影响
如表1所示,酒精发酵结果后,避雨栽培“桂葡6号”酒样的滴定酸、残糖和酒精度显著低于露天栽培酒样,而pH值、挥发酸含量、单宁及总酚含量则显著高于露天栽培酒样。
2.2 对葡萄酒色度色调的影响
由图1可知,随着瓶储期的增加,避雨与露天栽培“桂葡6号”酒样红-绿色调值(a)和色度值(C)均下降,黄-蓝色调值(b)增加,即红色调和色度降低,而黄色调增强。由表2可知,与露天栽培相比,避雨栽培酒样的亮度值(L)在瓶储1、3和6个月后皆呈降低趋势,但在瓶储9个月后上升,而露天栽培酒样的L值整体上升,即避雨栽培酒样在前3个瓶储期颜色逐渐加深,在4期颜色变浅,而露天酒样颜色整体越来越浅。
由表2可知,瓶储1个月后,避雨栽培酒样的a值、C值、b值及L值均显著高于露天栽培酒样。瓶储3个月后,避雨栽培酒样a值、C值均显著高于露天栽培酒样;避雨栽培酒样b值与露天栽培酒样没有显著差异;避雨栽培酒样L值显著低于露天栽培酒样。瓶储6个月后,避雨栽培酒样a值、C值及L值均显著高于露天栽培酒样;避雨栽培酒样b值与露天栽培酒样没有显著差异。瓶储9个月后,避雨栽培酒样a值、C值均显著高于露天栽培酒样;避雨栽培酒样L值及b值均显著低于露天栽培酒样。就避雨栽培酒样而言,4个时期b值均有显著差异且随着瓶储期的增加显著增加;随着瓶储时间增加a值显著降低;随着瓶储时间的增加C值显著降低,且只有瓶储9个月与瓶储1、3、6个月有显著差异,其他瓶储时间之间没有显著差异;L值4个瓶储期均无显著差异。就露天栽培酒样而言,随着瓶储期的增加a值及C值显著降低,且4个瓶储期均有显著差异;b值随着瓶储期的增加显著降低;L值随着瓶储期的增加显著增加。
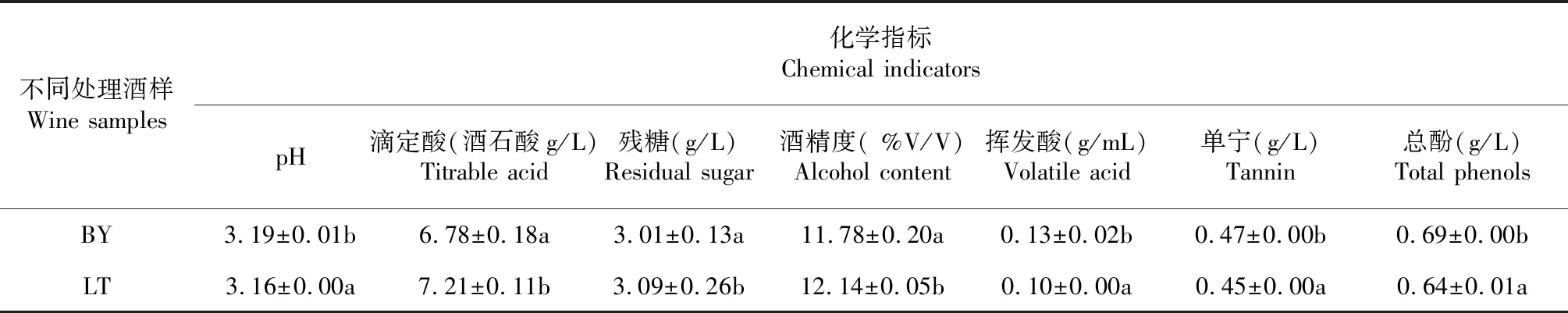
表1 “桂葡6号”葡萄酒的化学指标
注:不同处理相同指标间的差异显著用不同字母表示(T-检验,P<0.05)。 LT代表露天栽培,BY代表避雨栽培,下同。
Note: Values within a column followed by different letters differ significantly between different treatments (T-test,P<0.05).LT means open-field cultivation. BY means rain-shelter cultivation. The same as below.
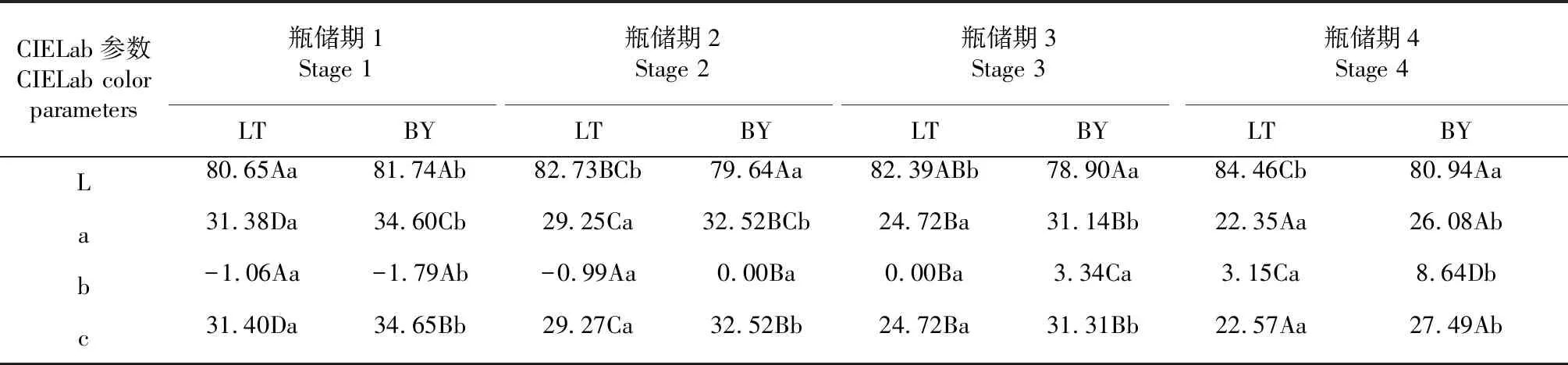
表2 避雨与露地栽培下“桂葡6号”葡萄酒的CIELab参数的显著性方差分析
注: 不同大小写字母表示差异在0.05显著水平(P<0.05),大写字母表示同一处理不同瓶储期的差异性,小写字母表示同一瓶储期不同处理的差异性。1为瓶储1个月后,2为瓶储3个月后,3为瓶储6个月后,4为瓶储9个月后。下同。
Note: Different capital letters and lowercase letters represent the significant at 0.05 probability level (P<0.05). Different capital letters mean the same treatment after different bottle storage. Different lowercase letters mean different treatments after one bottle storage.1 means after bottle storage for one month. 2 means after bottle storage for three months. 3 means after bottle storage for six months. 4 means after bottle storage for nine months. The same as below.
试验结果表明,与露天栽培酒样相比,避雨栽培酒样红色调和黄色调更强,颜色更深。随着瓶储期的增加,两种栽培模式酒样的红色调和色度都降低,黄色调增加。
2.3 避雨与露天栽培对不同瓶储期“桂葡6号”葡萄酒花色苷含量与比例的影响
由图2-A所示,所有瓶储期下避雨栽培酒样的花色苷总量始终显著高于露天栽培酒样。随着瓶储期的增加,避雨栽培酒样的花色苷总量呈波动变化趋势,且瓶储3、6及9个月差间异显著。就露天栽培酒样而言,随着瓶储期的增加,花色苷总量呈波动下降趋势,前3个瓶储期差异不显著,瓶储1和9个月差异显著。两种栽培酒样的双糖苷含量变化趋势与花色苷总量相似(图2-B)。除瓶储3个月时避雨栽培酒样的单糖苷含量显著高于露天栽培酒样外,在其他3个瓶储期两种栽培酒样均无显著差异;瓶储3个月的避雨栽培酒样的单糖苷含量与其他3个瓶储期均有显著差异;露天栽培酒样的单糖苷含量在4个瓶储期均无显著差异(图2-C)。瓶储3和9个月的两种栽培酒样的花翠素含量存在显著差异;其中,瓶储1、3及9个月的避雨栽培酒样间均存在显著差异;而瓶储9个月的露天栽培酒样与前3个瓶储期酒样分别存在显著差异(图2-D)。就花青素含量而言,2种栽培酒样的变化趋势与总花色苷含量相似,瓶储3及9个月的避雨栽培酒样显著高于露天栽培酒样;瓶储3个月的避雨栽培酒样显著高于瓶储6个月;露天栽培酒样仅在瓶储1和9个月时存在显著差异(图2-E)。2种栽培酒样的甲基化含量变化趋势与总花色苷含量相似,瓶储3和9个月的避雨栽培酒样显著高于露天栽培酒样;瓶储3个月的避雨栽培酒样显著高于瓶储6和9个月;瓶储1个月的露天栽培酒样中的甲基化花色苷含量显著高于瓶储9个月(图2-F)。就非甲基化含量而言,2种栽培酒样在4个瓶储期均无显著差异;避雨栽培酒样瓶储1个月时显著高于瓶储6个月,而露天栽培酒样瓶储1个月时显著高于其他3个瓶储期(图2-G)。就乙酰化含量而言,瓶储3个月及9个月避雨栽培酒样显著高于露天栽培;避雨栽培酒样瓶储1和3个月时无显著差异,且显著高于瓶储6和9个月;瓶储1个月的露天栽培酒样显著高于瓶储9个月(图2-H)。避雨栽培酒样的非酰化花色苷含量在瓶储3和9个月时显著高于露天栽培酒样;避雨栽培酒样瓶储3个月时显著高于瓶储6和9个月;露天栽培酒样瓶储1个月时显著高于瓶储9个月(图2-I)。避雨栽培酒样花色苷单体含量只在瓶储3个月时显著高于露天栽培酒样,其他瓶储期2种栽培酒样没有显著差异;避雨栽培酒样瓶储1个月显著高于瓶储6个月,瓶储3个月显著高于瓶储6和9个月;露天栽培酒样4个瓶储期均无显著差异(图2-K)。就聚合物含量而言,2种栽培酒样在4个瓶储期均无显著差异;避雨栽培酒样瓶储3个月与瓶储6个月无显著差异,且均显著高于瓶储1和9个月,瓶储1个月显著高于瓶储9个月;露天栽培酒样的变化趋势与避雨栽培酒样相似。

图2 避雨栽培和露天栽培模式下“桂葡6号”花色苷总量及各种修饰方式花色苷浓度随瓶储期的变化趋势Fig.2 The variation trend of total anthocyanins and different modified anthocyanins in ‘Guipu No.6’ wines with different bottle storage periods under rain-shelter and open-field cultivation
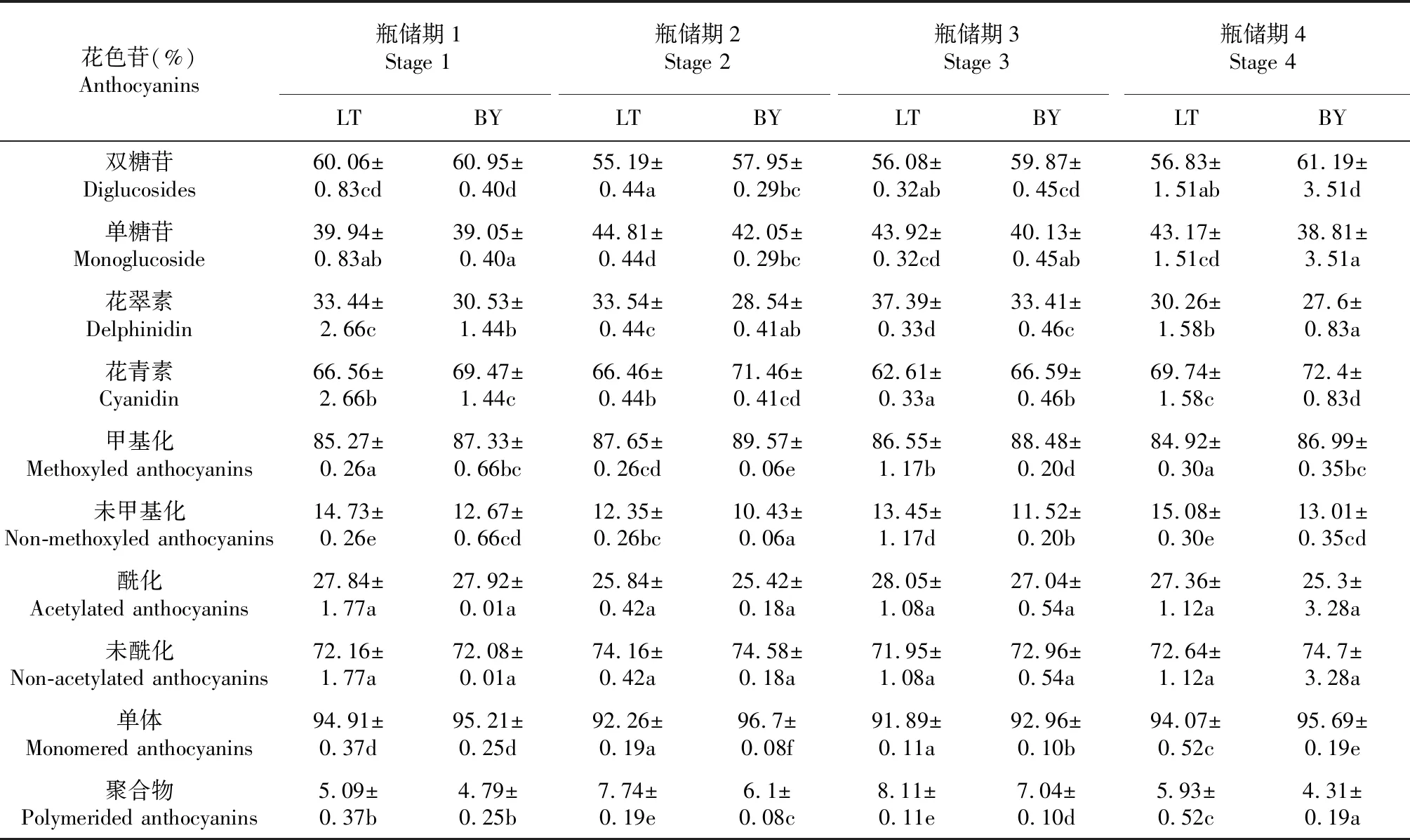
瓶储1个月直至瓶储9个月后“桂葡6号”葡萄酒各修饰类型花色苷占总花色苷比例如表3所示。结果表明,2种栽培酒样双糖苷比例大于单糖苷比例,花青素比例大于花翠素比例,甲基化比例大于非甲基化比例,未酰化比例大于酰化比例,单体比例大于聚合物比例。就双糖苷与单糖苷比例而言,瓶储3、6和9个月避雨栽培酒样双糖苷比例均显著高于露天栽培酒样;避雨栽培酒样瓶储1个月显著高于瓶储3个月,露天栽培瓶储1个月显著高于其他3个瓶储期。除了瓶储1个月2种栽培酒样单糖苷比例无显著差异,其他3个瓶储期露天栽培酒样均显著高于避雨栽培酒样;避雨栽培酒样瓶储3个月显著高于瓶储1个月,露天栽培酒样瓶储3、6和9个月均显著高于瓶储1个月。就花翠素与花青素比例而言,4个瓶储期露天栽培酒样花翠素比例均显著高于避雨栽培酒样;避雨栽培与露天栽培酒样瓶储6个月均显著高于其他3个瓶储期。4个瓶储期避雨栽培酒样花青素比例均显著高于露天栽培酒样;避雨栽培与露天栽培酒样瓶储1和3个月无显著差异,且均显著高于瓶储6个月。就甲基化与未甲基化比例而言,4个瓶储期避雨栽培酒样甲基化比例均显著高于露天栽培酒样;避雨栽培与露天栽培酒样瓶储1和9个月无显著差异,且均显著低于瓶储3和6个月。4个瓶储期避雨栽培酒样非甲基化比例均显著低于露天栽培酒样;避雨栽培与露天栽培酒样瓶储1和9个月无显著差异,且均显著高于瓶储3及6个月。就酰化比例及非酰化比例而言,4个瓶储期2种栽培酒样均无显著差异,且随着瓶储期的变化2种栽培酒样均无显著差异。就花色苷单体比例而言,避雨栽培酒样在瓶储3、6和9个月均显著高于露天栽培酒样,避雨栽培酒样瓶储1个月与露天栽培酒样无显著差异;避雨栽培酒样在4个瓶储期均存在显著差异,瓶储3个月显著高于其他3个瓶储期,瓶储9个月显著高于瓶储1和6个月;露天栽培酒样瓶储1个月显著高于其他3个瓶储期,瓶储9个月显著高于瓶储3和6个月。就聚合物比例而言,避雨栽培酒样在瓶储3、6和9个月均显著低于露天栽培酒样,瓶储1个月时2种栽培酒样无显著差异;避雨栽培酒样4个瓶储期均存在显著差异,瓶储6个月显著高于其他3个瓶储期,瓶储9个月显著低于其他3个瓶储期,瓶储3个月显著高于瓶储1个月;露天栽培酒样瓶储3和6个月见无显著差异,且均显著高于其他2个瓶储期,瓶储期9个月显著高于瓶储1个月。
表3避雨与露天栽培下“桂葡6号”葡萄酒中不同修饰类型花色苷所占总量比例
Table 3 The ratio of different modified anthocyanins in ‘Guipu No.6’ wines after different bottle storage periods under the rain-shelter and open-field cultivation
花色苷(%)Anthocyanins瓶储期1Stage 1瓶储期2Stage 2瓶储期3Stage 3瓶储期4Stage 4LTBYLTBYLTBYLTBY双糖苷Diglucosides60.06±0.83cd60.95±0.40d55.19±0.44a57.95±0.29bc56.08±0.32ab59.87±0.45cd56.83±1.51ab61.19±3.51d单糖苷Monoglucoside39.94±0.83ab39.05±0.40a44.81±0.44d42.05±0.29bc43.92±0.32cd40.13±0.45ab43.17±1.51cd38.81±3.51a花翠素Delphinidin33.44±2.66c30.53±1.44b33.54±0.44c28.54±0.41ab37.39±0.33d33.41±0.46c30.26±1.58b27.6±0.83a花青素Cyanidin66.56±2.66b69.47±1.44c66.46±0.44b71.46±0.41cd62.61±0.33a66.59±0.46b69.74±1.58c72.4±0.83d甲基化Methoxyled anthocyanins85.27±0.26a87.33±0.66bc87.65±0.26cd89.57±0.06e86.55±1.17b88.48±0.20d84.92±0.30a86.99±0.35bc未甲基化Non-methoxyled anthocyanins14.73±0.26e12.67±0.66cd12.35±0.26bc10.43±0.06a13.45±1.17d11.52±0.20b15.08±0.30e13.01±0.35cd酰化Acetylated anthocyanins27.84±1.77a27.92±0.01a25.84±0.42a25.42±0.18a28.05±1.08a27.04±0.54a27.36±1.12a25.3±3.28a未酰化Non-acetylated anthocyanins72.16±1.77a72.08±0.01a74.16±0.42a74.58±0.18a71.95±1.08a72.96±0.54a72.64±1.12a74.7±3.28a单体Monomered anthocyanins94.91±0.37d95.21±0.25d92.26±0.19a96.7±0.08f91.89±0.11a92.96±0.10b94.07±0.52c95.69±0.19e聚合物Polymerided anthocyanins5.09±0.37b4.79±0.25b7.74±0.19e6.1±0.08c8.11±0.11e7.04±0.10d5.93±0.52c4.31±0.19a
注: 不同小写字母表示差异在0.05显著水平(P<0.05)。
Note: Different lowercase letters represent the significance at 0.05 probability level (P<0.05).

表4 “桂葡6号”葡萄酒花色苷含量与CIELab参数的相关性分析
注:**表示相关性达到极显著水平(P<0.01),*表示相关性达到显著水平(P<0.05)。
Note: ** represents significant at 0.01 level, * represents significant at 0.05 level.
2.4 葡萄酒花色苷含量与CIELab参数的相关性分析
将4个瓶储期避雨栽培和露天栽培酒样的CIELab参数与不同类型花色苷含量进行相关性分析,得到参数之间的相关性系数,如表4所示。L值与a值、C值、总花色苷、双糖苷、单糖苷、花翠素、花青素、甲基化、酰化、未酰化和单体呈现负相关关系。a值与L值、b值之间呈负相关关系;a值与C值、总花色苷、双糖苷、单糖苷、花翠素、花青素、甲基化、非甲基化、酰化、非酰化和单体呈现显著正相关关系。b值与花翠素、聚合物呈现显著负相关关系。C值与L值呈现显著负相关关系;C值与a值、总花色苷、双糖苷、单糖苷、花翠素、花青素、甲基化、非甲基化、酰化、非酰化和单体呈现显著正相关关系。
3 讨 论
葡萄酒中花色苷的组成与葡萄果实类似[19]。同品种葡萄酒的花色苷组分受到年份、产区、栽培模式、酿造工艺等因素的影响,避雨栽培通过影响果实周围的光、温、水等微环境,从而改变果实品质[20-23]。本试验对2种栽培模式下的“桂葡6号”酒样的花色苷进行瓶储试验,结果表明,避雨栽培酒样整个瓶储期的总花色苷含量均大于露天栽培酒样,且2种酒样中整个瓶储期双糖苷比例均大于50 %,这是“桂葡6号”葡萄品种特性决定的,与成果等[15-16]对“桂葡6号”葡萄果实及其葡萄酒研究结果相符。本试验中,2种栽培酒样在瓶储1个月后总花色苷含量均显著高于其他3个瓶储期,这是因为随着瓶储期的增加,葡萄果实花色苷会随酒石酸盐沉淀而沉淀,氧化和水解使葡萄酒中花色苷含量减少[23]。双糖苷颜色浅,但是比同类型的单糖苷稳定[24]。本试验中,露天栽培酒样的总花色苷含量随着瓶储期一直降低且下降幅度大于避雨栽培酒样,因为每个瓶储期避雨栽培酒样双糖苷含量及比例均显著高于露天栽培酒样。
在酸性条件下,类黄酮结构骨架中B环上的取代基对花色苷的颜色影响很大,羟基越多颜色越红,甲氧基越多颜色越紫,稳定性也越强[25]。3’,5’-羟基取代花色苷包括:花翠素、甲基花翠素、二甲花翠素以及它们的衍生物;3’-羟基取代花色苷包括:花青素、甲基花青素以及他们的衍生物[26]。本试验中,避雨栽培酒样的花青素的含量及比例显著高于露天栽培酒样。B环的甲基化取代使酚羟基的化学活性减弱,但结构稳定性增强,甲基化花色苷主要包括:甲基花青素、甲基花翠素和二甲花翠素[27]。本研究中,避雨栽培酒样在每个瓶储期甲基化类花色苷比例及含量均大于避雨栽培酒样,说明避雨栽培模式对于“桂葡6号”葡萄酒的颜色稳定有积极作用。瓶储9个月后,两种栽培酒样的花翠素比例均下降,但避雨栽培酒样下降幅度小于露天栽培酒样,这说明在瓶储过程中葡萄酒紫色色调变弱,花色苷稳定性降低。花色苷的酰化能增强其稳定性[28]。本试验中,避雨栽培酒样的酰化含量整体显著高于避雨栽培酒样,但两种栽培酒样的酰化比例在整个瓶储期之间没有显著差异,说明避雨栽培模式对于“桂葡6号”葡萄酒的酰基化没有显著影响。花色苷的聚合体相对于其单体而言,稳定性更强,而双糖苷容易褐变[29-30]。本试验中,4个瓶储期两种栽培酒样聚合物花色苷含量均没有显著差异,就聚合物比例而言,避雨栽培酒样在瓶储3、6和9个月均显著低于露天栽培酒样,瓶储1个月时两种栽培酒样无显著差异这可能是由于避雨栽培酒样的双糖苷比例较高,C4和C5位无法进行成环加合反应。
花色苷是决定红色葡萄酒颜色非常重要的因素[31]。本试验中,在4个瓶储期里,避雨栽培酒样总花色苷含量、色度值(C)及红-绿色调值(a)均大于露天栽培酒样,即花色苷总量与C及a呈正相关关系,与王宏等[32]、陶永胜等[33]的研究结果相符;避雨栽培酒样亮度值(L)总体显著小于露天栽培酒样,即总花色苷含量与亮度值(L)呈负相关,但总花色苷含量与黄-蓝色调值(b)不相关,与王宏等[32]研究结果相符;随着瓶储期的延长,两种栽培酒样花色苷总量均显著降低,红色调和饱和度均减小,黄色调均增加。且有研究表明,对于刚酿制的新鲜红葡萄酒而言,L越小,颜色变化在深紫色到暗紫红之间,颜色偏暗,以纯正的暗红色为上品[34],这说明与露天栽培酒样相比,避雨栽培有利于“桂葡6号”葡萄果实花色苷的积累,对“桂葡6号”葡萄酒CIELab参数贡献更大,从而使葡萄酒外观品质更好。
4 结 论
避雨栽培能够显著性提升“桂葡6号”葡萄酒的花色苷总量、双糖苷含量及比例、甲基化含量及比例、花青素的含量及比例,但对酰化及聚合物的影响显著性不大,对葡萄酒的颜色品质有积极的稳定作用。与露天栽培酒样相比,避雨栽培酒样红色调和黄色调更强,颜色更深;且瓶储期的增加使两种栽培酒样的花色苷总量呈显著降低趋势,红色调及色度减弱,黄色调增强,因此避雨栽培更有利于得到颜色品质佳的“桂葡6号”葡萄酒。
