辣根过氧化物酶直接电化学传感器检测过氧化物的研究
2019-04-08杨绍明张小荣柏朝朋
曹 嫱,杨绍明,杨 杰,张小荣,柏朝朋,滕 渝
(华东交通大学 材料学院,江西 南昌 330013)
过氧化物广泛应用于化工、造纸、医药等领域,对人们的生产生活造成很大影响[1-2],如过氧化氢异丙苯溶于水后,不仅污染环境,若被生物体吸入,则会引起中毒,破坏正常的生物机理,阻碍正常的生物代谢[3]。目前,过氧化物检测的方法主要有分光光度法[4]、化学发光法[5]、荧光法[6]和酶传感器法[7-8]等,而基于辣根过氧化物酶的电化学传感器法,以灵敏度高、选择性好和仪器设备简单等优点,受到广大研究者的密切关注。辣根过氧化物酶电化学传感器检测过氧化物一般通过电子介体的中介作用,或酶的直接电化学法实现酶与电极之间的电子传递。直接电化学法的酶传感器法无需电子介体,可简化电极制备,但由于酶的电活性中心被蛋白质本体包覆,一般难以实现与电极之间的直接电化学。因此,纳米材料如碳纳米管[9]、石墨烯[10]、金纳米粒子[11]及复合纳米材料[12]等常被用来修饰电极表面以促进酶与电极之间的电子传递。如Yagati等[13]先将石墨烯/金纳米粒子复合物修饰到氧化铟锡(ITO)电极表面,然后通过共价键合将辣根过氧化物酶(HRP)固定到电极表面,实现酶直接电化学检测过氧化氢。
基于复合纳米材料的直接电化学HRP传感器的制备存在纳米材料的修饰与酶的固定化需分步完成及灵敏度较低等问题。本文以高比表面积和导电性好的泡沫镍(Ni foam)为基底材料,在碳纳米管(CNTs)修饰的泡沫镍表面,一步电沉积法制备了HRP-AuNPs/CNTs/Ni foam。首先,十六烷基三甲基溴化铵(CTAB)的表面活性剂作用使金在电极上形成纳米结构;其次,HRP在偏碱性溶液中带负电,CTAB通过吸附作用,在AuNPs的沉积过程中将其固定在电极上,制备了辣根过氧化物酶生物传感器。一步法制备的AuNPs-HRP使HRP与纳米材料充分接触,缩短了酶活性中心与电极表面的距离,为酶与电极之间的直接电子传递作用提供了良好的环境。该生物传感器可实现对过氧化氢、2-过氧化丁酮、过氧化氢异丙苯的灵敏检测。
1 实验部分
1.1 仪器与试剂
CHI660E电化学工作站(上海辰华仪器有限公司);JSM-6701F场发射型扫描电镜(日本电子JEOL公司);氯金酸(HAuCl4,分析纯,上海试剂一厂);碳纳米管(CNTs,≥97%,深圳纳米港有限公司);十六烷基三甲基溴化铵(CTAB,分析纯,上海展云化工有限公司);辣根过氧化物酶(HRP,250 U/mg,上海三杰生物技术有限公司);30%过氧化氢(西陇化工股份有限公司);过氧化氢异丙苯(化学纯,国药集团化学试剂有限公司);2-过氧化丁酮(分析纯,阿拉丁试剂有限公司)。
1.2 修饰电极的制备
按照文献[14]制备羧基化的多壁碳纳米管;然后将处理后的Ni foam(先用丙酮除油,再进行醇洗、水洗)置于1 mg/mL碳纳米管溶液中于-0.9 V恒电位沉积20 min,用去离子水清洗表面得CNTs/Ni foam修饰电极,再将该修饰电极置于2 mmol/L HAuCl4、10 mmol/L CTAB、3 mg/mL HRP的混合溶液(pH 7.5 磷酸缓冲溶液(PBS))中于-0.9 V恒电位下电沉积30 min,最后用去离子水淋洗,除去电极表面未牢固的粒子和酶,得到HRP-AuNPs/CNTs/Ni foam修饰电极,于4 ℃的冰箱中保存,备用。
1.3 电化学测定
本文所有电化学测试均在CHI660E电化学工作站进行,三电极体系:以修饰电极为工作电极,Ag/AgCl (饱和KCl)为参比电极,铂电极为对电极。
循环伏安(CV)曲线:于0.2 mol/L的PBS底液中以50 mV/s的速率获得CV曲线。
电化学交流阻抗(EIS):于5.0 mmol/L K3[Fe(CN)6]/K4[Fe(CN)6](1 ∶ 1)溶液中以振幅为0.005 V,在1~100 000 Hz频率范围内,测定得到电化字阻抗谱,并通过ZSimpwin软件模拟而成。
电流~时间(I~t)曲线:以0.2 mol/L PBS为底液,在一定电位条件下,连续滴加一定浓度的过氧化氢、2-过氧化丁酮、过氧化氢异丙苯得到。
2 结果与讨论
2.1 AuNPs/CNTs/Ni foam、HRP-AuNPs/CNTs/Ni foam的扫描电镜(SEM)及能谱表征
AuNPs/CNTs/Ni foam和HRP-AuNPs/CNTs/Ni foam的SEM图见图1,由图可见,无HRP存在时,沉积在电极表面碳纳米管表面的AuNPs分散均匀,且金纳米粒子直径小,约为十几个纳米(图1A);修饰HRP后,由于HRP与AuNPs共沉积到碳纳米管表面,碳纳米管的尺寸明显变大(图1B);另外,HRP-AuNPs/CNTs/Ni foam的能谱图(图1C)中可见Ni、C、O和Au元素,表明HRP-AuNPs/CNTs/Ni foam已成功制备。

图1 AuNPs/CNTs/Ni foam(A)和HRP-AuNPs/CNTs/Ni foam(B)的SEM图以及HRP-AuNPs/CNTs/Ni foam的能谱图(C)Fig.1 SEMs of AuNPs/CNTs/Ni foam(A),HRP-AuNPs/CNTs/Ni foam(B)and EDS of HRP-AuNPs/CNTs/Ni foam(C)
2.2 修饰电极的电化学性质
Ni foam、CNTs/Ni foam以及HRP-AuNPs/CNTs/Ni foam在5 mmol/L K3[Fe(CN)6]/K4[Fe(CN)6](1 ∶ 1)溶液中的电化学交流阻抗图见图2A,由图可见,在Ni foam(曲线a)电极表面电沉积一层CNTs后(曲线b),半圆直径变小,阻抗变小,表明CNTs的优良电子传导性能有效促进了[Fe(CN)6]4-/3-在电极表面的电子传递;再修饰HRP后,电极的阻抗明显增加,已大于Ni foam,进一步说明HRP已成功修饰到电极表面。
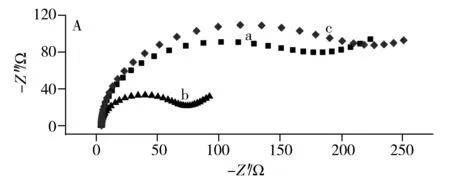
采用循环伏安法考察了HRP-AuNPs/CNTs/Ni foam修饰电极对过氧化氢的催化行为(图2B),结果显示,HRP-AuNPs/CNTs/Ni foam在pH 7.0 PBS缓冲溶液中出现一对可逆的氧化还原峰,这是HRP辅基血红素中的Fe(Ⅱ)/Fe(Ⅲ)氧化还原所产生的可逆峰[15]。向其中加入50 μmol/L过氧化氢后,体系的还原峰电流增大,氧化峰电流减小,出现了明显的催化还原特征,表明该修饰电极对过氧化氢产生了催化。
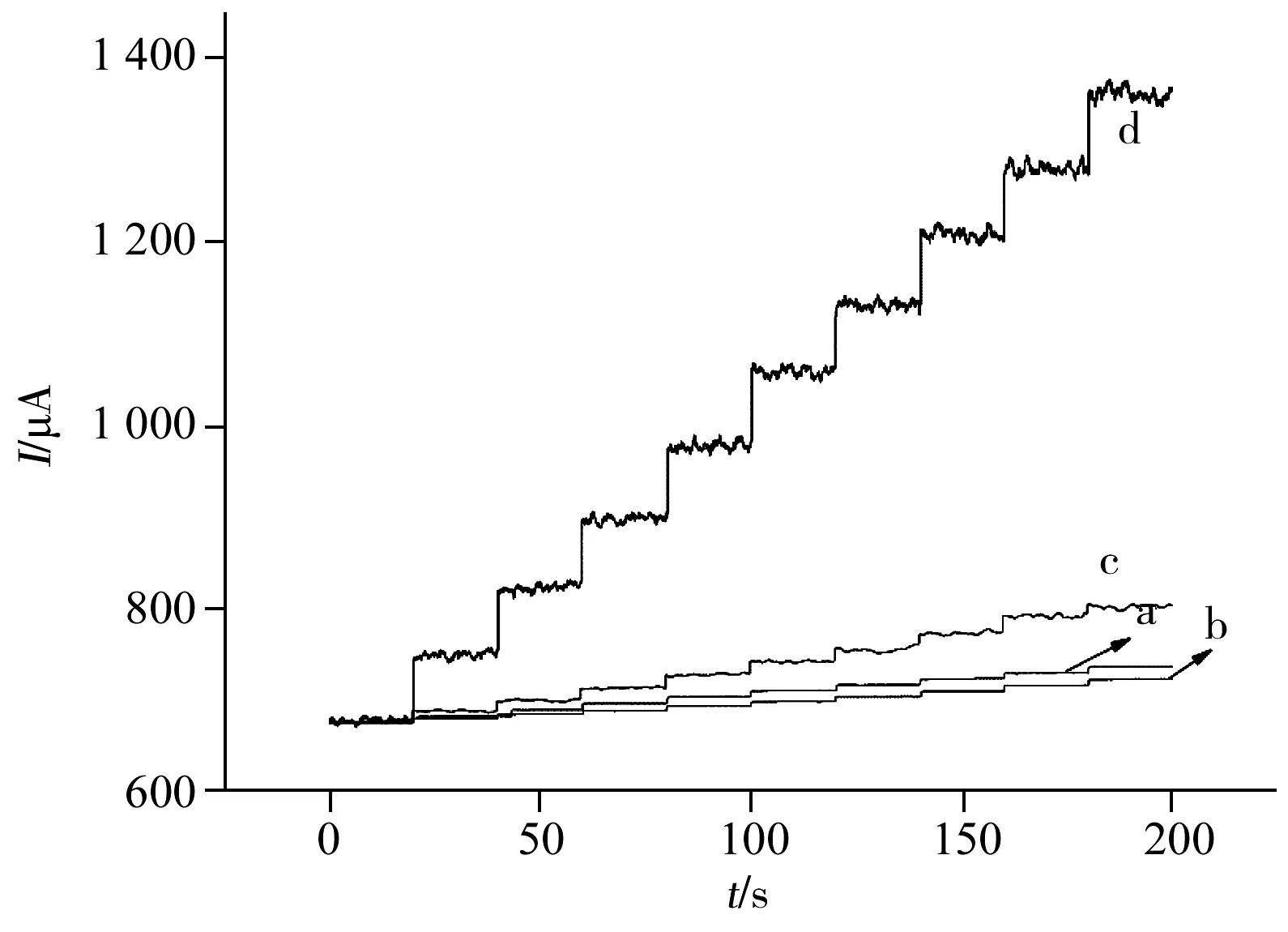
图3 不同修饰电极对连续滴过氧化氢(40 μmol/L)的时间~电流曲线Fig.3 I-t curves of the different electrodes on successive addition of 40 μmol/L H2O2a.Ni foam,b.CNTs/Ni foam,c.AuNPs/CNTs/Ni foam, d.HRP-AuNPs/CNTs/Ni foam;applied potential:-0.3 V
为进一步考察HRP-AuNPs/CNTs/Ni foam对过氧化物的催化响应,分别将Ni foam、CNTs/Ni foam、AuNPs/CNTs/Ni foam、HRP-AuNPs/CNTs/Ni foam 4种修饰电极于pH 7.0 PBS缓冲溶液中连续滴加40 μmol/L过氧化氢,考察其电流~时间响应(图3)。结果显示,Ni foam和CNTs/Ni foam对过氧化氢具有微小的催化作用,AuNPs/CNTs/Ni foam对过氧化氢的催化能力在金纳米粒子的作用下有所提升,而HRP-AuNPs/CNTs/Ni foam电极对过氧化氢的催化作用非常明显,说明HRP的加入显著提高了修饰电极的催化性能,该HRP-AuNPs/CNTs/Ni foam修饰电极可用于过氧化氢检测。
2.3 实验条件的优化
由于pH值对酶催化作用有较大影响,因此,实验以20 μmol/L过氧化氢为例,考察了测定底液的pH值(6.0~8.0)对HRP-AuNPs/CNTs/Ni foam电流响应的影响。结果显示,当测试底液pH值从6.0增至8.0时,修饰电极对过氧化氢的电流响应呈先增大后减小的趋势,且在pH 7.0时达最大值,表明此时修饰电极性能最好,酶催化效果最强,所以选择测试底液的pH值为7.0。
由于工作电位对修饰电极的性能也有较大影响,因此,实验在pH 7.0的PBS缓冲溶液中,采用电流~时间法考察了HRP-AuNPs/CNTs/Ni foam在不同工作电位(-0.15~-0.45 V)下对20 μmol/L过氧化氢的电化学响应情况。结果显示,在-0.15~-0.45 V工作电位范围内,响应电流呈先增加后降低的趋势,且在-0.3 V处达到最大值,因此选择-0.3 V为工作电位。
2.4 HRP-AuNPs/CNTs/Ni foam对过氧化物的分析检测
在优化条件下,采用电流~时间曲线考察了不同浓度的过氧化氢(2.5×10-7~5.4×10-4mol/L)、过氧化氢异丙苯(8.8×10-7~1.5×10-3mol/L)、2-过氧化丁酮(6.8×10-7~1.2×10-3mol/L)在HRP-AuNPs/CNTs/Ni foam电极上于0.2 mol/L PBS(pH 7.0)缓冲溶液中的电流响应。结果显示,过氧化氢、过氧化氢异丙苯、2-过氧化丁酮的电流值(I,A)随其浓度(c,mol/L)的增加而增大,且在相关浓度范围内呈良好的线性关系,线性方程分别为I=2.5×10-4+2.6c(r=0.999)、I=3.7×10-4+1.2c(r=0.998)、I=3.1×10-4+1.6c(r=0.998),修饰电极的检测灵敏度依次为2.6、1.2、1.6 A·L/mol,根据空白的标准偏差计算得三者检出限分别为1.2×10-7、4.5×10-7、2.5×10-7mol/L。
由于本文采用高比表面积的泡沫镍为基础电极,又结合了碳纳米管和纳米金的优异电化学特性,且采用一步法制备AuNPs-HRP使HRP与纳米材料充分接触,缩短了酶活性中心与电极表面的距离,为酶与电极之间的直接电子传递作用提供了良好的环境,使该传感器检测过氧化氢的灵敏度优于文献(表1)。

表1 HRP传感器直接电化学检测过氧化氢的性能Table 1 Performances of direct electrochemistry HRP sensor for the detection of H2O2
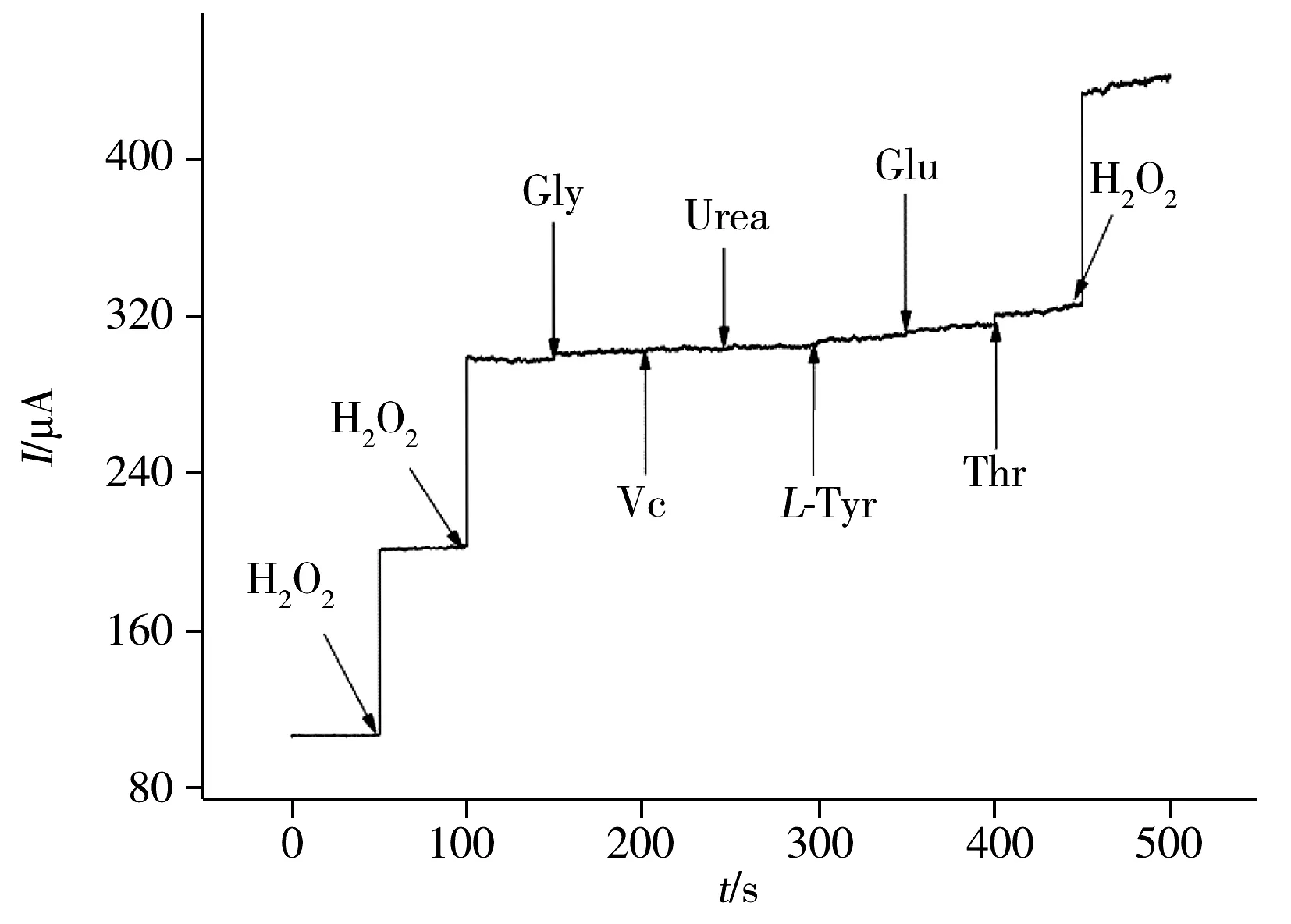
图4 修饰电极的抗干扰性能Fig.4 The anti-interference performance of modified electrode
2.5 抗干扰性能与回收率
实验考察了甘氨酸(Gly)、抗坏血酸(Vc)、脲(Urea)、L-络氨酸(L-Tyr)、葡萄糖(Glu)、凝血酶(Thr)对HRP-AuNPs/CNTs/Ni foam修饰电极测定过氧化氢的干扰情况。采用电流~时间曲线法,于-0.3 V电位下测试(图4),由图可见,10倍于过氧化氢浓度(500 μmol/L)的甘氨酸、抗坏血酸、脲、L-络氨酸、葡萄糖、凝血酶对该修饰电极的催化性能影响较小,不影响过氧化氢的检测,表明该修饰电极具有较强的抗干扰能力。
为了研究该修饰电极的实用性,分别于原始浓度为25.0、40.0、50.0 μmol/L的过氧化氢样品中,加入47.0、63.0、78.0 μmol/L的过氧化氢进行回收率实验,测得回收率为98.4%~102%。
2.6 HRP-AuNPs/CNTs/Ni foam修饰电极的重现性及稳定性
以过氧化氢为例,采用同一根HRP-AuNPs/CNTs/Ni foam对50 μmol/L的过氧化氢重复测定5次,发现电流响应的相对标准偏差(RSD)为3.5%。用5根平行制备的HRP-AuNPs/CNTs/Ni foam修饰电极对50 μmol/L的过氧化氢进行检测,其响应结果的RSD为3.2%。将该电化学传感器存储于4 ℃冰箱中,28 d后,在优化条件下对50 μmol/L的过氧化氢进行测定,发现修饰电极仍保留了87.5%的电流响应。表明该电化学传感器具有良好的重现性和稳定性。
3 结 论
本文以电沉积法制备了HRP-AuNPs/CNTs/Ni foam修饰电极,使用SEM、EDS和电化学方法对电极进行了表征,并采用电化学循环伏安法和电流~时间曲线研究了修饰电极对过氧化氢、过氧化氢异丙苯、2-过氧化丁酮的电化学性能。结果显示,修饰电极对上述3种过氧化物具有良好的催化检测性能,且抗干扰能力强,可用于实际检测。
