雷公藤柱层析中段和末段组分的急性毒性实验△
2019-04-08张辉王宜祥裘颖儿陈宗良方远书何忠平
张辉,王宜祥,裘颖儿,陈宗良,方远书,何忠平
金华市食品药品检验检测研究院,浙江 金华 321000
雷公藤TripterygiumwilfordiiHook.f为卫矛科植物,药用干燥去皮的根,别名菜虫药、黄藤、断肠草和红药。性味苦、辛,温。有毒[1]。主要分布在长江中下游地区,但目前野生资源面临枯竭。雷公藤化学成分非常复杂,目前已从该植物中分离出二萜类、三萜类、生物碱类和苷类等200多种化合物。治疗类风湿性关节炎、慢性关节痛等效果明显,但临床不良反应多发,肝毒性、肾毒性、生殖毒性、血液毒性等明显给临床合理用药带来一定的困难,限制了其广泛应用。造成不良反应多发的原因是多方面的,包括自身含有毒性成分、用药安全范围窄、缺乏药理毒理研究资料、提纯工艺复杂、所考察的指标成分不同,作为雷公藤上市制剂的原料提取物是由雷公藤柱层析中段和末段组分按一定比例混合而成,其有效成分、有效部位含量存在很大差异,继而导致不同上市制剂的临床疗效和不良反应差别很大[2]。今后需要在现有研究的基础上,加强对雷公藤柱层析各组分的基础研究,明确药效、毒性成分及作用机制,获得高效低毒的雷公藤提取物,为后续提取纯化及制剂研究提供理论基础;因此,有必要对其提取纯化的组分进行系统的有效成分(毒性成分)与毒性关系的研究。
1 材料
1.1 药物
雷公藤柱层析中段和末段组分[3](雷公藤醇提物经硅胶柱层析纯化,用乙醇-三氯甲烷梯度洗脱,收集中段和末段洗脱液,回收溶剂,无水乙醇精制),由浙江普洛康裕天然药物有限公司提供。
1.2 动物
清洁级ICR小鼠,(20.0±2.0)g,雌雄各半,由金华市实验动物中心提供,生产许可证号:SCXK(浙)2016-0001。普通级SD大鼠,(200±20)g,雌雄各半,由浙江省实验动物中心提供,生产许可证号:SCXK(浙)2014-0001。
1.3 对照品
雷公藤吉碱(wilforgine)购自上海安谱实验科技股份有限公司(批号:37239-47-7),雷公藤次碱(wilforine)购自上海源叶生物科技有限公司(批号:J23A7T19714)。雷公藤甲素(triptolide,批号:111567-201404)、雷公藤内酯甲(wilforlide A,批号:111597-200505)、雷公藤内酯酮(triptonide,批号:111972-201501)和雷公藤红素(celastrol,批号:111946-201501),均购自中国食品药品检定研究院。以上对照品纯度均大于98%,用于含量测定。
雷公藤多苷工作对照品(批号:1401702)由浙江普洛康裕天然药物有限公司提供,经浙江省食品药品检验研究院标化分装,仅用于毒理实验。
1.4 试剂盒
谷丙转氨酶(ALT)测试盒(批号:20171115),谷草转氨酶(AST)测试盒(批号:20171107),规格100 T/50样,均购自南京建成生物工程研究所。TUNEL细胞凋亡检测试剂盒(显色法)(批号:080817170911)、Proteinase K(批号:080717171031),均购自上海碧云天生物技术有限公司。
1.5 仪器
Agilent 1200 型高效液相色谱仪,XS205DU型十万分之一分析天平、MS204S型电子分析天平(梅特勒-托利多有限公司),CX31型OLYMPUS生物显微镜,日本岛津UV-2600紫外可见分光光度计。
2 方法
2.1 雷公藤柱层析中段和末段组分的含量测定(HPLC法)
参照何昱等[4]建立的测定雷公藤多苷中主要有效成分含量的HPLC方法,色谱柱:Hubble-C18(250 mm×4.6 mm,5 μm);流动相:A相为0.1%磷酸-0.2%三乙胺水溶液,B相为乙腈,梯度洗脱(0~15 min,10%→35% B;15~22 min,35%→35% B;22~30 min,35%→55% B;30~35 min,55% B;35~40 min:55%→60% B;40~70 min:60%→85% B;70~75 min:85%→95% B;75~80 min,95%→10% B);流速:0.75 mL·min-1;检测波长:0~65 min时为225 nm,65 min时切换为210 nm;柱温:35 ℃;进样量:20 μL。测定的有效成分:雷公藤甲素、雷公藤内酯酮、雷公藤次碱、雷公藤吉碱、雷公藤内酯甲、雷公藤红素。
2.2 中段和末段组分急性毒性实验
2.2.1 预实验 鉴于中段和末段组分的有效成分含量差别比较大,通过前期基础实验发现中段和末段组分对ICR小鼠的毒性表现强弱有别,故对中段组分、末段组分和雷公藤多苷对照品分别摸索能引起实验小鼠全死的剂量Dm(LD100)以及全活的剂量Dn(LD0)。在预实验基础上确定实验组数和各组小鼠给药量,相邻的两组间剂量的比值r=0.9。
2.2.2 急性毒性实验(经口LD50的测定) 根据预实验结果,正式实验中段和末段组分分别设置5个剂量组。取ICR小鼠100只,按体质量随机分成10组,每组10只,雌雄各半。分别称取雷公藤柱层析中段和末段组分适量,加聚山梨酯-80[0.1 mL·(20 mg)-1],搅匀,加热使溶解,逐滴加水稀释至所需最高浓度,再按等比数列依次稀释成其他相应浓度。小鼠夜间禁食不禁水12 h,于第2天上午9时灌胃给药1次,灌胃体积为0.20 mL·(10 g)-1。灌胃后各组雌雄分开,每笼5只,正常饲养。给药后于4、8、24 h分别观察1次,以后每天观察1次,连续观察7 d。观察各小鼠外观、活动状况、精神和食欲、对外反应、排泄物等情况,记录体质量变轻、呼吸急促、异常肌肉运动、异常神经活动、异常分泌物等毒性表现和小鼠出现中毒死亡情况(潜伏期、死亡时间、死亡数量),对濒死及死亡小鼠及时解剖,肉眼观察主要脏器有无变化。如有肉眼可见病变(脏器红肿、破裂、颜色异常等),进行组织病理学检查。观察期结束后其他存活的小鼠处死并解剖,根据各组小鼠的死亡数,计算LD50及95%的可信区间。
另取ICR小鼠50只,按体质量随机分成5组,每组10只,雌雄各半。取雷公藤多苷对照品按上述急性毒性实验方法,计算动物LD50及95%的可信区间。标准规定:对照品和供试品的LD50比值应为0.90~1.10(LD50平均可信限率不得超过15%,P=0.95)[2]。
2.3 大鼠急性肝损伤实验
取SD大鼠40只,按体质量随机分成5组,每组8只,雌雄各半。正常对照组、中段组分高剂量组、中段组分低剂量组、末段组分高剂量组、末段组分低剂量组(高剂量组灌胃量200 mg·kg-1,低剂量组灌胃量100 mg·kg-1)。大鼠夜间禁食不禁水12 h,第2天上午9时灌胃1次,正常对照组给予等体积0.9%氯化钠溶液。
2.4 测定大鼠血清中相关生化指标
48 h后,大鼠眼眶取血,血液室温下自然凝固15 min,3000 r·min-1,离心20 min,收集上清液,按照生化试剂盒要求比色法测定大鼠血清中AST、ALT浓度。
2.5 HE染色镜检
处死各组大鼠后,每只均取肝左外叶约10 mm×10 mm×5 mm组织块,10%福尔马林固定,脱水透明、浸蜡、包埋、切片(厚度为5 μm)、贴片、烤片脱蜡、HE染色、脱水封片,在光镜下观察肝组织病理形态变化。
2.6 TUNEL法检测肝组织细胞凋亡
每只大鼠各选一张石蜡切片,二甲苯中脱蜡5 min,换用新鲜的二甲苯再脱蜡5 min,无水乙醇5 min,90%乙醇2 min,70%乙醇2 min,蒸馏水2 min。每张切片滴加20 μg·mL-1不含Dnase的蛋白酶K工作液100 μL,室温作用30 min,PBS洗涤3次,滴加PBS配制的3%过氧化氢溶液室温孵育20 min,随后用PBS洗涤3次,再按照TUNEL细胞凋亡检测试剂盒(显色法)说明书进行操作。每张切片显色后光镜下随机观察5个高倍视野(×400)中凋亡细胞数和总细胞数,两者的比值即为肝细胞凋亡率。
2.7 统计学方法
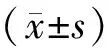
3 结果
3.1 雷公藤柱层析中段和末段组分的物质基础
精密称取雷公藤柱层析中段和末段组分各2份,制备供试品溶液,每个供试品溶液进2针,以混合对照品溶液作为对照,用外标法计算含量,结果见表1,色谱图见图1~3。由色谱图可知,雷公藤柱层析中段和末段组分中所测成分分离度较好,但峰高和峰面积差异较明显。

表1 雷公藤柱层析中段和末段组分中6种成分含量测定 %
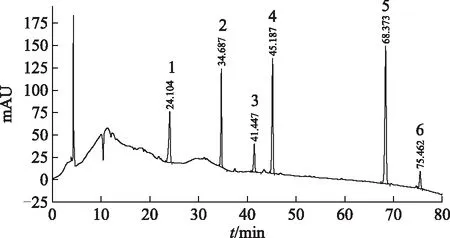
注:1.雷公藤甲素(triptolide);2.雷公藤内酯酮(triptonide);3.雷公藤吉碱(wilforgine);4.雷公藤次碱(wilforine);5.雷公藤红素(celastrol);6.雷公藤内酯甲(wilforlide A);下同。图1 雷公藤混合对照品HPLC图
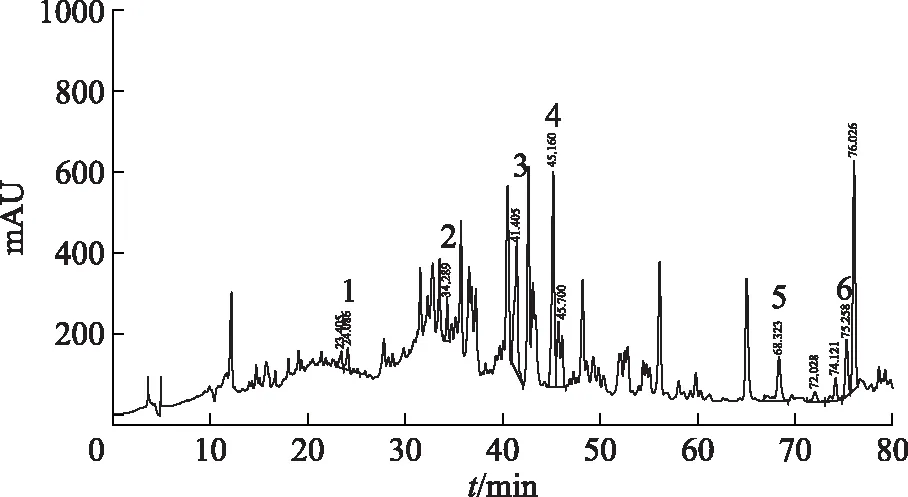
图2 雷公藤柱层析中段组分HPLC图
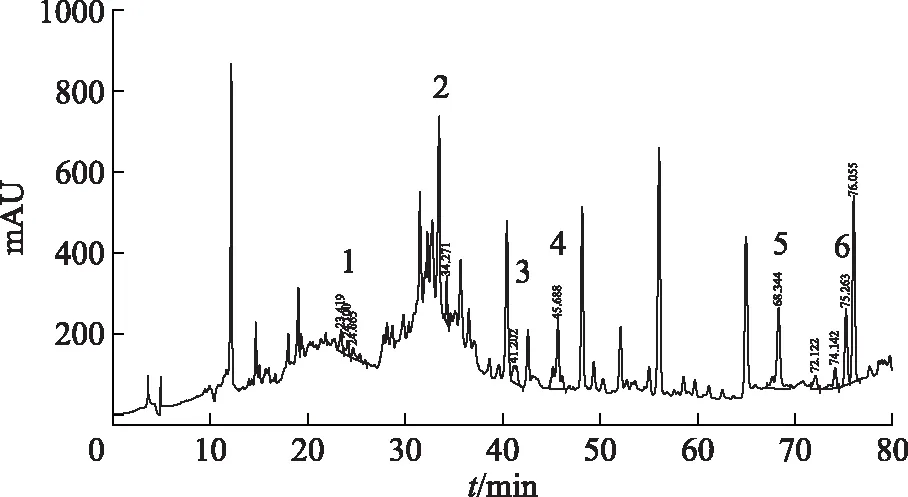
图3 雷公藤柱层析末段组分HPLC图
由表1可知,中段和末段组分中,在所测成分的含量上差异表现较大。中段组分里雷公藤甲素、雷公藤内酯酮、雷公藤吉碱、雷公藤次碱的含量明显高于末段,但雷公藤红素、雷公藤内酯甲的含量明显低于末段。
3.2 LD50的测定结果
3.2.1 预实验 分别摸索出中段组分、末段组分和雷公藤多苷对照品的LD100和LD0(mg·kg-1),见表2。

表2 雷公藤柱层析中段和末段组分的LD100和LD0值 mg·kg-1
3.2.2 经口LD50值 灌胃浓度高的小鼠毒性反应出现时间较早(8 h),给药后24 h有部分小鼠开始死亡,并伴随小鼠体质量减轻,步态不稳,身体扭曲,翻正反射消失,精神萎靡,无食欲,出现中毒情况,48 h中度死亡小鼠最多,毒性反应消失时间较慢,有的在观察结束依然体型消瘦,精神不振,有的在给药后第5天开始恢复正常。灌胃浓度低的小鼠毒性反应出现时间在给药24 h后,中毒反应较弱,毒性反应消失时间在给药后第3天,体质量逐渐恢复正常增长。解剖实验中死亡的小鼠,肉眼观察可见雷公藤中段和末段组分的高浓度组小鼠肝脏颜色变深变暗,表面有颗粒状,小肠充血明显。低浓度组主要脏器肉眼观察未见明显病理改变。各组小鼠的急性毒性结果见表3~5,各段组分和对照品的LD50值见表6。

表3 雷公藤柱层析中段组分对小鼠急性毒性结果
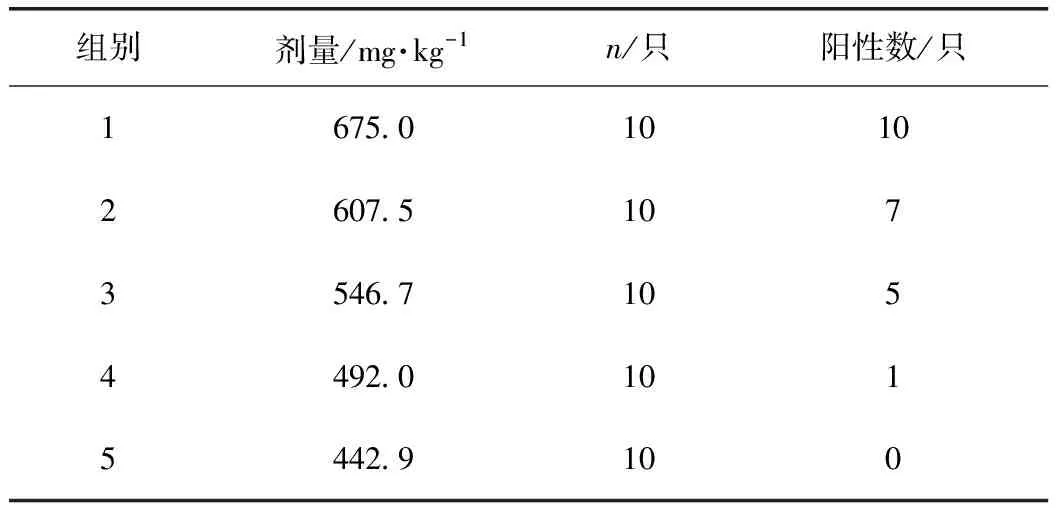
表4 雷公藤柱层析末段组分对小鼠急性毒性结果
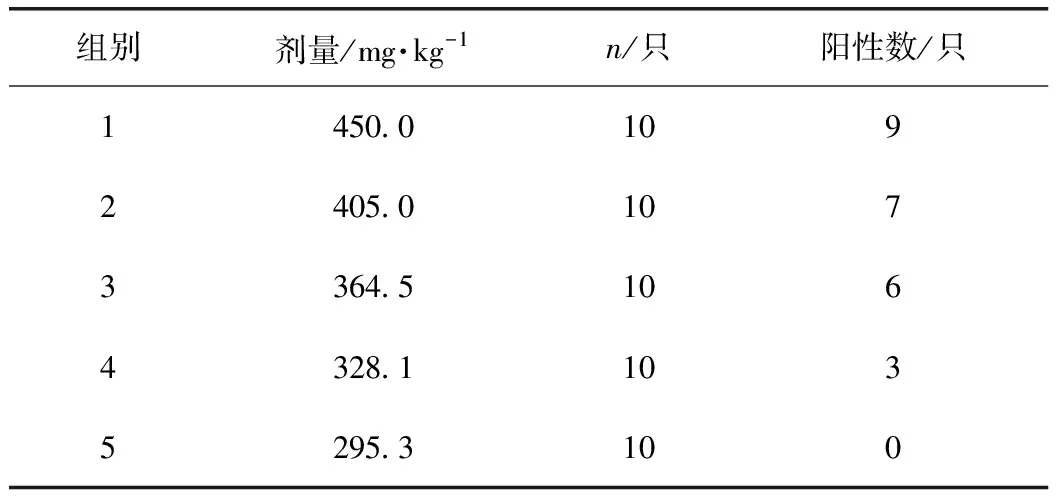
表5 雷公藤多苷对照品对小鼠急性毒性结果
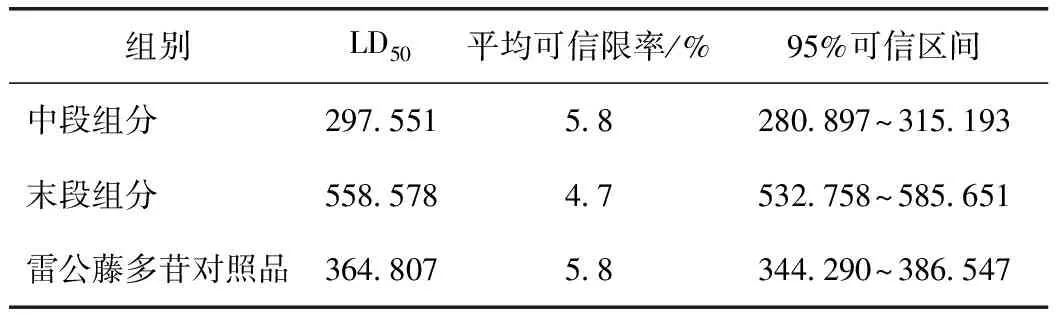
表6 雷公藤柱层析中段和末段组分LD50值 mg·kg-1
表6表明,中段组分毒性明显强于末段组分,雷公藤多苷对照品同中段组分和末段组分LD50比值均不在0.90~1.10,中段组分和末段组分要按合理的配比才能用于制剂。
3.3 雷公藤柱层析中段和末段组分对大鼠肝脏的影响
3.3.1 血清转氨酶 由表7血清转氨酶结果可知,中段组分高剂量组、末段组分高剂量组、中段组分低剂量组大鼠血清中AST和ALT活性均明显高于正常对照组(P<0.01),末段组分低剂量组和正常对照组的差异无统计学意义。相同剂量时,中段组分和末段组分大鼠血清中AST和ALT活性均有统计学差异(P<0.01)。同段组分时,该段的高、低剂量组大鼠血清中AST和ALT活性差异均有统计学意义(P<0.01)。说明灌胃雷公藤柱层析中段和末段组分引起肝细胞受损导致转氨酶释放入血,中段组分高剂量组会引起严重急性肝损伤。
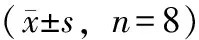
表7 雷公藤柱层析各段组分对大鼠急性肝损伤的影响 U·L-1
注:与正常对照组比较,**P<0.01,*P<0.05。
3.3.2 肝组织形态学 雷公藤柱层析中段和末段组分对大鼠肝组织HE病理形态的改变如图4所示,光镜下正常对照组大鼠中央静脉完好,肝细胞形态结构均完整,肝索排列规则,汇管区正常,肝血窦结构清晰。中段组分高剂量组肝细胞出现细胞水肿,并且细胞水肿的程度高于中段组分低剂量组;末段组分高剂量组出现轻度的细胞水肿(类似中段组分低剂量组的程度)和脂肪变性,末段组分低剂量组出现轻度的脂肪变性。表明灌胃雷公藤柱层析中段和末段组分后引发了不同程度的急性肝损伤。
3.3.3 肝细胞凋亡的影响 如图5所示,正常对照组无明显凋亡现象,给药组可见散在分布呈棕黄色或棕褐色的凋亡细胞,核固缩。
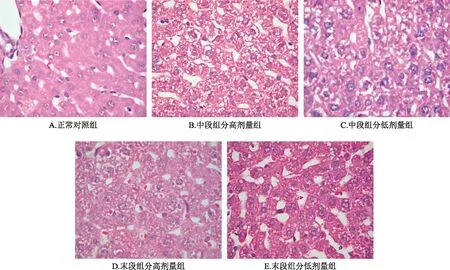
图4 雷公藤柱层析中段和末段组分对大鼠肝组织HE病理形态的改变(×400)
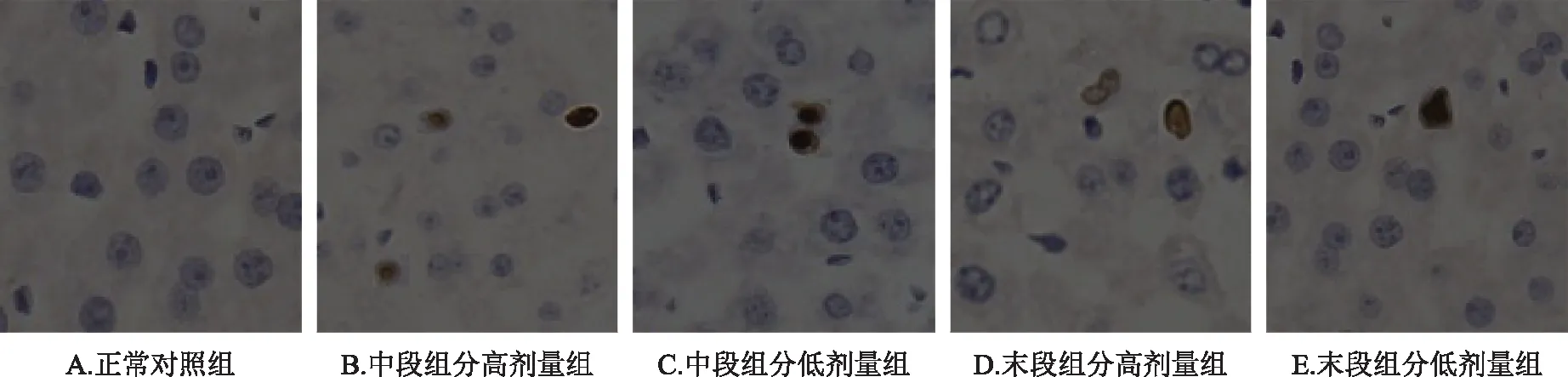
图5 各段组分对大鼠肝细胞凋亡的影响(×400)
由表8可知,中段组分高剂量组、末段组分高剂量组、中段组分低剂量组的细胞凋亡率与正常对照组比较,差异均有统计学意义(P<0.01),末段组分低剂量组和正常对照组无差异。相同剂量时,中段组分和末段组分大鼠肝细胞凋亡率差异均有统计学意义(P<0.05)。同段组分时,该段的高、低剂量组大鼠肝细胞凋亡率差异均有统计学意义(P<0.01)。
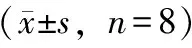
表8 TUNEL法检测肝细胞凋亡率
注:与正常对照组比较,**P<0.01,*P<0.05。
4 讨论
雷公藤是一种有毒中药,不同厂家经过提取和柱层析纯化后所得组分的化学成分基本相同,由雷公藤二萜类、生物碱及三萜类等成分组成,但是质量差异较大。另外现有的雷公藤提取工艺研究中,只规定了雷公藤甲素的上限和雷公藤内酯甲的下限,由于单体化合物含量较低,对整个提取物的影响力有限,不能充分反映雷公藤提取物的内在质量和整体情况。因此我们便对雷公藤柱层析中段和末段组分的多个有效成分进行毒性强弱和毒性物质基础的比较。
雷公藤粗提物经柱层析除杂洗脱后收集中段和末段组分,本实验为了更好地反映中段和末段组分中有效成分和毒性成分的组成情况,运用HPLC同时测定有代表性的成分,它们从化学结构上归属于二萜类、生物碱类、三萜类。由中段和末段组分中所测成分的含量表明二萜类和生物碱类柱层析时富集在中段,三萜类在柱层析最后洗脱。
雷公藤柱层析中段和末段组分中很多成分既是有效成分,又是毒性成分。已知雷公藤的毒性成分主要是二萜类(雷公藤甲素等)、生物碱、三萜类及苷类化合物等。环氧二萜内酯是雷公藤研究最广泛的化学成分,其代表成分是雷公藤内酯醇(triptolide),又称雷公藤甲素,具有显著的抗炎及免疫抑制活性,但易产生肝、肾、生殖系统等毒性[5]。生物碱类主要损害肝、肾及中枢神经系统,并可破坏红细胞,引起进行性贫血,甚至诱发肾小管缺氧性损害,吸收后损伤中枢神经系统,可导致严重营养不良性改变。在雷公藤制剂中,对生物碱的量进行质量控制,有助于提高制剂的有效性和安全性[6]。
我们采用经典的小鼠急性毒性实验对雷公藤柱层析中段和末段组分的毒性作用进行比较,结合所测成分的含量,进行毒性评价。各段组分的小鼠经口LD50值表明中段的毒性明显强于末段,同中段组分里雷公藤甲素、雷公藤内酯酮、雷公藤吉碱、雷公藤次碱的含量高相关,这些二萜和生物碱类成分决定了中段的毒性强、安全范围小。对死亡小鼠解剖和病理切片推测雷公藤柱层析中段和末段组分致小鼠急性毒性死亡原因跟灌胃剂量、毒性成分密切相关,病理方面主要以急性肝损伤为主。
雷公藤肝毒性的基础研究较多,对雷公藤肝毒性机制的了解尚不透彻[7]。马致洁等[8]通过体外人肝L02细胞培养发现雷公藤对肝细胞的损伤呈剂量依赖性,为开展中药配伍减毒增效提供新方法。这些基础研究为雷公藤临床合理用药提供了参考,从临床表现看雷公藤导致的肝毒性多为急性,大鼠的急性肝损伤实验结果显示中段组分高剂量组、末段组分高剂量组、中段组分低剂量组大鼠血清中AST和ALT活性、细胞凋亡率与正常对照组比较,差异均有统计学意义(P<0.01),HE切片显示给药组有不同程度的水肿和脂肪变性,表明雷公藤柱层析中段和末段组分能不同程度地造成急性肝损伤,引起肝细胞凋亡,说明毒性作用是多种毒性成分共同作用的结果,成分和含量的差异与毒性的强弱有关联,毒性成分一定浓度范围内(中段组分高剂量至中段组分低剂量,这段浓度范围内观测指标和毒性有明显差异)存在较好的含量-毒性关系,毒性机制需要进一步去研究。
