A型肉毒素治疗银屑病一例并文献复习
2019-04-04马坚池郑博文田翠翠谭国珍
郑 林 马坚池 郑博文 田翠翠 谭国珍
银屑病是一种由多基因遗传决定的免疫异常性炎症性皮肤病,部分患者可伴有关节或其它器官受累[1]。银屑病皮损的发生是皮肤常驻细胞固有免疫和适应性免疫失调共同作用的结果[1]。越来越多的研究支持神经与角质细胞或免疫细胞相互作用,促进银屑病皮损的发生。肉毒素是由肉毒杆菌产生的,最广为人知的作用是能抑制神经末梢乙酰胆碱的分泌从而引起肌肉迟缓性麻痹[2]。此外,肉毒素能显著抑制神经分泌P物质(SP)、降钙素基因相关肽(cGRP)等神经肽而减轻神经性炎症[3]。肉毒素根据毒素抗原性的不同分为A-G型,用于医疗注射的有A型和B型,主要为A型[4,5]。肉毒素除了在医疗美容中广泛应用,单用或者联合点阵激光用于面部除皱效果均较显著[6-8]。近年来,逐渐有报道将其运用于银屑病、海利病、线状IgA大疱病、毛囊角化症、带状疱疹后遗神经痛、多汗症[9,10]等疾病的治疗[2,9,10]。本文分析了1例用A型肉毒素治疗银屑病的临床资料,并进行相关文献复习。
1 临床资料
患者,男,61岁。因“反复全身红色斑块、鳞屑27年”就诊。患者于27年前开始全身出现红色斑块、鳞屑,在广州市皮肤防治所行病理活检,诊断为“斑块型银屑病”,间断治疗(具体方案不详)。近2年以“环孢素、美能、雷公藤”及外用药物治疗,但皮疹顽固不退(稳定期),伴明显瘙痒。3个月前无明显诱因出现左上肢麻木,1日之内扩张至左下肢,而身体其他部位未出现明显麻木感。于我院神经内科就诊,诊断为“脑卒中”,予“脑栓通、华佗再造丸”等治疗,但左侧肢体麻木感逐渐加重。2个月前患者发现伴有麻木感的左侧肢体皮损完全消退,而右侧肢体、躯干皮疹较“脑卒中”前无改善。患者有 “高血糖” 病史9年,控制可。“高血脂”病史7年,定期监测血脂。皮肤科查体:右侧大腿(图1)、小腿(图2)、右侧肘部伸侧(图3)、背部(图4)、臀部(图4)见红色斑块、鳞屑,蜡滴现象、薄膜现象、Auspitz征阳性。左侧肘部伸侧(图5)、左侧大腿(图6)、小腿(图7)见暗褐色色素沉着斑。神经内科查体:伸舌、鼓腮、露齿正常,双侧肢体肌力正常,左侧肢体痛觉、温度觉减退,右侧肢体身体其他部位感觉正常。
治疗:患者签署知情同意书。在维持原治疗方案不变的情况下,即口服环孢素75 mg日2次、复方甘草酸苷片2片日3次、雷公藤2片日3次,外用润肤膏(成分:尿素、水貂油、黄体酮等),选取右小腿外侧皮损(图2)为治疗靶皮损,使用衡力®(注射用A型肉毒素)治疗,臀部皮损(图4)为对照靶皮损。首先对右小腿及臀部两处靶皮损进行评分,参考PASI(psoriasis area and severity index)评分法(红斑0~4分,鳞屑0~4分,浸润0~4分,范围0~12分)。右小腿皮疹评分:红斑:3分;鳞屑:1分;浸润,3分;共7分。臀部皮疹评分:红斑:2分;鳞屑2分;浸润2分,共6分。治疗时,患者取仰卧位,常规消毒右小腿皮肤。环绕皮疹,旁开边缘1 cm,间隔1 cm取注射点(图8),共50个点,每个点注射2单位(U)衡力®至皮内,共100 U。A型肉毒素用于银屑病的治疗虽然是适应症以外,但因非试验性研究,不需要机构审查委员会(IRB)的同意。治疗过程患者无不适。治疗结束后嘱患者保持注射部位干燥清洁,避免按压。治疗后若无特殊不良反应或皮疹加重,则在注射后第1个月回访、第3个月电话随访。1个月后回访时皮疹评分并再次拍照记录,了解不良反应。该患者在注射过程及随访期间未出现皮肤或肌肉相关不良反应。
疗效:患者自觉右侧小腿皮损在注射A型肉毒素2周后开始变薄,瘙痒较前减轻,并逐渐好转,1个月后回访时右小腿皮疹较前明显好转(图9),评分1分;臀部对照皮损评分5分(图10)。3个月后电话随访,自诉右侧小腿皮疹完全消退,背部皮损较前无明显变化。
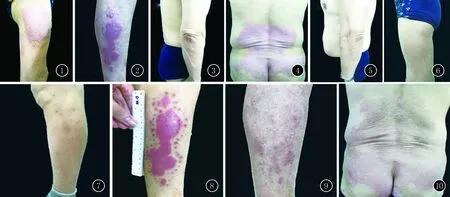
图1 右侧大腿外侧斑块、鳞屑图2 右侧小腿外侧斑块、鳞屑图3 右侧肘部伸侧丘疹、鳞屑图4 下背部、臀部红色斑块、鳞屑图5 左侧肘部伸侧色素沉着斑图6 左侧大腿外侧色素沉着斑图7 左侧小腿外侧色素沉着斑图8 右小腿皮疹注射衡力®前注射点标记图9 注射A型肉毒素1个月后回访,右小腿皮疹明显消退图10 注射A型肉毒素1个月后回访,下背部、臀部皮疹,面积增大,鳞屑减少
2 讨论
银屑病发病机制主要由免疫失调所介导,该观点已为学界所共识。具体的机制概括为3点:(1)由浆细胞样树突细胞介导的固有免疫和由T细胞介导的适应性免疫通过TNF-ɑ、IL-23、IFN-ɑ 等细胞因子相互作用促进银屑病皮炎的发生。(2)髓细胞分泌的IL-23促进T细胞向TH17细胞分化,TH17细胞能分泌IL-17A、IL-22、和IL-17F,从而促进角质细胞增殖和炎症。(3)角质细胞分泌的细胞因子、趋化因子和抗菌肽能趋化炎症细胞,从而形成正反馈[1]。越来越多的研究发现,感觉神经也参与银屑病皮损的发生。主要有以下4方面的证据:①临床上发现银屑病患者在感觉神经功能受损后,皮损好转甚至完全消退,并且皮疹随感觉神经功能恢复而复发[11,12]。本文所报道的患者因“脑卒中”导致左侧肢体麻痹,1个月后该侧皮疹完全消退。该病例有力地佐证了感觉神经在银屑病皮疹发生中的作用。在国内已发表的文献中,本文首次报道了感觉神经受损引起银屑病皮损消退的病例。②动物实验发现,银屑病小鼠皮肤去神经后,皮损处棘层肥厚程度以及CD4+T细胞、CD11c+细胞浸润程度明显减轻。该作用依赖于感觉神经末梢分泌的SP和cGRP[13]。③多个研究发现,银屑病患者皮损处感觉神经末梢分泌的神经肽增加。这些神经肽包括SP、cGRP、血管活性肠肽(VIP)、神经生长因子(NGF)、蛋白基因产物9.5(PGP9.5),在银屑病中发挥促进角质细胞增殖、炎症因子释放、神经生长、血管舒张并介导瘙痒和疼痛等作用[14]。④Blanco等[15]发现感觉神经与真皮树突细胞相互作用,促进IL-23/IL-17轴和下游炎症反应的发生,为神经和免疫相互作用在银屑病发病中的作用提供更直接的证据。
基于上述理论,抑制感觉神经与免疫相互作用的药物尝试用于银屑病的治疗。主要有以下2种药物:①CT327:CT327由Creabilis公司研发,是一种以NGF的受体-酪氨酸蛋白激酶A(TrkA)为靶点的选择性激酶抑制剂。NGF在银屑病的皮损部位及非皮损部位表达均升高[16],NGF-TrkA通路介导瘙痒、炎症并促进角质细胞增殖[17,18],因此CT327具有止痒和抑炎等作用。1项IIb期临床试验显示,CT327治疗伴有中重度瘙痒的银屑病患者,能显著减轻瘙痒和mPASI(modified psoriasis area and severity index)评分[19]。②A型肉毒素:Ward NL团队发现,A型肉毒素皮内注射到KC-Tie2银屑病小鼠的皮损,通过抑制神经末梢分泌SP、cGRP,能显著改善皮损的棘层肥厚和淋巴细胞浸润情况[20]。之后该团队为1例银屑病患者臀部的顽固性斑块注射A型肉毒素,3周后皮损完全消退并维持了7个月[21](表1)。Zanchi和Saber报道了A型肉毒素治疗反转型银屑病取得良好的效果[22,23](表1)。A型肉毒素治疗银屑病的另一个作用为改善瘙痒[23,24]。目前共有4篇文献报道使用A型肉毒素治疗27例银屑病患者,其中3篇报道中患者皮损明显消退[21-23];而唯一一项探索性临床试验(ClinicalTrials.gov, ID: NCT02577185)发现A型肉毒素组与对照组相比病情无明显改善,研究者认为单剂量疗法不足以控制银屑病皮损[25]。Bagherani等[26]对该试验进行评价,认为仍应该把肉毒素作为斑块型银屑病的潜在治疗手段。见表1。

表1 A型肉毒素治疗银屑病患者临床资料
注:U=Unit.
这4个报道为A型肉毒素在斑块型及反转型银屑病患者的治疗提供了一定的临床依据。类似地,本文报道的病例,患者在“脑卒中”后左侧肢体麻痹且持续不缓解,麻痹部位原有的银屑病皮疹逐渐好转直至完全消退。笔者考虑感觉神经在该患者的银屑病皮疹发生中作用显著,因此尝试使用A型肉毒素进行治疗,选取右小腿斑块为治疗靶皮损。在治疗2周后患者自觉皮损开始消退且瘙痒减轻,1个月后皮损明显好转(图8)。总体看来,A型肉毒素能较好地改善银屑病病情。A型肉毒素在医学美容中的常用剂量为数十单位到200单位不等,致死剂量为3000U以上,最常见的不良反应为注射部位不适、淤伤和短暂性头痛[27]。A型肉毒素治疗银屑病的剂量尚无依据,可参考其在医美中的应用。为了规范使用肉毒素治疗银屑病,需要更多的随机对照试验(RCT)提供临床证据,并且需要更多的基础研究提供理论依据,包括进一步探究肉毒素治疗前后皮疹处感觉神经末梢数量、神经肽表达及神经功能的变化。综合A型肉毒素治疗银屑病的有效性和安全性,笔者认为A型肉毒素可作为顽固性斑块型银屑及反转型银屑病患者的选择。
