噻托溴铵对OSAS患者血糖代谢的影响
2019-04-03解宝泉刘聪辉王红阳张静华
解宝泉,刘聪辉,王红阳,张静华
0 引言
阻塞性睡眠呼吸暂停综合征(OSAS)指睡眠时频繁出现上气道阻塞,导致呼吸暂停以及低通气呼吸,伴有打鼾、睡眠结构紊乱,导致机体长时间处于乏氧状态,造成全身各组织器官缺氧以及功能衰退,严重危害患者的健康[1]。据统计,我国至少有5 200万名OSAS患者[2],OSAS具有发病率高、并发症多的特点,正逐渐引起医学界的广泛关注[3]。OSAS往往会导致糖尿病的高发病率,甚至出现糖尿病相关并发症,从而加重肺功能下降,导致患者预后较差以及总生存期减少。本研究探讨OSAS患者血糖水平以及治疗药物的选择,以期能为临床治疗提供参考价值。
1 资料与方法
1.1 研究对象 选取2016年6月至2017年6月于华北理工大学附属医院呼吸内科住院的中重度OSAS患者60例为观察组,其中男33例,女27例,平均年龄(61.3±7.1)岁;选择同期门诊正常健康体检者50例为对照组,其中男26例,女24例,平均年龄(60.6±3.3)岁。
1.2 入组标准 ①《阻塞性睡眠呼吸暂停综合征的诊断及治疗》[4]中关于OSAS的诊断标准,且经呼吸暂停低通气指数(Apnea-hypopnea index,AHI)评估为中重度组;③意识清醒;④未接受呼吸机辅助通气治疗者。
1.3 排除标准 ①确诊为糖尿病以及其他内分泌系统疾病;②长期酗酒;③心脑血管疾病;④全身各系统感染;⑤严重的肝肾疾病。
1.4 研究方法 所有入组对象均行早晨空腹血糖和口服糖耐量-胰岛素释放试验(OGTT-IRT)检测,然后根据OGTT-IRT稳态模型计算胰岛素抵抗指数(HOMA-IR)。观察组同时给予噻托溴铵粉吸入剂(规格:18 μg),1次/d,早晨吸入,吸入治疗1个月后再次检测血糖各项指标,并与正常组进行比较。

2 结果
2.1 两组患者一般资料比较 两组患者一般临床资料如性别、年龄、体重指数比较差异均无统计学意义(P>0.05)。见表1。

表1 两组患者一般资料比较(例)
2.2 两组患者治疗前后FPG和HOMA-IR比较 治疗前,两组患者FPG、HOMA-IR比较差异有统计学意义(P<0.05);治疗1个月后,两组患者FPG、HOMA-IR比较差异无统计学意义(P>0.05)。见表2。
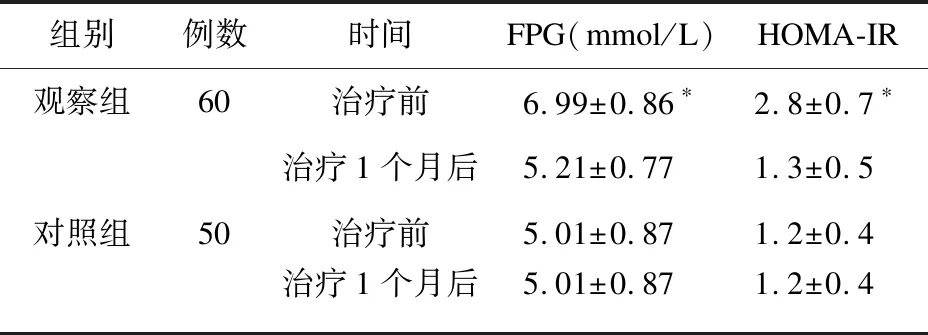
表2 两组患者治疗前后FPG和HOMA-IR比较
注:与对照组比较,*P<0.05
3 讨论
OSAS的发病机制与上气道阻塞频繁发生、氧化应激以及炎症反应增加、自主神经调节紊乱、机体免疫功能失调、睡眠呼吸模式变换等多因素有关,临床常用的治疗方法有呼吸机、药物治疗、手术解除阻塞等。由于呼吸机治疗舒适度及费用问题使得患者不能持续坚持,手术认可度不高,导致其致死率逐年增高,患者发生睡眠过程中猝死风险极高。分析原因可能与严重低氧血症有关,由于其可导致机体内分泌功能严重紊乱,使儿茶酚胺、肾素-血管紧张素及内皮素等物质分泌大量增加,危及患者生命。同时,因患者机体的交感神经兴奋性增高,引发间歇性缺氧,而缺氧后可反馈增强交感神经活性,同时激发下丘脑-垂体-肾上腺功能出现异常,进一步使糖代谢水平发生紊乱[5]。研究发现,OSAS可引起体内瘦素、脂联素、脂肪细胞型脂肪酸结合蛋白等多种细胞因子发生变化,而这些细胞因子均已被证实与胰岛素抵抗明显相关[6],造成OSAS患者血糖进一步波动[7]。在疾病发展过程中,由于重复间歇性低氧反复发生,促使活性氧不断产生,系统性炎症反应不断得到激活,最终侵害血管内皮细胞的结构和功能,致使OSAS患者出现代谢综合征[8-9]。本研究显示,OSAS患者空腹血糖及胰岛素抵抗指数较正常对照组明显升高,与大多数研究结果一致,提示需及早评估OSAS患者的血糖代谢情况,避免糖代谢紊乱,出现糖代谢并发症,造成血管内皮功能障碍,导致患者肺功能下降,进一步加重OSAS的病情,甚至发生呼吸衰竭。
噻托溴铵是一种新的长效季铵类抗胆碱能药物,研究表明,噻托溴铵不仅有强力支气管舒张功能,而且在抑制气道结构重塑、抵抗炎症反应、清除气道等方面具有显著效果[10-12]。OSAS患者由于长期乏氧负荷,使炎症介质释放增加。同时,研究发现,由迷走神经及其递质Ach所组成的胆碱能抗炎通路可显著调控炎症反应,迷走神经可以间接调控先天性免疫反应的过程。氧化应激是指体内氧化与抗氧化两种作用失衡,其氧化作用占主导地位,使中性粒细胞炎性浸润以及蛋白酶分泌增加,导致氧化中间产物大量产生[13],进一步启动氧化机制,直接或间接损伤DNA、蛋白质和脂类[14]。研究表明,受体或为抗炎治疗的作用靶点[15]。噻托溴铵是否存在其他抗炎机制,还需要大样本量的研究。
综上所述,噻托溴铵粉吸入剂可抑制副交感神经张力,减轻气道趋化及炎症反应,使患者高血糖代谢水平明显降低,为患者的药物治疗提供了新的思路及方法。
