Mg-2.4Nd-0.5Sr-0.3Zr生物镁合金表面耐蚀抑菌层的制备与表征
2019-03-20毛雨旭宋述鹏周和荣熊少聪
毛雨旭,宋述鹏,许 娜,周和荣,吴 润,熊少聪
(1. 武汉科技大学省部共建耐火材料与冶金国家重点实验室,湖北 武汉,430081;2. 武汉科技大学材料与冶金学院,湖北 武汉,430081;3. 武汉科技大学生命科学与健康学院,湖北 武汉,430065)
近年来,生物镁合金由于优异的机械性能与生物相容性,逐渐成为生物材料领域内的研究热点。生物镁合金具有较高的比强度和比刚度,其密度与人体密质骨的密度相似,特别是其弹性模量与人骨接近,能有效缓解骨科植入物的应力遮蔽效应[1]。另一方面,镁在人体的体液中可完全降解,是人体新陈代谢的必需元素,对骨骼生长具有促进作用[2]。然而,镁合金过快的腐蚀速率极大地制约了其在可降解生物材料领域的应用,并且由植入物引起的细菌感染也是亟需解决的问题。通常情况下,对材料进行表面改性能起到降低腐蚀速率的作用,其中水热法作为一种常见的表面改性手段,具有工艺简单、处理温度低、反应条件灵活可控等优点[3]。有研究表明,银作为抗菌材料使用时,具有广泛的抗菌活性及对细胞的低毒性[4]。因此,采用水热法制备含银表面耐蚀层来对镁合金表面进行改性,可以同时达到提高其耐蚀性和抗菌性能的目的。
针对生物镁合金的表面改性,近年来研究人员在处理工艺等方面取得了较大的进展。Feng等[5]采用原位水热法在AZ31镁合金表面沉积Mg(OH)2薄膜,并研究了pH值和水热时间对Mg(OH)2薄膜形貌和耐蚀性的影响,结果表明,在pH为10条件下反应3 h时所制Mg(OH)2薄膜的耐蚀性最佳。Bakhsheshi等[6]通过物理气相沉积法在Mg-2Ca-0.5Mn-6Zn合金表面制备了纳米结构的Ag掺杂ZnO涂层,结果显示,该涂层对大肠杆菌和金色葡萄球菌有着显著的抗菌作用。Hu等[7]通过化学转化法在Mg-2Zn-1Mn-0.5Ca合金上制备了Ag和羟基磷灰石复合涂层,该涂层显著提高了合金在Hank溶液中的生物耐蚀性,同时也具有良好的抗菌性能。
在生物镁合金的制备方面,本课题组前期针对不同成分的Mg-2.4Nd-xSr-yZr(x=0.1~1.1,y=0.1~0.5,质量百分数)系列合金进行了制备与性能表征,结果表明,Mg-2.4Nd-0.5Sr-0.3Zr合金的力学性能、电化学性能等综合表现最佳。基于此,本研究以该合金作为基底,以AgNO3溶液作为水热介质,通过水热法在合金表面制备了耐蚀-抑菌保护膜,考察了水热温度和时间对所制膜层表面形貌、物相组成、耐蚀行为及抗菌性能的影响。
1 试验材料及方法
本试验以Mg-2.4Nd-0.5Sr-0.3Zr镁基合金为基材(质量分数,%)。线切割得到尺寸为10 mm×10 mm×2 mm的样片,用不同型号的SiC砂纸逐级打磨样片表面(至2000#)并机械抛光后,用无水乙醇超声清洗5 min,干燥后备用。
水热试验在以聚四氟乙烯为内衬的不锈钢高压釜中进行。首先,将0.01 mol/L的AgNO3溶液倒入容量为20 mL的反应釜中,填充度为75%;随后将样片放置于反应釜中,通过恒温干燥箱加热至反应温度并保持一段时间后,取出试样冷却至室温,用无水乙醇清洗干净并吹干后,放置于干燥箱中备用。本实验采用的水热条件分别为:90 ℃×1.5 h、120 ℃×1.5 h、120 ℃×2.5 h、150 ℃×1.5 h。
采用X’Pert Pro MPD型X射线衍射仪(XRD)分析样品膜层的物相组成,衍射源为Cu靶Kα线,扫描范围2θ为10°~90°,扫描速率为2°/min。通过配备有能谱仪(EDS)的Nano Nova-400型场发射扫描电镜(SEM)对样品的表面形貌及微区成分进行表征,并根据SEM照片测量膜层的厚度。
电化学测试在Auto Lab PGSTAT204型电化学工作站上进行。采用三电极体系,工作电极为样品,辅助电极为Pt电极,参比电极为饱和甘汞电极(SCE),腐蚀介质为仿生溶液(SBF),其化学组分列于表1中,测试环境温度为室温。动电位极化曲线测定在开路电位测试1 h后进行,电位VOCP的范围为-250~+250 mV,扫描速率为1 mV/s。电化学阻抗谱(EIS)测试频率范围为105~107Hz,测试点数为71,交流电压幅值为10 mV。

表1 SBF溶液的化学组分(单位:g/L)
采用抑菌圈法测试样品的抗菌性能。菌种为金色葡萄球菌,具体步骤为:先将1 g蛋白胨、0.5 g酵母提取物、1 g NaCl、1.5 g琼脂粉﹑0.24 g MgSO4溶于100 mL蒸馏水中,制备LB固体培养基;然后将菌种通过LB液稀释至1×109CFU/mL,均匀涂布于平板表面;最后,将样品放置在固体培养基上,在37 ℃恒温箱中有氧培养24 h,用数码相机拍照并测量抑菌圈的直径。
2 结果与分析
2.1 膜层的表征
图1为不同水热反应条件下制得镁合金样品的XRD图谱。由图1可知,所制样品的膜层均主要由Mg(OH)2和Ag构成,其中90 ℃×1.5 h条件下,基体Mg的衍射峰强度最强,Mg(OH)2衍射峰强度较弱,这可能是由于反应温度较低,样片表面未能生成完整的Mg(OH)2膜层。当水热条件为150 ℃×1.5 h时,样品中Mg(OH)2相的衍射峰强度相对较高,表明该条件下Mg基体水热反应更完全,生成的Mg(OH)2的结晶程度更高;另外,此条件下制得样品的XRD衍射图谱中未观察到Ag相的衍射峰,可能与Mg(OH)2膜层较厚且膜层中含Ag量较少有关,并且其它水热条件下制得样品中Ag相的衍射峰强度相比于其他相也较弱。
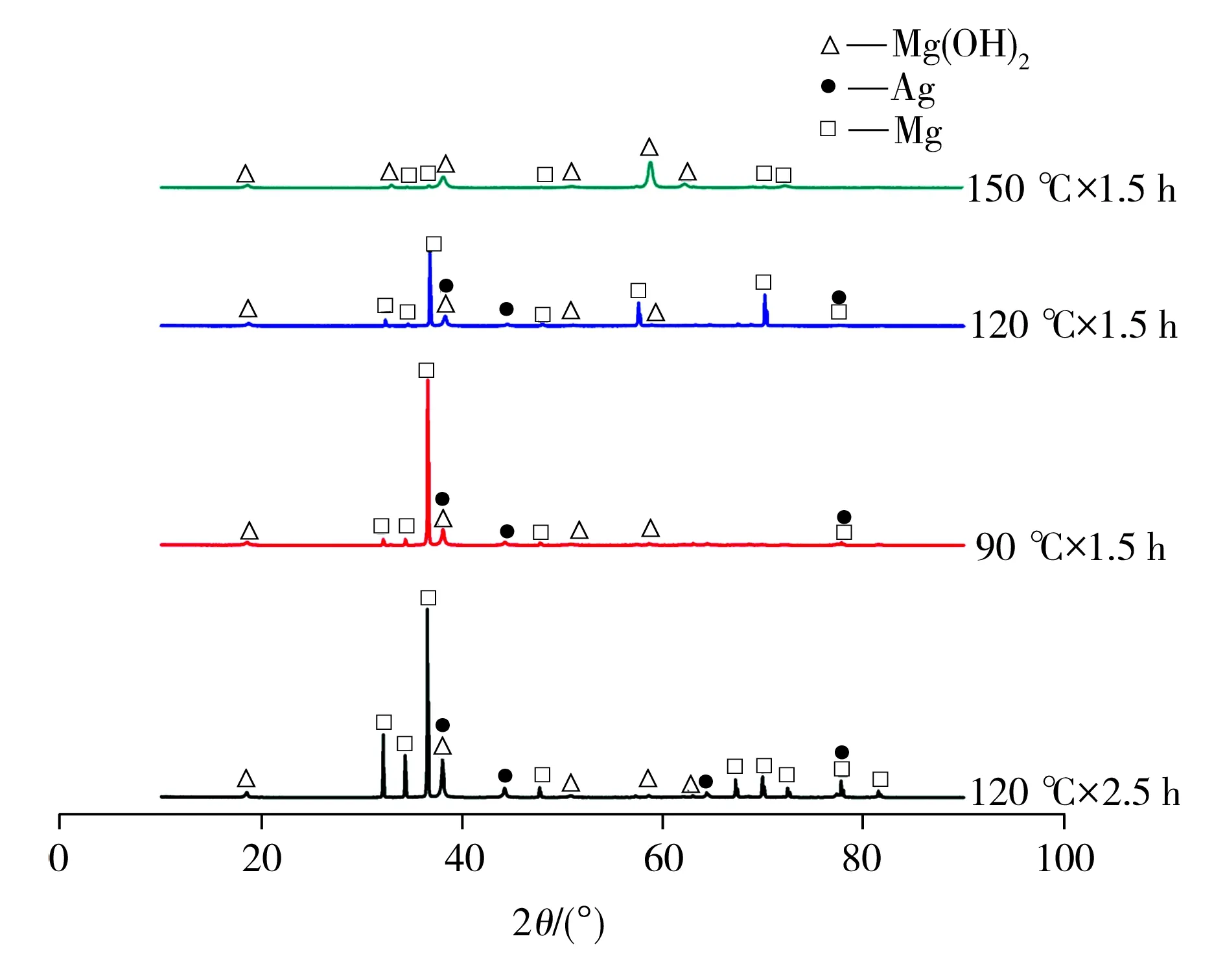
图1 试样的XRD图谱
图2为不同水热反应条件下制得镁合金样品的SEM照片。从图2中可以观察到,样品的膜层底部主要由层片状的物质组成,在其上方分布着聚集态的颗粒状物质,且膜层表面还存在由薄片组成的花状结构。随着水热温度的升高,样品表面膜层上的片状物质更为致密,颗粒状结构减少,其中当水热条件为150 ℃×1.5 h时,生成的纳米级层片状结构在基体表面形成了较好的保护膜层。
为进一步了解水热样品表面膜层的物相组成,对具有典型特征的120 ℃×2.5 h样品的膜层进行EDS分析,结果如图3所示。图3中EDS能谱分析结果显示,点A处纳米薄片中Mg、O元素的原子比约为1∶2,结合上述XRD分析可知,该区域主要是由片层状Mg(OH)2组成;点B处则主要是片层状Mg(OH)2和颗粒状Ag聚集形成的。

(a) 90 ℃×1.5 h (b) 120 ℃×1.5 h

(c) 120 ℃×2.5 h (d) 150 ℃×1.5 h
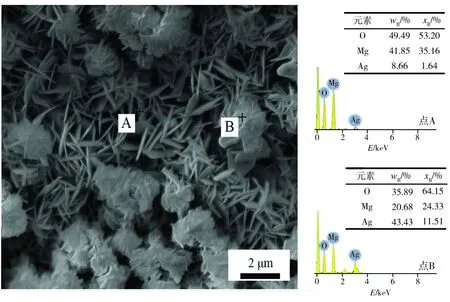
图3 120 ℃×2.5 h条件下所制样品的EDS图谱
图4为不同水热反应条件下制得镁合金样品截面的SEM照片及各元素在膜层附近的EDS线扫描分析结果,图中合金基体与深灰色环氧树脂所夹的中间层即为表面膜层。EDS线扫描结果显示,表面膜层主要元素为Mg、O,而C主要来自于环氧树脂。在90 ℃×1.5 h、120 ℃×1.5 h、120 ℃×2.5 h、150 ℃×1.5 h水热条件下,测得样品表面膜层的平均厚度依次为20、26、35、91 μm。可见,随着水热温度的提高及反应时间的延长,样品表面生成的膜层厚度逐渐增加。
Mg在AgNO3溶液中进行水热处理时,发生的化学反应可由下列方程式表示:

(1)

(2)

(3)

(4)

(5)

(a) 90 ℃×1.5 h (b) 120 ℃×1.5 h

(c) 120 ℃×2.5 h (d) 150 ℃×1.5 h
图4试样截面的SEM照片及EDS线扫描分析
Fig.4Cross-sectionalSEMimagesandEDSline-scanninganalysisofthesamples
在高压反应釜内进行水热反应时,H2O电离常数往往随着温度的升高及压力的增加而增大,故基体中的Mg与水电离生成的OH-反应加剧,在短时间内形成较厚的膜层[8]。水热处理开始阶段,基体与溶液界面处产生大量Ag和Mg(OH)2颗粒,聚集并覆盖在基体表面;随后,水通过颗粒间隙或孔隙,渗透进基底并与之反应,生成大量的Mg(OH)2晶体并聚集。通过不断重复以上过程,最终在Mg-2.4Nd-0.5Sr-0.3Zr镁合金基底表面形成了致密的膜层。此过程中,先前产生的Ag和Mg(OH)2颗粒一直聚集在膜层表面,这与图4所示在膜层内部未检测到Ag元素的结果相一致。
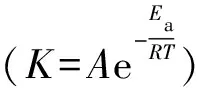
2.2 膜层的耐蚀性能分析
图5所示为镁合金基底及不同水热条件下制得样品在SBF溶液中的极化曲线,根据极化曲线拟合得到腐蚀电位Ecorr和腐蚀电流密度jcorr列于表2中。结合图5和表2可知,镁合金基底和水热试样的腐蚀电位Ecorr在-1.40~-1.53 V范围内变化,无明显的差异。一般而言,腐蚀电位越大意味着腐蚀倾向越小,但腐蚀电位与腐蚀速率并无直接关系,腐蚀速率主要由腐蚀电流密度决定[9]。与未处理的镁合金基底相比,具有膜层的Mg-2.4Nd-0.5Sr-0.3Zr合金腐蚀电流密度降低了至少约一个数量级,且下降程度随着膜层厚度的增加而增大。特别是当水热条件为150 ℃×1.5 h时,所制样品的膜层最厚且最为致密,对应的腐蚀电流密度最低,表明该水热条件下所制样品的耐蚀性最好。可见,表面Mg(OH)2膜层的形成能够有效提升Mg-2.4Nd-0.5Sr-0.3Zr镁合金的耐蚀性能。
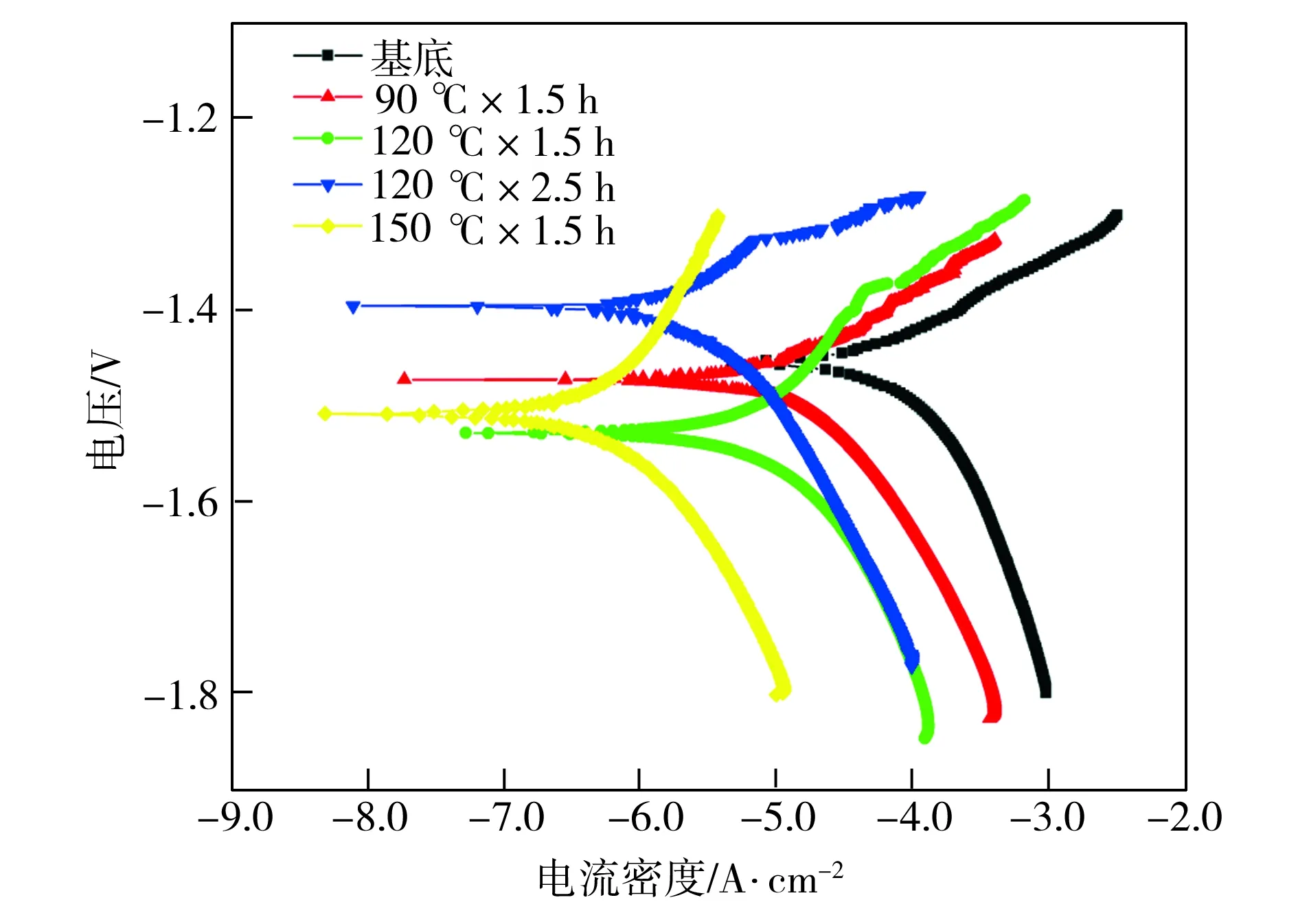
图5 试样在SBF溶液中的极化曲线
Fig.5PolarizationcurvesofthesamplestreatedinSBFsolution
表2试样的腐蚀电位和腐蚀电流密度
Table2Corrosionpotentialsandcorrosioncurrentdensitiesofthesamples

水热条件Ecorr/Vjcorr/A·cm-2未处理-1.4554.149×10-590 ℃×1.5 h-1.4738.055×10-6120 ℃×1.5 h-1.5283.807×10-6150 ℃×1.5 h-1.5094.702×10-7120 ℃×2.5 h-1.4011.878×10-6
图6所示为镁合金基底及不同水热条件下制得样品在SBF溶液中的电化学阻抗谱。从图6可以看出,水热处理后的试样在高频和中低频区存在有两个容抗弧,未处理的基底则由中高频的容抗弧和低频的感抗弧组成。中频容抗弧代表电荷传递电阻,一般反映腐蚀阻力的大小[10]。经过不同条件水热处理后,所制样品的容抗弧均大于镁合金基底的容抗弧,且随水热温度的升高,样品容抗弧越大。当水热条件为150 ℃×1.5 h时,制得样品的容抗弧最大,表明膜层对电荷传递阻力最大,极大降低了Mg-2.4Nd-0.5Sr-0.3Zr合金的腐蚀速率,这与图5所示样品的极化曲线测试结果一致。通常认为,高频区的容抗弧与试样/介质界面Cl-吸附有关[11],水热处理后还存在高频区的容抗弧表明,该膜层对Cl-有较好的吸附能力,可以减少溶液中Cl-含量,从而降低镁合金的腐蚀速率。此外,低频区域的数据点大多较为离散,这可能是由于低频区体系稳定性因发生了电位漂移而有所变化[12]。
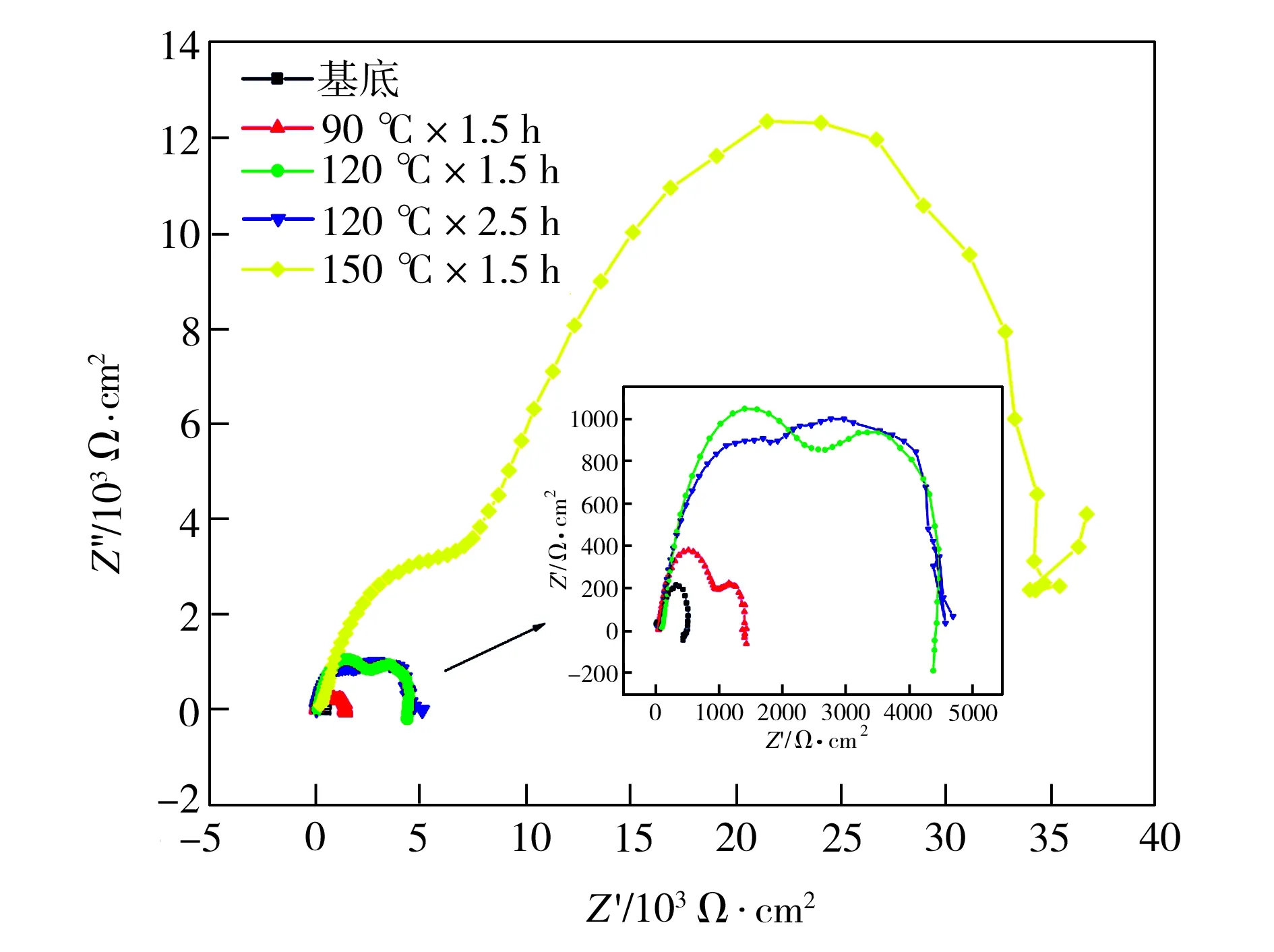
图6 试样在SBF溶液中的电化学阻抗谱
2.3 膜层抗菌性能分析
图7为镁合金基底及不同水热反应条件下制得的试样对金色葡萄球菌的抗菌效果照片。如图7所示,Mg-2.4Nd-0.5Sr-0.3Zr合金并未表现出抗菌性,而水热反应后的试样周围均出现了明显的抑菌圈。当水热条件为90 ℃×1.5 h、120 ℃×1.5 h、150 ℃×1.5 h、120 ℃×2.5 h时,制得样品的抑菌圈直径大小依次为22、23、13、22 mm,其中150 ℃×1.5 h条件下样品抑菌圈最小。结合图2所示的SEM照片可知,该样品表面颗粒状结构较少,对应于水热处理后样品表面Ag含量较少,并且Mg(OH)2膜层较厚减缓了Ag+的释放,而Ag+与金色葡萄球菌接触后会与细菌体内蛋白酶发生反应,使之丧失活性,同时也会破坏微生物的呼吸系统、电子运输系统和物质传输系统,导致细菌死亡[13]。综合上述分析可知,所制Mg-2.4Nd-0.5Sr-0.3Zr镁合金表面含Ag的Mg(OH)2膜层对金色葡萄球菌有明显的抗菌作用,但膜层较厚(含Ag少)可能会影响所制样品的抗菌效果。

(a)裸基体 (b) 90 ℃×1.5 h (c) 120 ℃×1.5 h

(d) 150 ℃×1.5 h (e) 120 ℃×2.5 h
图7试样的抑菌圈照片
Fig.7Inhibitionzonephotosofthesamples
3 结论
(1) 于不同的水热温度和时间条件下,在AgNO3溶液介质中对Mg-2.4Nd-0.5Sr-0.3Zr合金进行水热处理后,合金表面形成了厚度为20~91 μm且具有抑菌功能的耐腐蚀膜层,膜层均匀致密,主要由层片状Mg(OH)2和颗粒状Ag/Mg(OH)2聚集而成的。
(2) 随着水热温度的升高及反应时间的延长,所制镁合金样品的膜层厚度逐渐增加,且样品的耐腐蚀性能也随着膜层厚度的增加而提高。当水热条件为150 ℃×1.5 h时,所制样品的膜层最厚,腐蚀电流密度最小(4.702×10-7A·cm-2),耐蚀性能达到最佳。
(3) 水热处理后的镁合金样品对金色葡萄球菌均具有明显的抗菌作用,这主要由膜层中Ag的抗菌能力所主导。
