培门冬酰胺酶治疗结外NK/T细胞淋巴瘤的效果和安全性
2019-03-18金莉李朝辉徐宁宋楠
金莉 李朝辉 徐宁 宋楠
[摘要]目的 探讨培门冬酰胺酶治疗结外NK/T细胞淋巴瘤的效果和安全性。方法 选取鞍山市肿瘤医院2014年1月~2017年12月收治的60例结外NK/T细胞淋巴瘤患者作为研究对象,以随机数字表法分为对照组及观察组,每组各30例。对照组采用吉西他滨、奥沙利铂、地塞米松与左旋门冬酰胺酶治疗,观察组采用吉西他滨、奥沙利铂、地塞米松与培门冬酰胺酶治疗,比较两组患者的近期疗效及药物毒副反应。结果 观察组的总有效率为93.33%,对照组的总有效率为90.00%,两组比较差异无统计学意义(P>0.05)。观察组的消化道反应、高血糖及变态反应发生率明显低于对照组(P<0.05)。两组患者的粒细胞减少、血小板减少、肝功能损害发生率比较,差异无统计学意义(P>0.05)。结论 培门冬酰胺酶治疗结外NK/T细胞淋巴瘤近期效果确切,毒副反应较小,安全性高,值得临床推广。
[关键词]培门冬酰胺酶;NK/T细胞淋巴瘤;近期效果;安全性
[中图分类号] R733.4 [文献标识码] A [文章编号] 1674-4721(2019)1(b)-0074-03
[Abstract] Objective To investigate the effect and safety of Pegaspargase in the treatment of extranodal NK/T cell lymphoma. Methods A total of 60 patients admitted from January 2014 to December 2017 in Anshan Tumor Hospital were selected as the research objects. Patients were divided into the control group and the observation group by the random table method, 30 cases in each group. The control group was treated with Gemcitabine, Oxaliplatin, Dexamethasone and L-asparaginase, while the observation group was treated with Gemcitabine, Oxaliplatin, Dexamethasone and Pegaspargase. The short-term curative efficacy and drug toxicity side effect were compared between the two groups. Results The total effective rate was 93.33% in the observation group and 90.00% in the control group, the difference was not statistically significant (P>0.05). The incidence of digestive tract reaction, hyperglycemia and allergic reaction in the observation group was significantly lower than that in the control group (P<0.05). There was no significant difference in the incidence of neutropenia, thrombocytopenia and hepatic dysfunction between the two groups (P>0.05). Conclusion Pegaspargase in the treatment of extranodal NK/T cell lymphoma is effective in the short term, with less side effect and high safety. It is worthy of clinical promotion.
[Key words] Pegaspargase; NK/T cell lymphoma; Short-term effect; Safety
结外NK/T细胞淋巴瘤(extranodal NK/T-cell lymphoma,ENKTL)是一种特殊病理类型的淋巴肿瘤[1-2]。ENKTL在亚洲和拉丁美洲较为常见,占中国所有恶性淋巴瘤的5%~10%,是一种高度侵袭性肿瘤,进展快且预后不良[3]。L-门冬酰胺酶具有独特的抗肿瘤机制,当L-门冬酰胺被L-门冬酰胺酶耗尽时,肿瘤细胞因不能合成L-门冬酰胺导致DNA和RNA合成障碍而受到抑制[4]。培门冬酰胺酶是一种与聚乙二醇共价连接的大肠杆菌L-门冬酰胺酶,对急性淋巴细胞白血病有效,且无明显毒副反应[5]。目前,临床对于培门冬酰胺酶治疗ENKTL报道较少,本研究旨在探讨ENKTL患者应用培门冬酰胺酶的临床效果,现报道如下。
1资料与方法
1.1一般资料
选择鞍山市肿瘤医院2014年1月~2017年12月收治的60例ENKTL患者作为研究对象,以随机数字表法分为对照组及觀察组,每组各30例。纳入标准:患者均经病理学检查及免疫组化分型诊断为ENKTL;无化疗禁忌;体力ECOG评估分值<2分。排除标准:合并严重脏器功能不全患者;肿瘤侵犯脑部患者;罹患精神疾病难以配合患者。对照组中,男16例,女14例;年龄25~67岁,平均(55.6±7.9)岁;病程11~46 d,平均(28.1±5.3)d;分期:Ⅰ~Ⅱ期14例,Ⅲ~Ⅳ期16例。观察组中,男15例,女15例;年龄24~66岁,平均(56.1±8.2)岁;病程13~46 d,平均(27.6±5.0)d;分期:Ⅰ~Ⅱ期16例,Ⅲ~Ⅳ期14例。两组患者的性别、年龄等一般资料比较,差异无统计学意义(P>0.05),具有可比性。本研究所有患者均签署知情同意书,由医院医学伦理委员会批准实施。
1.2治疗方法
对照组第1、8天静脉滴注吉西他滨(上海创诺制药有限公司,国药准字 H20113194)1000 mg/m2,第1天静脉滴注130 mg/m2奥沙利铂(南京制药厂有限公司,国药准字 H20000686);第1~7天静脉滴注地塞米松(上海北杰集团关东药业有限公司,国药准字 H220 22648)10 mg;第1~7天静脉滴注5000 U/m2左旋门冬酰胺酶(协和发酵麒麟制药有限公司,国药准字 J20100138)。 研究组第1、8天静脉滴注1000 mg/m2吉西他滨;第1天静脉滴注130 mg/m2奥沙利铂;第1~7天静脉滴注10 mg地塞米松;第1天静脉滴注培门冬酰胺酶2500 U/m2(江都恒瑞医药股份有限公司,国药准字 H20090015)代替左旋门冬酰胺酶。以3周为1个疗程,一般进行2~3个疗程。同时两组患者均接受适型调强放疗,疗程结束时进行疗效评价。
1.3观察指标及评价标准
采用国际淋巴瘤工作组制定的非霍奇金淋巴瘤治疗反应标准[6]进行疗效判定,具体如下。完全缓解(complete response,CR):肿瘤完全消失达1个月以上;不确定的完全缓解(complete remission unconfirmed,CRu):肿瘤未达到CR但是超过部分缓解(partial response,PR)的情况;PR:肿瘤两个淋巴结最大直径的乘积缩小≥50%,其他病灶无增大,并且维持1个月以上;稳定(stable disease,SD):肿瘤两个淋巴结最大直径的乘积缩小<50%,或大小无明显变化;进展(progressive disease,PD):肿瘤增大超过或有新的转移灶出现。总有效=CR+CRu+PR。毒副反应评价采用WHO抗肿瘤药物毒副反应分度标准[7],包括消化道反应、粒细胞减少、血小板减少、肝功能损害、高血糖、变态反应。
1.4统计学方法
采用SPSS 20.0统计软件对数据进行分析,计量资料以均数±标准差(x±s)表示,采用t检验,计数资料以百分率表示,采用χ2检验,以P<0.05为差异有统计学意义。
2结果
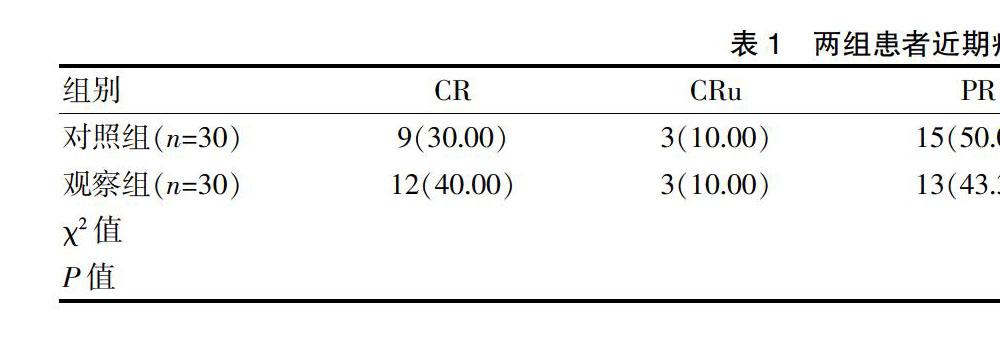
2.1两组患者近期疗效的比较
观察组的总有效率为93.33%,对照组的总有效率为90.00%,两组比较差异无统计学意义(P>0.05)(表1)。
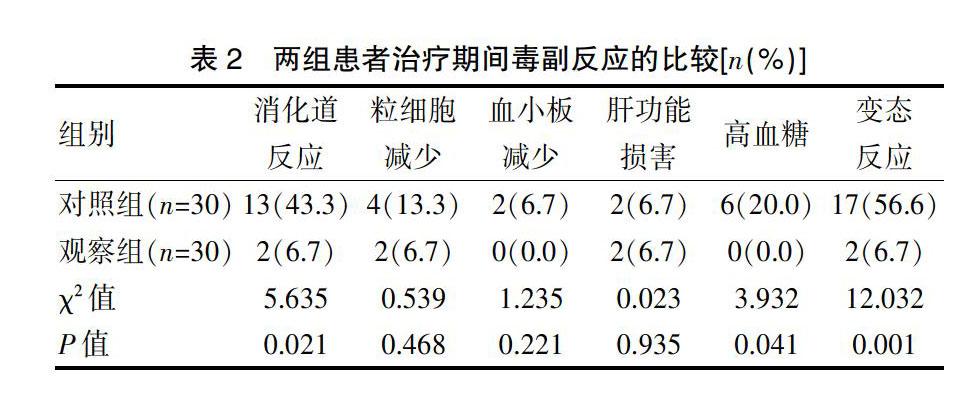
2.2 两组患者治疗期间毒副反应的比较
观察组的消化道反应、高血糖及变态反应发生率明显低于对照组,差异有统计学意义(P<0.05)。两组的粒细胞减少、血小板减少、肝功能损害发生率比较,差异无统计学意义(P>0.05)(表2)。
3讨论
ENTKL被认为是最严重的淋巴瘤之一,但是目前化疗效果欠佳,治疗失败的部分原因在于调控P-糖蛋白等的耐药相关基因的过度激活,导致药物外排[8]。L-门冬酰胺酶可消耗门冬酰胺蛋白质,抑制肿瘤细胞中的DNA和RNA合成,其抗肿瘤机制不受P-糖蛋白的影响,在急性淋巴细胞白血病和淋巴瘤中抗肿瘤效果确切。目前,L-门冬酰胺酶对ENTKL的疗效和安全性相关报道仍较少,而且,与高度免疫原性有关的严重毒性显著限制着L-门冬酰胺酶的通用性[9]。培门冬酰胺酶作为新一代的L-门冬酰胺酶,在急性白细胞白血病中疗效明确而且患者耐受性更佳[10]。在对ENKTL有限的病例报道和临床研究中,培门冬酰胺酶已经呈现出潜在的疗效,但是,这些证据对于确保在ENKTL中普及培门冬酰胺酶还远远不足。
在本研究中,培门冬酰胺酶呈现出较高的治疗有效率,观察组的总有效率达到93.33%,这一结果与其他几个研究相类似[11-12],再一次确定了培门冬酰胺酶治疗ENKTL的可行性。较L-门冬酰胺酶,培门冬酰胺酶显示出了较可接受的毒副反应,主要集中于粒细胞减少、血小板减少和肝功能损害,而消化道反应、高血糖、变态反应发生率则明显降低(P<0.05)。其中粒细胞减少和血小板减小可能是由骨髓抑制作用引起,而高血糖则被认为与L-门冬酰胺酶可诱发胰腺炎有关。另外,培门冬酰胺酶暂未发现变态反应等严重的可能致死的毒副反应。培门冬酰胺酶血浆半衰期约5.5 d,较L-门冬酰胺酶(大约20 h)大大延长,不需要皮试,临床使用较为方便[13]。
包含培门冬酰胺酶、吉西他滨的化学疗法在ENKTL治疗中显示出确切的效果,目前的研究对于门冬酰胺酶相关的疗效和安全性评价指标仍然较少,患者培门冬酰胺酶治疗的反应性被发现与血清骨髓相关蛋白-14(myeloid-related protein 14,MRP14)和血清类粘蛋白1(orosomucoid 1,ORM1)蛋白有关[2]。S100A9蛋白和ORM1蛋白在门冬酰胺酶、吉西他滨相关治疗方案不敏感的患者中常出现明显的升高。S100A9蛋白是衡量ENTKL恶性程度的重要指标[14],急性期蛋白ORM1则作为炎症因子在ENKTL患者血清中上调[15],目前这两种蛋白被认为对培门冬酰胺酶的疗效和毒副反应有一定的提示效果,是ENKTL预后的独立预测因子,但是其具体机制还不明确,其中ORM1蛋白升高所提示的炎症与ENKTL的关系更需进一步地探究。
综上所述,门冬酰胺酶治疗ENKTL近期效果確切,可有效缓解疾病进展,毒副反应小,消化道与变态反应发生率较低。想要对门冬酰胺酶的疗效和安全性进行更确切的评价,还需更侧重于寻找相关的分子标志物。
[参考文献]
[1]Reyes VE,Al-Saleem T,Robu VG,et al.Extra nodal NK/T-Cell lymphoma nasal type:efficacy of pegaspargase report of two patients from the united sates and review of literature[J].Leuk Res,2010,34(1):50-52.
[2]Zhou Z,Li Z,Sun Z,et al.S100A9 and ORM1 serve as predictors of therapeutic response and prognostic factors in advanced extranodal NK/T cell lymphoma patients treated with pegaspargase/gemcitabine[J].Sci Rep,2016,6(29):23-25.
[3]Tse E,Kwong YL.The diagnosis and management of NK/T-cell lymphomas[J].J Hematol Oncol,2017,4(14):85-88.
[4]Wang J,Wang L,Liu C,et al.Efficacy of combined gemcitabine,oxaliplatin and pegaspargase (P-gemox regimen) in patients with newly diagnosed advanced-stage or relapsed/refractory extranodal NK/T-cell lymphoma[J].Oncotarget,2016,7(20):29 092-29 101.
[5]Wang J,Wang H,Wang Y,et al.Analysis of the efficacy and safety of a combined gemcitabine,oxaliplatin and pegaspargase regimen for NK/T-cell lymphoma[J].Oncotarget,2016,7(23):35 412-35 422.
[6]Lahoud OB.High-dose chemotherapy and autologous stem cell transplant in older patients with lymphoma[J].Am J Hematol,2018,6(1):40-46.
[7]Sun Y,Narayan VA,Wittenberg GM.Side effect profile similarities shared between antidepressants and immune-modulators reveal potential novel targets for treating major depressive disorders[J].BMC Pharmacol Toxicol,2016,10(21):47-49.
[8]Zhang L,Jia S,Ma Y,et al.Efficacy and safety of cisplatin,dexamethasone,gemcitabine and pegaspargase (DDGP) regimen in newly diagnosed,advanced-stage extranodal natural killer/T-cell lymphoma:interim analysis of a phase 4 study NCT01501149[J].Oncotarget,2016,7(34):55 721-55 731.
[9]Zhang L,Li S,Jia S,et al.The DDGP (cisplatin,dexamethasone,gemcitabine,and pegaspargase) regimen for treatment of extranodal natural killer (NK)/T-cell lymphoma,nasal type[J].Oncotarget,2016,7(36):58 396-58 404.
[10]Xu PP,Xiong J,Cheng S,et al.A phase Ⅱ study of Methotrexate,Etoposide,Dexamethasone and Pegaspargase sandwiched with radiotherapy in the treatment of newly diagnosed,stage ⅠE to ⅡE extranodal natural-killer/T-cell lymphoma,nasal-type[J].EBioMedicine,2017,25(1):41-49.
[11]Chang Y,Fu X,Sun Z,et al.Utility of baseline,interim and end-of-treatment (18)F-FDG PET/CT in extranodal natural killer/T-cell lymphoma patients treated with L-asparaginase/pegaspargase[J].Sci Rep,2017,7(24):41 057-41 059.
[12]Liang J,Wang L,Peter Gale R,et al.Efficacy of pegaspargase,etoposide,methotrexate and dexamethasone in newly diag-nosed advanced-stage extra-nodal natural killer/T-cell lymphoma with the analysis of the prognosis of whole blood EBV-DNA[J].Blood Cancer J,2017,7(9):60-63.
[13]Bu S,Yuan F,Wei X,et al.L-asparaginase-based regimen as a first-line treatment for newly diagnosed nasal type extranodal natural killer cell/T-cell lymphoma[J].Exp Ther Med,2016,11(6):2437-2445.
[14]Kallberg E,Vogl T,Liberg D,et al.S100A9 interaction with TLR4 promotes tumor growth[J].PLoS One,2012,7(3):34 207-34 208.
[15]Gery S,Gombart AF,Yi WS,et al.Transcription profiling of C/EBP targets identifies Per2 as a gene implicated in myeloid leukemia[J].Blood,2005,106(8):2827-2836.
(收稿日期:2018-03-19 本文編辑:祁海文)
