金属有机框架及其衍生金属氧化物在锂和钠离子电池中的应用*
2019-03-14朱孔军刘鹏程刘劲松
徐 远 ,朱孔军 ,刘鹏程 ,王 婧 ,严 康 ,刘劲松
(1.南京航空航天大学,机械结构力学及控制国家重点实验室,南京 210016;2.南京航空航天大学,材料科学与技术学院,南京 210016;3.广州大学,机械与电气工程学院,广州 510006)
0 引 言
0.1 锂和钠离子电池的发展现状
随着煤、石油、天然气等传统化石能源的消耗,以清洁可再生新能源为基础的新型能源结构将成为今后世界经济和能源中最具影响的技术领域之一。但以太阳能和风能为代表的清洁能源在输出上不稳定,从而对要求高稳定性的电网产生了极大的影响。电化学储能提供了一个很好的解决方案:先将不稳定的清洁能源所产生的电能储存在储能设备中,再由储能设备以稳定的方式进行电能输出、并入。因此发展先进的电化学储能技术十分重要。
0.1.1 锂离子电池(Lithium ion battery,LIBs)发展现状
在众多储能技术中,锂离子电池因环境友好、能量密度高、无记忆效应、循环寿命长等优点受到广泛关注。其主要由电解液、隔膜、正极和负极材料组成,工作原理为:充电时,Li+从正极脱嵌,经过电解质嵌入负极,电流从外电路由负极流向正极;放电时则正好相反[1]。20世纪90年代初,日本索尼公司首次推出了以钴酸锂为正极、石墨为负极的商用锂离子电池[2]。近几十年来,商用锂离子电池的发展面临着一系列技术瓶颈,如锂离子电池内阻高,随容量变化时工作电压不稳定,成本高,存在安全隐患,能量密度无法满足实际使用需求等[3]。其中正负极活性材料对锂和钠离子电池的影响最大,决定了电池的使用性能,因此研究开发具有高能量密度、成本低廉的锂和钠离子电池电极材料具有十分重要的意义,能更有效解决能源和环境问题。 0.1.2 钠离子电池(Sodium ion battery,NIBs)发展现状
锂在地壳中的储量仅为0.006%,资源十分短缺,限制了锂离子电池在大型大功率储能设备中的进一步发展,因此,探索新的能量体系来代替锂离子电池体系很有必要[4]。钠与锂在元素周期表中是同一 主族,具有相似的物理和化学性质。钠的储备资源非常丰富,约占地壳元素储量的2.64%,分布广泛、提取简单,因此钠离子电池更适合替代锂离子电池在智能电网等大规模和长期储能上的应用[5]。虽然钠离子电池的应用已经有了许多研究进展,但仍然面临着一些亟需解决的问题,其中主要是钠离子半径大(0.102 nm),可供钠离子电池实现快速充放电的电极材料种类十分有限[4]。因此,对高性能钠离子电池电极材料的探索和开发必不可少。
0.2 金属有机框架
金属有机框架(metal-organic frameworks,MOFs)由YAGHI和LI在20世纪90年代末首次提出[6],主要由金属离子和有机连接物组成,金属离子可以是过渡金属、碱土金属或镧系元素的离子,有机连接物通常是带有N或多齿原子(吡啶基、多胺、羧酸盐等)的多齿分子。MOFs因为其轻质(~0.13 g/cm3)、高比表面积(10 000 m2/g)、结构和组成多样的特点而受到广泛关注,在气体存储或分离、催化、药物输送和成像等领域有着广泛的应用前景[7]。越来越多的研究显示MOFs材料具有的复杂体系结构和独特化学成分可用于电化学储能和转换,实现在二次电池、超级电容器和燃料电池等领域的应用[8-10],而可控合成的MOFs及其衍生纳米材料为研究和调整其应用提供了可能,图1和表1总结了各种制备MOFs及其衍生纳米材料的方法和特点。

图1 MOFs前驱体及其衍生纳米材料的合成策略综述[8]Fig.1 An overview of the synthetic strategies of MOF-based derived nanomaterials[8]
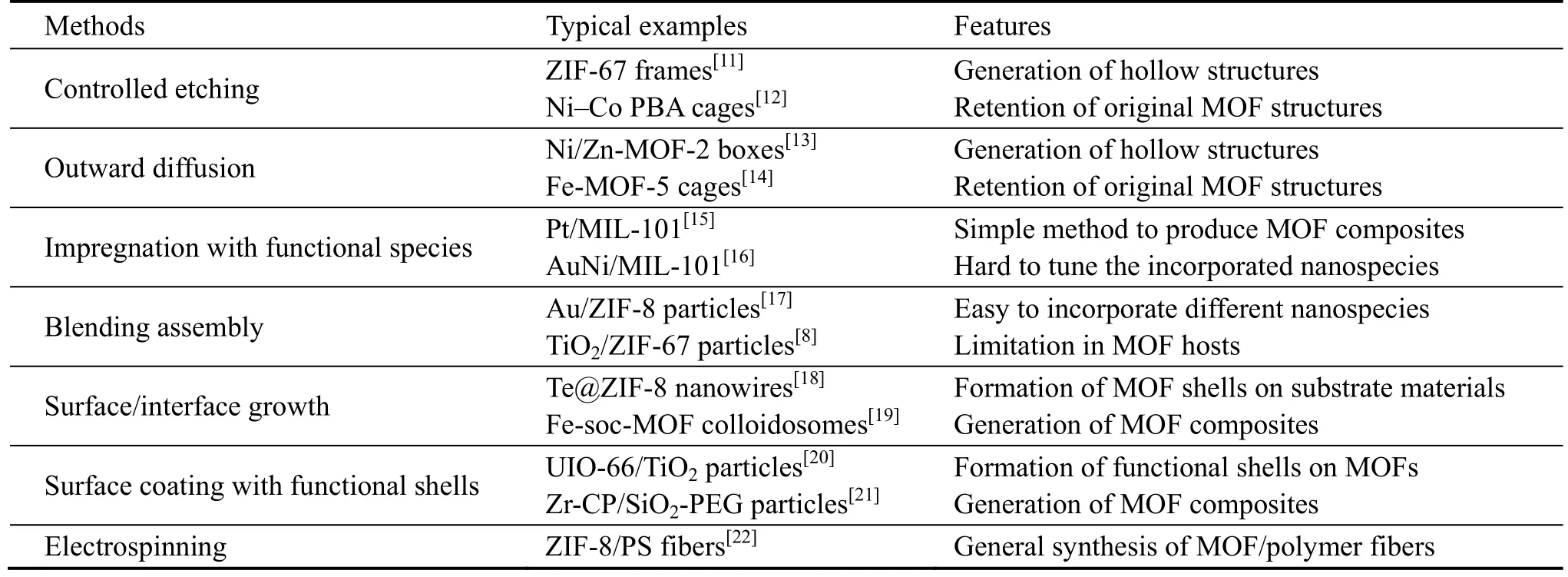
表1 MOFs前驱体合成方法综述[8]Table 1 Summary of synthetic methods for MOF-based precursors[8]

表2 MOFs衍生纳米材料合成方法综述[8]Table 2 Summary of synthetic methods for MOF-based precursors and their derived nanomaterials[8]
0.3 MOFs衍生金属氧化物
在所有已报道的锂和钠离子电池负极材料中,金属氧化物因高能量密度(600~1 500 mA·h/g)和经济环保的优势成为下一代负极材料的候选之一[30-31]。MOFs除了直接作为电极材料使用外,还可以通过一些简单的处理得到各种具有有趣结构的衍生金属氧化物[[32]。根据转化过程的反应机理,这些处理方法主要分为以下四类[33]:(1)惰性气氛自热解;(2)与气体/蒸汽的化学反应;(3)与溶液的化学反应;(4)化学刻蚀。通过以上方法,这些MOFs衍生材料可以容易地形成各种结构和成分可调的多孔或中空结构,而不需要额外的模板或繁琐的过程,与传统方法相比显示出显著的优点。本文总结的基于MOFs进一步处理得到的不同纳米结构金属氧化物如表2和图2所示[9]。MOFs和MOFs基复合前驱体将为合成结构复杂度高的纳米结构材料提供新的机会。关于金属氧化物作为锂离子电池和钠离子电池的综述很多[34-35],这里不做详细介绍和深入讨论,本文仅讨论MOFs衍生金属氧化物作为电极材料在锂离子电池和钠离子电池领域的应用。

图2 几种基于MOFs的纳米结构举例[9]Fig.2 Examples of some MOF-based nanostructures[9]
1 MOFs及其衍生金属氧化物在锂离子电池中的应用
1.1 MOFs的应用
锂离子电池是通过锂离子在正负极材料中的嵌入/脱出来实现能量的吸收和释放,因此具有多孔结构、高比表面积和优异导电性能的MOFs很适合作为锂离子电池电极材料。以下将介绍MOFs作为锂离子电池电极材料在正极和负极上的应用情况。
1.1.1 正极材料
FEREY等[36]报道了一种可作为LIBs正极材料的 FeIII(OH)0.8F0.2[O2C-C6H4-CO2](命名为 MIL- 53(Fe))。实验表明,在 C/40倍率下,每个 Fe3+层间可嵌入0.6个Li+,具有70 mA·h/g的能量密度,且其循环稳定性优异。PENG等[37]在2 C倍率下对MOFs材料Cu-TCA进行了锂离子电池充放电循环测试,充放电电压平台稳定在3.4 V,200次循环后放电比容量可达45.1 mA·h/g。因此,MOFs被认为是具有应用潜力的LIBs正极材料。
1.1.2 负极材料
除了作为正极材料,MOFs还可作为负极材料。MAITI等[38]通过溶剂法合成了 Mn-BTC-MOFs,MOFs中的羧基基团提高了 Li+的嵌入/脱出能力,初始放电容量可达 694 mA·h/g,在 100 mA/g 电流密度下循环100次后依然保持83%的容量,如图3所示。AN等[39]通过溶剂热法制备的二维Ni基MOFs(Ni-Me4BPZ:C20H24Cl2N8Ni)初始放电容量320 mA·h/g,100次循环后可达 120 mA·h/g。基于萘甲酸盐(naphthalenetetracarboxylates,NTC)与 Li、Ni优异 的结合性,HAN等[40]水热制备的 Li/Ni-NTC电化学性能稳定,初始放电容量高达 1 084 mA·h/g,80次循环后稳定在482 mA·h/g,如图4所示。

图3 (a)Mn-BTC-MOFs有机部分中与Li+配位的可能位点;Mn-BTC-MOF的恒电流充放电曲线(b)和循环性能(c)[38]Fig.3 (a) Probable Li+insertion/extraction sites for coordination with Li in the organic fraction of Mn-BTC MOF;galvanostatic discharge/charge profiles (b) and cycling performance (c) for Mn-BTC MOF[38]

图4 MOF(Ni-Me4BPZ)的配位模式(a)、平面结构(b)和sql拓扑结构(c)[39];(d)Li-NTC、Ni-NTC和Li/Ni-NTC的循环性能[40]Fig.4 Coordination mode (a),planar structure (b),and sql topological structure (c) of MOF (Ni-Me4bpz)[39];(d) cycling performance of Li-NTC,Ni-NTC,and Li/Ni-NTC[40]
1.2 MOFs衍生金属氧化物的应用
金属氧化物因能量密度高(600~1 500 mA·h/g)和经济环保的优势成为可供选择的下一代负极材料之一[23-24,41]。但金属氧化物作为LIBs负极材料时依然存在一些问题:其一,与碳基材料相比,金属氧化物的导电性差,这会影响电池内部电子的传输从而降低材料的倍率性能;其二,在充放电过程即Li+嵌入/脱出的过程中,作为电极材料的金属氧化物体积变化较大,使材料在长循环过程中粉化和团聚,加速新固态电解质膜的生成和电解液的消耗,进而导致材料倍率和循环性能的降低。这些问题严重制约了金属氧化物在电极材料中的广泛应用。研究表明,通过设计和构建微/纳米结构、层状多孔结构或空心纳米结构可有效解决上述问题[42]。其中,由MOFs材料衍生得到的金属氧化物因独特的多孔微/纳结构,在锂离子电池领域表现出高比容量和长循环寿命等优势,引起了越来越多的关注。以下介绍以MOFs材料为前驱体构建具有结构优势的金属氧化物在锂离子电池负极上的应用。
由于有机分子、金属元素或其他客体在 MOFs骨架中可实现共存,因此,MOFs及其复合材料可作为理想前驱体,合成具有较高孔隙率的多孔碳、金属氧化物或其他金属/碳基纳米材料[26]。XU等[43]以MIL-88-Fe为原料,通过在空气中加热分解,合成了纺锤形多孔α-Fe2O3,得益于纳米多孔结构提高了比表面积,增加了更多的电化学活性位点,0.2 C电流密度下50次循环后保持在911 mA·h/g,即使在10 C电流密度下,仍获得424 mA·h/g的比容量。另外,CuO因其资源丰富、价格低廉和环保等特点在各领域被广泛使用。BANERJEE等[44]热解MOF-199得到锥形纳米 CuO,其初始容量高达 1 208 mA·h/g,在所测试的40个循环中显示了良好的循环性能,库伦效率高达99%,表明铜基MOF衍生的多孔CuO具有优异的电化学性能,其循环性能如图5。
MOFs材料密度较低,在转化成金属氧化物时通常会产生较大的体积收缩,因此可以用该类化合物制备具有中空结构的金属基纳米材料。目前,大多数中空结构的MOFs基金属氧化物都是通过离子交换法合成的,这些方法过程复杂、耗能大、成本高,不利于大规模应用[26,45]。采用普鲁士蓝类化合物制备具有MOFs结构的纳米材料引起了研究人员的广泛关注。该方法操作简单、成本较低,得到的产物结构稳定,同时也展现出较优异的电化学性能。HU等[46]通过普鲁士蓝类似物(PBA,Co3[Co(CN)6]2)烧结获得多孔Co3O4纳米笼,在300 mA/g电流密度下50次循环后依然保持1 465 mA·h/g稳定容量,其优异的电化学性能归因于多孔 Co3O4纳米笼尺寸小、壳层多孔、表面积大的结构优势。在众多氧化物电极材料中,Fe2O3理论容量高(1 000 mA·h/g),无毒且成本低,被认为是一种很有应用前景的负极材料。ZHANG等[47]通过普鲁士蓝(PB)立方体在空气中的氧化分解合成了具有分层多孔的 Fe2O3空心盒子,如图6所示。

图5 以Cu-MOF为前驱体合成的纳米结构CuO在100 mA/g电流密度下容量可达 538 mA·h/g[44]Fig.5 Cu-MOF derived CuO nano structures for superior Li ion battery with capacity reaching 538 mA·h/g at 100 mA/g [44]

图6 不同退火温度处理得到的空心 Fe2O3盒子的 FESEM(a,b,d,e,g,h)和 TEM(c,f,i)图:a、b、c 温度为 350℃;d、e、f温度为 550℃;g、h、i温度为 650℃[47]Fig.6 FESEM (a,b,d,e,g,h) and TEM (c,f,i) images of hollow Fe2O3 microboxes obtained at 350°C (a,b,c),550°C (d,e,f),and 650°C (g,h,i)[47]
该类材料电化学性能优异,在200 mA/g电流密度下具有950 mA·h/g的高容量,这完全得益于其中空多孔的盒装结构(缓解体积膨胀,增加活性位点)。
通过创新的合成方法或对核壳形成过程进行精细调控,可从MOFs中产生具有多种核壳结构的空心颗粒[26]。ZHANG等[48]通过调节PB模板与不同碱性物质之间的简单反应来大规模合成复杂的空心结构,如图7。PB立方体与不同浓度NaOH溶液反应即可获得单层和多层 Fe(OH)3空心立方,进一步在空气中退火即可得到单层和多层Fe2O3空心立方。测试结果也证明这些多层Fe2O3空心立方作为LIBs负极材料的电化学性能得到显著提高,其首次放电容量高达1 473 mA·h/g,首次库伦效率为 65%,30次循环后可逆容量保持在650 mA·h/g,且该多层空心结构经过长循环后依然保持完好。这主要归因于分层空心Fe2O3电极中电解质能够充分渗透,Li+在活性物质间能够实现快速传递,以及空心结构能够有效地避免体积变化带来的材料粉化。

图7 室温和水热条件下 PB模板法合成 Fe(OH)3微盒: Fe4[Fe(CN)6]3立方的FESEM(a)和TEM(b);室温下得到的Fe(OH)3立方(c-e)和核壳Fe(OH)3立方(f)的FESEM (c,d)和TEM(e,f);水热条件下得到的单层(g-i)和多层(j-l)Fe(OH)3立方的FESEM(g)和TEM(h-l)[48]Fig.7 Formation of hierarchical Fe(OH)3 microboxes by PB templating at room temperature and hydrothermal conditions: FESEM (a) and TEM (b) images of Fe4[Fe(CN)6]3 microcubes;FESEM (c,d) and TEM (e,f) images of Fe(OH)3 microboxes (c-e) and yolk-shelled Fe(OH)3 microboxes (f) synthesized at room temperature;FESEM (g) and TEM (h-l) images of hierarchically single-shelled (g-i) and multiple-shelled (j-l) Fe(OH)3 microboxes synthesized under hydrothermal conditions[48]
2 MOFs及其衍生金属氧化物在钠离子电池中的应用
由于钠资源的广泛分布和低成本,钠离子电池被认为是替代锂离子电池作为大规模储能的选择,也是下一代能量储存体系的有力候选者之一[49]。钠离子电池的工作原理与锂离子电池相似,但Na+半径(0.102 nm)大于 Li+半径(0.076 nm),这需要更开放的通道来实现Na+在电极材料中的充分迁移。
2.1 MOFs的应用
与无机材料相比,有机化合物因其结构的多样性和灵活性可以提供充足Na+嵌入/脱出的通道[50]。由于具有高度开放的结构,一些MOFs已被探索作为钠离子电池的候选,特别是PB(A[FeIIIFeII(CN)6],A=Na+或 K+)及其类似物(K[MFe(CN)6],M=Fe、Co、Ni、Cu、Zn)[51-55],如图8所示。

图8 (a)PB类似物的晶体结构[55];(b)六氰高铁酸锰立方钠(左)的晶体结构和碱离子沿[111]轴位移菱形对称(右)[5]Fig.8 (a) Crystal structure of PB analogues[55];(b) crystal structure of a cubic sodium manganese hexacyanoferrate (left) and the alkali-ion displacement along the [111] axis resulting in rhombohedral symmetry (right) [5]
WESSELLS等[56]报道了可嵌入/脱出 Na+和 K+的块状PBA六氰铁酸镍纳米颗粒,该MOFs材料可在安全和低成本的水性电解液中操作。其开放式骨架结构为钠离子电池提供了优异的倍率性能、高的库伦效率和长的循环寿命。在41.7 C的高倍率下能保持67%的初始容量,而在8.3 C电流密度下5 000次循环不会出现容量衰减。WU等[57]报道了通过控制结晶法制备无空位的NaxCoFe(CN)6(NaCoHCF)纳米晶体,并研究了其在水性电解液中的储Na性能,利用其优异的结构可获得达130 mA·h/g的高容量,相当于每个NaCoHCF中可嵌入1.7个Na+,800次循环后依然具有90%的容量保持率,表明NaCoHCF在存储Na和循环稳定的可行性。WANG等[5]在研究KMnIIFeIII(CN)6时发现,其具有 3.82 V 和 3.56 V 的高可逆电压平台,还发现Na+浓度对材料的组成和结构影响较大:在高 Na+浓度下,Na+沿[111]方向位移,发生从立方对称到菱形对称的相变(图8b),该转变过程可逆,初始的菱形Na1.72MnFe(CN)6的容量为 134 mA·h/g,30 次循环后仍保持 120 mA·h/g,是一种很有前途的钠离子电池正极。WANG等[58]用水热法合成 K4Na2[Fe(C2O4)2]3·2H2O,该材料能提供可逆的Na+嵌入/脱出通道,在草酸桥接结构中有一维非密封通道,每个晶胞可容纳两个Na+,如图9,其首次充电容量为54.5 mA·h/g,放电容量为50.2 mA·h/g,平均电压可达2.7 V。

图9 K4Na2[Fe(C2O4)2]3·2H2O 的晶体结构:(a)Fe 与其他原子的协调;(b)3D铁草酸骨架(为了清晰而省略了如钾和钠的非桥原子);(c)沿c方向用于K1(通道1)的一维开放通道和用于Na/K2(通道2)的一维闭合通道[58]Fig.9 Crystal structure of K4Na2[Fe(C2O4)2]3·2H2O: (a) coordination environment around Fe;(b) 3D iron-oxalato framework (non-bridging atoms,such as potassium and sodium,are omitted for clarityO;(c) 1D open channel for K1 (channel 1) and 1D closed channel for Na/K2 (channel 2) along the c direction are shown[58]
2.2 MOFs衍生金属氧化物的应用
金属氧化物作为锂和钠离子电池负极材料时电子电导率低、结构稳定性差,而由于Na+半径大约是Li+的1.55倍,因此金属氧化物作为钠离子电池负极时会有更低的反应动力学和更严重的体积膨胀。对钠离子电池中金属氧化物作为负极的改进,采用和金属氧化物作为锂离子电池负极时相同的策略,利用设计多孔分级微纳结构和碳修饰等方法改善反应转化动力学、增强电子电导性和缓解充放电过程中的体积膨胀。使用MOFs为前驱体制备的金属氧化物可满足以上要求,已有部分MOFs衍生金属氧化物如 Fe2O3[59]、Co3O4[60]和 CuO[61]实现了相关应用。
以镍基MOFs为前驱体,可制备空心球形纳米结构的NiO/Ni/石墨烯钠离子电池负极材料[62],其倍率性能良好(2 A/g 电流密度下容量可达 207 mA·h/g)、循环稳定性佳(每个循环大约 0.2%的衰减)。这种优异的电化学性能源于精心设计的 NiO/Ni/石墨烯多层空心球结构,不仅减轻了NiO在循环过程中的体积膨胀,而且提供了连续的高导电石墨烯基体,促进快速电荷转移,形成稳定的固态电解质层,其结构及储钠性能如图10。

图10 Ni-MOF具有球中空结构、表面有针状结构的示意图及其作为钠离子电池材料的电化学性能[62]Fig.10 The Ni-MOF possesses a hollow,ball-in-ball structure with needles on the surface and the electrochemical performance of NiO/Ni/Graphene composite for SIBs [62]
此外 GE等[63]通过低温磷化处理金属有机框架物质ZIF-67衍生出介孔核壳多面体结构的CoP@C,并将其固定在 3D还原氧化石墨烯泡沫镍上,形成一种具有优异循环稳定性和高倍率性能的CoP@C-RGO-NF负极材料,如图11所示。小电流密度下循环100次后保持473 mA·h/g的容量,其优异的性能源于CoP@C多面体核/壳与RGO网络之间的协同效应,独特的核/壳结构可以为电极和电解质提供更多接触面积,促进Na+的扩散,而碳层可以提高电子导电性和缓冲体积变化,防止CoP粉碎和聚集。
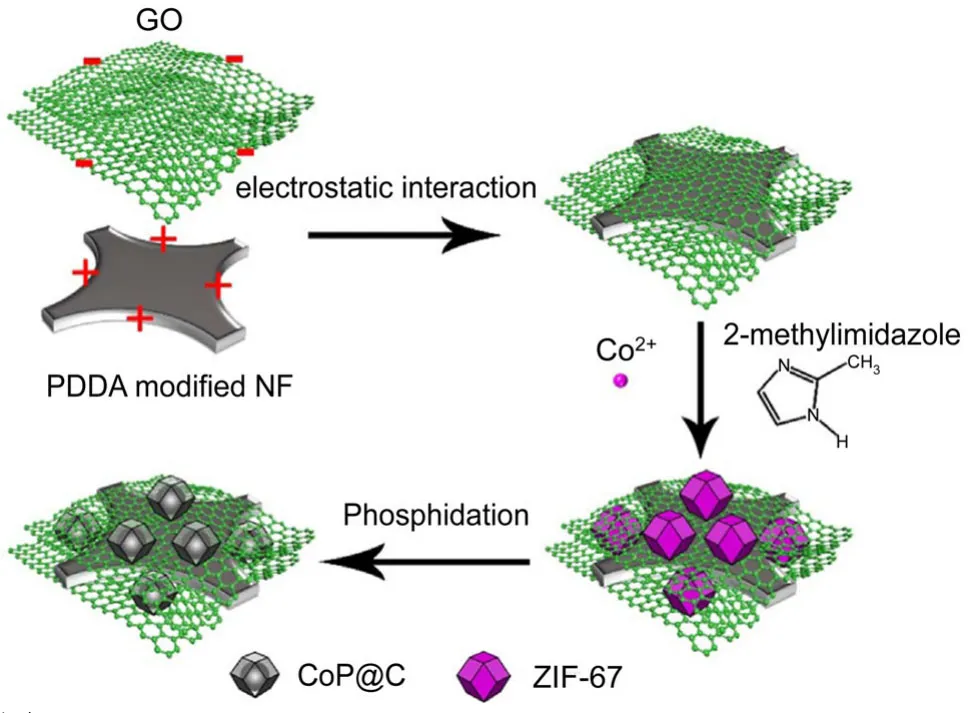
图11 COP@ C-RGO-NF 合成路线示意图[63]Fig.11 Schematic illustration of the synthesis process of CoP@C-RGO-NF[63]
随着对锂和钠离子电池的进一步研究,相信在不久的将来MOFs及其衍生金属氧化物将得到大规模应用。
3 结束语
本文综述了MOFs及其衍生金属氧化物作为锂和钠离子电池电极材料的最新研究进展,阐述了这些制备工艺简单、合成可控、比表面积大的 MOFs及其衍生金属材料在能源储存领域的应用潜力。
MOFs及其衍生金属氧化物距离实际应用依然面临着一些挑战:(1)MOFs材料的电化学稳定性依然是作为锂离子和钠离子电池电极材料需要首要考虑的问题,但是大多数MOFs在复杂的电池电化学环境中无法稳定存在,这也是MOFs电极材料倍率和循环稳定性低的原因。(2)MOFs及其衍生金属氧化物的导电性有待提高,这对锂离子和钠离子电池的容量和倍率性能非常重要。将碳元素和金属基引入MOFs及其衍生金属氧化物是目前提高电极材料电导率最有效的方法,复杂化纳米结构能够复合各种组分的优势,从而提高电化学性能。(3)目前对具有特定结构或功能的MOFs及其衍生金属氧化物已实现一定程度上的可控合成,而且这些MOFs基电极材料都具有优异的电化学性能,但是对复杂结构和电化学性能间存在的联系依然有待完善,若能通过足够的实验和理论分析理解各组分之间的联系,对设计合成具有明确结构优势的功能材料会有更好的指导作用。
