可逆加成-断裂链转移沉淀聚合法制备木犀草素分子印迹聚合物及其表征
2019-03-11苏立强楚善明王媛媛
苏立强, 楚善明, 谢 鹏, 王媛媛
(齐齐哈尔大学化学与化学工程学院,黑龙江齐齐哈尔 161006)
木犀草素(Luteolin,LTL)为一种典型的黄酮类化合物,是多种常见中草药和天然产物中的有效成分之一,因其可调节人体免疫功能以及良好的抗病毒性能,在医药方面有重要的应用价值。因合成药物产率低,且具有一定毒副作用,近年来人们更倾向于从植物中提取具有药用价值的化学成分[1 - 3]。目前,木犀草素提取的方法主要有:乙醇-水溶剂提取法、碱性稀醇提取法、超声波法、超临界流体萃取法、酶提取法和大孔树脂吸附法。但这些方法都不同程度存在有机溶剂消耗大,纯度低等问题。因此,针对合成以及提取的诸多弊端,建立高选择性的提取木犀草素的方法具有重要意义。
分子印迹技术(MIT)是指制备对某一特定目标分子具有特异选择性聚合物的过程。在分子识别、固相萃取、色谱分离等方面得到广泛应用。分子印迹聚合物(MIPs)的制备方法主要有本体聚合、悬浮聚合、沉淀聚合、表面聚合、原位聚合等。可逆加成-断裂链转移(RAFT)-沉淀聚合法具有单体适用范围广、聚合过程简单、特异性吸附量大等优点[4 - 6],同时又避免了传统沉淀聚合因自由基反应过程不受控制,使得所制备的MIPs粒径范围较宽,内部孔穴差异较大的缺点[7 - 9]。目前对木犀草素MIPs的制备大都采用传统聚合方法[16 - 20]。祁楚楚等[19]以木犀草素为模板分子,利用本体聚合法制备MIPs;曹红梅[20]以悬浮聚合法制备了木犀草素MIPs。本文采用RAFT-沉淀聚合法制备木犀草素MIPs,其吸附性能优于传统方法制备的聚合物,将其作为固相萃取材料,用于花生壳中木犀草素的分离富集,效果良好。
1 实验部分
1.1 仪器与试剂
P230型高效液相色谱仪(大连依利特公司)。
木犀草素(LTL)、香叶木素、芹菜素、丙烯酰胺(AM)(分析纯,天津科密欧化学试剂开发中心),乙二醇二甲基丙烯酸酯(EGDMA)(分析纯,东京化成工业株式会社),偶氮二异丁腈(AIBN)(分析纯,天津光复精细化工研究所),二硫化碳、无水NaSO4、四正丁基溴化铵、石油醚、甲醇、氯化苄均为分析纯(Sigma试剂有限公司),甲酸为优级纯(天津市科密欧化学试剂中心)。
1.2 链转移试剂二苄基三硫代碳酸酯的制备
参照文献方法[10]制备链转移试剂二苄基三硫代碳酸酯(DBTTC),并用红外光谱法进行表征。
1.3 分子印迹聚合物的制备
在100 mL圆底烧瓶中加入0.0715 g (0.25 mmol)模板分子LTL,0.0718 g (1 mmol)功能单体AM,超声溶解于40 mL甲醇中,预聚合8 h。再加入2.765 g (14 mmol)交联剂EGDMA,0.01 g 引发剂AIBN和0.05 g DBTTC,超声15 min,缓慢通入N2脱氧15 min,将圆底烧瓶密封后,置于60 ℃恒温水浴中热聚合24 h。用10%乙酸-甲醇溶液(V/V)对聚合物进行索氏提取24 h,以去除模板分子和未参加反应的功能单体及交联剂。再除去残留的乙酸,45 ℃真空干燥48 h,即得R-MIPs。除不加模板分子外,其他操作步骤同上,制备非印迹聚合物R-NIPs。不加入DBTTC,其他同上,制备传统印迹聚合物T-MIPs和非印迹聚合物T-NIPs。
1.4 MIPs吸附性能研究
1.4.1静态吸附实验配制浓度(c0)范围在0.00~100.00 μg/mL的木犀草素溶液,再分别向各溶液中加入10 mg的MIPs,静止12 h。然后取上层清液1 mL,用0.45 μm膜过滤后,加无水甲醇稀释至3 mL,利用紫外分光光度计测得各溶液的浓度ce,根据吸附前后木犀草素的浓度变化,计算洗脱后的MIPs的吸附量,然后按照公式:Q=(c0-ce)×V/m计算得出分子印迹聚合物对木犀草素(LTL)的饱和吸附容量Q。
1.4.2动态吸附实验称取0.0300 g MIPs,置于100 mL锥形瓶中,加入35 mL 100 μg/mL的木犀草素溶液,再加入15 mL无水甲醇,低频超声10 min。每间隔20 min吸取1 mL上层清液,离心5 min(800 r/min),用0.45 μm膜过滤后,利用紫外分光光度计测得相应浓度ce,根据公式计算MIPs的吸附容量Q。
1.4.3选择性吸附实验取吸附瓶三个,分别加入10 mL浓度为100 μg/mL的木犀草素溶液、芹菜素溶液、香叶木素溶液,各加入MIPs 10 mg,超声10 min后,置于25 ℃室温下静止12 h。利用紫外分光光度计测得相应的吸光度,通过标准曲线得出浓度ce,根据公式分别计算MIPs的吸附容量Q。用相同的方法进行R-NIPs的选择性吸附实验。
1.5 样品处理与固相萃取
取粉碎花生壳5 g溶解于200 mL 50%甲醇中,超声提取0.5 h,回流提取3次,将三次提取的甲醇溶液合并后过滤,再将滤液蒸发浓缩,离心5 min,取上清液用50%甲醇定容至250 mL。分子印迹固相萃取(MISPE)柱依次用3 mL水和5 mL甲醇活化,取已处理好的甲醇溶液上样,然后用3 mL乙腈淋洗,再用10 mL甲醇/乙酸(9∶1,V/V)作为洗脱液进行洗脱,将洗脱液浓缩至1 mL。浓缩液经高效液相色谱法(HPLC)检测。色谱柱:ACQUITY UPLC BEH C18柱(100×2.1 mm,1.7 μm);流动相:甲醇;紫外检测波长:348 nm;流速:0.5 mL/min。
2 结果与讨论
2.1 木犀草素印迹机理
木犀草素是一种多酚化合物,在预聚合中酚羟基上的H+与功能单体(AM)上的O原子发生强烈的氢键作用。加入交联剂、引发剂和RAFT试剂后,在60 ℃下反应,生成聚合物,洗脱除去模板分子后,在聚合物内部形成与模板分子结构、大小相匹配的孔穴,可以特异选择性吸附模板分子。在该分子印迹聚合物的末端,含有RAFT试剂,在相同的实验条件时,可以继续引发反应。
木犀草素分子内部含有四个酚羟基,从理论上讲功能单体与模板分子将以1∶4的比例形成配合物,在印迹孔穴中含有四个结合位点,依靠“四点作用”方式实现对模板分子的识别。酚羟基是氢键的良好供体,丙烯酰胺中的-NH2基与C=O基团均可作为氢键受体,-NH2中N上的孤对电子与相邻的C=O基团会产生共轭,与木犀草素中的酚羟基形成稳定的氢键。
2.2 R-MIPs与T-MIPs的扫描电镜图对比
采用传统沉淀聚合法与RAFT-沉淀聚合法分别制备木犀草素MIPs,对比其形貌上的差异,扫描电镜图见图1。传统方法合成的聚合物有粘连现象,粒径较小,且粒分布不均匀。加入RAFT试剂后,聚合物大小均一,粒径明显增大,大约为3.5 μm,更适合作为固相萃取填料。这是因为聚合过程中RAFT试剂的存在会导致活性种(生长链)和休眠种(RAFT基团链)之间能够形成快速的动力学平衡,从而使聚合速度可控。

图1 T-MIPs(A)与R-MIPs(B)的扫描电镜(SEM)图(5 μm)Fig.1 SEM images of T-MIPs(A) and R-MIPs(B) (5μm)
2.3 静态吸附性能
采用静态吸附实验考察聚合物吸附性能,绘制出R-MIPs、R-NIPs、T-MIPs、T-NIPs的静态吸附曲线,见图2。由图2可知,R-MIPs和T-MIPs的吸附容量明显高于R-NIPs和T-NIPs。这是因为MIPs内部存在与LTL结构相匹配的印迹孔穴,且孔穴内规则排列着与其结构相应的结合位点,吸附容量较大;而NIPs内部不存在这样的孔穴,主要依靠物理吸附,吸附容量较小。另外,R-MIPs的吸附容量(32.60 mg/g)高于T-MIPs的吸附容量(29.06 mg/g),这是因为在RAFT-沉淀聚合过程中引入DBTTC,抑制了自由基无序反应,稳定了增长自由基浓度,从而控制了反应进程,使粒径更加均匀有序,吸附容量更大。R-NIPs 的吸附容量(14.41 mg/g)低于T-NIPs的吸附容量(16.61 mg/g)是因为引入DBTTC后,聚合物粒径变大,表面积减小,使其物理吸附量变小。
2.4 动态吸附性能
为考察R-MIPs对模板分子的结合速率,进行动力学吸附实验。考察聚合物与模板分子结合的动力学性能。动力学吸附曲线如图3,吸附在2 h快速达到平衡,主要是由于RAFT-沉淀法制备的聚合物孔穴更均匀,表面更光滑,快速的吸附平衡可更好的应用于实际。
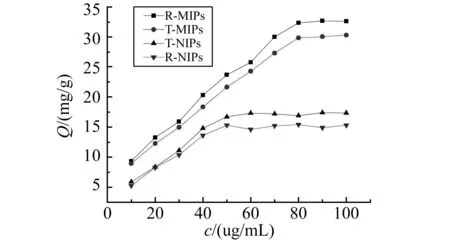
图2 R-MIPs、T-MIPs、T-NIPs和R-NIPs的吸附等温线Fig.2 Adsorption isotherm of R-MIPs,T-MIPs,T-NIPs and R-NIPs

图3 R-MIPs的动力学吸附曲线Fig.3 Kinetic adsorption curve of R-MIPs
对聚合物的动力学数据进行准一级动力学模型和准二级动力学模型拟合[12],见表1。准一级动力学模型公式为:ln(Qe-Qt)=lnQ1-K1t;准二级动力学模型公式为:t/Qt=1/(K2Q22)+t/Q2。式中,Qt为t时刻的吸附容量(mg/g);Qe为达到平衡时的吸附容量(mg/g);K1,K2分别为一级和二级动力学速率常数(h-1)。
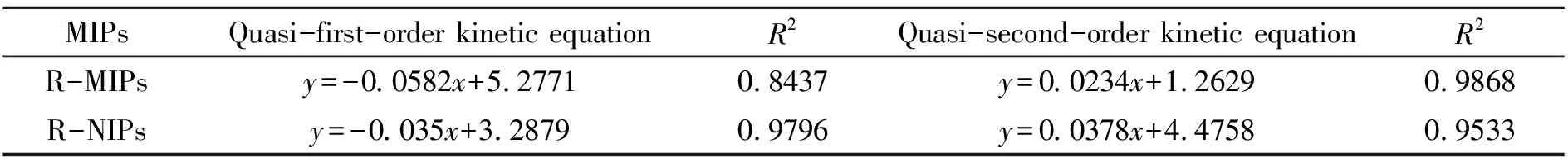
表1 聚合物准一级和准二级动力学模型参数
准一级动力学模型主要描述物理吸附,准二级动力学模型主要描述化学吸附,包含了吸附的所有过程(外部液膜扩散、表面吸附和颗粒内扩散等)。通过比较准一级动力学模型和准二级动力学模型的相关系数R2,可知R-NIPs对LTL的吸附过程更符合准一级动力学模型,属于物理吸附,R-MIPs对LTL的吸附过程更符合准二级动力学模型,属于化学吸附。说明其吸附过程受化学吸附机理的控制,这种化学吸附涉及到吸附剂与吸附质之间的电子共用或电子转移,即LTL的羟基与功能单体AM的羰基之间存在电荷转移。
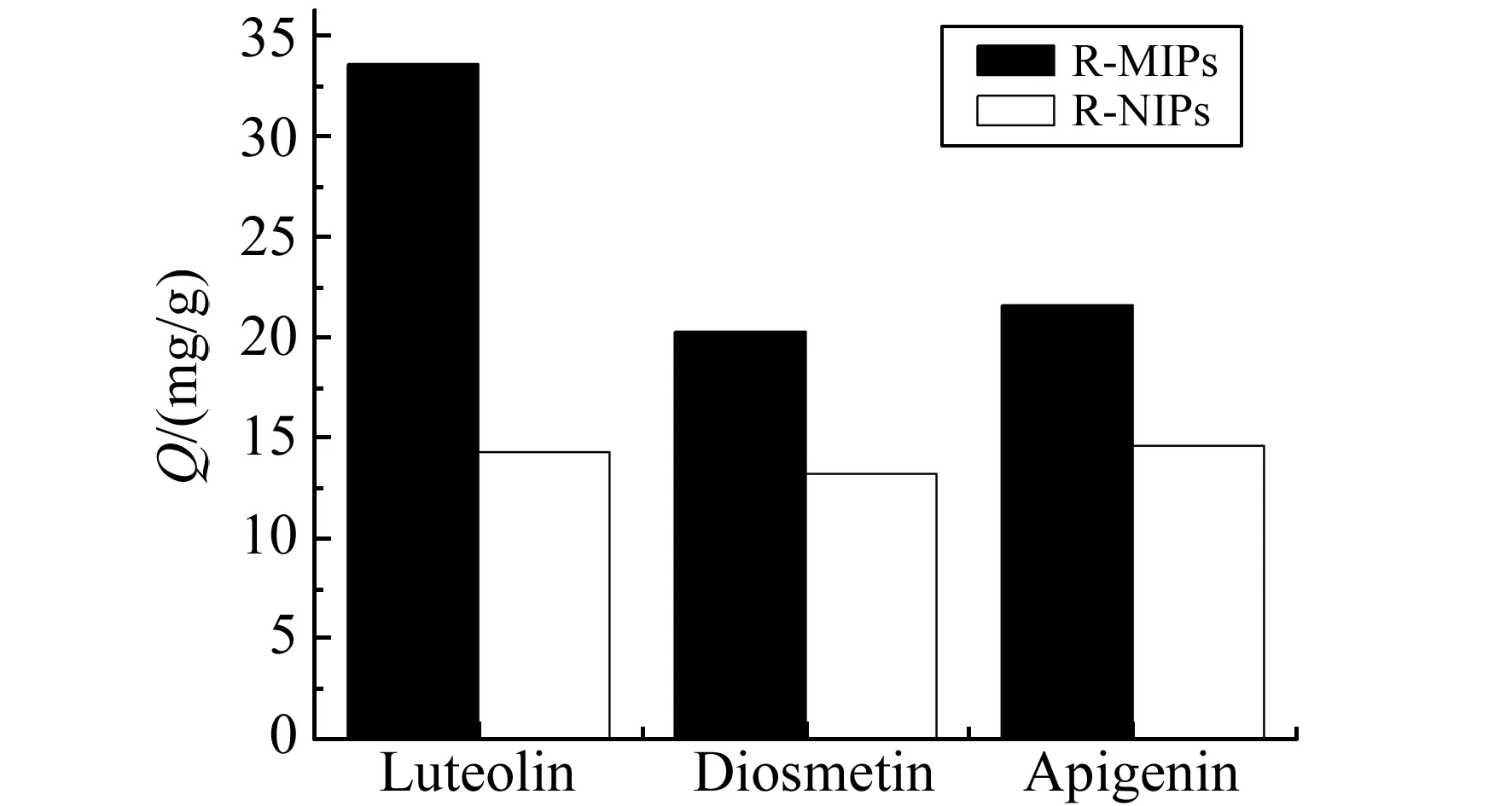
图4 R-MIPs与R-NIPs对三种底物的选择性吸附Fig.4 Selective adsorption of R-MIPs and R-NIPs on three kinds of substrates
2.5 吸附选择性
为考察MIPs对模板分子的选择性能,选用与木犀草素结构类似的香叶木素和芹菜素为对照物,测定聚合物对三者的吸附容量,实验结果见图4。由图可知,R-MIPs对木犀草素的吸附容量远大于对香叶木素(Diosmetin)和芹菜素(Apigenin)的吸附容量,这是由于在R-MIPs中有与木犀草素结构相匹配的印迹孔穴,这个印迹孔穴与其他两种物质的结构不匹配,而R-NIPs对三种物质的吸附容量无明显差别,这是因为R-NIPs中没有与模板分子相匹配印迹孔穴,所以在吸附容量上差别很小。

图5 花生壳在固相萃取前后的色谱图Fig.5 Chromatograms of peanut shell before and after solid phase extraction
2.6 花生壳中木犀草素的提取
以R-MIPs作为固相萃取填料制备MISPE柱,将MISPE与HPLC法相结合,用于花生壳中木犀草素的富集与检测。在花生壳中检测出木犀草素,经过测定其含量为5.69 mg/g,色谱图见图5,经过MISPE处理后有效地去除了基质杂质,得到较好的富集分离效果,表明该印迹材料可用于对复杂样品中木犀草素的分离纯化。
3 结论
采用RAFT-沉淀聚合法制备了木犀草素分子印迹聚合物(R-MIPs),并利用扫描电镜进行了表征。静态吸附实验表明,R-MIPs对LTL具有较大吸附容量,饱和吸附容量达到32.6 mg/g。以R-MIPs作为固相萃取填料对花生壳中木犀草素进行分离富集,能有效去除基质杂质,该印迹聚合物表现出对LTL优异的分离富集效果,为工业生产中LTL的分离提纯提供了一种可能的途径。
