三聚氰胺分子印迹光子晶体水凝胶膜传感器的制备及应用
2019-03-08刘哲涵梁阿新孙立权罗爱芹
刘哲涵, 张 鑫, 梁阿新, 孙立权, 罗爱芹
(北京理工大学生命学院, 北京 100081)
三聚氰胺(melamine, MEL),是一种重要的三嗪类含氮杂环有机化工材料,广泛应用于塑料、木材加工、皮革制造、医疗、电气等行业[1]。由于三聚氰胺具有高达66%的含氮量并且价格低廉,故常被不法商贩添加到牛奶、奶粉等食品中提高含氮量[2],以造成高蛋白质含量的假象,引发了一系列的食品安全问题,对人们健康造成了极大的危害和影响。三聚氰胺在进入人体后会水解成三聚氰酸,三聚氰酸与三聚氰胺能形成不溶性的结晶复合物,从而导致膀胱炎、肾衰竭,严重甚至能导致尿石症及膀胱癌[3]。传统检测牛奶中蛋白含量的凯氏定氮法只能测定氮的总量,却并不能有效区分氮的来源和种类。现有的三聚氰胺分析方法主要有高效液相色谱(HPLC)法[4]、高效液相色谱-质谱联用(HPLC-MS)法[5,6]、气相色谱-质谱联用检测(GC-MS)法[7]、酶联免疫吸附(ELISA)法[8-10]、表面增强拉曼光谱(SERS)法[11]等。这些方法需要昂贵而精密的仪器、专门训练的技术人员、检测耗时长、成本较高。因此,建立一种简便、快捷、低成本的检测三聚氰胺的方法很有必要。
分子印迹技术(molecularly imprinted technique, MIT),是指以某一特定的目标分子(模板分子、印迹分子)为模板,制备对该分子有特异选择性识别能力的聚合物的技术[12],当除去模板分子后,聚合物中就形成了与模板分子形状和功能基团空间位置相匹配的具有多重作用点的印迹空穴,这些印迹空穴对模板分子具有特异识别性。光子晶体是指介质材料在空间上按照一定的周期性顺序排列形成的有序结构材料,光子晶体的这种特殊的结构对可见光的衍射服从布拉格衍射定律[13,14],布拉格衍射峰的波长受到介质材料的折射率与晶格参数的影响,因此光子晶体可以作为传感材料,在生物和化学传感器方面有着很好的应用前景[15,16]。将分子印迹技术与光子晶体结合,可以制备出同时具有二者优点的材料。这种材料对目标物分子具有特异性识别能力,同时光子晶体能够将分子印迹聚合物同目标分子结合的过程转化为光学信号[17-22]的检测。
本研究利用单分散二氧化硅(SiO2)微球垂直沉降自组装的方法获得蛋白石结构的光子晶体模板,并选择三聚氰胺作为模板分子,甲基丙烯酸(MAA)作为功能单体,乙二醇二甲基丙烯酸酯(EGDMA)作为交联剂,采用后填充的方法,经紫外光引发聚合,再利用氢氟酸将二氧化硅蛋白石模版刻蚀下来,最终制备得到具有反蛋白石结构的分子印迹光子晶体水凝胶膜(molecularly imprinted photonic hydrogels, MIPHs),实现了对三聚氰胺的检测,对于食品及环境样品中的三聚氰胺的检测分析具有很好的应用价值。
1 实验部分
1.1 仪器、试剂与材料
UV-1800型紫外分光光光度计(日本SHIMADZU公司), DH-101型电热恒温鼓风干燥箱(天津中环实验电炉有限公司), KQ5200型超声波清洗器(昆山市超声仪器有限公司), Acquity UPLC超高压液相色谱仪(美国沃特世科技有限公司)。
单分散二氧化硅微球(直径260 nm,质量分数为20%)购自北京市通广精细化工公司;三聚氰胺(纯度99.5%)、双氰胺(纯度99.0%)、三聚氰酸(纯度99.0%)、丙烯酰胺(纯度99.0%)均购自天津光复精细化工研究所;MAA(分析纯)和EGDMA(纯度98%)购自北京百灵威科技有限公司;偶氮二异丁腈(AIBN,分析纯)购自上海市四赫维化工有限公司;辛烷磺酸钠(纯度99%)购自上海麦克林生化科技有限公司;柠檬酸(分析纯)、浓硫酸(质量分数98%)、过氧化氢(质量分数30%)、氢氟酸(质量分数≥40%)均购自北京化工厂;无水甲醇(分析纯)和无水乙醇(分析纯)均购自北京试剂化学公司;乙腈(色谱纯)购自中国Amthyst Chemicals公司。实验用水为去离子水。色谱柱:COSMOSIL C18反相色谱柱(200 mm×4.6 mm, 5 μm)。将载玻片裁成76 mm×8 mm×1 mm大小,并用纯水超声清洗,浸泡在H2SO4-H2O2(7∶3, v/v)混合液中24 h,后用去离子水洗涤3次,用氮气吹干,得到亲水化载玻片。将厚度约为1 mm的聚酯薄膜(PET)裁剪成75 mm×8 mm大小。
1.2 MIPHs的制备
利用垂直沉降自组装的方法制备蛋白石结构模板。将粒径为260 nm的单分散SiO2微球均匀分散到无水乙醇中,配制成2%(质量分数)的胶体分散体系。将亲水化载玻片基质插入SiO2溶液中,采用垂直自组装的方式,将其置于电热恒温鼓风干燥箱(30 ℃)。待乙醇挥发完毕,制备得到蛋白石结构的光子晶体模板。
将0.15 mmol三聚氰胺(19.92 mg)、14 mmol MAA(1 200 μL)、0.50 mmol EGDMA(100 μL)溶于2.0 mL甲醇-水(3∶2, v/v)中,配制成预聚液,超声1 h使其充分混合,再通氮气10 min以除去氧气。然后向预聚液中加入20 mg引发剂AIBN,超声10 min,取蛋白石光子晶体模版,在表面覆盖一层75 mm×8 mm PET,形成下层为载玻片,中间为蛋白石光子晶体模板,上层为PET的结构。将预聚合溶液采用后填充技术均匀铺满膜片与光子晶体的空隙。然后在365 nm紫外灯照射下紫外引发聚合3 h。
将上述聚合得到的光子晶体膜在质量浓度为1%的氢氟酸中浸泡12 h,去除SiO2颗粒,得到反蛋白石结构的MIPHs。采用甲醇-乙酸(3∶2, v/v)作为洗脱剂,将MIPHs置入洗脱剂中振荡1 h,重复此步骤3次,以充分洗脱模板分子三聚氰胺。制备得到的MIPHs在去离子水中保存备用。非分子印迹光子晶体水凝胶(non-molecularly imprinted photonic crystal hydrogels, NIPHs)制备方法除在预聚液中不加三聚氰胺外,其他步骤与上述方法相同,过程见图1。
1.3 实际样品的制备及检测方法
奶粉样品提取:称取2 g奶粉,加入6 mL去离子水充分溶解,分4次加入4 mL乙腈,同时振荡30 s,全部加完后充分振荡5 min,以8 000 r/min的速度离心10 min,取上清液。于50 ℃用氮气吹干,用6 mL去离子水溶解沉淀物,得到待测溶液。
色谱条件为流动相:乙腈-0.01 mol/L pH 3.3庚烷磺酸钠溶液(1∶9, v/v);流速:1.0 mL/min;检测波长:240 nm;柱温:室温;进样量:10 μL。
1.4 三聚氰胺MIPHs的表征
MIPHs的形貌用扫描电镜进行观测。将MIPHs分别浸入浓度为10-11~10-6mol/L的待测溶液中,待稳定后,取出MIPHs,使用紫外-可见分光光度计测定其紫外-可见吸收光谱,并记录最大布拉格衍射峰波长。
2 结果与讨论
2.1 MIPHs的制备及检测原理
制备蛋白石光子晶体模板是将载玻片以一定角度插入SiO2微球-乙醇胶体分散液,在微球颗粒毛细管力和乙醇蒸发所形成弯曲液面的表面张力作用下,SiO2微球会在玻璃基片上发生有序自组装,形成规则排列的蛋白石结构[23]。分子印迹光子晶体薄膜对目标物的检测原理符合布拉格衍射定律。三维大孔结构的布拉格衍射方程为:
(1)


图 2 (a)光子晶体模板与(b)MIPHs的扫描电镜图Fig. 2 SEM images of (a) the photonic crystal template and (b) MIPHs
2.2 MIPHs制备条件优化
在极性环境下,以MAA为功能单体制备的水凝胶具有较好的分子识别能力及较宽的布拉格衍射峰位移,MAA可与模板分子形成较强的静电相互作用和疏水相互作用,MAA可与三聚氰胺的氨基氢原子相互作用形成氢键。EGDMA具有较好的亲水性,有利于水凝胶膜的形成。预聚液中水能够影响聚合物的孔和表面积,水的量可能干扰氢键的形成和疏水相互作用,当水分质量分数低于10%时,氢键发挥重要作用。当水分质量分数超过65%时,疏水性相互作用是主要的影响[21],为了提高MIPHs在水中的识别能力,以及考虑到三聚氰胺的溶解度,保证有足量的功能单体参与反应,确保结合位点充分形成,考察了制孔剂甲醇和水的体积比(7∶3, 3∶2, 1∶1, 2∶3),最终选择甲醇-水(3∶2, v/v)为最佳致孔溶剂,此时MIPHs具有优良的性质。
单体与交联剂的比例对MIPHs的三维结构、强度、溶胀性能具有较大影响,交联剂EGDMA含量对MIPHs形貌影响较大。考察了功能单体和交联剂摩尔比为20∶1, 24∶1, 28∶1, 32∶1时制备的MIPHs的形貌和传感性能。当交联剂含量较少时,膜的机械强度较差,膜易破碎,从SEM图可以看出连接处会发生断裂(见图3a);若加入过多的交联剂,膜的溶胀性能降低,表面会发生团聚,不能形成规整的有序排布大孔结构(见图3c),不能获得有效光学信号。因此确定功能单体和交联剂最佳摩尔比为28∶1,此时制得的MIPHs形貌如图3b所示,MIPHs具有均匀规整的三维大孔结构,且表面平整,有利于获得重复性好且稳定的光学信号。

图 3 不同MAA/EGDMA物质的量比下制得MIPHs的SEM图Fig. 3 SEM images of MIPHs prepared using different amount of substance ratios of methacrylic acid (MAA)/ethylene glycol dimethacrylate (EGDMA)Amount of substance ratios of MAA/EGDMA: (a) 24∶1; (b) 28∶1; (c) 36∶1.
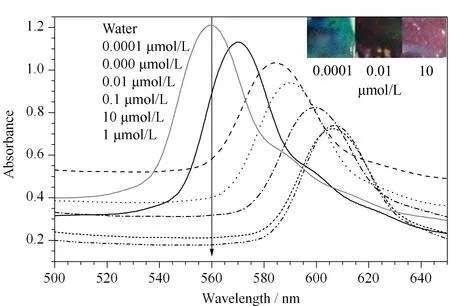
图 4 MIPHs的传感性能及颜色变化Fig. 4 Sensing abilities and color changes of MIPHs
2.3 MIPHs对三聚氰胺及其结构类似物的检测
对MIPHs和NIPHs对三聚氰胺的响应情况进行了考察。分别将MIPHs和NIPHs浸入浓度为10-11~10-6mol/L的三聚氰胺水溶液中,测定其布拉格衍射峰变化。如图4所示,去离子水中MIPHs衍射峰为563 nm,随着三聚氰胺浓度增大,MIPHs衍射峰逐渐红移,最大为608 nm,同时膜的颜色由绿变红。当把NIPHs浸入三聚氰胺溶液中,衍射峰位移变化不明显。这表明三聚氰胺印迹的MIPHs对于三聚氰胺有特异性识别作用,并且可以通过颜色变化以及光学信号分析的途径对样品中是否含有三聚氰胺进行快速识别定性。作为对照,NIPHs由于不含有与三聚氰胺的结合位点,对三聚氰胺的结合为非特异性结合,结合量较少,所以在含有三聚氰胺的样品中衍射峰位移变化很微小。采用紫外可见分光光度仪检测衍射峰位移变化,在0.000 1 μmol/L三聚氰胺溶液中,MIPHs衍射峰即开始发生位移。若用裸眼观测,0.01 μmol/L三聚氰胺溶液可以引起表观颜色变化(见图4)。则此MIPHs的检出限估算为0.01 μmol/L,因此不论是使用紫外可见分光光度仪还是仅用裸眼观测的检出限均低于卫生部公告中的限量值,即婴儿配方食品中三聚氰胺的限量值为1 mg/kg,其他食品中三聚氰胺的限量值为2.5 mg/kg[24]。
为了进一步考察MIPHs对三聚氰胺的特异性识别能力,进行了MIPHs的选择性试验。以入双氰胺、三聚氰酸、丙烯酰胺作为三聚氰胺的结构类似物,将MIPHs分别浸入不同浓度的双氰胺、三聚氰酸、丙烯酰胺的标准溶液中,并测定它们布拉格衍射峰的变化,每个浓度下重复测量5次,取平均值,测量最大偏差不超过2.5 nm。从图5可以看出,MIPHs对结构类似物及NIPHs对三聚氰胺均无响应,这表明制备的MIPHs对三聚氰胺具有较高的选择性和灵敏度,可以用于样品中目标物的特异性识别分析。

图 5 MIPHs的选择性(n=5)Fig. 5 Selectivities of MIPHs (n=5)DCD: dicyanamide; AM: acrylamide; CYA: cyanuric acid.
2.4 MIPHs的动力学及重复利用性
本研究所制备的MIPHs具有三维孔洞网状结构,有着很高的比表面积,可以为待测分子提供充分的结合位点。同时因为孔状结构有利于分子扩散,所以待测物质分子可以快速、高效与选择性识别位点结合。如图6a所示,在10-9mol/L的三聚氰胺水溶液中,MIPHs的最大衍射峰位置可以在45 s左右达到平衡,具有快速响应的特性。
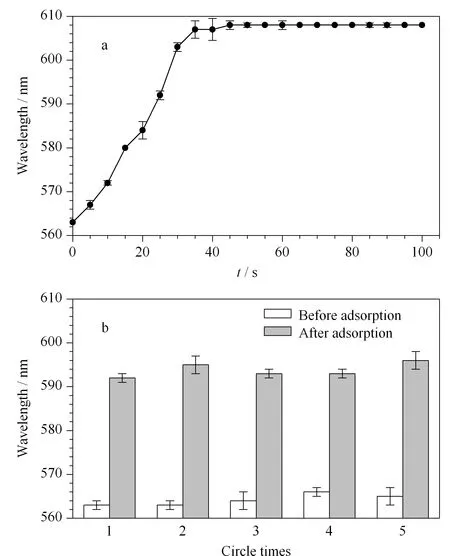
图 6 MIPHs的(a)响应速度和(b)重复性(n=5)Fig. 6 (a) Responding speeds and (b) recover abilities of MIPHs (n=5)
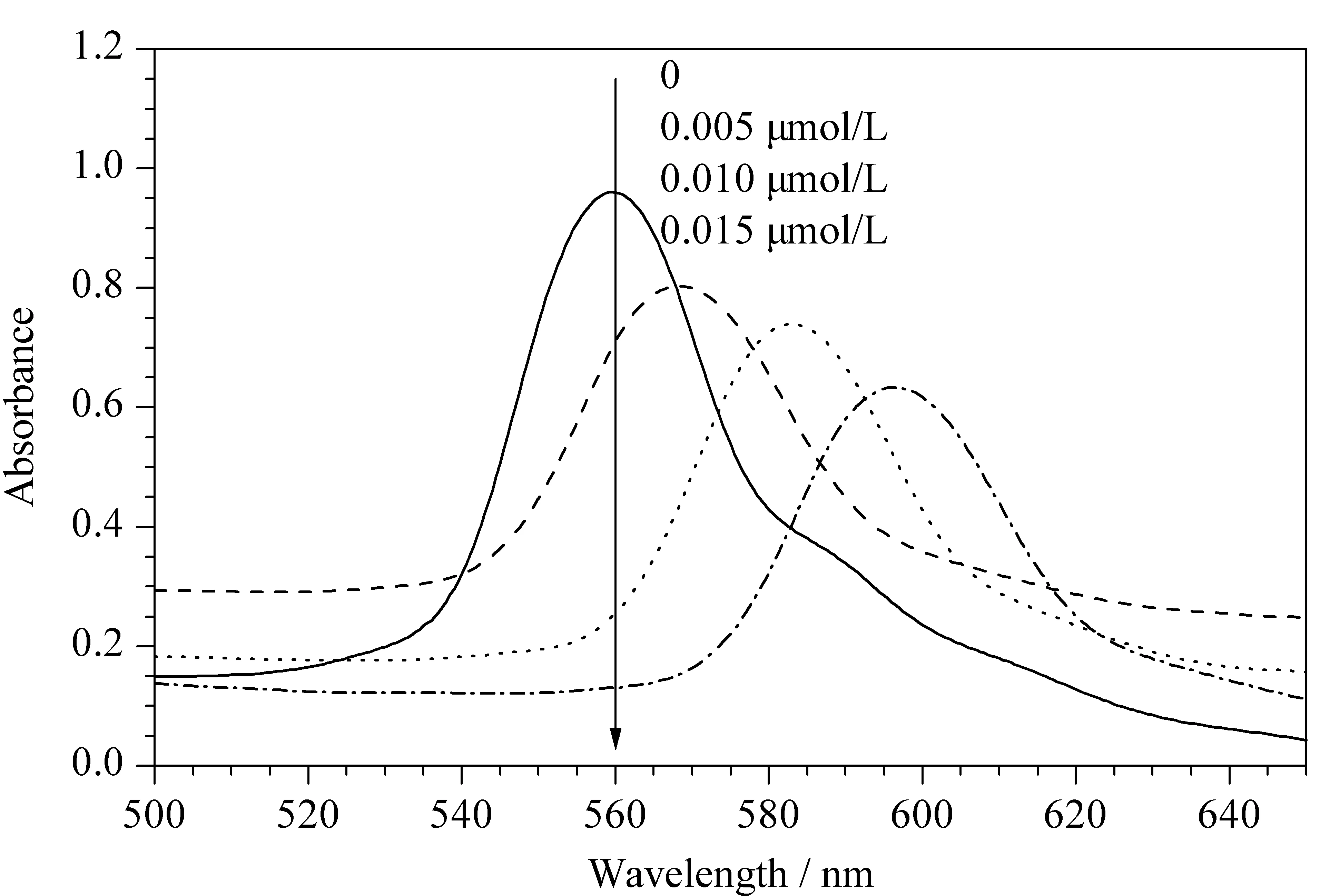
图 7 MIPHs在奶样品中的传感性能Fig. 7 Sensing abilities of MIPHs in a milk sample
由于MIPHs是高度交联的聚合物,具有良好的物理稳定性和化学稳定性。MIPHs与待测分子是非共价作用结合的,可以用乙酸-甲醇(2∶3, v/v)进行洗脱,然后在去离子水中平衡,恢复到空白状态。试验对制备的MIPHs的重复利用率进行了测试,在5次洗脱/吸附循环中,利用同一个MIPHs对10-9mol/L的三聚氰胺水溶液进行反复测定,结果如图6b所示,在重复使用5次后,MIPHs对三聚氰胺仍有着良好的识别能力,表明MIPHs具有很好的稳定性和重复利用性,满足实际使用时多次实验分析的需要。
2.5 MIPHs在奶制品中的传感性能
对MIPHs在奶制品中的传感性能进行了考察。奶制品采用上述2.3节方法进行处理,并采用HPLC进行分析,检测结果表明样品中不含三聚氰胺。MIPHs在空白奶制品溶液中无明显响应,这表明MIPHs在奶制品中具有良好的抗干扰能力。将处理后的奶制品溶液加入三聚氰胺,使三聚氰胺浓度为0.005、0.01和0.015 μmol/L,再将MIPHs加入进行检测,MIPHs的布拉格衍射峰逐渐红移(见图7),颜色由绿变红。三聚氰胺MIPHs在奶制品中仍具有高选择性和高灵敏度的响应能力,这表明此传感器具有良好的实用性能。
3 结论
本文制备了MIPHs,并作为三聚氰胺的光学传感器,实现样品中三聚氰胺快速识别分析。这种传感器成本低廉、操作简单,并具有灵敏度高、选择性好、响应快、检测时间短的特点,可以用于样品中痕量三聚氰胺的快速识别,检出限低于卫生部[24]公告中的限量值。此外,由于MIPHs有明显颜色变化,可对三聚氰胺进行裸眼识别,从而快速定性检测,进一步降低了检测成本和操作要求,满足对一些样品快速定性分析的要求。制备的MIPHs还具有稳定性高,重复利用性好的优点,可以作为一种有效工具用于食品中有害成分或环境污染物的快速分析检测。
