高效液相色谱法测定人血浆中阿托伐他汀的浓度
2019-03-08封永莉欧亚青张丽娟童荣生
封永莉,欧亚青,边 原,张丽娟,陈 岷,陈 璐,童荣生
(1.电子科技大学医学院,个体化药物治疗四川省重点实验室,四川 成都 610072;2.四川省医学科学院·四川省人民医院药学部,四川 成都 610072)
阿托伐他汀为临床广泛使用的降脂药,口服吸收快,在肝细胞中代谢,通过抑制羟甲基戊二酰辅酶 A还原酶(HMG-CoA)而发挥药理作用,可以减少内源性胆固醇在肝脏的合成,从而降低总胆固醇及外周血中的低密度脂蛋白胆固醇(LDL-C),同时阿托伐他汀还具有稳定斑块的作用。临床上,阿托伐他汀主要用于治疗高胆固醇血症、冠心病、外周动脉粥样硬化疾病[1]。有文献显示阿托伐他汀的代谢过程易受细胞色素P450(CYP)3 A4和有机阴离子转运多肽(OATP)C和P-糖蛋白的影响,加之首过效应明显,临床实际应用疗效差异较大,可见不良反应[2]。临床上使用阿托伐他汀发生的不良反应以胃肠消化系统和骨骼肌肉系统受损为主,如恶心、肝酶的升高、横纹肌溶解等[3],针对患者可能存在的高危风险因素(如肝损、高龄、体型瘦小、甲状腺功能减退、合并使用具有相互作用药物等情况),有必要通过监测阿托伐他汀血药浓度,结合药动药效学理论,以建立适当的剂量方案,减少不良反应并维持降脂效果[4]。故本实验建立一种简便快捷的高效液相色谱法(HPLC)测定人血浆中阿托伐他汀的浓度,以用于下一步阿托伐他汀特殊人群药代动力学研究,对给出临床个体化用药方案具有重要意义。
1 材料
1.1仪器Waters 2690高效液相色谱仪(美国Waters 公司)、BP211D电子天平(德国Sartori μs公司)、优普UPR-II-5 T超纯水器(成都超纯科技有限公司)、高速离心机320R(德国Hettich公司)。
1.2试剂阿托伐他汀(Solarbio公司,批号:308A021,含量≥98%,标准品)、醋酸铵(科密欧公司,含量≥98.0%)、冰醋酸(诺尔施,含量99.5%)、乙腈(Fisher公司,含量99.97%)、甲醇(Dikma公司,含量99.9%),使用溶剂均为色谱级。
2 方法与结果
2.1色谱条件采用Aglient Eclipse HPLC色谱柱(150 mm×4.6 mm,5 μm);流动相条件:乙腈:0.02 mol/L醋酸铵缓冲溶液(冰醋酸调至pH=5.2)=40:60;柱温:30 ℃,流速:1 ml/min;进样量:20 μl;检测波长:245 nm。
2.2溶液配制精密称取阿托伐他汀标准品适量,用甲醇∶水(90∶10)的溶剂定容于10 ml的容量瓶,即得1.445 mg/ml阿托伐他汀贮备液。从贮备液中取1 ml,用上述溶剂定容于10 ml的容量瓶,即得144.5 μg/ml的阿托伐他汀工作液,放入4 ℃冰箱保存。
2.3样品处理取阿托伐他汀工作液20 μl,加入200 μl血浆,涡旋1 min后加入乙腈400 μl,涡旋3 min,14000 r/min离心7 min,取上清液进样。
2.4方法的专一性考察阿托伐他汀标准溶液后,取空白血浆和含阿托伐他汀的血浆样品及某病人血浆,按照“2.3”项下方法处理,进样检测记录色谱图,结果见图1。阿托伐他汀出峰时间为7.5 min,此时检测专一性好,与生物内源性物质分离,无杂质干扰,且色谱峰型对称。

图1 阿托伐他汀色谱图 a:阿托伐他汀标准溶液;b:空白血浆;c:阿托伐他汀的血浆;d:某病人血浆
2.5线性关系考察取阿托伐他汀144.5 μg/ml工作液20 μl,用甲醇∶水(90∶10)的溶剂依次等比例稀释后,取适量加入血浆样本200 μl,得系列浓度为14.45、8.76、5.20、3.13、1.87、1.12、0.67、0.41 μg/ml的血浆样品,按照“2.3”项下方法处理后。以阿托伐他汀的质量浓度(X)为横坐标、峰面积(Y)为纵坐标,计算回归直线(采用加权最小二乘法),得到回归直线方程为Y=1.54×104X-5130(R2=0.9993),表明阿托伐他汀在0.41~14.45 μg/ml范围内线性关系良好,定量限为0.41 μg/ml。
2.6准确度与精密度取适量阿托伐他汀工作液,加入适量空白血浆得到0.64、3.03、12.89 μg/ml低、中、高浓度的阿托伐他汀血浆质控样品,按照“2.3”项下方法处理后,每日每个浓度连续进样6 份,连续测定3 d,用当日制得随行标准曲线计算各浓度值,考察准确度和精密度。结果如表1,阿托伐他汀血浆质控样品日内和日间的RSD 均小于10% (n=6)。
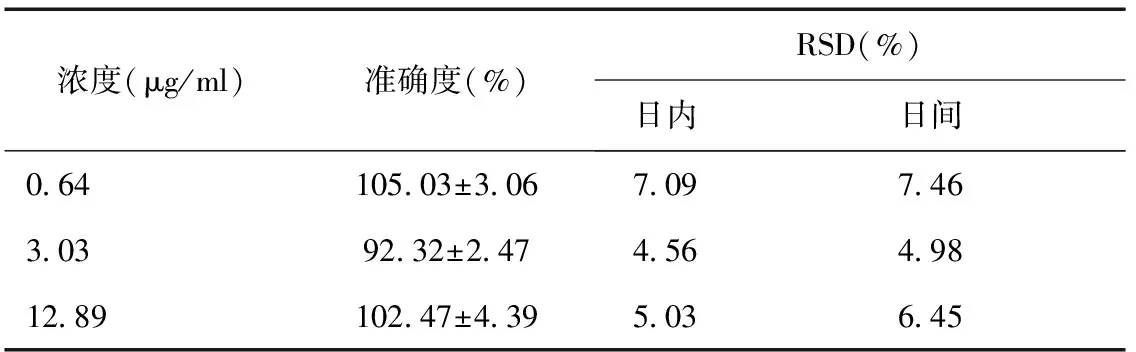
表1 精密度与准确度(n = 6)
2.7提取回收率
2.7.1相对提取回收率 将配制好的0.64、3.03、12.89 μg/ml低、中、高浓度的阿托伐他汀血浆样品,按照“2.3”项下方法处理后,每个浓度连续进样6 份,测定得峰面积A;另取空白血浆200 μl,按照“2.3”项下方法处理后,加入适量阿托伐他汀工作液,制成质量浓度为0.64、3.03、12.89 μg/ml的低、中、高浓度的阿托伐他汀血浆样品,每个浓度连续进样6 份,测定得峰面积B;用A/B的值表示相对提取回收率。结果可见表2,符合中国药典生物样品分析方法的要求。
2.7.2绝对提取回收率 另取阿托伐他汀工作液,加入流动相(乙腈:0.02 mol/L 醋酸铵缓冲溶液(冰醋酸调pH=5.2)=40:60)溶液稀释至质量浓度为0.64、3.03、12.89 μg/ml的低、中、高浓度的阿托伐他汀溶液,每个浓度连续进样6 份,测定得峰面积C;用A/C的值表示绝对提取回收率,见表2。符合中国药典生物样品分析方法的要求。
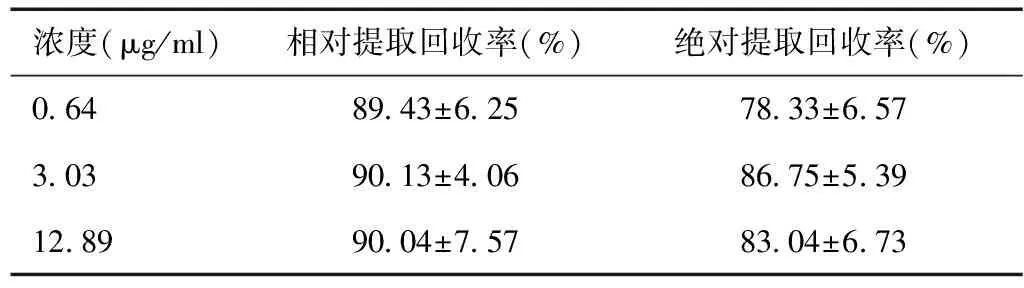
表2 提取回收率(n = 6)
2.8残留效应在高浓度质控样品进样后,再以空白血浆进样,考察残留效应。结果显示,空白血浆中无阿托伐他汀响应出现。
2.9稳定性考察阿托伐他汀工作液在1、2、3、5、7 d的稳定性,考察含有低、中、高浓度的阿托伐他汀血浆样品在室温放置4 h、4 ℃冰箱保存1、2、3、5、7 d 及反复冻融3次的稳定性,每时按照“2.3”项下方法处理,每个浓度连续进样6 份,测定其浓度用以评价该方法的稳定性。结果显示,上述条件下的RSD 均小于10%,符合生物样品分析方法要求。
3 讨论
阿托伐他汀具亲脂性,易溶于甲醇、乙醇,极微溶于水,故本实验选用甲醇∶水(90∶10)的比例溶液作为溶剂,阿托伐他汀在该溶液保存下溶解性及稳定性均良好。由于阿托伐他汀含有开环羟基酸结构,故显弱酸性,其对pH敏感,有文献显示他汀类药物及其代谢产物易发生内脂结构和开环结构的互变现象,pH>6时促进离子形式下的互变现象,相反,pH降低时促进非离子形式下的互变现象[5],所以液相条件摸索的关键在于确定流动相的pH值,大多文献采用流动相pH在4~5.5范围内,并多用到甲酸铵、醋酸铵溶液[6~9]。还有文献指出阿托伐他汀甲醇中的稳定性比乙腈低[10]。为了寻找合适的流动相比例及pH值,该实验在摸索过程中扩大比较了pH在3.5~7.5范围内的水相条件,以及乙腈比例在35%~60%范围内阿托伐他汀的保留时间及峰型,实验发现pH值增高和/或乙腈比例提高都能够显著地减少保留时间,最终本实验采用Aglient 的中等长度色谱柱(150 mm×4.6 mm,5 μm),在流动相比例为乙腈:0.02 mol/L 醋酸铵缓冲溶液(冰醋酸调pH=5.2)= 40∶60条件下进行,用冰醋酸调低pH值是为了有效抑制阿托伐他汀的解离,使其更多以分子形式存在,这将有助于阿托伐他汀与内源性物质区分并且峰对称性好,无拖尾,基线无干扰,保留时间为7.5 min,也利于临床快速开展监测。该实验使用的高效液相色谱法连接的是紫外检测器,通过观察阿托伐他汀在保留时间范围内的全波长扫描结果,发现检测波长为245 nm时阿托伐他汀响应最大,故采用245 nm作为检测波长。此外,为了建立简便快速的样本前处理方法,本实验比较了甲醇、乙腈直接沉淀法和二氯甲烷、乙酸乙酯液-液萃取等多种处理方法,发现相比复杂的萃取过程,单纯使用1:2比例的乙腈沉淀蛋白,既能去除内源性物质的干扰,又简便、快速、准确,可用于日常阿托伐他汀的血药浓度监测。该方法采人血浆量少,专一性强,简便快捷,适用推广于阿托伐他汀特殊人群血药浓度监测、药代动力学及其相关性研究。
