HS-GC/MS法分析乌龙茶挥发性成分
2019-03-08黄旭建易国春许思敏郭雅玲
王 蔚,黄旭建,易国春,许思敏,郭雅玲
福建农林大学园艺学院,福州 350002
乌龙茶属半发酵茶,因其具有丰富多样而又独特的花果香,深受消费者喜爱。茶叶的香气作为茶叶品质鉴定的重要因子之一,密切影响茶叶品质等级的划分,其品质评价和组成成分的分析一直是茶叶科研领域的一项重要课题。为了客观系统的检测乌龙茶的挥发物以进行产地判别,真伪判别,香型归类,运用仪器辅助检测乌龙茶挥发物意义重大。气相色谱质谱联用技术(GC-MS)是气相色谱高分离和质谱高灵敏性能的结合,广泛应用于复杂样品组分的分离与鉴定,可对样品中风味物质的种类和含量进行检测。目前已有不少研究者采用GC-MS对不同季节不同工艺加工而成的乌龙茶[1,2]以及不同产地[3]、不同品种[1]等的乌龙茶挥发物进行了研究。
茶叶的香气成分较为复杂,在客观量化测定茶叶香气方面,选择适当的提取技术是分析香气的前提与基础[4]。目前提取挥发物的方法有很多,最常用的为同时蒸馏萃取法(SDE)、固相微萃取法(SPME)、顶空进样法(HS)。顶空法(Headspace,HS)按挥发性组分的提取方式不同,可分为静态法(Static)和动态法(Dynamic)两类。其中静态顶空法(Static headspace,SHS) 是将具有挥发性的样品置于密闭样品瓶中,保持恒定温度,使其上部(顶空)的气体与样品中的组分达到相平衡,抽取上部的气体进行GC分析,在该平衡过程中,平衡温度、平衡时间、加样量等都会对其产生影响。虽然HS提取的挥发物种类和数量没有SPME和SDE法多,但它是一种简单、环保、有效的样品前处理方法,操作过程中不用其他试剂,避免假象现象的产生,因其容易实现全自动化,可将人为因素带来的误差降至最低,同时HS直接抽取茶样顶空的气体进行分析,所得到的香气成分与人体嗅觉所感觉到的气味最接近[4],所以最易普及、适合推广使用。目前顶空进样法在酒类、水质、药材等挥发物检测中都应用广泛。
基于此本试验以金观音(乌龙茶)为材料,通过对比试验,优化了影响静态顶空-气质联用(SHS-GC/MS)灵敏度的主要因素,确定了平衡温度、平衡时间、茶/NaCl 、加样量等较佳的样品前处理方法参数,建立了乌龙茶香气物质的可靠分析方法。在对所建立方法进行稳定性考察后,将其应用于金观音挥发性成分的分析,以期为乌龙茶天然香气成分的开发和利用、判别产地、鉴定真伪提供科学依据。
1 实验部分
1.1 材料
选取 2016 年春季平和金观音(茗科1号)毛净茶,磨碎,过 40 目筛,装于铝箔袋,密封备用。
1.2 试剂与仪器
NaCl(上海国药集团化学试剂有限公司;分析纯,≥ 99.5%),实验用水皆为蒸馏水。
Clarus SQ8T 型气质联用仪、Elite-FFAP色谱柱(30 m×0.25 mm×0.25 μm)、Turbo Matrix 40 Trap自动顶空进样器、20 mL顶空瓶(美国 Perkin Elmer 公司) ;电子分析天平(梅特勒-托利多仪器(上海)有限公司;0.000 1 g);WK-400B高速药物粉碎机(山东青州市精诚机械有限公司);40目标准检验筛(上虞市银河测试仪器厂);实验室超纯水器(科尔顿水务有限公司);KQ-600KDE型高功率数控超声波清洗机(昆山市超声仪器有限公司);电热恒温鼓风干燥箱(上海精宏实验设备有限公司)。
1.3 试验方案设计
顶空分析法中,平衡温度、平衡时间、茶/NaCl(茶粉质量与饱和NaCl水溶液体积之比)以及加样量均会影响顶空进样的测试结果,故把这4个因素同时作为考察因素,并采用单因素试验方案,分别研究平衡时间与平衡温度对乌龙茶挥发物测定结果的影响,确定其较优水平变化范围后,采用正交试验优化并确定乌龙茶挥发物的最佳顶空分析条件。
1.3.1 单因素试验设计
本台气质联用仪在加水的样品处理条件下,平衡温度(炉温)范围为40~80 ℃,故选用此范围的炉温首先进行单因素优化。
根据前人[5]实验结果及预实验结果,本试验将平衡时间范围设定为15~90 min,进行单因素试验。
1.3.2 正交试验影响因素及水平的选择
本试验选用4因素3水平9次实验的正交试验表 L9(34)。
根据单因素试验(图1和图2)筛选出较优的平衡温度与平衡时间变化范围,分别选择3个水平,其中平衡温度包括60、70、80 ℃,平衡时间包括45、60、75 min。
利用盐离子效应减少被分析物(有机物)在水溶液中的可溶性,能使更多的挥发性物质挥发至顶空,从而降低该方法的检测限,提高香气物质的响应值[6]。窦洪亮实验结果为[6]以加入饱和 NaCl(0.32 g/mL)为最佳。 故本试验以饱和 NaCl水溶液代替纯水与茶粉混合,进行试验。
加样量的多少直接影响挥发性成分的含量,进而影响吸附量;吸附过少,影响检测效果;吸附过多,超出仪器检测范围,则会影响谱库匹配结果[7];由于顶空瓶的体积为 20 mL,并且试验体积不宜超过顶空瓶体积的 20%[8]。吕海鹏等[5]研究发现当茶水比在 1∶3 时,样品挥发成分色谱峰强度较高且峰数量较多,样品挥发成分在顶空的平衡也较快。故经过反复预实验,本试验考察了 20 mL顶空瓶中不同样品装载质量 (0.5~1.5 g) 以及不同茶/NaCl(1∶2~1∶4)对出峰个数和总峰面积的影响。
正价表设计如下,其影响因素和水平见表1。
1.4 HS方法
准确称取一定质量的茶粉(精确至0.000 1 g)于20 mL顶空瓶中,加入一定比例的溶于蒸馏水的饱和NaCl溶液,用配有聚四氟乙烯垫的密封盖密封,设置好顶空参数,将密封的顶空瓶放入自动进样器等待进样。

表1 正交试验因素与水平
注:A:平衡温度;B:平衡时间;C:茶/NaCl;D:加样量。
Note:A:extraction temperature(equilibrium temperature);B:extraction time;C:tea/NaCl;D:sample amount.
1.5 仪器条件
1.5.1 顶空条件
炉温40~80 ℃(以10 ℃ 递增),取样针温度100 ℃,传输线温度120 ℃,样品平衡时间15~90 min(以15 min递增),捕集阱Hi 280 ℃,Lo 40 ℃,保持5 min,干吹1 min,解析0.5 min,顶空瓶压力40 psi,色谱柱压力12 psi,解析压力15 psi,顶空出口分流。
1.5.2 GC -MS条件
升温程序: 50 ℃保持5 min,以3 ℃/min升至125 ℃,保持2 min,以5 ℃/min升至180 ℃,保持3 min,以15 ℃/min升至230 ℃,保持5 min。载气为高纯度 He(99.999%)。
1.5.3 质谱条件
电子轰击(EI)离子源,电子能量70 eV;离子源温度230 ℃,质谱传输线温度250 ℃,质量扫描范围m/z45~500。
1.6 稳定性考察
取金观音茶样0.5 g,重复3次,按最终的优化参数进样,得到结果后,分别考察各物质的出峰时间与峰面积的相对标准偏差(RSD)。
1.7 数据分析
通过检索 NIST 2011在线质谱数据库,核对质谱匹配度并参考相关文献资料[1,3,9-11,13],然后再从特征离子、实际成分、保留指数等方面,分别对各峰所代表的挥发性物质的化学结构和名称加以确认。其相对含量采用峰面积归一法分析,即以各香气组分的峰面积占总峰面积之比值表示组分相对含量。
采用Excel对数据进行极差分析,采用SPSS 21对数据进行方差分析。
2 结果与分析
2.1 单因素试验结果
2.1.1 平衡温度对挥发物总峰面积与出峰个数的影响
样品平衡温度的适当增加,能加快待测组分的运动,促进富集过程进行,有助于加快液体与气相空间目标物的平衡速度,同时可减小目标物在液体中的溶解度[14]。但过高的温度会影响待测物在气相与涂层间的分配系数,反而不利于萃取的平衡[7]。取1g茶粉,加入3 mL 饱和的NaCl溶液,平衡时间固定为60 min,分别考察平衡温度为40、50、60、70、80 ℃时挥发物的出峰个数与总峰面积。结果如图1所示,随着平衡温度的升高,挥发物出峰个数与总峰面积均大幅度上升,其中60 ℃前总峰面积增势较缓,60 ℃以后增势迅猛,相比70 ℃的挥发物总峰面积,80 ℃的总峰面积增加了164.46%,故选择60、70、80 ℃继续进行正交试验。

图1 平衡温度对挥发物总峰面积与出峰个数的影响Fig.1 Effect of equilibrium temperature on total peak area and peak number of volatile compounds
2.1.2 平衡时间对挥发物总峰面积与出峰个数的影响
平衡时间直接影响萃取达到平衡,平衡时间短,则吸附不完全;平衡时间过长,则吸附组分可能发生解吸[7]。取1 g茶粉,加入3 mL饱和的NaCl溶液,平衡温度固定为80 ℃,分别考察平衡时间为15、30、45、60、75、90 min时挥发物的出峰个数与总峰面积。结果如图2所示,平衡时间的变化对出峰个数影响不大,各个平衡时间出峰个数均在76个左右,这与前人的研究结果相同[15]。平衡时间的变化对总峰面积影响较大,在15~90 min,随着保留时间的延长,总峰面积呈现先增加后降低的变化趋势,并在60 min时达到最大值。在该单因素试验中,平衡时间为45、60、75、90 min的挥发物总峰面积较大,因平衡时间为90 min的总峰面积相较平衡时间为45 min的总峰面积增加了14.63%,相差不大,且考虑到平衡时间过长影响效率,故选择45、60、75 min进行正交试验。
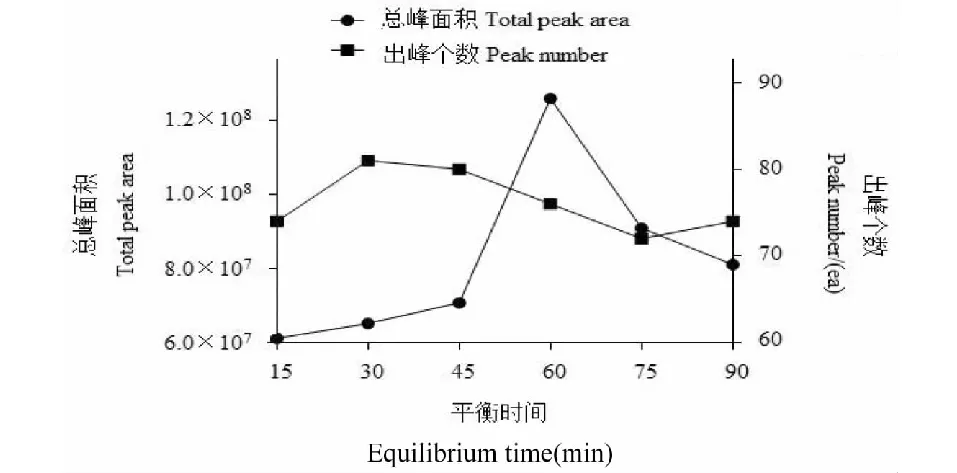
图2 平衡时间对挥发物峰面积与出峰个数的影响Fig.2 Effect of equilibrium time on total peak area and peak number of volatile compounds
2.2 正交试验结果
根据单因素试验的结果,本试验选用的4因素3水平9次实验的正交试验表 L9(34),其结果如表2所示。
2.2.1 正交试验极差分析
正交试验对出峰个数和总峰面积影响的极差分析见表 3,由表3极差(R 值)分析结果可以看出,不论以出峰个数还是总峰面积为考察指标,各因素对萃取效果影响的大小顺序均为平衡温度(A)>茶/NaCl(C)>加样量(D)>平衡时间(B)。当以出峰个数为考察指标时,各因素水平对于峰个数影响力排序依次为A1(80 ℃)>A2(70 ℃)>A3(60 ℃),B2(60 min)>B3(45 min)>B1(75 min),C1(1∶2)>C2(1∶3)>C3(1∶4),D1(1 g)>D2(0.5 g)>D3(1.5 g),较优组合为80 ℃、60 min、1∶2、1 g (A1B2C1D1)。当以总峰面积为考察指标时,各因素水平对于峰面积影响力排序依次为A1(80 ℃)>A2(70 ℃)>A3(60 ℃),B2(60 min)>B1(75 min)>B3(45 min),C1(1∶2)>C2(1∶3)>C3(1∶4),D2(0.5 g)>D1(1 g)>D3(1.5 g),较优组合为80 ℃、60 min、1∶2、0.5 g (A1B2C1D2)。可见极差分析中分别以出峰个数和总峰面积为考察指标时,分析得出的较优组合在D因素(加样量)之间略有差异,该差异将与正交试验结果相比对并进行综合分析。

表2 正交试验结果

表3 正交试验对峰个数和总峰面积影响的极差分析
2.2.2 正交试验方差分析
正交试验对出峰个数和总峰面积影响的方差分析(采用邓肯法进行多因素方差分析)分别见表4与表5,可以看出当以出峰个数为考察指标时,因素A与C对金观音挥发物出峰个数分别有极显著与显著影响,因素B、D对其无显著影响。A因素水平影响力排序依次为A1(80 ℃)>A2(70 ℃)>A3(60 ℃),A1、A2、A3彼此之间差异极显著;C因素水平影响力排序依次为C1(1∶2)>C2(1∶3)>C3(1∶4),C1与C2、C1与C3有显著差异,C2与C3无显著差异。因为B、D因素对金观音挥发物峰个数响应值无显著影响,可根据实际情况进行调整,故选择平均值最大的B2,以及平均值较大的D2(D1平均值为65.33,D2平均值为65.17,两者极为接近),最终得出峰个数因素与水平优化组合结果为80 ℃、60 min、1∶2、0.5 g (A1B2C1D2)。
当以总峰面积为考察指标时,4种因素对金观音挥发物总峰面积均有极显著影响。各因素水平影响力排序与极差分析结果相同。此外在A因素3个水平中,A1、A2、A3彼此之间差异极显著;在B因素3个水平中,B2与B1无显著性差异,而B2与B3、B1与B3均有极显著差异;在C因素3个水平中,C1与C2无显著性差异,而C1与C3、C2与C3均有极显著差异;在D因素3个水平中,D2与D1无显著性差异,而D2与D3、D1与D3均有极显著差异。峰面积因素与水平优化组合结果为80 ℃、60 min、1∶2、0.5 g (A1B2C1D2),与极差分析结果一致。

表4 正交试验对峰个数影响的方差分析
注:F0.05(2,9)=4.26 F0.01(2,9)=8.02;a.R2=0.913(调整R2=0.836)。
Notr:F0.05(2,9)=4.26 F0.01(2,9)=8.02;a.R2=0.913(AdjustedR2=0.836).
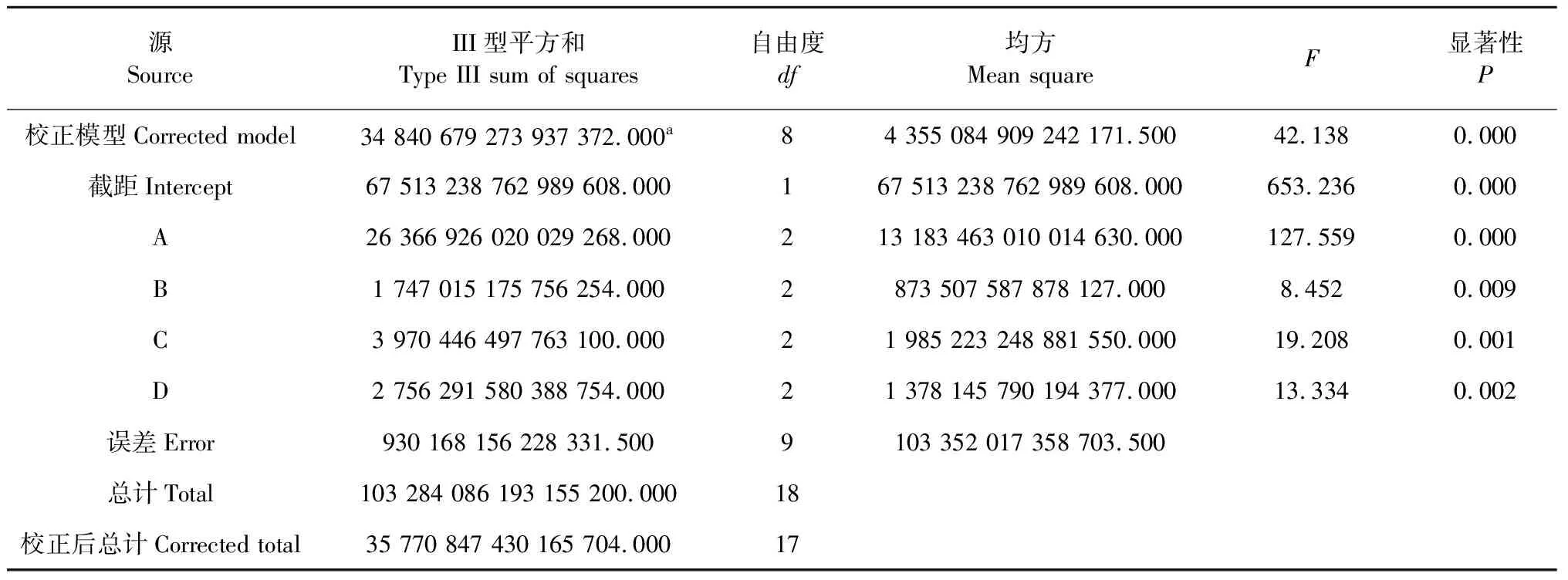
表5 正交试验对总峰面积影响的方差分析
注:F0.05(2,9)=4.26 F0.01(2,9)=8.02;a.R2=0.974(调整R2=0.951)。
Note:F0.05(2,9)=4.26 F0.01(2,9)=8.02;a.R2=0.974(AdjustedR2=0.951).
2.2.3 正交试验结果分析
根据正交试验的极差分析与方差分析,得出以金观音为代表的乌龙茶GC-MS顶空进样法的最优条件为A1B2C1D2,即平衡温度80 ℃,平衡时间60 min,茶/NaCl=1∶2,加样量0.5 g。
2.3 HS/GC-MS 方法学考察
为考察优化方法的稳定性,对金观音茶样进行3次重复取样,分别以优化的参数进样分析。结果表明,在3次重复中,各主要色谱峰保留时间的相对标准偏差 (RSD) 均≤1.0%,而各色谱峰峰面积的相对标准偏差,除了香叶基芳樟醇(69%),二十一烷为(25%)、2,5,5-三甲基-1-己烯-3-炔(25%)、未知-18(24%)、芳樟醇氧化物II(22%)、苯乙腈(21%)、alpha-柏木烯(20%)、1,3-cis,5-cis-Octatriene(19%)、未知-11(19%)、γ-松油烯(17%)、2-氨基苯甲酸-3,7-二甲基-1,6-辛二烯-3-醇酯(16%)、正庚醇(16%)RSD值较大外,其他挥发物的RSD值 均≤15%(相较于干茶,此RSD数值可能偏大,这是因为水溶液对挥发物总峰面积的RSD会有一定负影响,该结果与谭和平[16]茶汤RSD结果相似),但整体来说该方法的稳定性较好,符合检测方法的要求。
2.4 对最优萃取条件下金观音挥发物的考察
正交试验后,在选定的最优静态顶空进样条件下(平衡温度80 ℃,平衡时间60 min,茶/NaCl=1∶2,加样量0.5 g)进行挥发物提取与鉴定实验,由 GC-MS 分析得到的质谱数据经计算机在NIST 2011标准谱库中检索对物质进行初步定性,采用峰面积归一化法算出各成分的相对含量(组分峰面积占总峰面积的百分比)。金观音挥发物的总离子流色谱图如图 3 所示。
金观音香气成分经HS-GC/MS最佳分析条件提取进样分析,所得出峰个数为104个,总峰面积为128 759 897,结果与表 2 的结果相比较,较优组合出峰个数远远超过正交试验中的任何一个,且总峰面积也较多,由此可以看出最优组合对提取金观音香气成分效果更好。在所有检测到的挥发物中,共鉴定(完全鉴定与初步鉴定,鉴定标准见表6下方的注)出86种成分,占挥发物总量的97.48%,包括醇类(15种,32.56%)、碳氢类化合物(24种,14.72%)、醛类(10种,12.82%)、氧化物(7种,11.15%)、氯化物(2种,10.84%)、含氮化合物类(7种,9.91%)、酮类(10种,3.14%)、酯和内酯类(7种,1.59%)、硅氧烷(3种,0.46%)、酚类(1种,0.30%)。其中含量最高的前30种挥发物的定性结果与峰面积相对含量见表6。
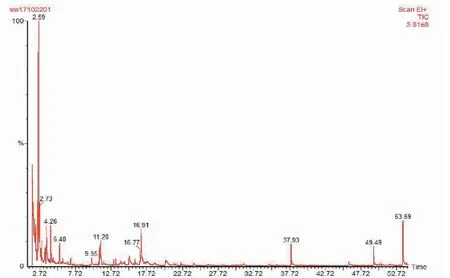
图3 金观音挥发物的总离子流色谱图Fig.3 Total ion current chromatogram of volatile components of JGY

保留时间Retention tim(min)化合物CompoundCAS峰面积Peak area(×106)定性结果Qualitative results2.60±0.011-戊烯-3-醇1-Penten-3-ol616-25-118.41±1.59∗1.71±0.01一氯甲烷Chloromethane74-87-312.70±0.91∗2.47±0.012-甲基丁醛2-Methylbutanal96-17-310.79±0.96∗1.82±0叔戊基胺2-Methylbutan-2-amine594-39-89.83±1.19ο3.67±0.02正戊醇Pentanol71-41-06.54±0.70∗3.71±0.02顺-2-戊烯醇cis-2-Penten-1-ol1576-95-06.54±0.70∗1.97±0.01甲基环氧丙烷Isobutylene oxide558-30-56.44±0.73ο16.95±0.03脱氢芳樟醇Hotrienol20053-88-75.48±0.45∗4.29±0.031,1,2,3-四甲基环丙烷1,1,2,3-Tetramethylcyclopropane74752-93-55.06±0.32ο
续表3(Continued Tab.3)

保留时间Retention tim(min)化合物CompoundCAS峰面积Peak area(×106)定性结果Qualitative results53.59±0.011-二十二烯1-Docosene1599-67-34.85±0.63ο2.74±0.012-乙基呋喃2-Ethylfuran3208-16-04.24±0.19∗2.40±0.013-甲基丁醛Isovaleraldehyde590-86-32.80±0.22∗37.94±0.01(Z,E)-a-法呢烯(Z,E)-a-Farnesene26560-14-52.40±0.09ο11.32±0.042-正戊基呋喃2-Amylfuran3777-69-31.61±0.23∗15.30±0.03芳樟醇氧化物II(呋喃型)Linalool oxide II34995-77-21.58±0.35ο3.02±0.01乙胩Isocyanoethane624-79-31.55±0.06ο11.16±0.04甲基庚烯酮6-Methylhept-5-en-2-one110-93-01.42±0.08∗5.53±0.032,5,5-三甲基-1-己烯-3-炔2,5,5-Trimethyl-1-hexen-3-yne37439-53-51.39±0.35ο2.15±0.01未知-1 Unknown-1-1.27±0.07-10.00±0.03苯甲醛Benzaldehyde100-52-71.27±0.10∗16.80±0.032-氨基苯甲酸-3,7-二甲基-1,6-辛二烯-3-醇酯3,7-Dimethylocta-1,6-dien-3-yl 2-aminobenzoate7149-26-01.27±0.21ο3.45±0.021-氯戊烷1-Chloropentane543-59-91.25±0.04ο16.11±0.04顺-Alpha,Alpha-5-三甲基-5-乙烯基四氢化呋喃-2-甲醇2-[(2R,5S)-5-Methyl-5-vinyltetrahydro-2-furanyl]-2-propanol5989-33-30.95±0.14∗20.35±0.03顺式-马鞭烯醇cis-Verbenol1845-30-30.75±0.03ο17.95±0.2苯乙醇Phenylethyl alcohol60-12-80.72±0∗49.51±0.01香叶基芳樟醇Geranyl linalool1113-21-90.72±0.50∗7.10±0.042-庚酮2-Heptanone110-43-00.68±0.06∗5.97±0.03顺-3-己烯醇cis-3-Hexen-1-ol928-96-10.58±0.02∗13.13±0.05D-柠檬烯D-Limonene5989-27-50.58±0.06∗3.92±0.022-甲基-1-己烯-3-炔2-Methylhex-1-en-3-yne23056-94-20.55±0.05ο
注:在搜索NIST 2011质谱库并与前人文献比较分析后,如果该物质匹配度 > 750(总值为1000),且匹配度最高的物质与匹配度第二高的物质匹配度差值>100,则将匹配度最高的物质定义为完全鉴定,标记为“*”;如果匹配度 > 700,但没有在前人文献中找到可借鉴的资料,则将匹配度最高的物质定义为初步鉴定,标记为“ο”; 如果匹配度< 700,则该保留时间的物质不能被鉴定出来,标记为"-"。
Note:After referring to the mass spectrometry database(NIST 2011) and compared with previous literature,if the matching degree is greater than 750(the total value is 1000),and the probability of the first matching compound is as higher as 100 than the second possible compound,then we defined the first matching compound as complete identification,marked "*";if the matching degree is greater than 700,but don’t testified by previous literature,then we defined the result as preliminary identification,marked "ο";if the matching degree is less than 700,so the compound can’t be identified,then we defined it as unknown,marked "-".
3 结论
本试验在前人研究的基础上,通过对金观音挥发性成分HS-GC/MS工艺进行单因素试验和正交试验,以出峰个数和总峰面积为依据,确定了金观音挥发性成分静态顶空进样法的最佳分析条件,即平衡温度80 ℃,平衡时间60 min,茶/NaCl=1∶2,加样量0.5 g,建立了适用于以金观音为代表的乌龙茶香气物质分析的HS-GC/MS方法。该方法操作简便快捷,减少人为因素可能导致的误差,且与人嗅觉闻到的香气最为接近。在本实验室后期的实验中,我们将该方法用于乌龙茶、白茶、红茶、绿茶、茉莉花茶的香气提取和鉴定中,可良好区分不同地区、不同品种、不同等级、不同加工工序的茶样,说明该方法普适性较强,但该方法是以乌龙茶为样品进行优化的,对于其他茶类应该用该类别的茶样进行针对性优化,并扩大样本,更加合理。
在检测出的104个金观音香气物质组分中,醇类、碳氢类化合物和醛类的种类与峰面积值最高,说明这3类物质可能为金观音香型的主要贡献成分。其中醇类通常具有芳香或酸败气味,植物挥发油通过中一般都含有多种萜醇和芳香醇。比如具果香的1-戊烯-3-醇、可用作香料定香成分的香叶基芳樟醇、具有清甜玫瑰花香的苯乙醇等。金观音中检测出的碳氢类化合物包括十二烷、二十一烷和二十四烷3种烷烃类物质,但由于饱和烷烃类物质阈值较高、香气无特色、不典型,故非主要风味物质[17]。还有具柠檬香的D-柠檬烯,具柑橘香味的α-松油烯,具木香的α-柏木烯等物质。有文献[18]报道醛类化合物阈值很低,对产品的风味贡献较大。在金观音中检测出来的醛类包括3-甲基丁醛(苹果香味)、苯甲醛(杏仁味)、β-环柠檬醛(凉香、果香和清香)等。此外本实验中氯化物含量也较高,主要是受所添加的饱和NaCl溶液的影响。
2015年,王自琴等[19]对以金观音、铁观音、黄棪3个高香乌龙茶良种春、夏梢制成的红茶进行了生化成分以及香气的测定。其中金观音中具极好花果香的脱氢芳樟醇(7.29%)显著高于其他品种,且检测出了橙花叔醇。本实验中脱氢芳樟醇含量也较高,占总峰面积的4.26%,但没有检测到橙花叔醇。本实验与以青岛茶区的金观音[1]茶树品种的夏季茶鲜叶加工而成的绿茶检测出来的相同成分有苯甲醛、邻伞花烃、D-柠檬烯、十二烷、β-环柠檬醛、(Z)-己酸-3-己烯酯、α-柏木烯、β-紫罗兰酮。与以金观音茶树品种加工而成的乌龙茶[20]共有的成分有正戊醇、顺-3-己烯醇、正己醇、2-庚酮、庚醛、苯甲醛、甲基庚烯酮、2-正戊基呋喃、苯乙醛、苯乙醇、α-松油醇、β-环柠檬醛、紫罗兰酮、香叶基丙酮、β-紫罗酮、二十一烷、二十四烷。可以看出同样的工艺相似的挥发物更多,这可能是由于加工工艺以及检测条件不同而导致的挥发物种类与含量的差异。这些挥发物共同形成了金观音馥郁鲜爽的香气特征。
