高效液相色谱法同时测定骨密度片中6种大豆异黄酮和淫羊藿苷的含量
2019-03-08高洋马方圆禹珊珊赵倩倩金向群刘霞
高洋,马方圆,禹珊珊,赵倩倩,金向群※,刘霞
(1.吉林大学药学院,长春 130020;2.吉林农业大学中药材学院,长春 130118)
骨密度片是以大豆、淫羊藿、骨碎补等为配伍研制出的拟用于治疗骨质疏松的一种中成药。大豆中的大豆异黄酮可用于防治骨质疏松[1],既能促进人骨的形成又能抑制骨的吸收,对于维持髋部骨矿物质密度以及全身的骨矿含量具有适当作用[2]。张建东[3]使用大豆异黄酮对去势大鼠进行了研究,实验结果显示,大豆异黄酮对于骨质疏松模型大鼠的骨密度具有明显的提高作用。已有研究发现,淫羊藿苷对破骨细胞的生成具有抑制作用,抗骨质疏松的作用明显[4]。骨碎补是水龙骨科植物槲蕨的干燥根茎,骨碎补具有补肝肾、强筋骨的功效[5]。实验室通过大量实验研究,将3 种药材制成了具有抗骨质疏松功能的骨密度片。通过药理活性实验研究,该制剂具有抗骨质疏松的功效[6]。为控制该制剂质量,简单方便的含量测定方法亟待解决。分别测定6 种大豆异黄酮[7]和淫羊藿苷[8]含量的方法已有报道,但同时测定这7 种成分的方法仍未见报道。本试验建立了可同时测定增加骨密度片中7 种有效成分(大豆苷、黄豆黄苷、染料木苷、大豆苷元、黄豆黄素、染料木素和淫羊藿苷)含量的简单方便方法,为控制骨密度片的质量提供参考依据。
1 仪器与试剂
1.1 仪器
1525-2489 高效液相色谱仪(Waters公司);AB204-N 电子分析天平(上海方瑞仪器有限公司);5TC-C18(4.6 mm×250 mm,5m)(Agilent 公司);US-10D 数控超声波清洗器(中国科技仪器设备厂)。
1.2 材料与试剂
供试样品 骨密度片由吉林大学药学院药剂实验室自制(批号:20160612)
大豆苷标准品(批号:14100905)、染料木苷标准品(批号:14060511)、染料木素标准品(批号:1604141)、淫羊藿苷标准品(批号:15081811)(北京世纪奥科生物生物技术有限公司);黄豆黄苷标准品(批号:151224)、大豆苷元标准品(批号:151209)、黄豆黄素标准品(批号:160107)(北京中科质检生物技术有限公司);色谱纯甲醇、乙腈(美国费世尔公司);磷酸为色谱纯。
2 方法与结果
2.1 色谱条件
2.2 溶液的制备
2.2.1 混合标准品溶液的制备 分别精密称取大豆苷、黄豆黄苷、染料木苷、大豆苷元,黄豆黄素、染料木素和淫羊藿苷(经五氧化二磷干燥)标准品适量,制备成0.3600mg/mL、0.0407mg/mL、0.3570mg/mL、0.4050mg/mL、0.080 7 mg/mL、0.075 4 mg/mL、0.200 0 mg/mL 的混合对照品溶液。
2.2.2 供试品溶液的制备 取样品骨密度片(批号:20160612)20 片,除去薄膜衣层后粉碎,混合均匀称,取粉末4.05g放置在烧杯中,精密加入50mL80%甲醇。放置30 min 后进行超声(30 min,30 ℃),放至室温,过滤。60℃将续滤液减压浓缩,用50mL20%乙醇溶解后,上柱〔预先处理过的D101大孔树脂柱(1.5 cm×20 cm)〕,分别用100 mL 无水乙醇、250 mL 超纯水、100 mL 无水乙醇进行洗脱,再用100 mL20%乙醇洗脱后收集洗脱液,蒸干,将残余物用80%甲醇溶解,转移至100 mL容量瓶中,80%甲醇定容,混匀,0.22m 微孔滤膜滤过,滤液为供试品溶液。
2.2.3 阴性样品溶液的制备 按骨密度片的处方比例分别配制不含大豆和淫羊藿的阴性样品,按“2.2.2”项下方法制备成2 种阴性样品溶液。
2.2.4 测定

图1 混合对照品(A)、样品(B)、缺大豆阴性样品(C)、缺淫羊藿阴性样品(D)的高效液相色谱图Fig.1 HPLC chromatograms of mixture of reference substances(A),sample(B),negative sample without Soybean(C),negative sample without Epimedium(D)
2.3 标准曲线
精密吸取混合标准品溶液0.2mL、0.4mL、0.6mL、0.8 mL、1.0 mL 分别置于10 mL 容量瓶中,用洗涤液〔A(V)∶B(V)=88∶12〕定容至10 mL,配制出不同浓度的混合标准品溶液备用。分别精确吸取各浓度的混合标准品溶液10L,注入色谱仪,以X轴为标准品浓度、Y 轴为峰面积积分值做回归曲线。得到大豆苷、黄豆黄苷、染料木苷、大豆苷元、黄豆黄素、染料木素和淫羊藿苷回归方程,见表1。

表1 线性方程、相关系数Table 1 Linear equation、correlation coefficient
结果表明,大豆苷、黄豆黄苷、染料木苷、大豆苷元、黄豆黄素、染料木素和淫羊藿苷分别在7.200g/mL~36.000g/mL、0.814g/mL~4.070g/mL、7.140g/mL~35.700g/mL、8.040g/mL~40.200g/mL、1.620g/mL~8.100g/mL、1.500g/mL~ 7.500g/mL、0.040g/mL~0.240g/mL 范围内线性关系良好。
2.4 精密度试验
2.5 稳定性试验
2.6 重复性试验
精密称取20161116批次样品6 份,除去薄膜衣层,研细,精密称定,采用“2.2.2”项下方法制备供试品溶液,精密吸取10L 进样,进行含量测定。结果表明,大豆苷、黄豆黄苷、染料木苷、大豆苷元、黄豆黄素、染料木素和淫羊藿苷的含量均值分别为0.362mg/g、0.0382 mg/g、0.324 0 mg/g、0.308 0 mg/g、0.063 4 mg/g、0.079 6mg/g和0.8020mg/g,RSD分别0.80%、0.52%、0.46%、0.48%、0.50%、0.67%和0.33%。表明该方法重复性良好。
2.7 加样回收率试验
分别称取已知含量的样品粉末6 份,每份1.0g,每份分别加入适量大豆苷,黄豆黄苷,染料木苷,大豆苷元,黄豆黄素,染料木素和淫羊藿苷对照品溶液,按照“2.2.2”项下方法进行处理,进样测定各成分的含量,并计算回收率。结果,大豆苷、黄豆黄苷、染料木苷、大豆苷元、黄豆黄素、染料木素和淫羊藿苷平均回收率(n=6)分别为98.54%、98.42%、98.42%、98.62%、98.42%、98.23%和98.24%;RSD 分别为0.54%、0.56%、0.89%、1.01%、0.86%、0.62%和0.56%。结果表明,各组分的平均加样回收率均在95%~105%之间,加样回收率良好。见表1。
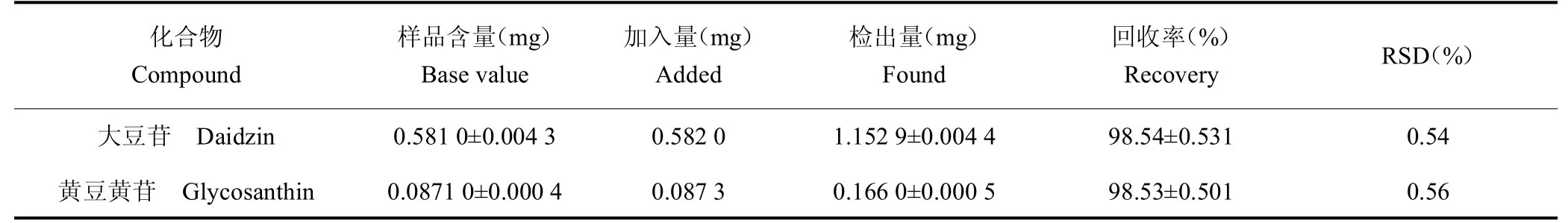
表1 回收率测结果Tab 1 Recovery results
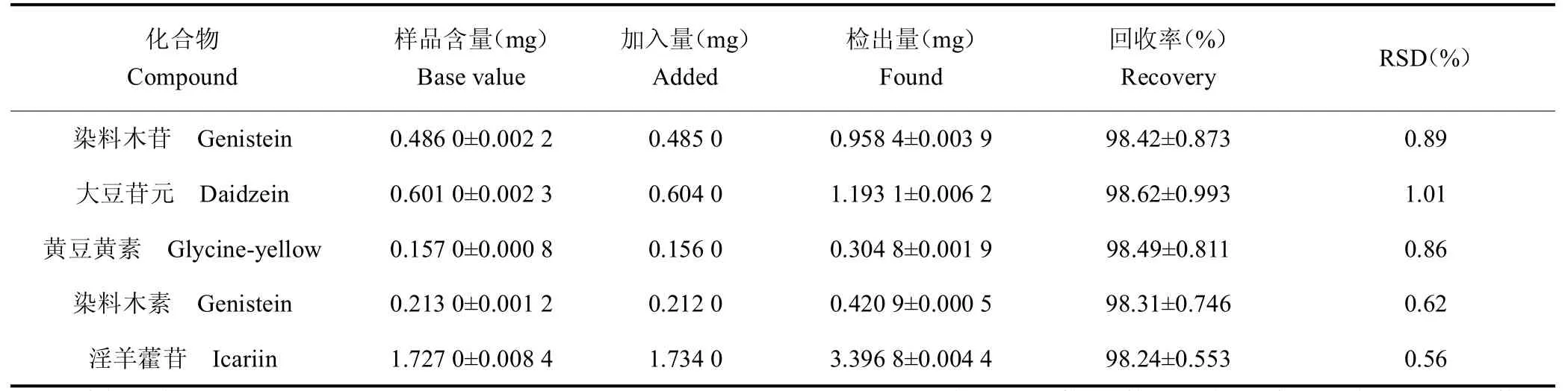
续表1
2.8 样品含量测定
分别取批号为201611116、20161120、20161124 3批样品,每批样品取3 份,按照“2.2.2”项下方法制备供试品溶液,按照“2.2.1”项下色谱条件进样,进样量为10L,对大豆苷、黄豆黄苷、染料木苷、大豆苷元、黄豆黄素、染料木素和淫羊藿苷峰面积进行记录,并计算各个成分的含量。见表2。

表2 样品含量测定Tab 2 Assaying of sample (mg/g)
3 讨论
3.1 流动相的选择
根据《中华人民共和国药典》2015 版,淫羊藿苷采用乙腈-水(30∶70)为流动相,由于样品种类繁多,并不能使7 种样品达到分离效果。本试验还尝试了水-磷酸:甲醇为流动相,结果淫羊藿苷与染料木素也无法分离。为保证分离效果好,最后根据《中华人民共和国药典》2015 版大豆异黄含量测定使用的水-磷酸(pH=3):乙腈作为流动相,并对流动相比例进行了调整。
3.2 波长的选择
根据全波长扫描,大豆苷、黄豆黄苷、染料木苷、大豆苷元、黄豆黄素、染料木素和淫羊藿苷最大吸收波长分别为250 nm、257 nm、260nm、249 nm、260 nm、261 nm、270nm,为保证7 种成分均有较好的吸收,选用260nm作为测定波长。
3.3 供试品的制备
样品中成分较多,传统测定大豆异黄酮和淫羊藿苷的方法不能达到理想的分离度,为了除去部分杂质,达到基线分离,采用D101 大孔树脂对样品进行洗脱处理,并对水及20%、30%、40%乙醇洗脱情况进行了考察,在使用20%乙醇进行洗脱后,样品的分离度最好,符合含量测定要求,并对含量的影响很小(加样回收率符合要求)。故选择20%乙醇溶液作为洗脱剂,进行洗脱,弃去洗脱液,再用无水乙醇洗脱,收集无水乙醇洗脱液,蒸干,用80%甲醇定容,作为供试品溶液。
4 小结
本试验建立了同时测定骨密度片中大豆苷、黄豆黄苷、染料木苷、大豆苷元、黄豆黄素、染料木素和淫羊藿苷7 种有效成分含量的方法,为骨密度片的质量控制提供了依据。同时也为其他含有大豆和淫羊藿药材的中药制剂质量标准的建立提供参考依据。
