脂蛋白a和超敏C反应蛋白联合检测对糖尿病肾病早期诊断的临床价值
2019-03-05孙文早李红玲范丽娜秦前安崔梅芳
孙文早 李红玲 范丽娜 邹 毅 黄 晶 秦前安 崔梅芳
2010年,全球成年糖尿病患者约为2.85亿,预计到2030年糖尿病患者将增加1倍以上,高达4.39亿[1]。但国际糖尿病联盟最新公布数据显示在2017年全球糖尿病患者已达4.25亿,估计到2045年糖尿病患者将达到6.29亿。我国糖尿病发生率也急剧增加,目前成为仅次于心血管和肿瘤之后的第3大疾病[2]。2型糖尿病为一种胰岛素抵抗、脂代谢、高血压、高血糖和肥胖等联合构成的代谢紊乱综合征,是一种自身免疫性和慢性炎症所引起的血糖升高的慢性疾病,常伴其他并发症存在[3]。糖尿病肾病(diabetic nephropathy,DN)是糖尿病的慢性并发症之一,在我国DN的发生率每年呈递增趋势,也是糖尿病并发症中致残、致死的重要原因[4]。目前,2型糖尿病肾病的发病机制尚不明确,患者尿蛋白的检测常作为临床诊断糖尿病肾病的重要证据[5, 6]。由于DN呈进行性发展,并且这种改变是不可逆的,所以对患者的预后和生命质量造成了严重影响,并且治疗难度较大,无特效药物能改变这种变化。因此早期对DN进行诊断,并进行相应治疗,将对提高患者生存质量,延长患者生命具有重要意义。本研究通过探讨2型糖尿病患者血清中Lp(a)及 hs-CRP 的含量及两者联合检测对糖尿病肾病病情发展的相关性,旨在为DN患者的早期诊断、临床转归、以及终末期发展方向提供新思路。
材料与方法
1.一般资料:选取2016年9月~2017年6月来笔者医院住院就诊治疗的2型糖尿病患者120例,糖尿病的诊断根据1999年WHO糖尿病诊断标准确诊。其中男性65例,女性55例,患者年龄45~70岁,病程2~21年。根据24h尿蛋白排泄率(UAER)将其分为两组,其中单纯糖尿病组73例,UAER<30mg/24h;糖尿病肾病组47例,UAER>30mg/24h。另选笔者医院同期健康体检者50例作为本研究的健康对照组,其中男性34例,女性16例,年龄35~81岁,均无器质性病变,血糖、血脂、UAER 均在正常范围,尿糖均为阴性。该实验方案经医院医学伦理委员会批准并经患者知情同意。
2.血清Lp(a)和 hs-CRP的检测:所有研究对象均空腹8~12h,于次日清晨空腹抽静脉血3ml,分离血清检测血清Lp(a)及 hs-CRP,同时留取24h尿(晨起8:00时~次日8:00时)。免疫比浊法测定UAER。 UAER计算公式:UAER=尿白蛋白(mg/ml)×24h 尿量(ml)。笔者医院检验科检测各组Lp(a)、hs-CRP水平。脂蛋白a和hs-CRP试剂由北京利德曼公司提供,采用德国Roche公司COBAS6000全自动生化分析仪分别检测,使用与试剂配套的校准品及质控品。

结 果
1.一般临床资料比较:各组性别、年龄、体重、身高等比较,差异无统计学意义(P> 0.05),详见表1。
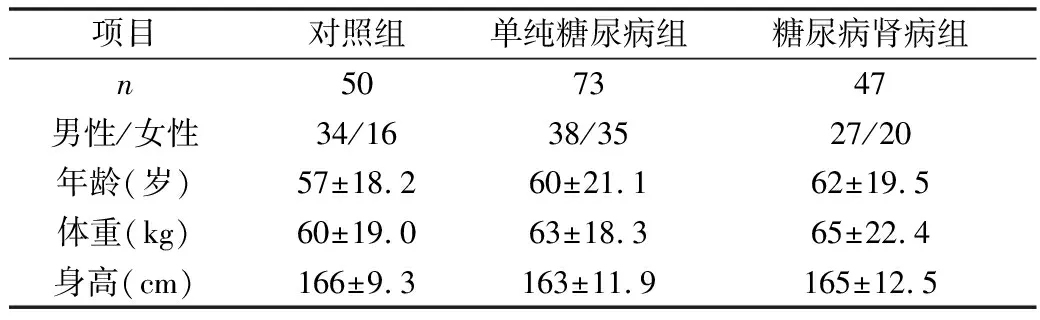
表1 一般临床资料比较
2.3组Lp (a)、hs-CRP及UAER的比较:与对照组比较,单纯糖尿病组与糖尿病肾病组UAER增加,Lp (a)、hs-CRP水平增高,差异有统计学意义(P<0.01)。同时,随着2型糖尿病发展,即随着UAER逐步升高,与单纯糖尿病组比较,糖尿病肾病组Lp (a)、hs-CRP均显著升高,差异有统计学意义(P<0.05),详见表2。
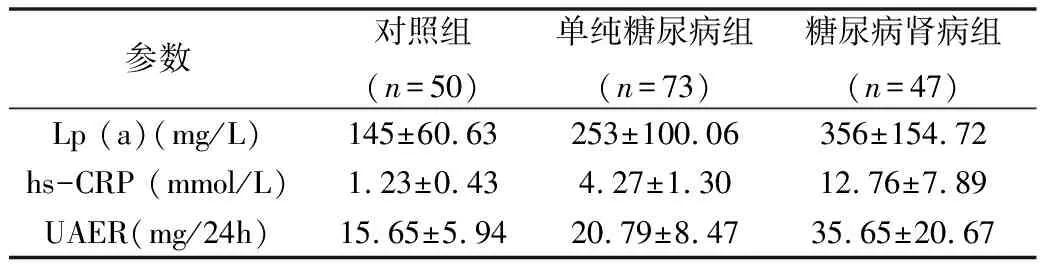
表2 3组中Lp(a)、hs-CRP及UAER的比较
3.Lp (a)、hs-CRP与UAER相关性分析:多因素线性相关分析显示,Lp (a)、hs-CRP与UAER均呈显著正相关(r=0.387,P<0.05;r=0.782,P<0.01), Lp(a)与 hs-CRP 变量间呈显著正相关(r=0.793,P<0.05)。
讨 论
研究表明,我国2 型糖尿病的发生率呈逐年上升的趋势,且其严重并发症DN患者也逐年增多,糖尿病肾病患者死亡的主要原因为长期的高血糖刺激导致肾脏严重受损,最终致肾衰竭,严重威胁患者的生命健康[7]。DN患者临床表现可以分为5期,即肾小球高滤过和肾脏肥大期、正常白蛋白尿期、早期糖尿病肾病期(持续微量白蛋白尿期)、临床糖尿病肾病期和终末期肾衰竭期。由于DN病情进展缓慢,起病较隐匿,糖尿病肾病早期仅表现为肾小球体积轻微增大,基膜轻微增厚,肾小球滤过率相对增加,但相关尿蛋白的监测则完全在正常范围内,即便是糖尿病肾病Ⅲ期,其临床表现也仅为微量蛋白尿,现有诊断方法很难发现,部分实验室检测指标特异性与敏感度仍处于探索阶段,故急需寻求特异性与灵敏性较高的实验室诊断指标,早期发现DN,早期进行相关治疗[8~10]。
2型糖尿病作为一种慢性炎性疾病,高血糖导致患者的血清Lp(a)含量增加,对冠状动脉粥样硬化、肾动脉硬化以及其他部位的动脉硬化起着重要的作用。近年来随着脂质学说和炎症学说概念的提出,Lp(a)和重要的急性时相反应蛋白hs-CRP在糖尿病及DN的发生、发展中的作用逐渐引起人们的关注[11, 12]。因此本研究通过对正常健康对照者、糖尿病患者及DN患者血清中Lp(a)、hs-CRP与UAER的检测,探究Lp (a)、hs-CRP与糖尿病患者及DN患者之间的关系,为DN患者的早期诊断提供重要的临床依据。
研究显示,Lp(a)常沉积于肾小球微血管中,经氧化或糖基化修饰后,导致肾小球肥大及其他相应的病变。当Lp(a)升高,糖尿病微血管病变程度增加[13, 14]。糖尿病所导致的微血管病变中,Lp(a)升高能导致纤溶酶原的活性受到抑制[15]。本研究通过对3组检测对象血清中Lp(a)及hs-CRP的检测,发现单纯糖尿病组与DN组UAER增加,Lp(a)、hs-CRP水平明显增高,同时随着2型糖尿病发展,即随着UAER逐步增加,与单纯糖尿病组比较,DN组Lp (a)、hs-CRP也显著升高,这表明Lp(a)在糖尿病及DN的发生发展过程具有重要作用,同时也显示出Lp(a)在DN的早期诊断中的重要意义。
而作为慢性炎症型疾病的2型糖尿病,由于糖尿病患者自身持续高血糖浓度,从而导致患者血流变的变化,继发机体的炎性反应。同时由于患者早期脂质等在肾脏的沉积,导致肾小球毛细血管变性硬化,进一步加重肾脏本身的缺血缺氧性改变,形成恶性循环,导致糖尿病患者处于高hs-CRP状态,导致DN的形成,这也是DN形成的一个重要原因[16]。因此,这种模式会形成一种递增性的循环,导致血清Lp(a)、hs-CRP水平与肾脏的损害程度呈正相关。而本研究通过多因素线性相关分析也显示, Lp(a)、hs-CRP与UAER均呈显著正相关,Lp(a)与 hs-CRP 变量间呈显著正相关。
综上所述,通过当前对2型糖尿病及其发展致DN过程致病机制的认识,同时结合本研究,笔者提出2型糖尿病患者通过Lp(a)、hs-CRP的检测能早期间接反映患者的肾脏损害程度,尤其当两者联合检测时,更能及时预警患者肾功能的减退与损伤,起到早发现、早治疗的理想效果。
