*磁性纳米颗粒负载离子液体催化合成聚甲醛二甲醚
2019-03-05张桐露刘康军赵变红张朝峰李瑞丰
张桐露,刘康军,李 静,赵变红,张朝峰,李瑞丰
(1.太原理工大学 化学化工学院,太原 030024;2.阳煤集团寿阳化工有限责任公司,山西 寿阳 045400)
随着石油资源的日益枯竭和对环境保护要求的日益增高,研究者正致力于找到一种能代替柴油,减少排放污染的新型柴油燃料或柴油添加剂[1]。根据柴油燃料的燃烧特征表明,含氧组分能增加十六烷值和提高燃烧过程中的热效率[2]。作为含氧组分的一种,聚甲醛二甲醚,又名聚甲氧基二甲醚(polyoxymethylene dimethyl ethers,PODEn)是一类多醚物质的通称,通式为:CH3O(CH2O)nCH3(n≥1,n为整数,一般情况下3≤n≤8).PODEn具有较高的含氧量和十六烷值,其中PODE1~2的沸点和闪点较低,需要对发动机进行改造,而PODEn>5会在低温下结晶,均不适合作柴油添加剂。最适宜的组分是PODE3~5,不仅能够与柴油混溶,且无需对发动机结构进行任何改造[3],在柴油中添加10%~20%(体积分数),能够实现清洁燃烧,有效减少烟尘、PM等颗粒物的排放[4]。另外,合成PODEn的原料主要是甲醇及甲醇的衍生物,因此,PODEn的研究对促进甲醇下游高附加值产品的开发及石油化学工业的健康发展具有重要意义。

本文在前期研究工作[14-17]基础上,制备了磁性纳米颗粒负载离子液体催化剂,以三聚甲醛和甲醇作原料,进行了催化缩合制备聚甲醛二甲醚反应的研究。通过XRD、TEM、FT-IR等手段对催化剂的结构和形貌进行分析,考察了反应温度、反应时间、醇醛比及催化剂用量等因素对反应的影响。
1 实验部分
1.1 主要试剂
咪唑、三聚甲醛、(3-氯丙基)三甲氧基硅烷,均为AR,阿拉丁化学试剂有限公司;无水甲醇、无水乙醇、氢氧化钠,均为AR,天津市科密欧化学试剂有限公司;1,4-丁磺酸内酯(质量分数97%),萨恩化学技术有限公司;四水合二氯化铁(FeCl2·4H2O),为CP,北京化工厂;六水合三氯化铁(FeCl3·6H2O),为CP,上海华东化工学院芳庄第三助剂厂;对甲苯磺酸,为AR,成都市科龙化工试剂厂。
1.2 催化剂的制备
1.2.1 磁性纳米四氧化三铁的制备[18]
称取一定量的FeCl3·6H2O和FeCl2·4H2O于250 mL锥形瓶,加入去离子水溶解,超声振荡加热,待温度上升至60 ℃,快速滴加2 mol/L NaOH溶液直至溶液pH=10~12,此时混合液由橙红色逐渐变成深黑色;在60 ℃下反应一段时间后,用去离子水反复洗涤至上清液pH=7.0,磁铁分离除去上清液,60 ℃真空干燥10 h,研磨即得磁性纳米Fe3O4粒子。
1.2.2 磁性纳米颗粒负载离子液体的制备[19]
磁性纳米颗粒负载离子液体的制备过程如图1所示。称取一定量Fe3O4纳米粒子及(3-氯丙基)三甲氧基硅烷于500 mL三口烧瓶中,加入适量甲苯作溶剂,恒速搅拌,110 ℃冷凝回流6 h;向反应混合物中加入等物质的量的咪唑,继续反应12 h;反应结束后,加入等物质的量的1,4-丁磺酸内酯,60 ℃下反应12 h;最后加入等物质的量的对甲苯磺酸,室温下反应12 h;反应混合物于60 ℃下旋蒸,除去未反应的原料,60 ℃真空干燥4 h,所得固体产物即为磁性纳米颗粒负载离子液体催化剂(Fe3O4@ILs).
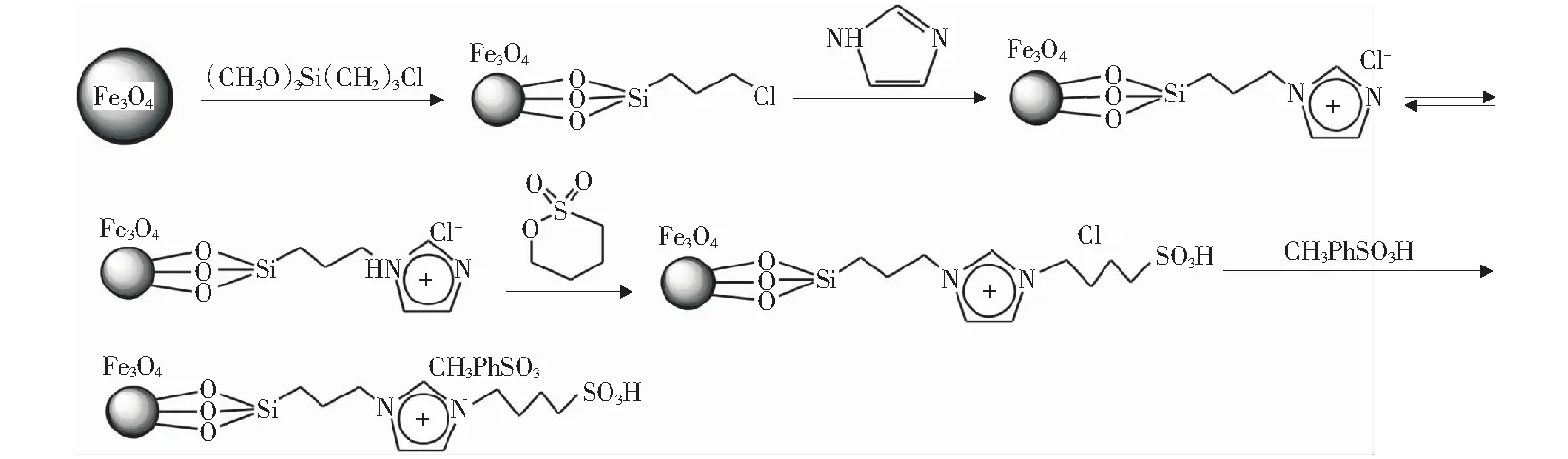
图1 催化剂的合成示意图Fig.1 Scheme of the preparation of catalyst
1.3 催化剂的表征
X射线衍射(XRD)测试采用日本岛津公司生产的Simadzu XRD-6000型X射线衍射仪,辐射光源为Cu靶,Kα射线(λ=0.154 18 nm),石墨单色器,电压40 kV,电流30 mA,扫描范围为20°~70°,扫描速度为8 (°)/min,Sd(divergence slit)为1°,Sr(receiving slit)为1°,Ss(scatter slit)为0.15 mm.
催化剂的结构通过日本岛津公司的Shimadzu IR Affinity-1型傅里叶变换红外光谱仪(FT-IR)进行表征,KBr压片,测试范围为500~4 000 cm-1.
采用日本电子JEM-1011型透射电子显微镜对催化剂的内部结构变化进行观察,加速电压100 kV.
1.4 催化剂的催化性能评价
催化剂的活性测试在100 mL高压反应釜中进行,依次向釜内加入无水甲醇、三聚甲醛和催化剂,用氮气置换反应釜中的空气,最终加压至2.0 MPa,控制反应温度80 ℃~130 ℃,反应时间1 h~6 h,醇醛物质的量比1.2~6.0,催化剂质量分数0.5%~5.0%.反应方程式如下:

使用GC-4000A型气相色谱仪分析反应产物。色谱柱为Agilent DB-1毛细管柱(60 m×0.25 mm×0.25 μm);检测器:FID检测器;程序升温法检测,内标法定量[20]。三聚甲醛的转化率c(TOX)和PODEn的选择性S(PODEn)(n=1,2,…,N)分别按式(1),式(2)计算:
c(TOX)=(m(TOX)in feed-m(TOX)in product)/
m(TOX)in feed×100% .
(1)
S(PODEn)=m(TOX)PODEn/(m(TOX)in feed-
m(TOX)in product)×100% .
(2)
式中:m表示某物质的质量,m(TOX)PODEn表示生成PODEn所消耗三聚甲醛的质量。
2 结果与讨论
2.1 催化剂的表征
新制备的Fe3O4纳米粒子(图2曲线a)有6个明显的尖锐的特征衍射峰,分别对应Fe3O4纳米粒子晶体的(220),(311),(400),(422),(333),(440)晶面,根据谢乐公式计算得出Fe3O4纳米粒子的粒径约为13.72 nm(<30 nm),说明所制备的磁性纳米颗粒属于纳米级别,为尖晶石结构,具有超顺磁性。由图2曲线b可以看出,同载体Fe3O4纳米粒子一样,新制备的催化剂Fe3O4@ILs同样具有6个特征衍射峰,说明在制备催化剂的过程中,Fe3O4纳米粒子的晶相结构并未受到破坏。

a-Fe3O4;b-Fe3O4@ILs;c-Fe3O4@ILs of being reused 4 times图2 催化剂的XRD谱图Fig.2 XRD patterns of catalysts
使用日本电子JEM-1011型透射电子显微镜(TEM)对Fe3O4纳米粒子表面形貌进行表征,如图3所示。
由TEM照片可以看出,通过超声共沉淀法制备的Fe3O4纳米粒子为大小一致的球形颗粒,粒径

图3 催化剂TEM照片Fig.3 TEM images of catalysts
范围在8~15 nm之间,如图3(a)所示,与上述XRD表征数据相符,该Fe3O4纳米粒子符合磁性分离要求。由图3(b)新制备的Fe3O4@ILs的TEM照片可看出,离子液体成功包覆到了Fe3O4纳米粒子的表面。
图4为载体及催化剂的红外光谱,图4曲线a上,1 634 cm-1和3 426 cm-1分别是—OH的弯曲振动和伸缩振动,2 921 cm-1处是C—H伸缩振动[21]。图4曲线b上1 598 cm-1和3 440 cm-1处分别为N—H的变形振动和伸缩振动,表明有仲胺N—H键的存在;在1 640 cm-1处为N—C伸缩振动,说明该样品中有咪唑环。其中1 587 cm-1认定为对甲苯磺酸根苯环的红外吸收峰,在1 189 cm-1处出现了—SO3H的特征吸收峰,说明该样品中存在对甲苯磺酸根。此外,在1 090.3~1 137.9 cm-1为Si—O键伸缩振动吸收峰,峰形变宽,说明(3-氯丙基)三甲氧基硅烷成功锚定在Fe3O4纳米粒子表面。
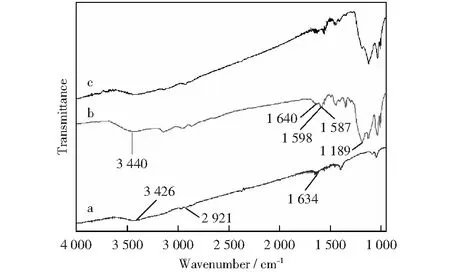
a-Fe3O4;b-Fe3O4@ILs;c-Fe3O4@ILs of being reused 4 times图4 催化剂的红外谱图Fig.4 FT-IR spectra of catalysts
2.2 催化剂用量的影响
由表1可以看出,在质量分数为0.5%~5.0%的范围内,随着催化剂用量的增加,三聚甲醛的转化率先增大后基本保持不变,但PODE3~5的选择性先增加后减少。在催化剂的质量分数为2.0%时,PODE3~5的选择性达到最大值,反应达到平衡。继续加入催化剂,PODE3~5的选择性有所下降,原因可能是过多的催化剂促进了PODE3~5的水解[13]503,导致平衡逆向移动,生成的PODE3~5减少,选择性降低。
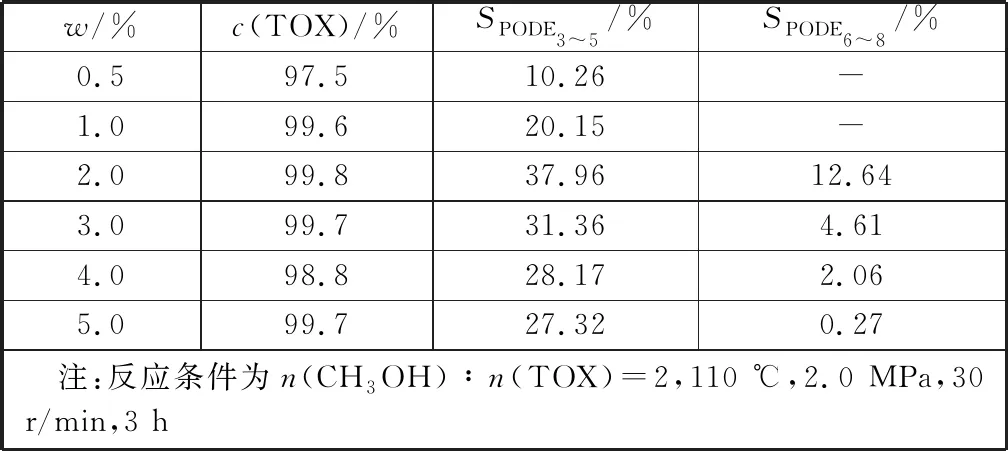
表1 催化剂的质量分数w对产物分布和三聚甲醛转化率c(TOX)的影响Table 1 Influence of dosage of catalyst (w) on the product distribution and trioxane conversion rate c(TOX)
2.3 反应温度的影响
表2是反应温度对缩醛化反应影响的结果。在80~110 ℃范围内,随着反应温度的升高,三聚甲醛的转化率变化不大,但PODE3~5的选择性逐渐增大;当温度达到110 ℃时,PODE3~5选择性达到最大;继续升高温度,三聚甲醛的转化率和PODE3~5的选择性都逐渐下降。因此,从能耗与选择性两方面综合考虑,适宜的反应温度为110 ℃.

表2 反应温度θ对产物分布和三聚甲醛转化率c(TOX)的影响Table 2 Influence of reaction temperature θ on the product distribution and trioxane conversion rate c(TOX)
2.4 反应投料比的影响
从表3可以看到,随着甲醇与三聚甲醛物质的量比的增大,三聚甲醛的转化率和PODE3~5的选择性均先增加后减小。这是因为当甲醇与三聚甲醛的物质的量比较小时,过量的甲醛会和已经生成的PODEn进一步聚合形成PODEn+1,进而影响PODE3~5的选择性;当甲醇与三聚甲醛的物质的量比较大时,反应生成较多的副产物水,致使生成的聚甲醛二甲醚在酸性条件下水解,不利于PODE3~5的合成。合适的原料比对反应至关重要,当甲醇与三聚甲醛的物质的量比为2∶1时,最有利于PODE3~5的生成。
2.5 反应时间的影响
表4列出了反应时间对缩醛化反应的影响结果。随着反应时间的增加,三聚甲醛的转化率也随之增加,但增加的幅度不大,而PODE3~5的选择性却先升后降;当反应时间为3 h时,PODE3~5的选择性达到最大值。对于间歇反应,在一定条件下,适当增加反应时间可以提高反应物的转化率和产物的选择性,但反应时间过长,一方面使得能耗增加,另一方面,PODE3~5会发生不同程度的水解,时间越长,水解的程度越大。综合考虑,最佳反应时间为3 h.

表4 反应时间t对产物分布和三聚甲醛转化率c(TOX)的影响Table 4 Influence of reaction time t on the product distribution and trioxane conversion rate c(TOX)
2.6 催化剂重复循环利用
反应结束后,催化剂经磁铁分离、过滤,用甲醇洗涤3次,60 ℃真空干燥4 h后回收,重新用于下次反应。图2曲线c是使用4次后催化剂的XRD图,和新鲜催化剂(图2曲线b)相比,在(311)晶面和(440)晶面衍射峰强度变大,峰宽变窄,推测是随着使用次数增多,晶粒发生团聚而变大造成的。进一步由图3(c)的TEM照片可看出,4次循环使用对Fe3O4纳米粒子磁核无明显影响,但晶粒分散度变小,发生团聚,与XRD表征结果一致。图4曲线c是循环使用4次后的Fe3O4@ILs红外谱图,与新制备的Fe3O4@ILs相比,1 189 cm-1峰强度变小,说明多次使用过程中,负载在Fe3O4表面的离子液体有部分流失,导致Fe3O4@ILs的活性有所降低。
从图5也可以看出,Fe3O4@ILs重复使用4次后,催化活性稍有下降,PODE3~5的选择性从37.2%
降至32.3%,三聚甲醛的转化率从99.5%降至98.6%.与文献[13]报道的游离的离子液体催化活性相比,使用Fe3O4@ILs为催化剂,三聚甲醛的转化率基本保持不变,均为98%左右,但选择性从PODE3~8的32.54%提高到PODE3~5的37.2%,而且回收方法简单,可多次使用。说明制备的Fe3O4@ILs催化活性高,稳定性较好,可重复使用。

反应条件:催化剂的质量分数为2.0%,n(CH3OH)∶n(TOX)=2,110 ℃,2.0 MPa,30 r/min,3 h图5 催化剂重复循环利用效果Fig.5 Repeated recycling of catalysts
3 结论
1) 通过化学键合作用制备了磁性纳米颗粒负载离子液体催化剂Fe3O4@ILs,在催化剂质量分数为2.0%,反应温度110 ℃,甲醇与三聚甲醛物质的量比2∶1,反应时间3 h的条件下,三聚甲醛的转化率为99.8%,PODE3~5的选择性为37.96%,说明该催化剂具有良好的催化性能。
2) 催化剂Fe3O4@ILs易于分离回收,在重复使用4次后,催化活性没有明显变化,可以循环使用,降低生产成本。
