帕博西尼胶囊的制备及体外溶出评价
2019-03-04张银龙汤继辉李巧霞高文远霍彩霞
张银龙,汤继辉,李巧霞,高文远,霍彩霞
帕博西尼(palbociclib)是全球首个上市的细胞周期蛋白依赖性激酶(cellular-dependent kinase,CDK)4 /6 抑制剂,联合来曲唑用于绝经后妇女雌激素受体阳性(estrogen-receptor-positive,ER+)、人表皮生长因子受体2阴性(human-epidermal-growth-receptor-2-negative,HER2-)的晚期或转移性乳腺癌的初始内分泌治疗。美国食品药品监督管理局(food and drug administration,FDA)于2015年2月加速批准原研厂家辉瑞制药的帕博西尼胶囊上市,商品名:IBRANCE®,规格:125 mg、100 mg和75 mg,推荐初始剂量:每天125 mg,与食物同服,连续服药21 d后,停药7 d[1]。本产品市场潜力巨大但目前尚未在国内上市[2]。
本试验自2015年6月至2016年12月以125 mg规格帕博西尼胶囊原研参比制剂为对照,根据参比制剂说明书中公布的辅料种类为基础,首先以自制制剂和参比制剂在pH 4.5醋酸盐缓冲液和含0.5 %十二烷基硫酸钠(sodium dodecyl sulfate ,SDS)的水溶液中溶出曲线相似因子(similarity factor,f2)为评价指标,进行帕博西尼胶囊处方筛选,然后测定优化后的自制制剂在四种溶出介质的溶出曲线,并与参比制剂溶出曲线相比较,以期获得在四种溶出介质与参比制剂体外溶出曲线一致的帕博西尼胶囊自制制剂。
1 仪器与试药
1.1仪器BSA2202和CPA225D电子天平(德国赛多利斯有限公司);RC8M溶出实验仪(天大天发科技有限公司);UV-2450型紫外可见分光光度计(日本岛津有限公司);HTD200柱式料斗混合机(浙江迦南科技股份有限公司);Z40F胶囊填充机(山东新马制药装备有限公司)。
1.2药品与试剂帕博西尼原料(北京澳合药物研究院有限公司,批号:20150801,含量:99.8%);帕博西尼原料(廊坊高博京邦制药有限公司,批号:160401,含量:99.9%;批号:160402,含量:99.6%;批号:160501,含量:99.7%);帕博西尼胶囊(美国辉瑞制药有限公司,批号:J7977OP2);帕博西尼胶囊(北京四环制药有限公司,批号:160501,160504,160507);无水直压乳糖(美国Kerry有限公司,批号:1320020633);微晶纤维素PH102(microcrystalline cellulose,MCC,山东聊城阿华制药股份有限公司,批号:20150404);羧甲淀粉钠(台湾永日化学工业股份有限公司,批号:SSG2015004);二氧化硅(湖州展望药业有限公司,批号:20160408);硬脂酸镁(辽宁奥达制药有限公司,批号:20150402);胶囊壳(苏州胶囊有限公司,批号:12860434);十二烷基硫酸钠(天津福晨化学试剂有限公司,批号:20150108)。其他试剂均为分析纯。
2 方法和结果
2.1溶出测定方法
2.1.1检测波长的选择 精密称取帕博西尼标准品,配制浓度约为10 μg/mL的帕博西尼对照溶液,取对照溶液,在190~400 nm进行紫外扫描(图1),选择最大吸收波长365 nm作为检测波长。
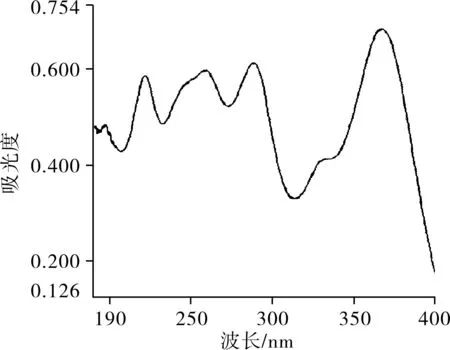
图1 帕博西尼紫外吸收光谱图
2.1.2方法专属性 空白辅料在365 nm波长处无吸收(图2),不干扰样品测定,符合专属性规定。
2.1.3线性关系与范围 精密称取帕博西尼标准品,配制浓度约为200 μg/mL的帕博西尼对照储备液,分别精密量取0.5、1、2、3、4、5 mL对照储备液于50 mL容量瓶中,用0.1 mol/L盐酸溶液稀释至刻度,摇匀,配制实际浓度(C)分别为2.026、4.052、8.140、12.156、16.208、20.260 μg/mL的帕博西尼溶液,分别在365 nm处测定吸光度值,以吸光度值(A)对浓度进行线性回归,得回归方程A=0.058 6C+0.009 6(R2= 0.999 9),结果表明,在2.206~20.260 μg/mL浓度范围内,吸光度值与浓度线性关系良好(图3)。

图2 空白辅料紫外扫描图谱
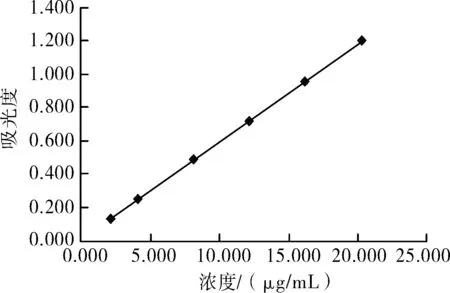
图3 帕博西尼标准曲线
2.1.4回收率试验 精密称取处方量辅料15份,分别置于500 mL容量瓶中,分别精密称取主药约75、60、45、22.5和11.25 mg各3份加入各容量瓶中,加0.1 mol/L盐酸溶液溶解,定容,过滤,取续滤液适量用0.1 mol/L盐酸溶液制成帕博西尼浓度分别为15、12、9、4.5和2.25 μg/mL的溶液各3份,365 nm波长处分别测定吸光度,按外标法计算回收率。各浓度水平回收率均在98.0%~102.0%之间(表1),RSD均小于2.0 %,溶出回收率符合要求。
2.1.5仪器精密度 取对照溶液,在365 nm处重复6次测定吸光度值分别为0.600、0.601、0.602、0.599、0.602、0.601,平均0.601,计算仪器精密度,RSD为0.19%,小于2.0 %,符合仪器精密度要求。
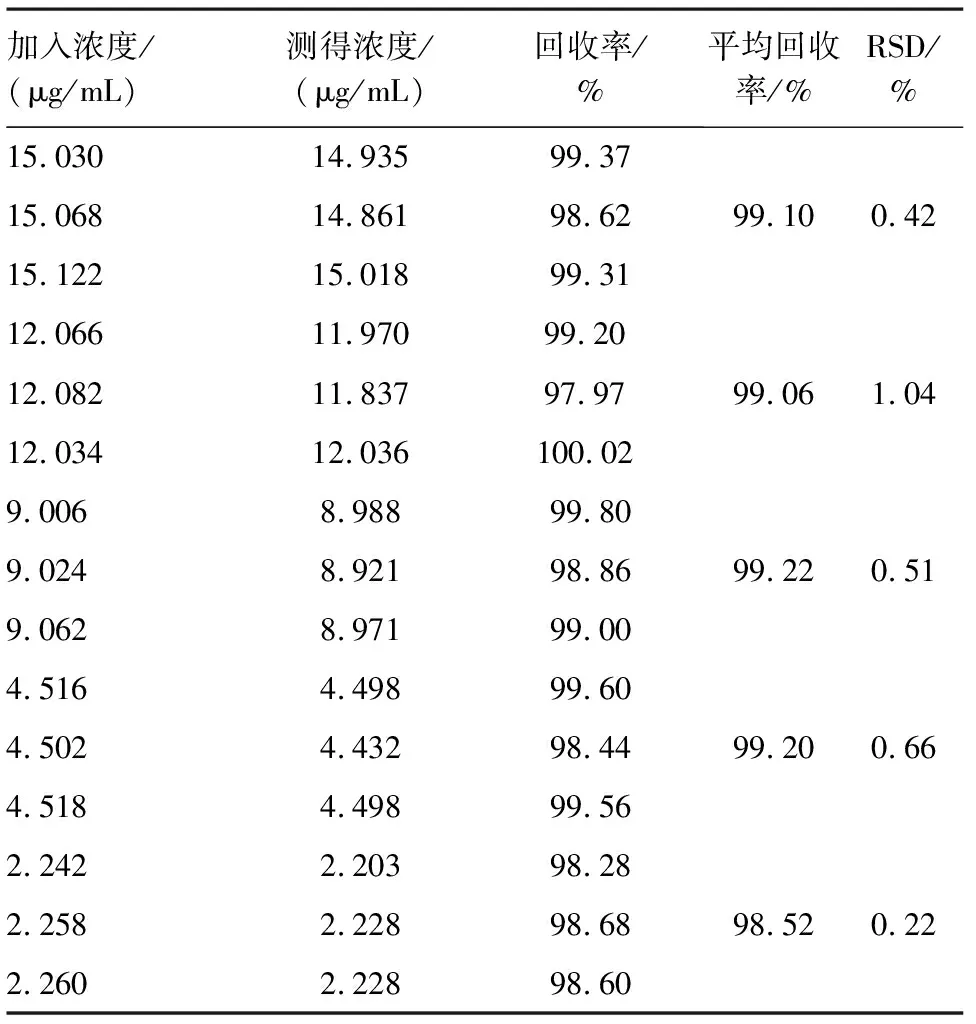
表1 帕博西尼回收率实验结果
2.1.6溶液稳定性 取各溶出介质的样品溶液,分别在(37±0.5)℃放置8 h,分别于0、2、4、6、8 h,在365 nm处测定样品吸光度值,结果表明,各溶出介质下的样品溶液的吸光度值在8 h内无明显变化,RSD均小于2.0 %,符合规定,表明各介质的样品溶液在(37±0.5)℃下,8 h内稳定(表2)。
2.1.7溶出介质选择 测定帕博西尼胶囊参比制剂在0.1 mol/L盐酸溶液、pH 4.5醋酸盐缓冲液、pH 6.8磷酸盐缓冲液和纯化水的溶出曲线(图4)。显示在pH 6.8磷酸盐缓冲液和纯化水中60 min仅溶出约14.0 %,几乎没有区分能力。因此进一步考察其在不同浓度SDS的水溶液和pH 6.8磷酸盐缓冲液中的溶出曲线(图5),显示在含0.5% SDS的水溶液和含0.5% SDS的pH 6.8磷酸盐缓冲液中60 min可溶出90.0%以上,综合考虑,选择0.1 mol/L盐酸溶液、pH 4.5醋酸盐缓冲液、含0.5% SDS的pH 6.8缓冲液和含0.5% SDS的水溶液作为帕博西尼胶囊溶出测定的溶出介质。
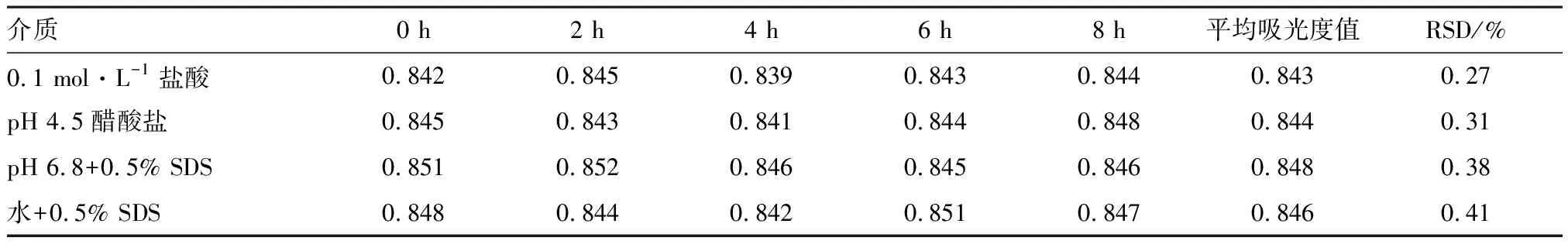
表2 各溶出介质的帕博西尼溶出溶液在不同时间吸光度值比较

图4 帕博西尼胶囊在不同介质中的溶出曲线

图5 帕博西尼胶囊在含不同浓度的SDS水溶液中的溶出曲线
2.1.8溶出测定方法 参照FDA[3]公布的帕博西尼胶囊溶出方法,具体测定方法如下:
取帕博西尼胶囊,照溶出度测定法[《中国药典》(ChP)2015年版四部通则0931第二法],溶出介质(① 0.1 mol/L盐酸溶液;②pH 4.5醋酸盐缓冲液;③含0.5 % SDS的pH 6.8磷酸盐缓冲液;④含0.5 % SDS的水溶液)900 mL,转速为50 r/min,依法操作,经指定时间点(5、10、15、30、45和60 min),取溶液7 mL(同时补加等温介质7 mL),经0.45 μm水系滤膜滤过。精密量取续滤液1 mL,置10 mL量瓶中,加0.1 mol/L盐酸溶液稀释至刻度,摇匀,作为样品溶液。照紫外-可见分光光度计[《中华人民共和国药典》(ChP)2015年版四部通则0401],在365 nm波长处测定吸光度值,按照外标法计算溶出度,绘制溶出曲线。采用f2法评价自制制剂和参比制剂的体外溶出行为一致性。
2.2处方筛选原研参比制剂说明书中披露了帕博西尼胶囊内容物所含有的非活性成分:乳糖、微晶纤维素、羧甲淀粉钠、二氧化硅和硬脂酸镁。参照原研参比制剂帕博西尼胶囊内容物辅料组成,选择无水直压乳糖、微晶纤维素PH102、羧甲淀粉钠、二氧化硅和硬脂酸镁进行处方筛选。
原研参比制剂帕博西尼胶囊内容物不含有黏合剂,推测其内容物采用干法制粒或直接混合工艺制成。观察其内容物性状,为均匀的粉末,未发现有颗粒,进一步确定参比制剂采用原辅料粉末混合,直接灌装胶囊的基本工艺。将内容物称重,为450 mg。初步确定制备工艺如下:
准确称取处方量的帕博西尼、无水直压乳糖、微晶纤维素PH102、羧甲淀粉钠和二氧化硅,混合均匀,称取处方量的硬脂酸镁,混合均匀,得帕博西尼胶囊总混粉末,灌装0 #胶囊,每粒450 mg。
2.2.1填充剂比例筛选 设计不同填充剂比例的处方(表3),测定其在pH 4.5醋酸盐缓冲液和含0.5% SDS的水溶液中的溶出曲线,结果见表4。试验结果表明:三批自制制剂与参比制剂在pH 4.5醋酸盐缓冲液中溶出曲线均一致(f2> 50),相似性顺序:R3>R2>R1。三批自制制剂与参比制剂在含0.5% SDS的水溶液中的溶出曲线均不一致(f2<50),相似性顺序:R2>R1>R3。综合考虑优选MCC /乳糖比例为1∶4(R2)。
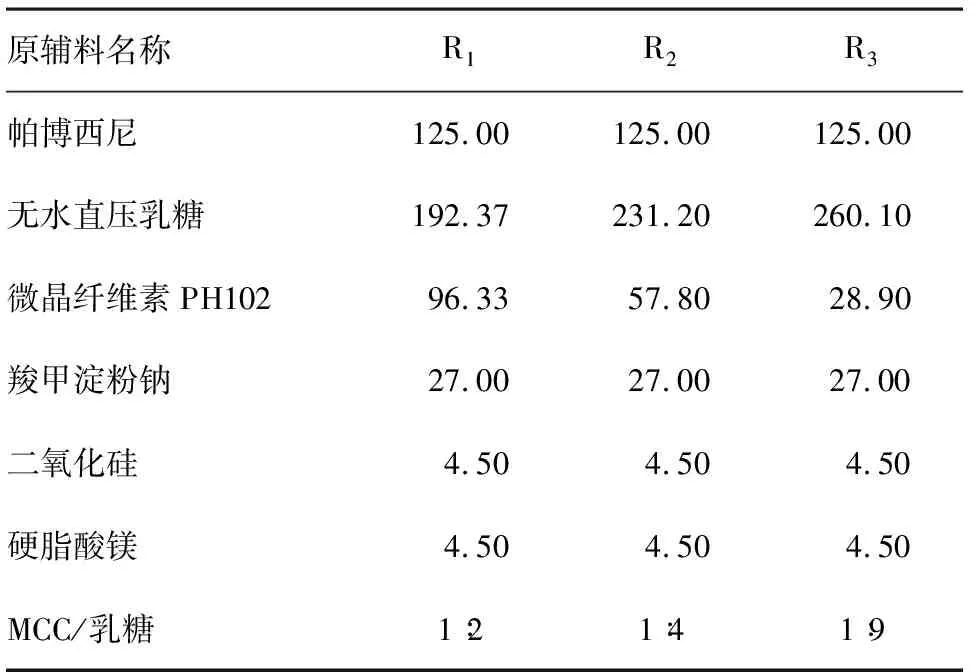
表3 填充剂比例筛选处方表/(毫克/片)
2.2.2崩解剂用量筛选 设计不同崩解剂用量的处方(表5),测定其在pH 4.5醋酸盐缓冲液和含0.5% SDS的水溶液中的溶出曲线,结果见表6。试验结果表明:自制制剂在pH 4.5醋酸盐缓冲液中前期溶出随着崩解剂用量的增加而变快,与参比制剂在pH 4.5醋酸盐缓冲液中溶出曲线均一致(f2> 50),相似性顺序:R2>R5>R4。崩解剂用量在3.00~9.00 %范围内,对自制制剂在含0.5% SDS的水溶液中的溶出无明显影响,与参比制剂溶出曲线均不一致(f2< 50),因此需要进一步优化处方。
2.2.3崩解剂厂家筛选 在处方R2基础上,设计不同崩解剂厂家的处方,测定其在pH 4.5醋酸盐缓冲液和含0.5 % SDS的水溶液中的溶出曲线,结果见表7。试验结果表明:三批自制制剂与参比制剂在pH 4.5醋酸盐缓冲液中溶出曲线均一致(f2> 50)。采用法国罗盖特和台湾永日化学的羧甲淀粉钠制备的自制制剂R6和R7与参比制剂在含0.5% SDS的水溶液中的溶出曲线一致(f2> 50),因法国罗盖特制药的羧甲淀粉钠无进口注册证,优选台湾永日化工的羧甲淀粉钠作为本产品的崩解剂。

表4 填充剂比例筛选溶出结果
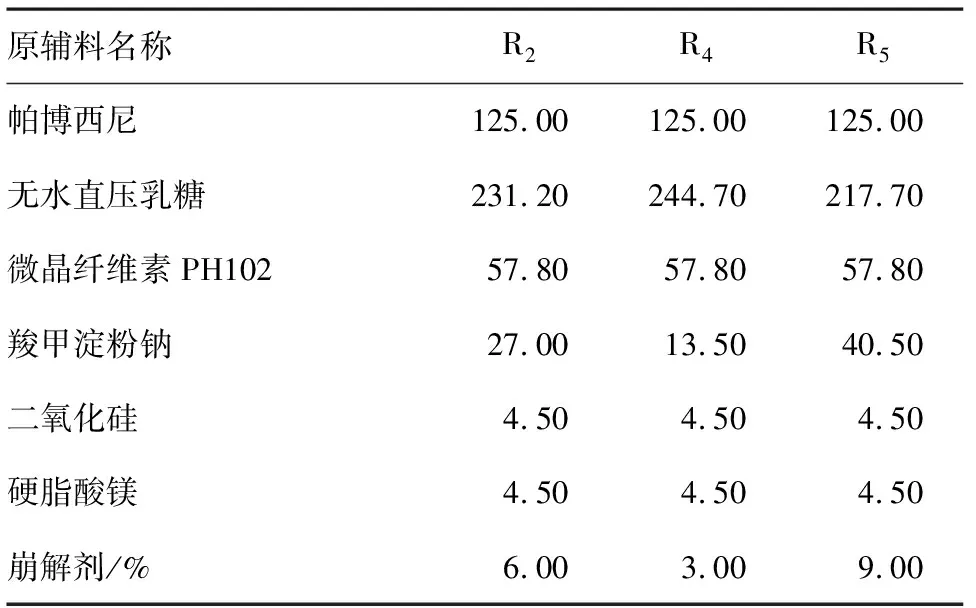
表5 崩解剂用量筛选处方表/(毫克/片)
2.2.4原料粒度筛选 在处方R7基础上,设计不同原料粒度的处方,测定其在pH 4.5醋酸盐缓冲液和含0.5% SDS的水溶液中的溶出曲线,结果见表8。试验结果表明:自制制剂在pH 4.5醋酸盐缓冲液和含0.5% SDS的水溶液中的溶出随着原料药粒度的减小而明显变快,自制制剂R7和R8与参比制剂在pH 4.5醋酸盐缓冲液中溶出曲线一致(f2>50),相似性顺序:R7>R8。自制制剂R7和R9与参比制剂在含0.5% SDS的水溶液中溶出曲线一致(f2>50),相似性顺序:R7>R9。
测定自制制剂R7在0.1 mol/L盐酸溶液和含0.5% SDS的pH 6.8磷酸盐缓冲液中的溶出曲线,自制制剂R7和参比制剂在0.1 mol/L盐酸溶液(15 min累积溶出度大于85.0 %)和含0.5% SDS的pH 6.8磷酸盐缓冲液(f2>50)中的溶出曲线一致。
综合自制制剂溶出测定结果,初步确定处方R7为最优处方。
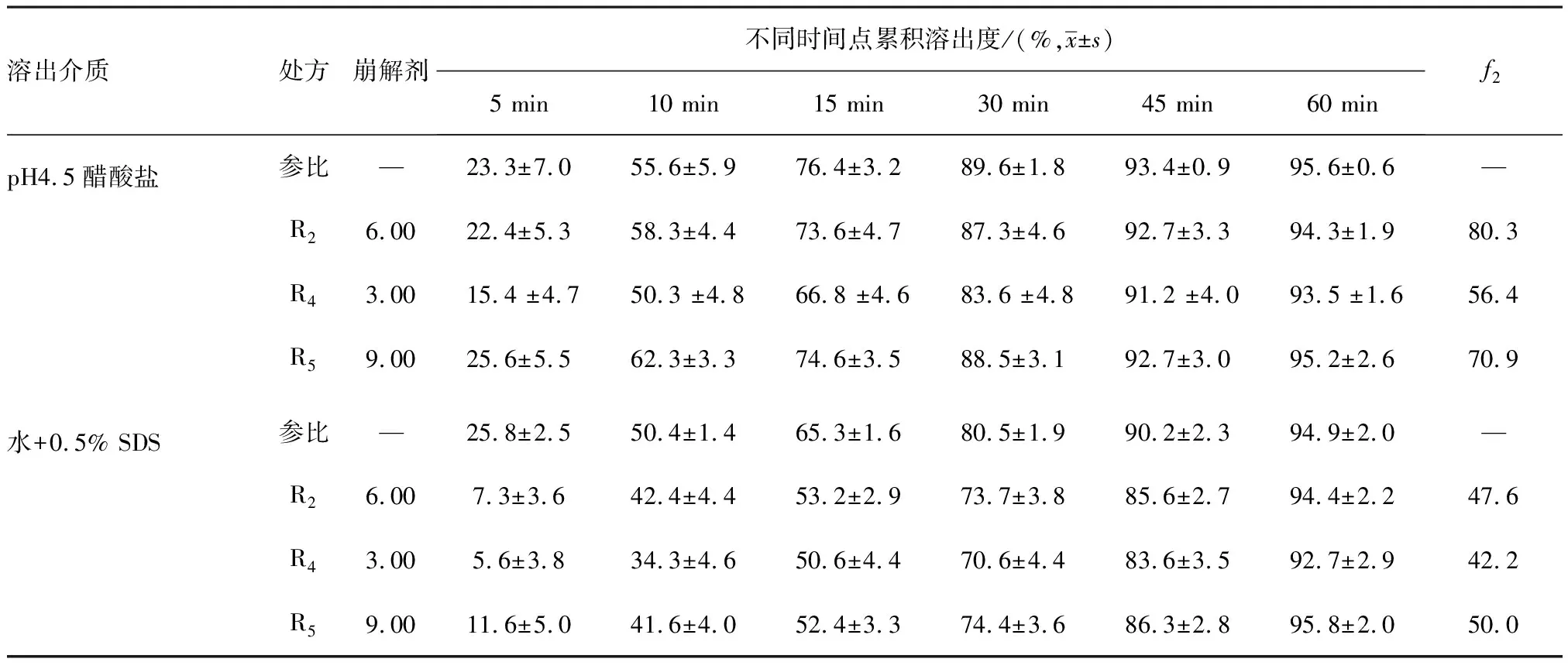
表6 崩解剂用量筛选溶出结果
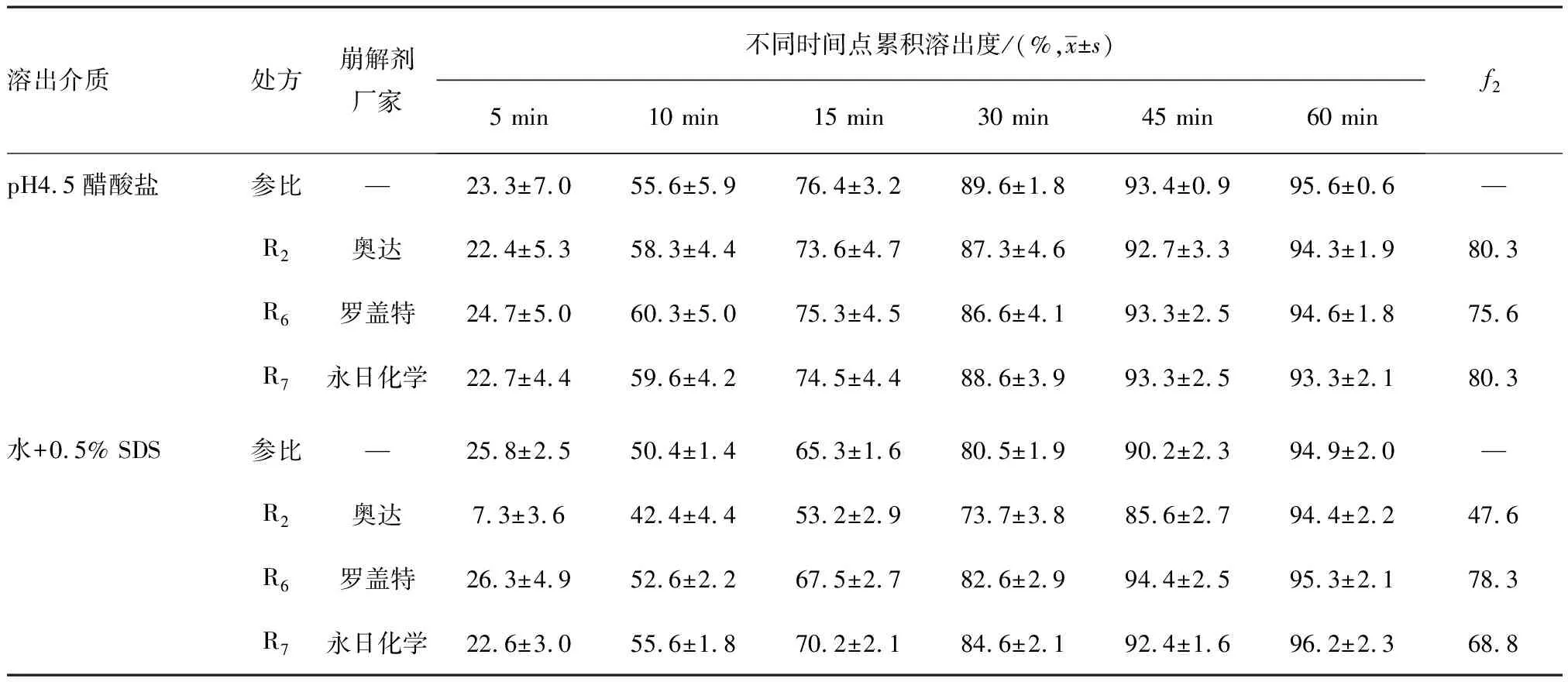
表7 崩解剂厂家筛选溶出结果
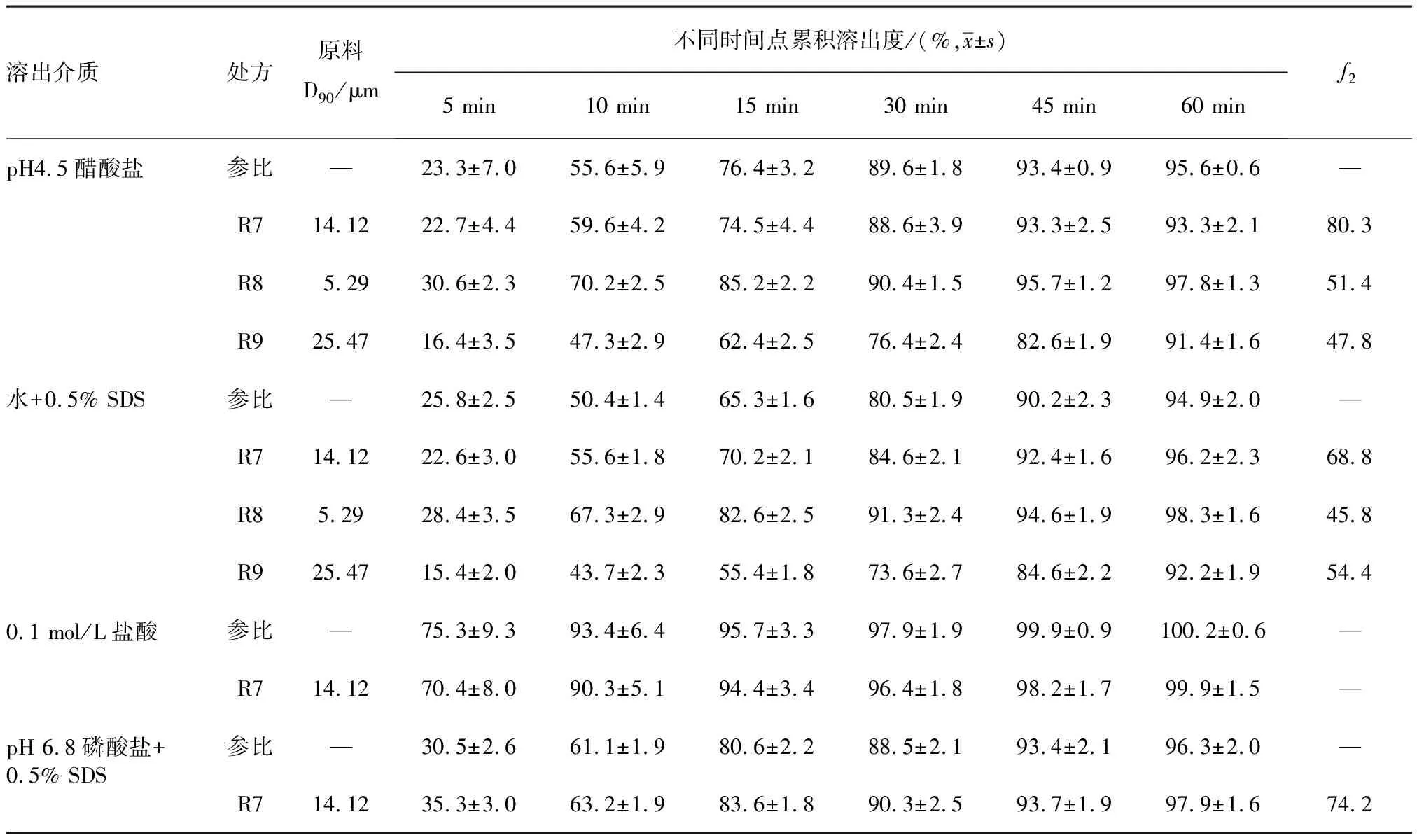
表8 原料粒度筛选溶出结果
2.3中试样品制备在上述处方R7原辅料种类不变的基础上,分别采用三批原料药(D90分别为15.39、17.65和12.48 μm),原辅料混合后直接灌装胶囊的基本工艺,进行3批2.4万粒的中试样品的制备,测定3批中试样品在四种溶出介质中的溶出曲线,并与原研参比制剂比较,结果见表9和图6~9。由表9和图6~9可知,自制制剂与参比制剂在四种溶出介质中的溶出曲线均一致,表明处方工艺可行。
最终确定帕博西尼胶囊内容物:微晶纤维素 PH102 / 无水直压乳糖为1∶4,台湾永日化学的羧甲淀粉钠为6.00 %,原料药粒度D90为12.00~18.00 μm。单剂量处方:帕博西尼125.00 mg,无水直压乳糖231.20 mg,微晶纤维素PH102 57.80 mg,羧甲淀粉钠27.00 mg,二氧化硅4.50 mg,硬脂酸镁4.50 mg。

表9 自制制剂和参比制剂溶出曲线比较

图6 帕博西尼胶囊在0.1 mol·L-1盐酸溶液中的溶出曲线

图7 帕博西尼胶囊在pH 4.5醋酸盐缓冲液中的溶出曲线
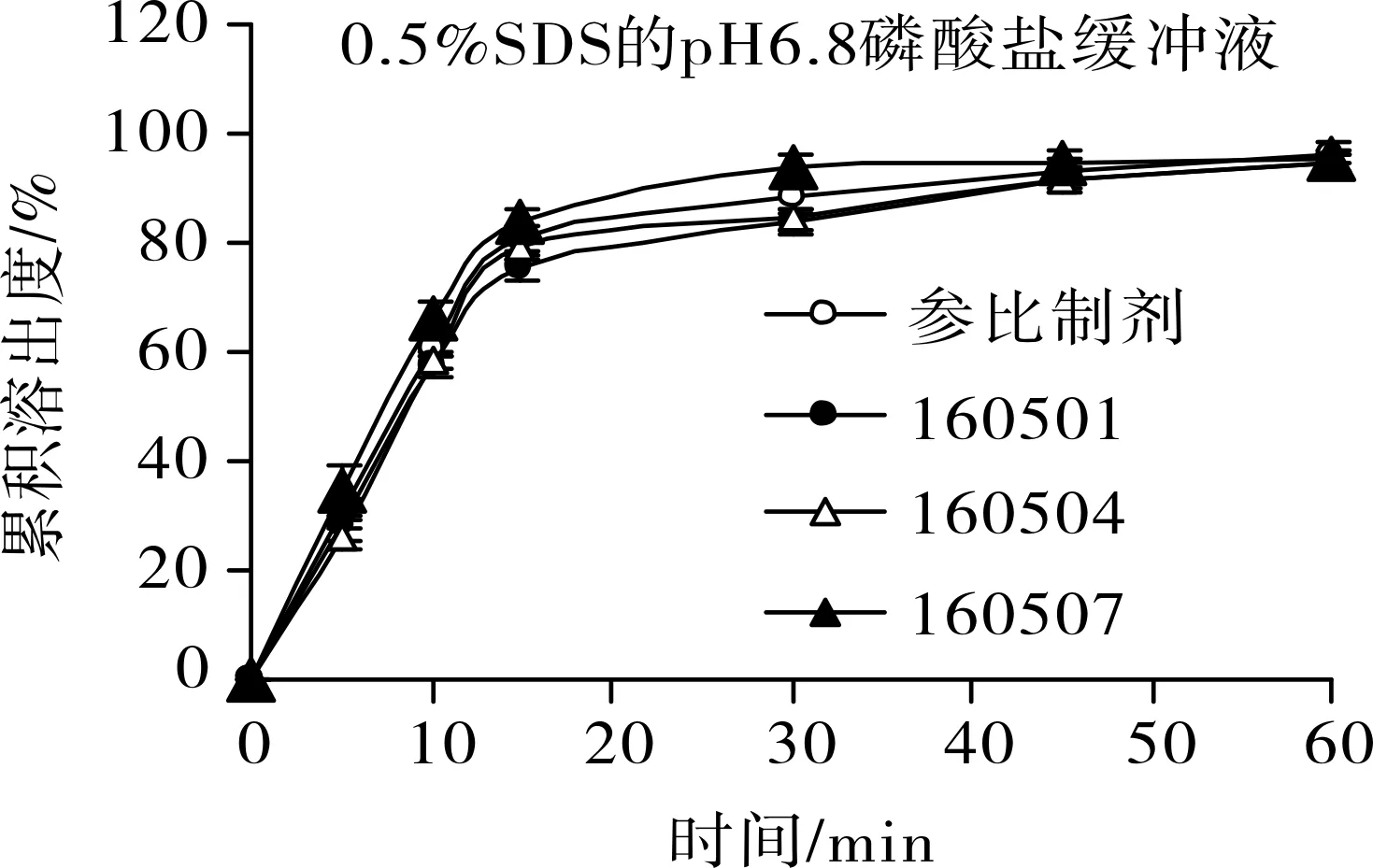
图8 帕博西尼胶囊在含0.5 % SDS的pH 6.8磷酸盐缓冲液中的溶出曲线
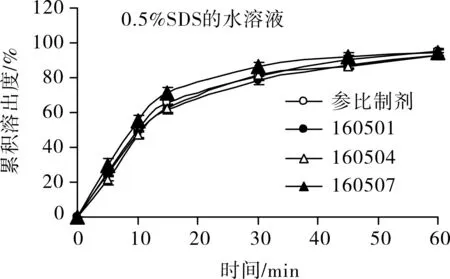
图9 帕博西尼胶囊在含0.5 % SDS的水溶液中的溶出曲线
2.4溶出、性状和水分稳定性研究以高密度聚氯乙烯塑料瓶(内加干燥剂)为包装材料,经加速条件(40 ℃±2 ℃,RH 75%±5%)下放置6个月,考察帕博西尼胶囊溶出曲线、内容物性状和水分,结果见表10~11。由表11可知,自制制剂加速条件下放置6个月,与0月相比,溶出曲线、内容物性状和水分无明显变化。
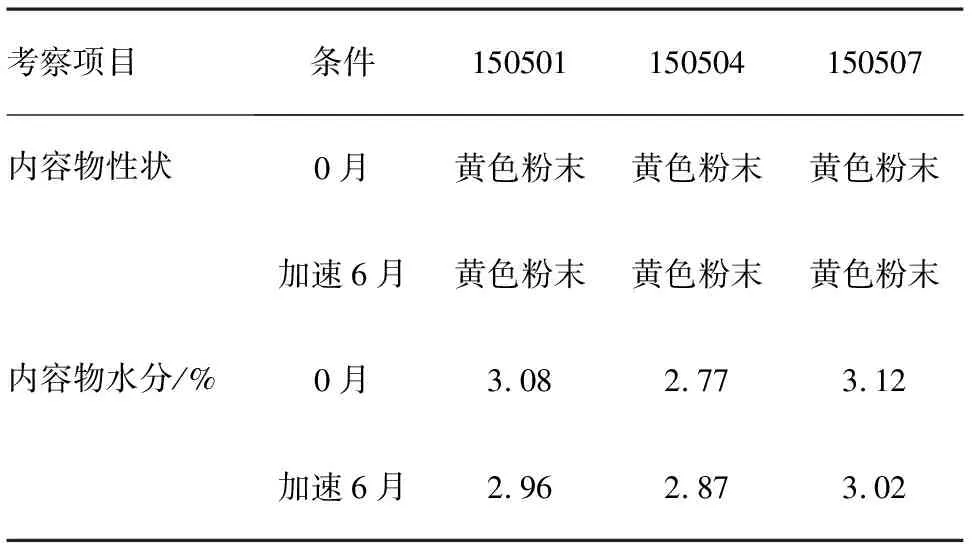
表10 自制制剂内容物性状和水分稳定性考察结果
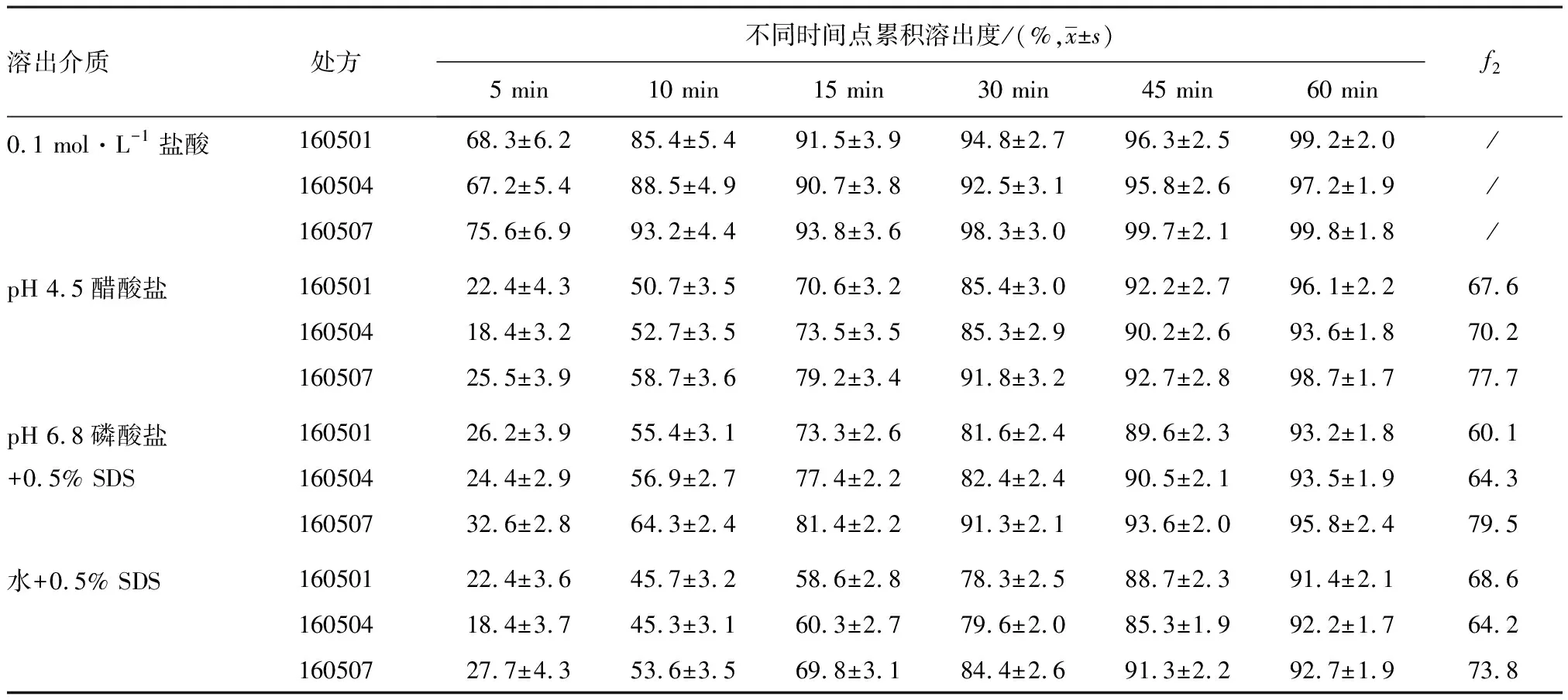
表11 自制制剂加速(40 ℃±2 ℃,RH 75%±5%)6个月样品溶出数据
3 讨论
羧甲淀粉钠由淀粉经过适度交联反应后,在适宜的碱性条件下与一氯乙酸进行醚化反应得到,产品的黏度和取代度影响其崩解性能[4]。与辽宁奥达制药的羧甲淀粉钠相比,采用法国罗盖特和台湾永日化学的羧甲淀粉钠制备的帕博西尼胶囊在含0.5 % SDS的水溶液中累积溶出度明显变快,推测可能是不同厂家羧甲淀粉钠的的黏度和取代度不同所致。
原料药粒度是影响药物体外溶出的重要因素,一般来说,原料药粒度越小,表面积越大,体外溶出越快[5-6]。本文考察帕博西尼原料药粒度对帕博西尼胶囊体外溶出的影响,体外累积溶出度随着原料药的粒度的减少而变快。
体外溶出度实验是筛选制剂处方和控制其质量的重要手段,因为它和药物的生物利用度相关。以f2评价自制制剂和参比制剂的溶出度曲线现已被广泛应用[7-9]。当f2值在50~100时,认为两制剂的体外溶出行为一致;f2值愈接近100,相似程度就愈高;f2值< 50时,则认为两制剂的体外溶出行为不一致。
本课题通过原辅料直接混合,然后灌装胶囊的基本工艺,制备帕博西尼胶囊,工艺简单易行,制备的3批自制制剂与参比制剂在四种溶出介质中的溶出曲线均一致。自制制剂加速条件下放置6个月,与0月相比,溶出曲线、内容物性状和水分无明显变化,表明筛选的帕博西尼胶囊处方可行。
