一种智能营养筛查系统用于住院肿瘤患者营养风险的预测性分析
2019-03-04王艳莉龚丽青辛晓伟商维虎
王艳莉,龚丽青,辛晓伟 ,刘 妮,商维虎,方 玉
(1北京大学肿瘤医院暨北京市肿瘤防治研究所营养科,北京 100142;2北京康爱营养医学研究院,北京 102206)
近年来,我国恶性肿瘤的发病率和死亡率逐渐增高,成为威胁居民健康的主要因素之一,而营养不良是恶性肿瘤患者的主要死亡原因[1]。研究发现,45%~80%的肿瘤患者会出现营养不良[2-5]。据报道,每年有200万肿瘤患者死于严重营养不良,20%~50%的患者死于营养不良或恶液质,而非肿瘤本身。2002 年欧洲肠外肠内营养学会(ESPEN)提出营养风险概念,即现存或潜在营养和代谢状况所导致的疾病或手术后出现相关的临床结局的机会[6],对营养风险或者营养不足患者给予营养支持可改善其临床结局[7]。国内外指南均推荐,应在患者入院24h内进行营养风险筛查,对于存在营养风险的患者,需进行营养评估;对于没有营养风险的患者,每隔1w应再筛查1次。营养风险筛查的滞后,导致一部分肿瘤病人得不到及时的营养风险筛查及干预,可能会造成营养不良风险的增加及不利的临床结局。J.Abbott等[8]发表了一种可用于肿瘤门诊预测营养风险的自动化的营养筛查系统研究,针对300名门诊化疗患者的研究,发现与PG-SGA结果对比后灵敏度和特异度分别为63%和76.7%[8]。本研究采用ESPEN和CSPEN推荐的营养风险筛查2002(NRS 2002)方法对新入院的肿瘤患者进行营养风险调查,了解各科室新入院患者的营养风险发生概率,验证智能化营养风险筛查系统的灵敏度和特异度。
1 材料和方法
1.1 研究对象
2017年12月4—15日,连续选取本院放疗科、消化内科2个科室的新入院的肿瘤患者作为研究对象。入组标准:符合肿瘤诊断的住院患者、年龄>18周岁、获得知情同意。排除标准:急诊手术、住院不足1d、孕期及哺乳期患者。
1.2 样本量计算
文献报道灵敏度为63%,设定本研究目标为75%。采用PASS 2008 软件估算样本含量,采用confidence interval for proportion设计,根据文献报道,诊断试验的灵敏度75%、特异度75% 。灵敏度、特异度容许误差取0.1;选取置信度1-α=0.95,Alpha取0.05(双侧检验),通过软件运行取最大样本量:306,再加10%失防,共需337例。本次先开展预试验,每个科室各连续采样筛查100例新入院患者。
1.3 营养风险筛查
1.3.1NRS 2002 研究对象入院后24h内,由受过专门培训的营养师采用NRS 2002 方法进行营养风险筛查,NRS 2002 评分≥3 分为有营养风险。
1.3.2智能化营养风险筛查系统—一键筛查 一键筛查系统与医院HIS、LIS、电子病历系统对接后,通过提取患者营养相关信息,自动识别出存在营养风险的患者。
1.4 质量控制
由接受过标准化培训的专业人员采用统一调查表收集数据,所有量表、身体测量及生化指标检查均于入院第2天完成。身高、体质量测定要求晨起排尿、排便、穿单衣、脱鞋,精确至0.1kg,身高精确至0.1cm。生化指标包括:白细胞(WBC)、淋巴细胞(LY)、红细胞、血红蛋白(HGB)、总蛋白(TP)、白蛋白(ALB)。
1.5 操作流程
新入院患者营养风险筛查:对新入院患者进行床旁营养风险筛查,同时记录每一例患者筛查开始时间点和完成时间点,相关信息记录在筛查量表中。新入院患者营养评估:采用NRS 2002量表对新入院患者进行营养评估,相关信息记录在营养评估量表中。第2天,由智能筛查系统对前1天的新入院患者进行智能筛查,并导出相关筛查结果。复核每例患者定量资料和定性资料。相关信息填写在病例报告表中。
1.6 统计分析

2 结果与分析
2.1 一般资料
共调查205例患者,其中消化内科99例、放疗科106例。其中男性134例(65.4%)、女性71例(34.6%)。平均年龄56.5岁,平均身高165.5cm,平均体重63.6kg,平均BMI 23.2。按病种分类,头颈颌面部肿瘤(鼻咽肿瘤、口腔肿瘤)48例(23.4%)、消化系统肿瘤(食管肿瘤、结直肠肿瘤、胰腺肿瘤、胆囊肿瘤、肝肿瘤)110例(53.7%)、肺部肿瘤35例(17.1%)、妇科肿瘤(宫颈肿瘤、外阴肿瘤)9例(4.4%)、乳腺肿瘤1例(0.5%)、其他部位肿瘤(黑色素肿瘤、神经内分泌肿瘤)2例(0.9%)。肿瘤患者BMI分布情况,从性别来看,男性超重比例高于女性;从病种看,肺癌患者超重比例最高,头颈癌消瘦比例最高(表1)。
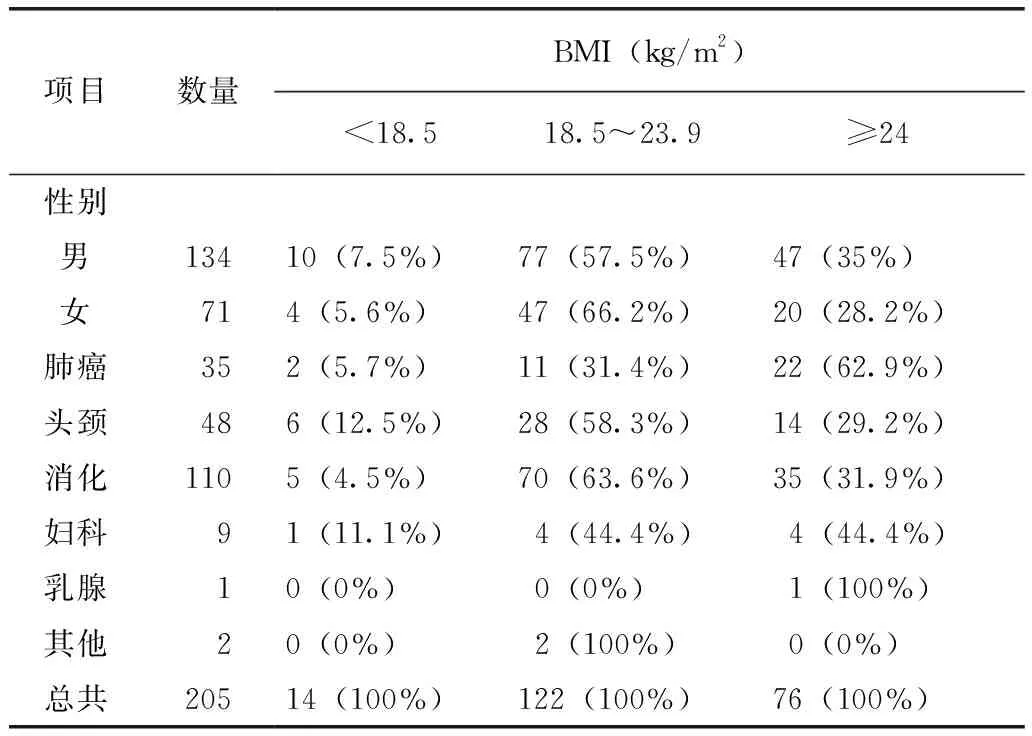
表1 肿瘤患者BMI分布情况
2.2 灵敏度、特异度、准确性计算
与NRS 2002营养风险结果相比,智能筛查系统的灵敏度、特异度、准确性计算见表2。
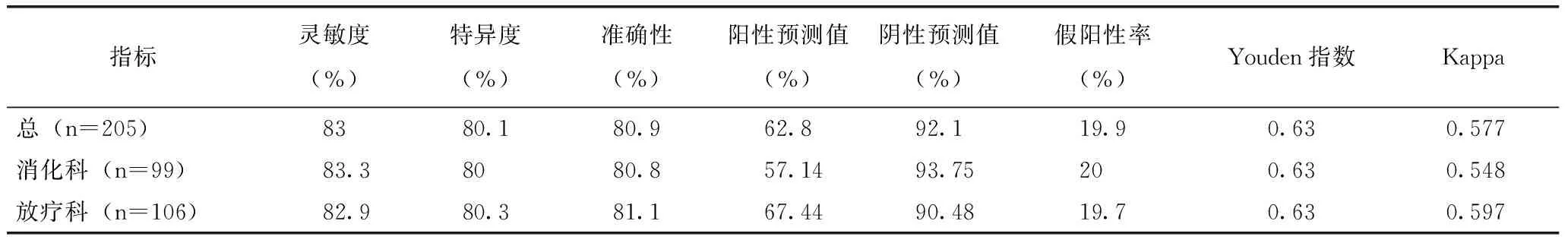
表2 灵敏度、特异度、准确性计算
2.3 智能筛查系统与NRS 2002筛查结果比较
消化科、放疗科应用智能筛查系统与NRS 2002筛查结果比较(表3)。

表3 智能筛查系统与NRS 2002筛查结果比较
2.4 NRS 2002、智能筛查系统与客观指标的相关性分析
NRS 2002和智能筛查系统均与体重、体重下降、BMI、影响进食的症状存在明显相关性(P<0.01),均与年龄、身高无明显相关性。但智能筛查系统在影响进食症状、体重下降、BMI的相关性优于NRS 2002;NRS 2002在体重的相关性优于智能筛查系统。NRS 2002与智能筛查系统也存在明显的相关性(r=0.349,P<0.000)(表4)。

表4 NRS 2002、智能筛查系统与客观指标的相关性分析
2.5 营养筛查工具评价营养风险和营养正常组相关指标比较
按NRS 2002评分分组,NRS 2002<3分组较NRS 2002≥3分组的体重、BMI、TP、ALB、LY、HGB、RBC存在统计学差异(P<0.05);而智能筛查系统评分分组,无营养风险组较营养风险组只有在体重、BMI、ALB、HGB、RBC存在统计学差异(P<0.05)(表5)。

表5 营养筛查工具评价营养风险和营养正常组相关指标比较
3 讨论
癌症相关营养不良高发,营养筛查有利于早期发现存在营养风险的患者,对其进行合理、有效的营养治疗可以减少患者的住院时间、住院费用[9-10]。现有的营养筛查多集中在人工筛查,智能筛查比较少见,筛查工具包括NRS 2002、MST、MUST等。NRS 2002 是欧洲肠内肠外营养学会(ESPEN )推荐住院患者最常使用的营养风险筛查方法,也是中华医学会肠外肠内营养学分会推荐使用的营养筛查工具[11],其应用更为简单,筛查时间短,不仅考虑手术对患者营养风险的影响,同时也将患者年龄考虑在其中,更为全面,其灵敏度及特异度均较高[12-14]。
3.1 肿瘤营养风险发生率
本研究采用智能筛查系统与NRS 2002进行比对。智能化营养筛查系统与医院HIS、LIS、电子病历系统对接后,通过提取患者营养相关信息,如BMI、进食减少、体重下降等,自动识别出存在营养风险的患者。本研究显示,与NRS 2002相比,智能筛查系统灵敏度、特异性、准确性均较好;Kappa用于评价一致性,Kappa ≥0.75 两者一致性较好;0.4 ≤Kappa≤0.75两者一致性一般;Kappa≤0.4 两者一致性较差。Kappa值越低,表明与传统营养评价方法一致性较低。本研究Kappa为0.577,两者具有一致性。智能筛查系统的营养风险发生率为38%,较NRS 2002筛查(28.8%)率高,差异有统计学差异(P<0.05)。可见智能筛查较NRS能筛出更多的营养异常风险患者。这与其他应用MNA-SF、MUST、NRS 2002进行营养筛查的研究结果相似[15-16]。本研究发现,消化科营养不足的发生率为5.1%,营养风险发生率智能筛查系统、NRS 2002分别为35.4%、24.2%;放疗科营养不足的发生率为8.5%,营养风险发生率智能筛查系统、NRS 2002分别为40.6%、33%。其他研究发现,肿瘤患者营养风险发生率为31.8%~45.83%,其中消化系统肿瘤患者营养不足、营养风险发生率分别为12.4%、38.2%~44.7%,放疗肿瘤患者营养不足、营养风险发生率为分别36.8%、50.5%[17-19],营养风险筛查结果与本研究结果相似,其中本研究营养不足发生率低于既往研究,可能与患者分期较早,不良反应轻,大城市患者接受营养支持率高等相关。
3.2 两种筛查工具与客观指标相关性的比较
既往有研究提示,NRS 2002虽灵敏度、特异度较高,但测评结果并不客观,与客观指标的相关性并不理想[20-22]。本研究结果提示,NRS 2002和智能筛查系统均与体重、体重下降、BMI、影响进食的症状存在明显相关性(P<0.01),但智能筛查系统在影响进食症状、体重下降、BMI的相关性明显优于NRS 2002;可能两种筛查方法的侧重点并不完全一致,NRS 2002的优点是能反映较近的或者急性的营养状况的改变,易发现早期的营养不良,简单易行,但其不足之处是当患者卧床,或有水肿、腹腔积液等影响体质量的测量及患者意识不清时该工具的使用受到限制。因此,对是否适用于肿瘤患者及是否可以作为营养治疗的依据一直有争论[23-27]。智能筛查系统里面,为肿瘤病人添加了食欲下降、恶心、呕吐、乏力、腹胀、腹痛、腹泻等与影响进食的关键词,实验室检查中的ALB、HGB,医生的膳食医嘱中的流食、半流食、禁食等,以确定患者是否存在营养风险。在评价营养风险和营养正常组相关指标比较方面,智能筛查系统与NRS 2002两者均在体重、BMI、ALB、HGB、RBC存在统计学差异。在WBC方面,智能筛查系统与NRS 2002两者均无统计学差异,可能由于WBC低下组一般都会在围放化疗期注射白细胞刺激因子或口服升白细胞药物,导致白细胞数值不能真实反映患者的客观营养水平。
现代化医学信息在向智能化发展,智能化便利、省时、准确,但如果不能合理的实施,也存在着风险。目前的智能筛查研究显示与体重下降、影响进食的症状相关性高,但并没有体重下降或改变的具体时间段,也没有进食量较少的具体量,因此仍然需要进一步的人工营养筛查与评估。建议对将来的研究可考虑添加更多相关的营养指标。
4 结论
本研究结果提示,智能筛查系统对营养风险异常的检出率相当高,比较敏感,准确。可作为初步筛查,这样大大节省了人力、物力及时间。有营养风险的患者,可结合NRS 2002进一步进行筛查评估。但是,需要在更多的病种和患者中进行验证。◇
