CPDB单一柱撑蒙脱石与CPDB/Al复合柱撑蒙脱石对水中Cr(Ⅵ)的吸附研究
2019-03-02吴笑江赵彬侠刘田野韩锐暄任海月
吴笑江,赵彬侠,刘田野,岳 能,韩锐暄,任海月,陈 蓉
(西北大学 化工学院, 陕西 西安 710069)
铬(Cr)存在于土壤、水体、植被及大气中,被广泛应用在冶金、电镀、制革、采矿、炼钢、染料等行业。在自然界中Cr最常见的形式是Cr(Ⅲ)和Cr(Ⅵ)。其中,Cr(Ⅵ)具有高毒性可引发过敏、肺癌,已被世界癌症协会确认为重要的致癌物质[1-2]。因此,含铬废水必须经过严格的处理工序。常用的含铬废水处理方法有电解法、离子交换法、吸附法等。Dhal B[3]和王湖坤[4]等利用电解法将Cr(Ⅵ)转化为Cr(Ⅲ),罗斌[5]等利用树脂的离子交换性将CrO72-回收。相比以上方法,吸附法效率高、选择性好、操作简单等优点。常用的吸附材料有活性炭、SiO2、蒙脱石(MONT)等。本课题在溴化十六烷基吡啶(CPDB)柱撑蒙脱石的基础上继续通过聚合羟基铝引入铝源制备复合改性MONT吸附剂。对模拟Cr(Ⅵ)溶液去除率进行比较并结合必要的表征手段对其机理做出一些推测。
1 实 验
1.1 实验步骤
将一定质量的MONT加入蒸馏水中,配制成质量比1∶100的MONT悬浮液; 将一定量的CPDB粉末,溶解于蒸馏水中,得到CPDB柱化剂;将一定量的NaOH 溶液逐滴加入到 AlCl3·6H2O溶液中,使c(OH-)/c(Al3+)=2.0,得到Al源柱化剂,再将CPDB柱化剂和Al源柱化剂混合均匀静置30min后,加入至MONT悬浮液,经搅拌、老化、静置过夜。多次离心洗涤至无Br-。将白色固体于60℃下干燥12h,得到CPDB单一柱撑蒙脱石(CPDB-MONT)与羟基铝复合柱撑蒙脱石(Al-CPDB-MONT)。实验中以K2Cr2O7为铬源配制含铬废水。将称量的0.1g CPDB-MONT和Al-CPDB-MONT加入至100mL,10 mg/L的含铬废水中,进行搅拌吸附反应,每隔一定时间间隔后取样,过滤,通过吸光度检测溶液中Cr(Ⅵ)的浓度,计算Cr(Ⅵ)去除率。
1.2 吸附剂的表征
XRD分析采用XRD-6100型X射线衍射仪(Cu Kα靶射线,λ=0.154 056nm,40kV,数据收集在10-80的2θ范围内,步长为0.02°/min。)实验中所有吸附剂在进行比表面积分析(BET)采用美国康塔仪器公司NOVA4000e分析仪,F-Transform I-Spectroscopic(FT-IR)采用T-Nicolet 6700红外光谱仪。①波数范围400 cm-1~4 000 cm-1,②扫描速率为0.6318cm/s,③扫描次数32次,采用德国Carl Zeiss公司生产的SIGMA型扫描电子仪。
2 结果与讨论
2.1 改性蒙脱石的表征
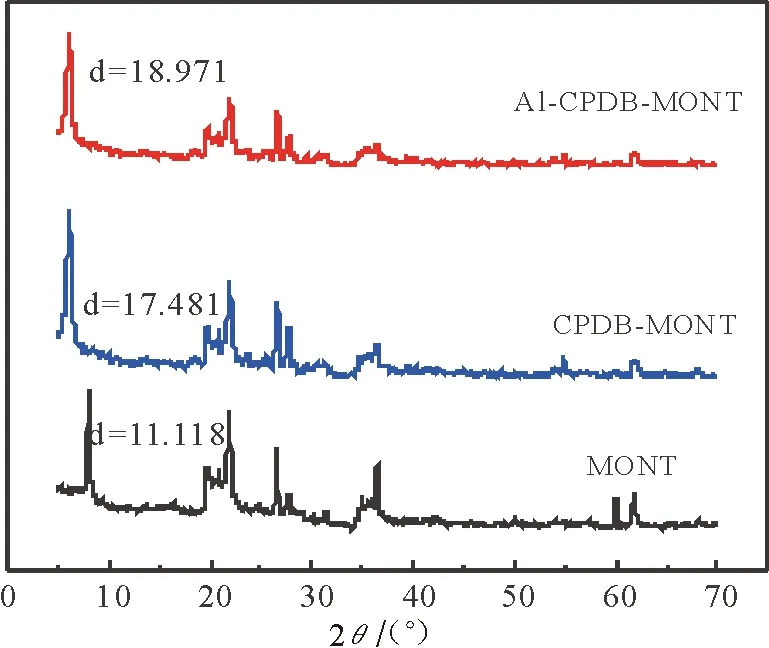
图1 不同样品XRD衍射图谱Fig.1 XRD patterns of Al-CPDB-MONT,CPDB-MONT and MONT
2.1.1 XRD表征 图1为Al-CPDB-MONT, CPDB-MONT与原MONT的XRD图谱。 对比MONT, CPDB-MONT, Al-CPDB-MONT可知, 三者的峰形较为相似。 在2θ=7.945°附近可看到明显的蒙脱石特征衍射峰, MONT在此处对应的d(001)值为1.111 8nm,而CPDB-MONT和Al-CPDB-MONT在此处的对应d(001)分别增加到1.898 7nm,1.935 4nm,表明了CPDB分子与羟基铝已成功柱撑进入蒙脱石层间。Al-CPDB-MONT的d(001)值较CPDB-MONT更大,这表明复合柱撑可以更进一步扩大蒙脱石的分子层间距,其吸附能力可能更强。经过改性后的Al-CPDB-MONT相比于原CPDB-MONT片层厚度多0.910nm左右,该结果与文献[8]所述羟基铝片层厚度结果一致,表明了羟基铝已成功进入MONT层间。对比三者在2θ=21.860°和2θ=26.559°两处附近的SiO2特征衍射峰[9]。可以看到两种柱撑土的峰强度均有所减弱,这表明有部分SiO2晶型被破坏,可能是由于CPDB分子破坏了原本蒙脱石结构中的Si—O键导致的。在2θ=36.420°,61.798°两处归属于Fe2O3的衍射峰上也有相似现象,可能是因为CPDB分子与蒙脱石层间发生了离子交换,置换了部分Fe。
2.1.2 N2吸附脱附 表1为不同样品BET表征参数。显然经过柱撑后,CPDB-MONT与Al-xCPDB-MONT比表面积、孔径、总孔容都有了明显增加。相比之下,Al-CPDB-MONT的平均孔径、总孔容和比表面积都要比CPDB-MONT大,也表明了Al-CPDB-MONT可能有更强的吸附能力。
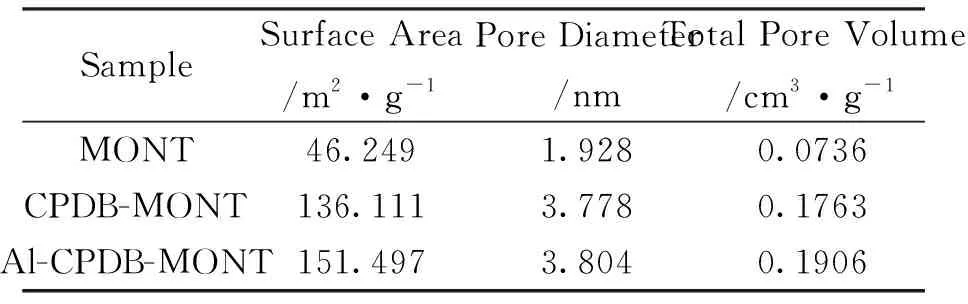
表1 样品的BET表征结果Tab.1 BET characterization results of the samples
从吸附-脱附等温线图(图2所示)可以看出,Al-CPDB-MONT,CPDB-MONT与MONT一样,均属第IV类吸附脱附等温线。这表明柱撑后的蒙脱石和原蒙脱石都具有介孔结构[10]。除了面积有较小差异,其都具有B类“滞洄环”形状特征,说明在MONT中引入Al和CPDB并未改变原土孔结构[11]。
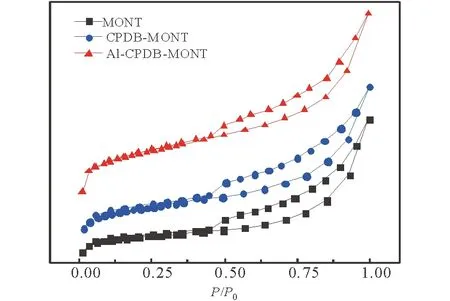
图2 Al-CPDB-MONT、CPDB-MONT和MONT3种吸附剂的氮气吸-脱附等温线Fig.2 Nitrogen adsorption-desorption isotherms of three adsorbents
2.1.3 FT-IR表征 图3为MONT及CPDB-MONT的红外吸收光谱图。 3 428cm-1和1 633cm-1处[12]分别对应土层间结合水的伸缩振动和弯曲振动,CPDB-MONT与Al-CPDB-MONT在此处的增强是由于制备过程中柱撑土未经焙烧,分子层间含有较多结合水的缘故。1 090cm-1~1 030cm-1与518cm-1~468cm-1两处吸收区变宽,分别对应Si—O键的伸缩振动与Al—O键、Si—O键的弯曲振动,表明蒙脱石中的Si—O键与Al—O键被羟基铝和CPDB分子所替换[13]。3 623cm-1处为羟基伸缩振动峰,Al-CPDB-MONT在此处的增强页说明羟基铝在进入蒙脱石分子层间的同时带入了大量羟基[14]。此外,Al-CPDB-MONT在914cm-1,870 cm-1和803cm-1处出现了新峰,此处归属于Al—O—H的伸缩振动,表明羟基铝已进入蒙脱石分子层间。
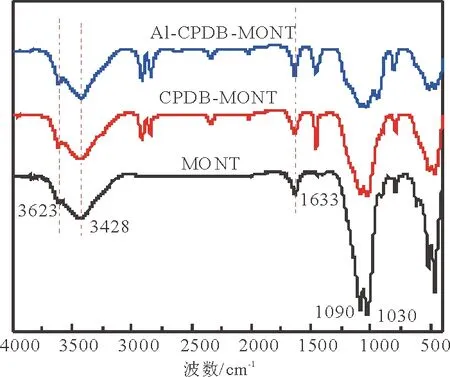
图3 复合柱撑土、单一柱撑土和蒙脱石的红外光图谱Fig.3 FT-IR spectra of Al-CPDB-MONT,CPDB-MONT and MONT
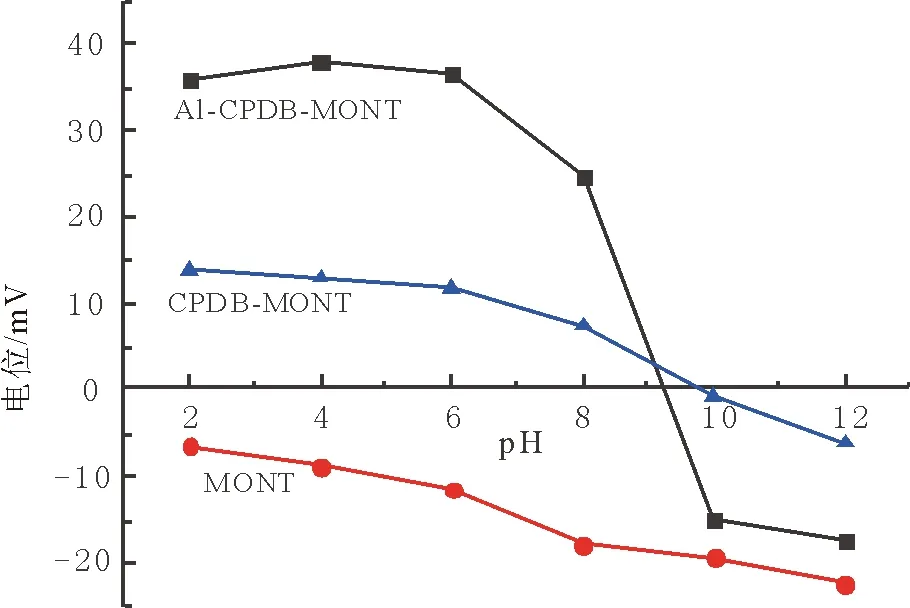
图4 Al-CPDB-MONT, CPDB-MONT和MONT的Zeta 电位Fig.4 Zeta potential of Al-CPDB-MONT, CPDB-MONT and MONT
2.1.4 Zeta电位 图4为3种蒙脱石的Zeta电位图。由此可知,MONT在整个pH范围内始终在负电位,而CPDB-MONT与Al-CPDB-MONT在酸性与弱碱性环境中表现正电位,柱撑后由负电转为正电,更有利于吸收以Cr2O72-形式存在的Cr(Ⅵ)[15]。这也表明了柱撑剂起到了改变电性的作用。
2.2 改性蒙脱石吸附 Cr(Ⅵ)的研究
2.2.1 改性蒙脱石对Cr(Ⅵ)吸附效果比较 不同吸附剂对溶液中Cr(Ⅵ)吸附率如图5所示。可以看出,柱撑土的吸附性能明显优于原蒙脱石,且Al-CPDB-MONT的吸附效果好于CPDB-MONT,去除率达到98.55%。这可能是由于羟基铝的加入进一步增大了蒙脱石分子层间距与比表面积。并且,羟基铝的加入也会使蒙脱石具有刚强的正电势(图4),对阴离子Cr2O72-产生更强的静电吸附。此外,羟基铝与CPDB二者之间可能产生了某种协同效应[16]。
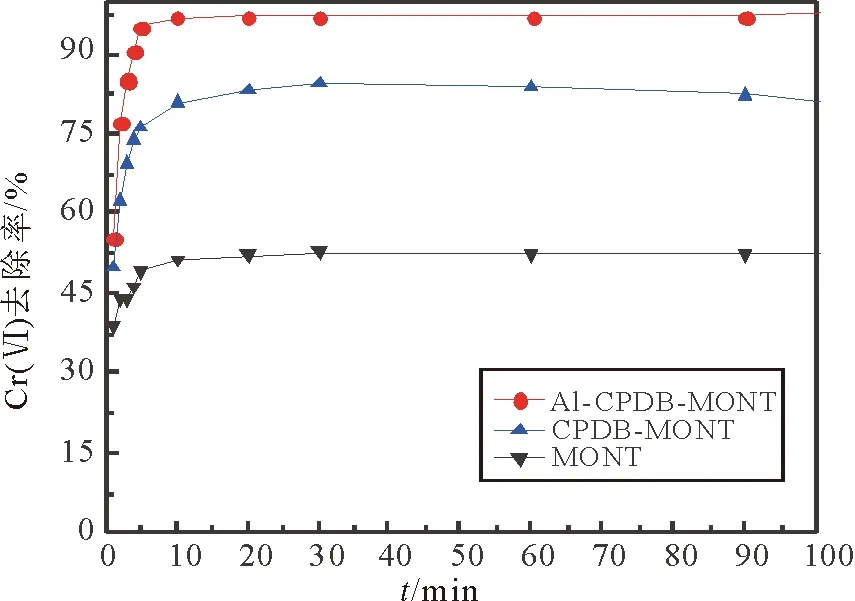
图5 Al-CPDB-MONT, CPDB-MONT和MONT对Cr(Ⅵ)去除率与反应时间对应关系Fig.5 Corresponding relationship between Cr(VI) removal rate and reaction time by Al-CPDB-MONT, CPDB-MONT and MONT
2.2.2 吸附动力学 称取0.1g CPDB-MONT和 Al-CPDB-MONT,在室温下分别加入到pH=6.0的100mL浓度为10mg/L的含Cr(Ⅵ)溶液中进行搅拌吸附2h。
将图5中数据分别用拟一级、拟二级动力学模型拟合,拟合方程式如下(1)~(4)。其中t为反应时间,qe为平衡吸附量,mg/g,qt为t时刻的吸附量,mg/g,k1是拟一级反应速率常数,min,k2为拟二级反应速率常数,g/mg·min-1。
拟一级、拟二级动力学方程表达式:
ln(qe-qt)=lnqe-k1t
(1)
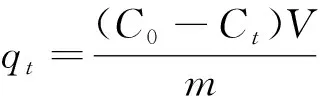
(2)
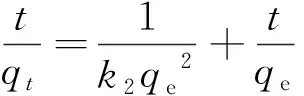
(3)
Δq(%)为实验值与理论值的标准偏差:

(4)
其中:qt,exp为实验值qt,cal为理论值。
图6可以看出,吸附剂CPDB-MONT和Al-MONT-CPDB上的Cr(Ⅵ)吸附量均随吸附时间的增加而增加,并且有呈现出先、后两个不同阶段。在吸附的初始阶段(t=0~10min)吸附速率最快,反应继续进行在(t=10~120min)吸附曲线趋于平缓,最终吸附反应呈平衡态。

图6 接触时间与CPDB-MONT和Al-CPDB-MONT对Cr(Ⅵ)单位吸附量的影响关系Fig.6 Effect of contact time and CPDB-MONT and Al-CPDB-MONT on adsorption amount of Cr(VI) units
表2为两种吸附剂的动力学拟合参数,由此可知,拟二级模型对本实验的拟合度更为符合(R2>0.999),标准差较低(Δq<1.5%)。CPDB-MONT的k值大于Al-CPDB-MONT的k值,说明前者能更快达到吸附平衡。当CPDB-MONT和Al-CPDB-MONT吸附剂表面活性吸附位点被Cr(Ⅵ)离子基团占据后,改性MONT吸附Cr(Ⅵ)方式主要由正、负电荷引力转换为蒙脱石颗粒内扩散形式。由于羟基铝的加入导致Al-CPDB-MONT的孔道遭到一定程度的堵塞,使Cr(Ⅵ)在两种吸附剂孔内的扩散速度不同,反应速率也有所不同。
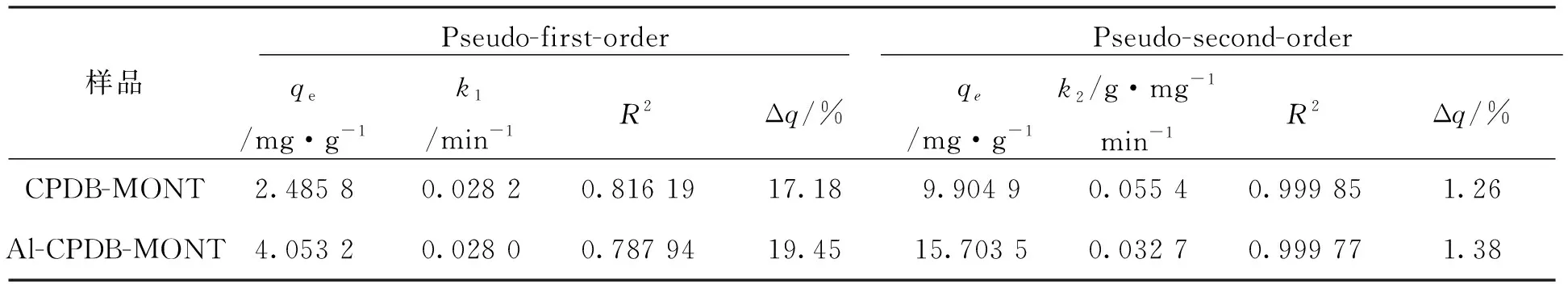
表2 CPDB-MONT和Al-CPDB-MONT吸附Cr(Ⅵ)的动力学参数Tab.2 Kinetic parameters for Cr (Ⅵ) adsorption on CPDB-MONT and Al-CPDB-MONT
2.2.3 吸附等温线 吸附等温线可以反映吸附剂的吸附性能,本实验采用 Langmuir 和 Freundlich 等温方程拟合分析。表达式如下(5)~(8):
Langmuir 方程:
(5)
(6)
Freundlich方程:
qe=KFCe1/n
(7)
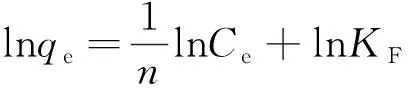
(8)
式中:C0为溶液初始浓度,mg/L,Ce为平衡浓度,mg/L,qe为平衡吸附量,mg/g,KF为Freundlich系数,KL是自由吸附能相关常数,n为Freundlich 常数。
称取0.1g CPDB-MONT和 Al-CPDB-MONT,分别加入到100mL pH=6.0,浓度为5,10,20,30,40mg/L的K2Cr2O7溶液中反应。分别在25℃,35℃和45℃的条件下进行反应,时间为2h。拟合结果如表3,4。

表3 CPDB-MONT和 Al-CPDB-MONT吸附Cr(Ⅵ)过程拟合Langmuir方程结果Tab.3 Adsorption of Cr(VI) on CPDB-MONT and Al-CPDB-MONT to fit Langmuir equation
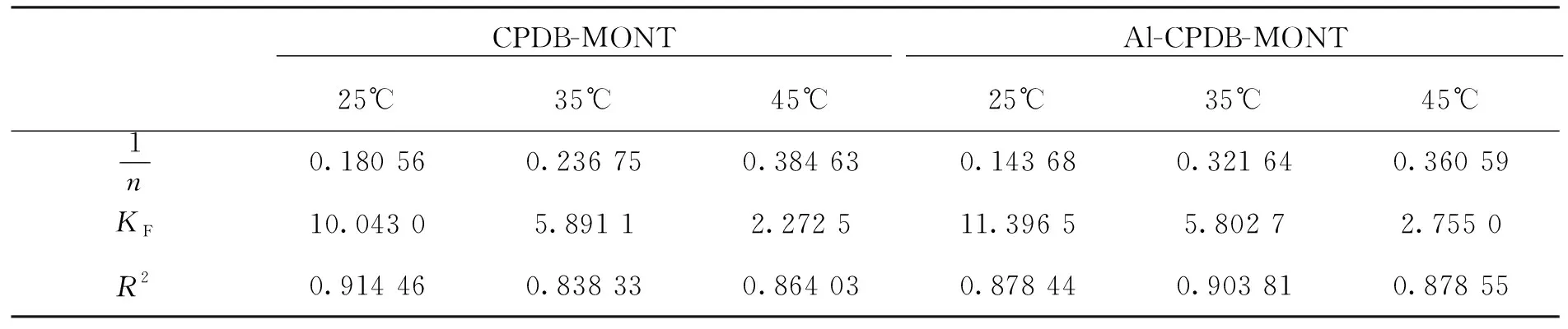
表4 CPDB-MONT和 Al-CPDB-MONT吸附Cr(Ⅵ)过程拟合Freundlich方程结果Tab.4 Adsorption of Cr(VI) on CPDB-MONT and Al-CPDB-MONT to Fit Freundlich Equation
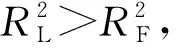
3 结 语
1)以蒙脱石为载体,CPDB与羟基铝为柱撑剂,制备单一柱撑吸附剂CPDB-MONT与复合柱撑吸附剂Al-CPDB-MONT。结果发现,CPDB与羟基铝已成功进入蒙脱石分子层间,增大了蒙脱石的层间距与比表面积,提高了蒙脱石的吸附性能。
2)对MONT,CPDB-MONT,Al-CPDB-MONT3种吸附剂的表征结果与吸附效果的研究发现,复合柱撑吸附剂Al-CPDB-MONT对Cr(Ⅵ)的吸附性能最佳,单一柱撑吸附剂CPDB-MONT次之。在酸性、低温条件下,两种柱撑吸附剂的吸附效果更好。吸附剂对Cr(Ⅵ)的吸附平衡时间为10min,在10min之后吸附率基本不变。吸附动力学和等温线研究发现,Al-CPDB-MONT与CPDB-MONT对Cr(Ⅵ)的吸附符合拟二级动力学模型和Langmuir等温方程,其吸附机理和吸附反应分别为物理吸附和放热过程。复合柱撑吸附剂吸附Cr(Ⅵ)的推动力主要为溶液中正-负离子之间的引力作用,吸附行为主要为单分子层吸附。
