左乙拉西坦对癫痫患者主穹窿蛋白水平及认知功能的影响
2019-02-28张丽霞王一晶
张丽霞 王一晶
癫痫是一种慢性脑功能障碍疾病,主要发病原因为大脑皮质神经元异常放电,其发病不仅对患者造成身体危害,还会导致患者发生认知功能障碍和心理功能障碍[1-2]。癫痫具有癫痫发作易感性的临床特征,如经临床治疗或多次治疗仍未达到理想效果,则提示可能存在耐药性的发生[3]。研究结果表明,在儿童癫痫患者中,因产生耐药性而经正规治疗无效者占20%~30%[4]。主穹窿蛋白(major vault protein,MVP)是癫痫耐药性机制研究中的一个热点。研究发现,MVP可能是通过调控细胞核与细胞质之间的物质交换和囊泡运输参与多药耐药的机制[5],癫痫患者病变部位的血管内皮细胞、神经元以及脑组织中发现有MVP大量表达[6-7]。本研究通过检测左乙拉西坦治疗癫痫患者外周血MVP表达水平及认知功能的变化,旨在探讨左乙拉西坦改善患者认知功能的可能机制。
1 对象和方法
1.1研究对象收集2013年1月至2016年1月作者医院收治的经口服左乙拉西坦治疗的癫痫患者120例,其中男77例、女43例,年龄7~63岁、平均(35.1±6.1)岁;病程为2~10年、平均(6.7±3.1)年。入组标准:年龄4岁以上;经临床及脑电图检查确诊为癫痫[8];入组前3个月内癫痫发作在2次以上并未接受抗癫痫药物治疗;患者未合并其他严重系统疾病、内分泌系统疾病及其他影响本研究观察指标的疾病。排除标准:精神病史者、情绪极端者及其他原因导致的神经认知功能异常者、依从性较差者、无法完成研究者或中途脱落者。所有患者及家属知情同意。
1.2方法
1.2.1治疗方案:给予患者口服左乙拉西坦口服溶液〔药品名:开浦兰,购自优时比(珠海)有限公司,批准文号:H20160153,规格:10%(150 mL∶15 g)〕,以适量水吞服,服药不受进食影响。按体重及年龄用药:(1)针对体重50 kg以上且年龄在12岁以上的儿童及成人,起始治疗剂量为500 mg,2次/d,根据治疗效果和耐受性,可按照2~4周调节最高剂量为1500 mg/次,2次/d;(2)针对11岁以下儿童及体重在50 kg以下的12岁以上儿童,起始治疗剂量按体重10 mg/kg,2次/d,根据治疗效果及耐受性,每2周按体重10 mg/kg增加或减少,调整最高剂量为30 mg/kg;(3)儿童和体重≥50 kg的青少年,其剂量和成人一致;(4)对于年龄在65岁以上者,根据实际情况调节用药剂量。治疗时间为12个月,治疗期间监测患者的肝功能、血常规和电解质等,若患者出现严重不适症状应当及时停止用药。
1.2.2外周血MVP基因检测:采用RT-PCR技术进行检测。分别于用药前、用药6个月和用药12个月时,于清晨抽取空腹外周血2 mL,分离细胞,应用Trizol试剂并按照说明书提取RNA。引物序列为:MVP基因:上游序列为5′-AGCTCAGCGGTACTTC-3′、下游序列为5′-GCCCGCGGGTCTCGAAC-3′;β-actin:上游序列为5′-GATTACTGCTCTGGCTCCTAGG-3′,下游序列为5′-GACTCATCGTACTCCT-GCTTGC-3′。扩增产物应用琼脂糖凝胶电泳分析,并采用凝胶成像系统拍照保存。应用紫外分光光度计测定260 nm、280 nm处吸光度〔D(λ)〕值。按下列公式计算RNA纯度:RNA纯度=D(λ)260 nm/D(λ)280 nm,数值范围在1.7~2.0有效;按下列公式计算RNA浓度:RNA浓度(μg/μL)=4×D(λ)260 nm。
1.2.3外周血MVP蛋白检测:采用Western-blot法进行检测。分别于用药前、用药6个月和用药12个月时,于清晨抽取空腹外周血2 mL,使用RIPA裂解液提取包膜蛋白,制备7%(质量浓度)SDS-PAGE凝胶,加样电泳,待溴酚蓝电泳至分离胶底部时结束电泳。采用湿转法转膜,将硝酸纤维素膜浸入含1 g脱奶粉的20 mL缓冲液封闭液中,置水平摇床上,温室封闭2 h,然后用缓冲液清洗3次,每次5 min;用封闭液配置一抗孵育,4℃过夜。第2天复温30 min,用缓冲液清洗3次,每次5 min;放入用碱性磷酸酶标记的二抗IgG,室温2 h。缓冲液清洗3次,双蒸水清洗1次,化学显色后将光片采用Bio-Rad2000型凝胶成像系统扫描后,应用Quantity One软件分析其灰度值,计算MVP蛋白条带与β-actin灰度值的比值表示MVP蛋白相对表达量。
1.2.4认知功能检测:于用药前、用药6个月和用药12个月应用韦氏智力量表对患者的认知功能进行评分,包括总智商、语言智商以及操作智商等,短时记忆采用短时视觉记忆进行评分。检测时应保证每组所处的时间、空间和外部环境一致。
1.3统计学处理采用SPSS22.0软件进行统计分析,符合正态分布的计量资料以均数±标准差示,多组均数比较采用重复测量的方差分析,两两比较采用LSD-t检验。以P<0.05为差异有统计学意义。
2 结果
120例患者均完成各指标观察和检测,无脱落、中止和死亡病例。
2.1患者外周血MVPmRNA和MVP蛋白表达比较用药6个月和用药12个月时外周血MVP mRNA表达水平和MVP蛋白相对表达水平均较用药前降低(均P<0.05),且用药12个月时外周血MVP mRNA表达水平和MVP蛋白相对表达水平低于用药6个月时(均P<0.05)。结果见表1、图1。
表1 癫痫患者用药不同时间外周血MVP mRNA和MVP蛋白表达比较
注:MVP:主穹窿蛋白,图1同;与用药前比较,aP<0.05;与用药6个月比较,bP<0.05
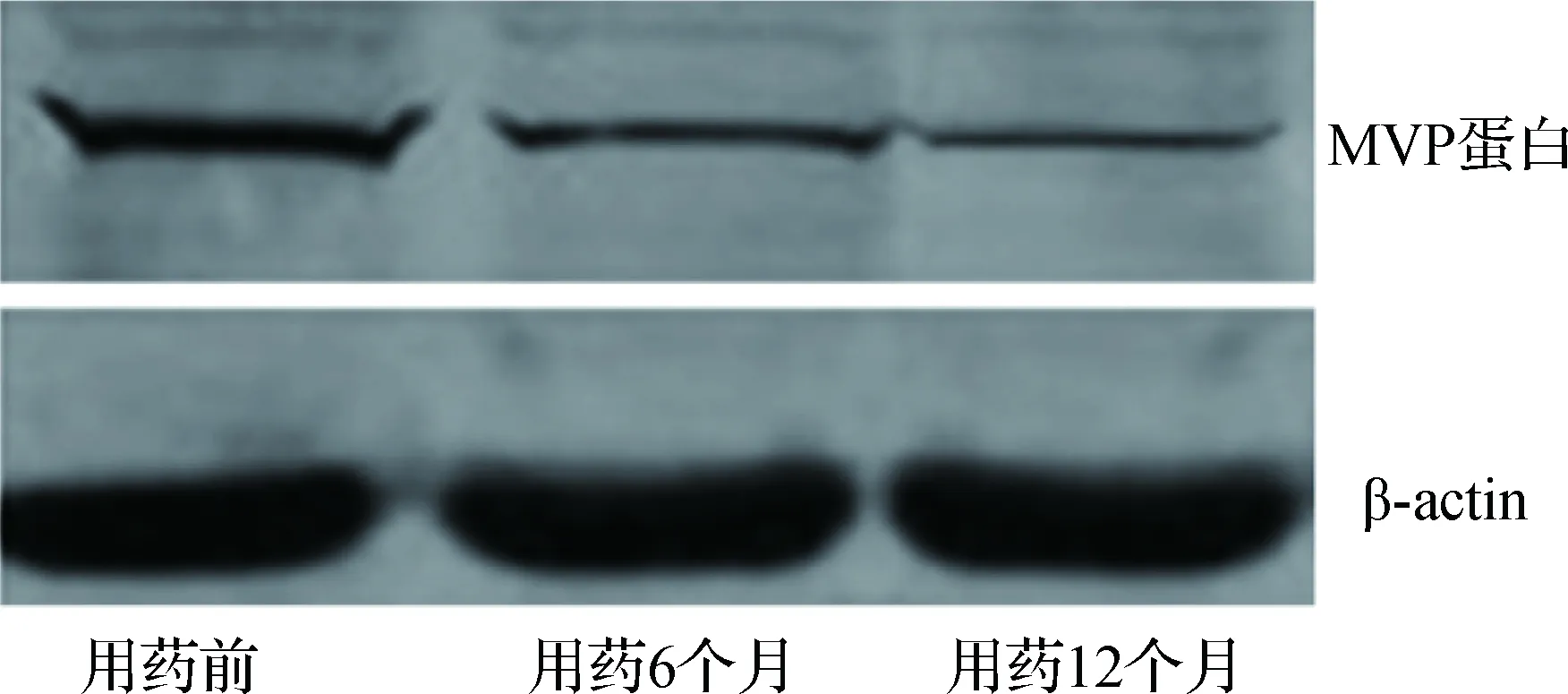
图1 癫痫患者治疗不同时间外周血MVP蛋白表达(Western blot)
2.2各组患者认知功能评分用药12个月后,患者总智商、语言智商、操作智商及短时视觉记忆评分较用药前和用药6个月后均有改善(均P<0.05),而用药6个月上述评分与用药前比较无统计学差异(P>0.05)。结果见表2。
表2 各组癫痫患者认知功能评分比较
注:与用药前和用药6个月分别比较,aP<0.05
2.3不良反应患者治疗期间出现情绪激动5例、嗜睡3例、心悸2例、头晕3例、恶心2例,上述不良反应均在患者的耐受及可控范围内,未给予特殊处理。
3 讨论
MVP是目前发现的与癫痫联系密切的耐药基因之一,首次发现于大鼠肝组织标本中。MVP不仅参与正常生理功能过程,还参与多种病理状态的发生发展,如肿瘤、癫痫和血液病等[9]。MVP作为一种胞质蛋白颗粒,能与进入胞质中的药物形成囊泡,并通过胞吐作用排出细胞,导致靶点药物有效浓度降低而产生耐药[10];此外,MVP还可能通过改变药物在细胞内的分布,使药物呈房室性分布,在胞内隔离药物,导致药物与细胞内作用靶点隔离而产生耐药[11]。有学者在38例难治性癫痫患者手术切除的额叶致痫灶皮质中发现了MVP的阳性表达[12],亦有研究在癫痫患者脑组织中发现MVP大量表达,其被认为是导致抗癫痫药物治疗失败的一个因素,推测MVP可能参与癫痫耐药的形成[13]。
左乙拉西坦属于吡咯烷酮衍生物,短期通过抑制细胞内钙离子(Ca2+)水平调节神经细胞兴奋性,长期疗效则通过特异性结合突触囊泡蛋白SV2A,降低神经递质释放,并阻止癫痫发作。在局限性和全面性癫痫发作的动物模型中,左乙拉西坦具有神经保护作用,并开始用于儿童癫痫的治疗[14-15]。研究结果显示,左乙拉西坦在控制青少年癫痫发作的同时,可部分改善患者的认知功能[16]。本研究结果显示,癫痫患者经左乙拉西坦治疗12个月后,患者总智商、语言智商、操作智商及短时视觉记忆评分较用药前和用药6个月后均有显著改善,且用药期间未发现严重并发症,提示长期服用左乙拉西坦能有效改善癫痫患者的认知功能,且安全性较高,可能利于癫痫的病情控制。
生理状态下,MVP基因及MVP蛋白存在微量表达,是组织器官正常生理代谢产物。本研究结果显示,经左乙拉西坦治疗后患者外周血MVP mRNA及其蛋白表达量均较用药前降低,且用药12个月后MVP mRNA和MVP蛋白表达量低于用药6个月,表明左乙拉西坦并非MVP底物,但能降低MVP的表达而改善癫痫认知功能障碍。
综上所述,应用左乙拉西坦能有效改善癫痫患者认知功能,其作用机制可能与下调MVP的表达有关。由于本研究未对用药人群的年龄、用药剂量以及体重等进行多因素的校正,因此左乙拉西坦对癫痫患者认知功能的确切疗效及机制尚需进一步研究。
