吲哚布芬四氢异喹啉衍生物的设计、合成及生物活性研究
2019-02-27张荣泉张恩立
汤 泉,张荣泉,王 杰,张 晖,张恩立
(蚌埠医学院公共基础学院,安徽蚌埠 233030)
心脑血管疾病是一类严重威胁人类健康的常见病和多发病。据报道,我国2014年农村和城镇心脑血管疾病死亡率高达295.6/10万人和262.0/10万人[1]。研究显示,心脑血管疾病的发病与血栓形成有着密切关系,而血小板聚集是导致血栓形成的主要原因之一[2]。因此,研发新型的抗血小板聚集药物对治疗心脑血管疾病具有重要意义。
吲哚布芬(图1(a))是一种通过抑制环氧化酶达到抗血小板聚集的非类固醇类药物,可用于治疗血栓栓塞、卒中及心肌梗死,但其对胃肠道具有一定的刺激作用及存在出血风险[3-4]。因此通过对吲哚布芬结构进行修饰,研发高效低毒的吲哚布芬衍生物备受关注。李丰[5]等通过拼合原理,设计合成了3个吲哚布芬酯类化合物,后期其药理活性显示,化合物吲哚布芬川芎嗪酯(图1(b))具有较好的抗血小板聚集活性。
我国中药资源丰富,以中药小分子为模型化合物,研发新型抗血小板药物已成为药物研发领域的重点之一。四氢异喹啉类生物碱广泛分布于自然界罂粟科、马兜铃科等植物中。近代药理学研究表明,该类生物碱具有较好的抗血小板聚集、抗肿瘤等生物活性[6]。谢迪[7]等设计合成了15个新型川芎嗪四氢异喹啉类化合物,其中化合物7o(图1(c))对ADP诱导的血小板聚集活性优于奥扎格雷钠。另外,Yang[8]等研究显示,1-邻氯苯基-1,2,3,4-四氢异喹啉衍生物(图1(d))对ADP诱导的血小板聚集也具有较好的活性。综上,四氢异喹啉类化合物在抗血小板聚集研究中具有较高的研究价值。
基于以上基础,本文认为吲哚布芬与四氢异喹啉骨架拼合物可能具有更好的抗血小板聚集活性,同时可以降低吲哚布芬结构中羧基对胃肠道的刺激。因此,本文依据拼合原理,设计合成了3个吲哚布芬四氢异喹啉衍生物,并对其体外抗血小板聚集活性进行了初步筛选,合成路线及3个合成化合物结构见图2。
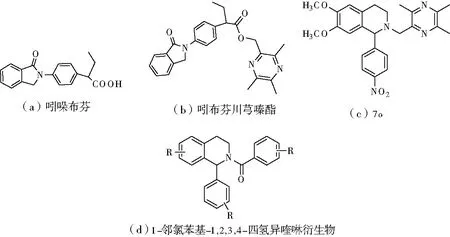
图1 化合物吲哚布芬、吲哚布芬川芎嗪酯、7o和1-邻氯苯基-1,2,3,4-四氢异喹啉衍生物结构
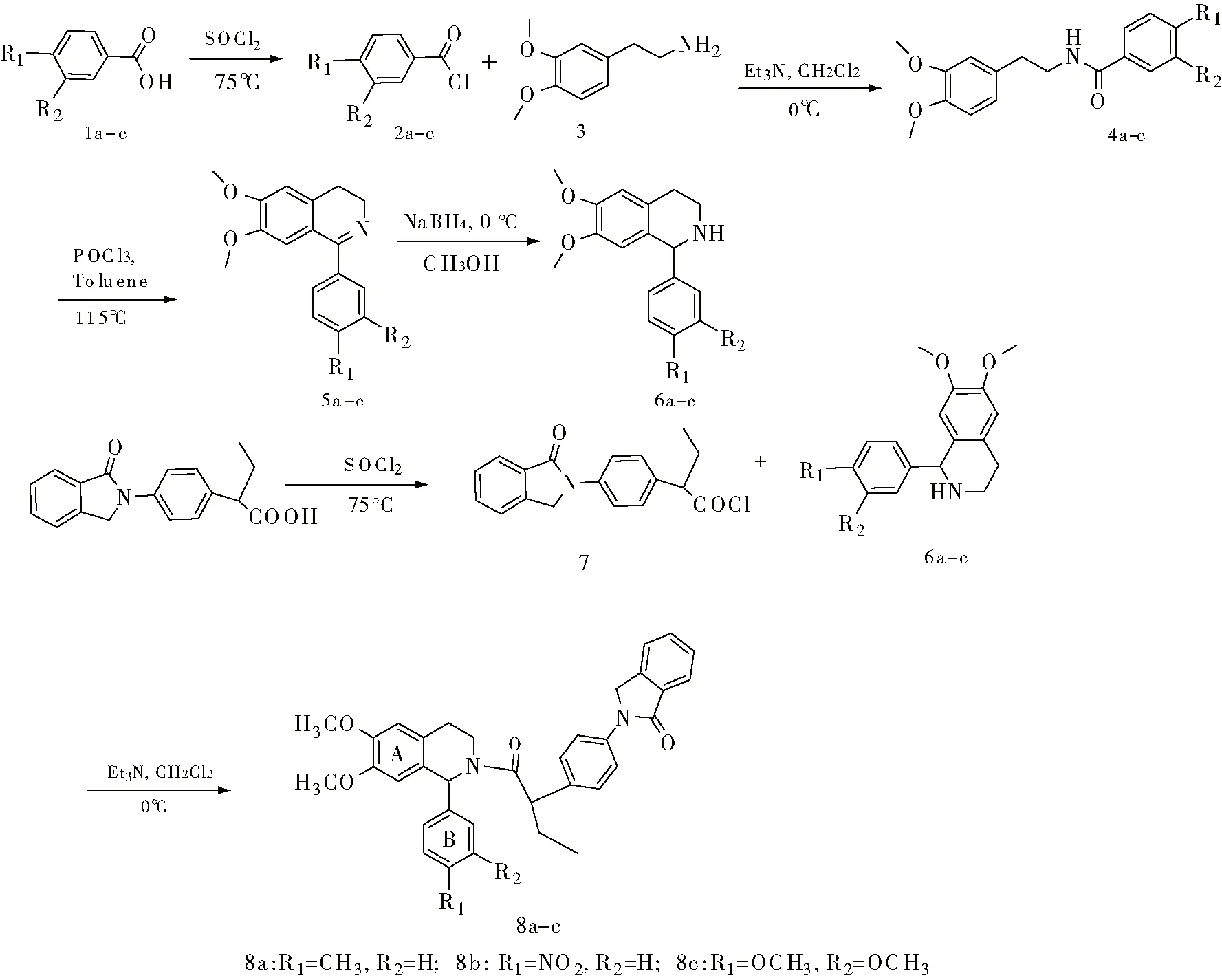
图2 Scheme吲哚布芬四氢异喹啉衍生物的合成路线
1 实验部分
1.1 仪器与试剂
R-1020旋转蒸发仪(郑州长城科工贸有限公司)、HWCL-5恒温集热式磁力搅拌器(郑州长城科工贸有限公司)、FA1204B电子天平(上海精密仪器仪表有限公司)、SGW X-4型显微熔点仪(上海精密科学仪器有限公司)、LCQ ADVANTAGE MAX液质连用质谱仪(FINNIGAN公司)、Bruker 400 MHz超导核磁共振仪(CDCl3为溶剂,TMS为内标)。
3,4-二甲氧基苯甲醛、4-硝基苯甲醛、4-甲基苯甲醛、3,4-二甲氧基苯乙胺、吲哚布芬均购自上海卓锐化工有限公司;二氯甲烷、三乙胺、甲醇、甲苯等试剂均为市售分析纯,均购自合肥宝添科贸有限公司;薄层和柱层析用硅胶购自合肥中皖化学试剂有限公司。
1.2 合成方法
1.2.1 化合物6a的制备[9]
将甲苯50 mL、4-甲基苯甲酸(4 g,29.4 mmol)、SOCl220 mL依次加入一装有回流装置的150 mL圆底烧瓶中,加热升温至75℃搅拌反应4 h,TLC[V(氯仿)∶V(甲醇)=5∶1]检测反应完全,减压蒸除甲苯和SOCl2,用无水甲苯带蒸3次(30 mL/次),得化合物2a,用20 mL CH2Cl2溶解备用。
将CH2Cl260 mL、3,4-二甲氧基苯乙胺(5.3 g,29.3 mmol)、三乙胺6 mL依次加入一150 mL圆底烧瓶中,冰浴条件下,将用CH2Cl2溶解的化合物2a通过恒压滴液管缓慢加入,滴完后,撤去冰浴,常温继续反应2.5 h,TLC[V(乙酸乙酯)∶V(石油醚)=2∶1]检测反应完全,分别用HCl(3 mol·L-1)、NaOH(1 mol·L-1)饱和NaCl各洗涤3次,每次洗涤用HCl 50 mL、NaOH 80 mL和饱和NaCl 60 mL,洗涤后用无水硫酸钠干燥,抽滤,旋蒸浓缩,无水CH3CH2OH重结晶,抽滤,干燥,得灰色固体4a(7.1 g),收率81.1%。
将甲苯50 mL、4a(3.0 g,10.0 mmol)依次加入一150 mL三颈烧瓶中,升温至85℃,搅拌条件下,通过恒压滴液漏斗缓慢加入POCl3(7.0 mL,24.2 mmol),滴加完毕后,升温至115℃反应7 h,TLC[V(乙酸乙酯)∶V(石油醚)=2∶1]检测反应完全,蒸除甲苯和过量POCl3,用乙酸乙酯60 mL稀释,转移到分液漏斗,加水提取3次(50 mL/次),合并水层,在冰浴条件下用浓氨水调pH,使pH为9~10,静置10 min,转移至分液漏斗,用CH2Cl2提取3次(50 mL/次),用饱和NaCl洗涤合并后的CH2Cl23次(60 mL/次),无水硫酸钠干燥,抽滤,减压蒸除CH2Cl2,得黄色油状物5a(2.4 g),收率85.2%。
用无水甲醇40 mL将化合物5a(2.4 g,8.5 mmol)溶解,在冰浴搅拌条件下,分批将NaBH4(0.4 g,19.2 mmol)加入,撤去冰浴,常温反应4 h,TLC[V(乙酸乙酯)∶V(石油醚)=2∶1]检测反应完全,减压蒸除甲醇,用CH2Cl230 mL溶解,加入50 mL水,转移至分液漏斗,取CH2Cl2层,继续用水洗涤2次(50 mL/次),无水硫酸钠干燥,抽滤,减压蒸除CH2Cl2,甲醇重结晶,得白色固体6a(1.8 g),收率75.0%。
1.2.2 化合物8a(2-(4-(1,(6-,7-二甲氧基-1-(对甲苯基)-3,4-二氢异喹啉-2(1H)-基)-1-氧代丁基-2-基)苯基)异吲哚啉-1-酮)的制备用制备化合物2a的方法合成化合物7,此步所投原料吲哚布芬1g(3.4 mmol),化合物7用30 mL CH2Cl2溶解备用。
将CH2Cl250 mL、6a(1.0 g,3.5 mmol)、三乙胺4 mL依次加入一150 mL圆底烧瓶中,冰浴条件下,将用CH2Cl2溶解的化合物7通过恒压滴液管缓慢加入,滴完后,撤去冰浴,常温继续反应2.5 h,TLC[V(二氯甲烷)∶V(甲醇)=10∶1]检测反应完全,分别用HCl(3 mol·L-1)、饱和Na2CO3、饱和NaCl各洗涤3次,每次洗涤用HCl 40 mL、饱和Na2CO350 mL和饱和NaCl 50 mL,无水硫酸钠干燥,浓缩,过硅胶柱,得白色固体8a(1.2 g),产率60.6%。m.p.144.3~144.9℃;1H NMR(400MHz,CDCl3)δ∶7.83(d,J=7.2 Hz,1H,PhH),7.76(d,J=8.8 Hz,1H,PhH),7.70(d,J=8.8 Hz,1H,PhH),7.50(t,J=8.4 Hz,1H,PhH),7.43(d,J=7.6 Hz,2H,PhH),7.27~7.22(m,1H,PhH),7.08(d,J=8.4 Hz,1H,PhH),7.02(d,J=8.4 Hz,1H,PhH),6.98(d,J=6.8 Hz,1H,PhH),6.94(d,J=6.8 Hz,1H,PhH),6.82(s,1H,PhH),6.58(s,1H,PhH),6.50(s,1H,NCH),6.40(d,J=7.2 Hz,1H,PhH),4.74(t,J=2.8 Hz,2H,NCH2),3.80(s,3H,OCH3),3.69(s,3H,OCH3),3.36~3.18(m,1H,NCH2CH2),3.08~3.01(m,1H,NCH2CH2),2.90~2.85(m,1H,COCH),2.25(s,3H,PhCH3),2.18~2.06(m,2H,CH2CH2),1.74~1.68(m,2H,CHCH2CH3),0.85~0.79(m,3H,CH2CH3);13C NMR(CDCl3,100 MHz)δ∶170.3,166.5,147.0,146.8,146.5,146.4,139.0,138.4,137.1,136.1,135.8,135.3,132.1,131.1,127.8,127.4,126.4,126.0,125.7,125.4,123.1,121.6,118.6,118.4,110.4,110.1,54.9,53.6,53.4,49.7,38.2,27.8,27.3,20.0,11.5.ESI-Mass:m/z 561.00(M++H)。
参照化合物8a合成方法合成目标化合物8b和8c。
8b:(2-(4-(1,(6-,7-二甲氧基-1-(对硝基苯基)-3,4-二氢异喹啉-2(1H)-基)-1-氧代丁基-2-基)苯基)异吲哚啉-1-酮),淡黄色固体,产率65.2%,m.p.151.2~151.7℃;1H NMR(400MHz,CDCl3)δ∶8.07(d,J=8.8 Hz,1H,PhH),7.97(d,J=8.8 Hz,1H,PhH),7.83(d,J=7.6Hz,1H,PhH),7.78(d,J=8.4 Hz,1H,PhH),7.72(d,J=8.8 Hz,1H,PhH),7.52(t,J=7.6 Hz,1H,PhH),7.44(t,J=7.2 Hz,2H,PhH),7.39(d,J=8.8 Hz,1H,PhH),7.29~7.23(m,2H,PhH),7.21(d,J=8.0 Hz,1H,PhH),6.84(s,1H,PhH),6.61(s,1H,PhH),6.47(s,1H,NCH),4.76(t,J=4.4Hz,2H,NCH2),3.82(s,3H,OCH3),3.71(s,3H,OCH3),3.65~3.54(m,1H,NCH2CH2),3.06~3.00(m,1H,NCH2CH2),2.91~2.85(m,1H,COCH),2.64~2.59(m,1H,CH2CH2),2.11~2.08(m,1H,CH2CH2),1.75~1.69(m,2H,CHCH2CH3),0.84~0.80(m,3H,CH2CH3);13C NMR(CDCl3,100 MHz)δ∶171.0,166.6,149.1,148.6,147.6,146.9,146.7,146.0,139.0,137.4,134.6,132.0,131.2,128.6,128.2,127.6,127.4,127.3,125.6,124.8,123.1,122.5,122.4,121.7,118.7,110.3,55.0,53.6,49.7,49.5,38.8,27.6,27.1,11.4.ESI-Mass:m/z 592.04(M++H)。
8c:(2-(4-(1,(6-,7-二甲氧基-1-(4,5-二甲氧基苯基)-3,4-二氢异喹啉-2(1H)-基)-1-氧代丁基-2-基)苯基)异吲哚啉-1-酮),白色固体,产率73.8%,m.p.164.5~165.2℃;1H NMR(400MHz,CDCl3)δ∶7.83(s,1H,PhH),7.76(d,J=6.4 Hz,1H,PhH),7.69(d,J=6.8Hz,1H,PhH),7.51(s,1H,PhH),7.42(t,J=6.0 Hz,2H,PhH),7.26(t,J=5.6 Hz,2H,PhH),6.87(s,1H,PhH),6.83(d,J=7.6 Hz,1H,PhH),6.66(d,J=8.0 Hz,1H,PhH),6.59(s,1H,NCH),6.56~6.48(m,1H,PhH),6.42~6.35(m,1H,PhH),4.76(t,J=2.8 Hz,2H,NCH2),3.82(s,3H,OCH3),3.77(s,3H,OCH3),3.71(s,3H,OCH3),3.67(s,3H,OCH3),3.25~3.21(m,1H,NCH2CH2),3.07~3.01(m,1H,NCH2CH2),2.65~2.61(m,1H,COCH),2.37~2.33(m,1H,CH2CH2),2.12~2.10(m,1H,CH2CH2),1.73~1.70(m,2H,CHCH2CH3),0.84~0.82(m,3H,CH2CH3);13C NMR(CDCl3,100 MHz)δ∶170.4,166.5,147.8,147.0,146.5,139.0,137.2,135.2,134.1,132.1,131.1,127.6,127.4,127.3,126.1,125.5,123.1,121.6,120.1,119.8,118.6,118.5,110.6,110.4,110.1,109.1,55.0,54.8,53.5,49.7,49.3,38.1,27.9,27.3,11.5.ESI-Mass:m/z607.07(M++H) 。
1.3 药理实验[10]
本文以阿司匹林为阳性对照药,采用Born比浊法测试吲哚布芬四氢异喹啉衍生物的体外抗血小板聚集活性。选取新西兰雄性家兔,体重1.8~2.2 kg,枸橼酸钠与10 mL生理盐水配制成3.8%的枸橼酸钠溶液,用1%盐酸普鲁卡因对家兔进行局部麻醉,颈动脉插管放血,和枸橼酸钠溶液以9∶1混合,以800~1000 r·min-1离心10 min,取富血小板血浆(PRP),剩余部分以3000 r·min-1离心,取贫血小板血浆(PPP),聚集诱导剂用10 ug·mL-1的二磷酸腺苷(ADP)、10 ug·mL-1的花生四烯酸(AA)。每管280 uL PRP中加入不同浓度的药物(吲哚布芬四氢异喹啉衍生物均用DMSO溶解,加纯净水稀释至所需浓度分别为0.8 ug·mL-1、4 ug·mL-1、20 ug·mL-1、100 ug·mL-1、500 ug·mL-1,阿司匹林用DMSO溶解,加纯净水稀释至与哚布芬四氢异喹啉衍生物相同浓度)10 uL,对照组PRP中加入生理盐水10 uL,37℃温浴3 min,然后加入上述诱导剂,用LG-PABER-1型血小板聚集仪检测血小板聚集率,并计算IC50值。
2 结果与讨论
2.1 结果
通过氯化反应、酰胺化反应、Bischler-Napieralski反应等步骤合成了所设计的3吲哚布芬四氢异喹啉衍生物,其结构均经核磁和质谱确证,详细结构见图2。
采用Born比浊法测试了吲哚布芬四氢异喹啉衍生物的体外抗血小板聚集活性,结果见表1。

表1 化合物8a-8c及阿司匹林对AA和ADP诱导的血小板聚集抑制活性
2.2 讨论
化合物4a经Bischler-Napieralski反应得化合物5a,反应过程中需升温至80~85℃后再将三氯氧磷缓慢加入,然后升温至115℃反应,为最佳反应条件,如果在低于80℃或高于85℃时将三氯氧磷加入,反应过程中产生黑色粘稠状物质,导致5a产率极低。在加入硼氢化钠时,需分批缓慢加入,以防液体溅出。
通过Born比浊法测试了吲哚布芬四氢异喹啉衍生物的体外抗血小板聚集活性,结果显示,3个合成化合物均具有一定的抗血小板聚集活性,其中化合物8b、8c对AA诱导的血小板聚集抑制活性优于阿司匹林,同时8b对ADP诱导的血小板聚集抑制活性也优于阿司匹林,可能在B苯环上引入吸电子基团会增加该类化合物的体外抗血小板聚集活性,有待进一步研究。
