R8GD多肽修饰大黄素脂质体的处方优选及含量测定
2019-02-25刘晶晶蔡馥伊姚雪敏李学涛
符 敏,刘晶晶,荆 鸣,蔡馥伊,姚雪敏,程 岚,李学涛
(辽宁中医药大学 药学院,辽宁 大连 116600)
大黄素是大黄、望江南、虎杖等多种中药的主要活性成分之一,具有抑菌、消炎及泻下等药理作用[1]。近年,关于大黄素抗肿瘤活性的研究日益增多,可从多种途径、多个靶点发挥疗效,其作用机制主要与抑制肿瘤新生血管生成、抑制肿瘤细胞增殖、促进肿瘤细胞凋亡等途径相关[2]。然而,大黄素在体内生理环境pH下溶解度低,很难通过血液运输被机体肿瘤组织吸收[3-4]。脂质体作为一种新型药物载体,利用磷脂双分子层结构对药物进行包载,可提高难溶性药物的溶解度,降低药物毒性,改善药物在体内的分布,从而提高大黄素的体内生物利用度及肿瘤治疗效果[5]。R8GD多肽是一种小分子的细胞穿膜肽,毒性低,且不会产生细胞膜永久性损伤,能有效地将脂质体转运穿过细胞膜,提高细胞对脂质体中药物的摄取及药物对细胞的靶向作用[6]。二硬脂酰磷脂酰乙醇胺-聚乙二醇2000(DSPE-PEG2000)的PEG亲水基团镶嵌在脂质体表面,使脂质体亲水性增强并形成一定的空间位阻,减少血浆蛋白与脂质体膜的相互作用,从而减缓药物在体内的清除速率,延长大黄素在循环系统的滞留时间[7]。本实验采用星点设计-效应面法优选R8GD多肽修饰大黄素脂质体的最佳处方,并用HPLC测定R8GD多肽修饰大黄素脂质体中的药物含量,从而对制剂进行质量控制。
1 材料
1.1 仪器
FA1004型电子天平(上海越平);电热恒温水浴锅(上海医疗器械公司医疗器械五厂);SG3300H型超声波清洗器(上海冠特超声仪器公司);RE52CS型旋转蒸发器(上海亚荣生化仪器厂);JY92-2D型超声波细胞捣碎机(宁波新芝);20AT型液相色谱仪(UV检测器,岛津色谱工作站,日本岛津);葡聚糖凝胶(Sephadex)G-50柱(上海华蓝);C18色谱柱(250 mm×4.6 mm,5 µm,上海月旭)。
1.2 药品与试剂
大黄素(大连美仑,批号:MB5674);蛋黄卵磷脂(EPC,日本NF公司,批号:120015);胆固醇(Chol,大连美仑,批号:MB6750);DSPE-PEG2000(相对分子质量2800.5,日本精化株式会社,批号:B10206);DSPE-PEG2000-R8GD(辽宁中医药大学实验室合成)。
2 方法与结果
2.1 脂质体的制备
薄膜-超声分散法制备脂质体。精密称取处方量的EPC、Chol、DSPE-PEG2000,用氯仿溶解于圆底烧瓶中,40 ℃水浴减压蒸发除去氯仿,用pH 7.2,浓度0.01 mol/L的PBS水溶液5 ml 将圆底烧瓶底部形成的脂质膜充分水化,然后将水化液转至10 ml EP管中,置超声波细胞捣碎机中超声(超声5 s,间歇5 s,功率500 W)10 min,过0.22 μm微孔滤膜2次,即得空白脂质体。制备R8GD多肽修饰大黄素脂质体。精密称取处方量的EPC、Chol、DSPE-PEG2000、大黄素和DSPE-PEG2000-R8GD,用氯仿溶解于圆底烧瓶中,其他操作与空白脂质体制备同。4 ℃密封保存。
2.2 大黄素含量测定方法学研究
2.2.1 溶液的制备
2.2.1.1 空白溶液的制备 按2.1项方法制备空白脂质体,精密吸取空白脂质体1 ml于10 ml量瓶中,甲醇定容,超声破乳,过0.45 μm微孔滤膜,取续滤液,即得。
2.2.1.2 供试品溶液的制备 精密吸取1 ml R8GD多肽修饰大黄素脂质体于10 ml量瓶中,甲醇定容,超声破乳,过0.45 μm微孔滤膜,取续滤液,即得。
2.2.1.3 对照品溶液的制备 精密称取大黄素对照品0.24 mg,置于10 ml量瓶中,用甲醇溶解并定容。另用甲醇配制浓度为5,10,15,20,25,30,35 μg/ml系列对照品溶液。
2.2.2 色谱条件 色谱柱:C18色谱柱(250 mm×4.6mm,5 μm,上海月旭);流动相:甲醇-水(80:20);进样量:20 μl;检测波长:254 nm;流速:1.0 ml/min;柱温:30 ℃;理论塔板数:以大黄素的色谱峰计算不得低于3000。
2.2.3 标准曲线的建立 分别精密吸取大黄素对照品溶液,按2.2.2项下色谱条件测定,记录对照品峰面积,然后以对照品的浓度(μg/ml)为横坐标,相应的峰面积为纵坐标进行线性回归。得大黄素的线性回归方程为Y=128 391X+18 016,(r=0.9996,n=7)。结果表明:大黄素对照品在5~35 μg/ml的浓度范围内线性关系良好。
2.2.4 重复性实验 精密吸取R8GD多肽修饰大黄素脂质体1 ml,按2.2.1.2项方法制备供试品溶液,按2.2.2项色谱条件进样分析(n=5)。结果大黄素峰面积的RSD为0.94 %,说明该方法的重复性良好。
2.2.5 稳定性实验 精密吸取同一供试品溶液,按2.2.2项下色谱条件分别于0,2,4,8,12,24 h进样分析,测定相应的峰面积。结果大黄素峰面积的RSD为1.03 %;说明供试品溶液24 h内稳定性良好。
2.2.6 加样回收率实验 将空白脂质体与等体积的浓度为480.00 μg/ml的大黄素对照品溶液混匀,按2.2.1.2项方法制备供试品溶液,按2.2.2项色谱条件进样分析(n=5)。计算得脂质体中大黄素平均加样回收率为97.20 %,RSD为0.94 %,结果表明该方法符合含量测定方法要求。
2.3 包封率测定
过柱前脂质体:精密吸取 R8GD多肽修饰大黄素脂质体0.5 ml,置入5 ml量瓶中,PBS定容。将该脂质体稀释液与5 ml甲醇混匀,超声破乳,然后过0.22 μm微孔滤膜,作为过柱前样品备用。按2.2.2项色谱条件测定。
过柱后脂质体:称取2.0 g Sephadex G-50,于PBS中浸泡24 h,使其充分溶胀,湿法装柱(10 cm×1.5 cm)备用。待凝胶柱上柱面与PBS液面平齐时,精密吸取0.5 ml R8GD多肽修饰大黄素脂质体上柱,PBS缓慢洗脱,用5 ml量瓶收集橙色部分洗脱液,之后用PBS定容,混匀。将该脂质体稀释液与5 ml甲醇混匀,超声破乳,过0.22 μm微孔滤膜,按2.2.2项色谱条件测定,每个脂质体重复过柱3次,并按下式计算包封率。
包封率(%)=过柱后脂质体中药物含量/过柱前脂质体中药物含量×100 %
2.4 处方优选
根据单因素考察结果,选择对脂质体中大黄素包封率影响较显著的3个因素作为考察因素,包括EPC/Chol(质量比,X1)、EPC/大黄素(质量比,X2)、超声波细胞捣碎机的功率(X3),并确定其用量范围为:X1:3.0~7.0,X2:10~20,X3:300~700。采用星点设计-响应面法可连续对各个水平进行分析。根据Box-Behnken的中心组合试验设计原理,以大黄素包封率(Y)作为测定指标进行考察。试验设计及结果见表1、表2。

表1 因素与水平(处方量为5 ml)
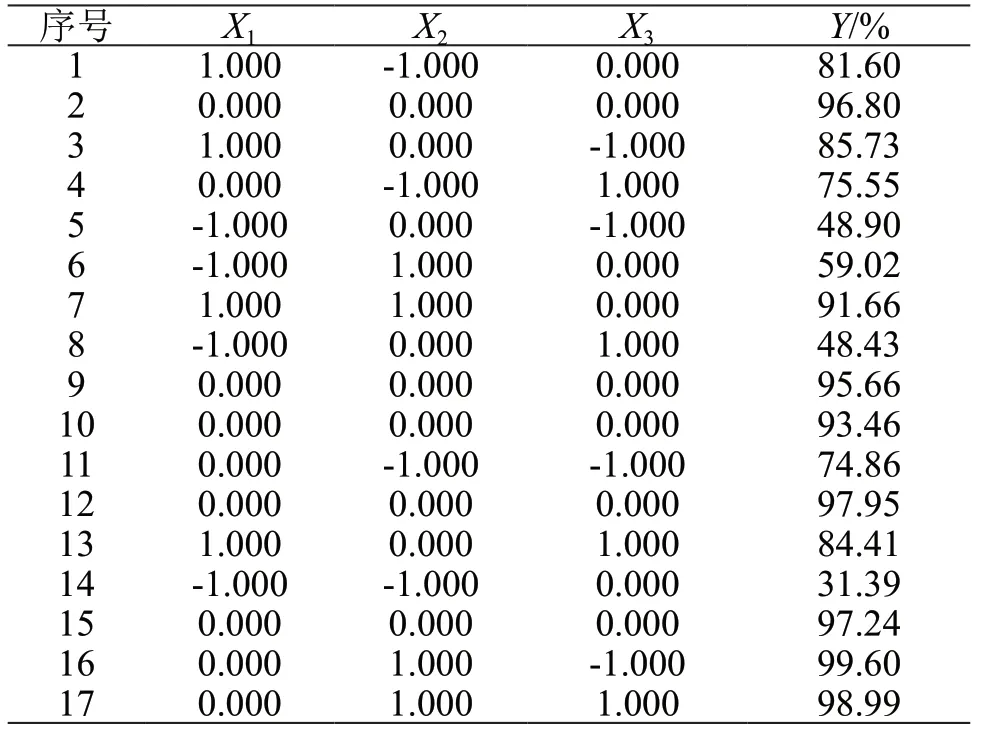
表2 星点设计与结果
将表2中数据输入Design-Expert8.0.6.1软件,拟合方程为Y=-248.91263+ 79.94188X1说明模型能很好地反映响应值的变化,可用于分析和预测R8GD多肽修饰大黄素脂质体的最优处方。对上述拟合模型进行显著性检验,结果显示,X1、X2、X1X2、、对Y有显著影响(P<0.01);X3、X1X3、X2X3对Y没有显著影响(P>0.05)。固定一个因素的水平为0,使用Design-Expert8.0.6.1软件生成各因素对脂质体包封率影响的三维响应面和二维等高线图,响应面图见图1,等高线图见图2。由图1和图2可见,在磷脂量固定不变的情况下X3对Y的影响不大,但X1和X2对Y有显著影响。
根据最优处方制备3批R8GD多肽修饰大黄素脂质体,测定包封率。结果显示,3批样品的包封率为95.78 %±0.64 %。表明该处方合理,方法可行。
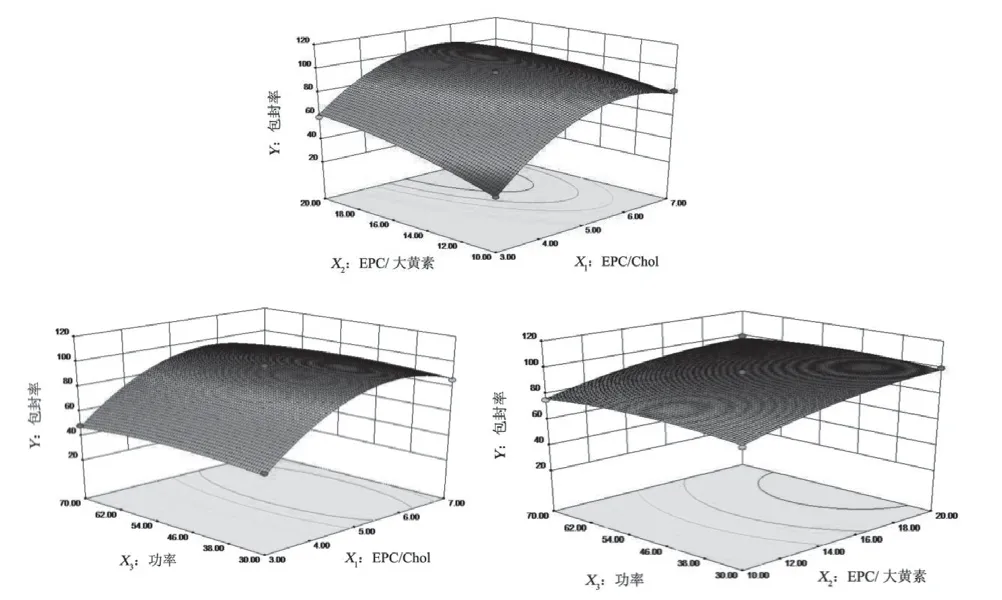
图1 各因素对脂质体包封率影响的三维响应面图

图2 各因素对脂质体包封率影响的二维等高线图
2.5 含量测定
精密吸取R8GD多肽修饰大黄素脂质体,按2.2.1.2项方法制备供试品溶液,按2.2.2项色谱条件进样分析,进样量20 μl,记录脂质体中大黄素的峰面积及含量。结果见表3。

表3 脂质体中药物含量
脂质体中大黄素含量为229.872±1.53 μg/ml,RSD值小于1.0 %。综上,结合实验室脂质体处方考察经验及脂质体制备的实际要求和脂质体性状等因素,确定最优处方为磷脂22 mg、胆固醇4.5 mg、大黄素1.2 mg,处方量为5 ml。
3 讨论
体外实验表明,大黄素对乳腺癌、肝癌、肺癌等多种癌症都有较好的抑制效果,其作用机制主要与抑制肿瘤新生血管生成、抑制肿瘤细胞增殖、促进肿瘤细胞凋亡等途径相关[8]。同时大黄素对抗肿瘤药物的治疗起到协同增效作用,还能增加肿瘤细胞对放疗的敏感性并减轻其副作用,因此具有较好的临床应用潜能。R8GD多肽是一种小分子细胞穿膜肽,可很好地提高脂质体穿过细胞膜的能力,从而发挥更好的肿瘤靶向治疗效果。本实验为改善大黄素的体内水溶性,提高药物靶向治疗效果,制备了R8GD多肽修饰大黄素脂质体。
已有的文献报道中,大黄素HPLC测定的流动相大多为甲醇:0.1 %磷酸溶液(80:20),考虑到色谱柱对酸的耐受性,本实验将流动相改为甲醇:水,考察85:15、80:20、75:25等配比流动相的分离效果。结果表明,流动相为甲醇:水(80:20),样品峰与溶剂峰分离完全且柱效较高,所以本实验最终确定流动相为甲醇:水(80:20)。
本实验利用星点设计-响应面法试验次数少、试验精密度高及可连续对各水平进行分析等特点,对处方进行优选。确定制备R8GD多肽修饰大黄素脂质体(5 ml)的最优处方为磷脂22 mg、胆固醇4.5 mg、大黄素1.2 mg, R8GD多肽4 mg,DSPEPEG20001.5 mg。2015年版《中国药典》规定,脂质体包封率应为80 %以上[9],经验证该R8GD多肽修饰大黄素脂质体最终处方的平均包封率为95.78 %±0.64 %(n=3),表明该R8GD多肽修饰大黄素脂质体处方符合质量要求。
