基于系统药理学探究丹参治疗冠心病的作用机制Δ
2019-02-21秦旭华李浩田高思佳孟祥博赵艳玲
徐 卓,秦旭华,王 涛,,李浩田,高思佳,,王 丹,,孟祥博,张 璐,赵艳玲#
(1.成都中医药大学药学院,四川 成都 611137; 2.解放军总医院第五医学中心药学部,北京 100039; 3.浙江中医药大学药学院,浙江 杭州 310053)
冠心病(coronary heart disease,CHD)是临床常见的心血管疾病,是由于冠状动脉供血和供氧不足,导致心肌急剧、短暂性地缺血与缺氧而引起的发作性心脏疾病[1];如不及时治疗,极易发展为心肌梗死,危及生命。近年来,全球范围内CHD的发病率和患病率呈逐年升高趋势,严重威胁着人类健康[2]。高血压病、糖尿病患者或有吸烟、不运动等不良生活习惯的人群,患有CHD的概率明显高于其他人群[3-6]。长期以来,丹参一直被应用于多种心血管微循环障碍性疾病的治疗,其含有的水溶性丹酚酸类成分作用于血管和心肌,具有扩张冠状动脉、抗氧化及保护心肌等效应,其脂溶性丹参酮等成分还具有抗动脉粥样硬化等作用[7-8]。但以往对丹参的研究主要集中在其单个成分的生物活性或者其在处方中发挥的功效,而丹参作为一种多组分协同系统,可以对疾病的整体调节起到治疗作用,采用传统方法研究其多组分的药理作用机制有很多局限性[9]。因此,基于系统药理学的整合策略框架,寻找丹参治疗CHD的基因、通路、生物过程和已知药物靶点可以揭示其新的研究方向。同时,以往对丹参及其化合物的研究主要集中在防治器官微循环障碍和靶器官损伤,在CHD方面的作用机制研究较少,现有的机制依旧不明晰[10]。因此,本研究旨在通过系统药理学的方法,预测和分析丹参中主要效应化合物对CHD的作用机制,以期为后续实验研究和临床用药提供参考依据。
1 资料与方法
1.1 数据的建立及网络构建
通过检索中草药综合数据库(traditional Chinese medicine database @Taiwan,TDT)(http://tcm.cmu.edu.tw/)、中药系统药理学数据库和分析平台(traditional Chinese medicine systems pharmacology database and analysis platform,TCMSP)(http://ibts.hkbu.edu.hk/LSP/tcmsp.php),获得丹参所含的115种活性成分,再通过中草药活性成分数据库(herbal ingredients’ targets database,HIT)(http://lifecenter.sgst.cn/hit/)和治疗靶点数据库(therapeutic target database,TTD)(http://bidd.nus.edu.sg/group/cjttd)筛选与CHD相关靶点,建立丹参靶点数据集。通过人类孟德尔遗传综合数据库(online mendelian inheritance in man,OMIM)(http://www.omim.org/)筛选CHD相关基因和蛋白靶点,建立CHD靶点数据集,其中靶点连接蛋白通过交互蛋白数据库(database of interacting protein,DIP)(http://dip.doe-mbi.ucle.edu)获得。本研究所使用的药物体内过程[吸收(absorption)、分布(distribution)、代谢(metabolism)及排泄(excretion),ADME]模型主要是口服生物利用度(OB)。OB是口服药物最重要的药动学特性之一,其体现了口服药物后,药物进入体内循环的效率。采用计算机筛选模型(OBioavail 1.1)计算丹参活性成分的OB,OB≥30%的化合物被认为是进一步研究的活性成分。为便于统一分析,以上所有靶点均转化为UniProt数据库识别码格式。将丹参的化学成分、成分对应的靶点、疾病对应的靶点和交互蛋白对应的靶点整合,构建“成分-靶点-疾病”交互网络。网络中,节点表示活性成分、靶点或作用通路。
1.2 京都基因与基因组百科全书(Kyoto encyclopedia of genes and genomes,KEGG)通路富集及生物基因本体(gene ontology,GO)分析
为更合理地阐明丹参中活性成分与CHD之间的关系,对其体内疗效机制进行通路富集分析。利用Cytoscape 3.5.1软件将以上网络进行可视化分析,并对每个节点的中介中心性、点度中心性和接近中心性等3个拓扑参数通过CentiScape 1.2软件进行评估,选择点度中心性≥2倍中位数的靶点,作为丹参治疗CHD的目标靶点。通过蛋白质-蛋白质相互作用(http://www.genome.jp/kegg/)分析,将丹参的化学成分、成分对应的靶点、疾病对应的靶点和交互蛋白对应的靶点整合筛选,进行KEGG通路富集分析。此外,为使通路更为清晰地展现,进一步使用生物GO分析进行“靶点-生物功效”关联分析,对丹参治疗CHD的具体生物功效进行整合分析。丹参对应的靶蛋白直接映射到通路上,药物靶点富集的通路被认为是药物调控的通路。
2 结果
2.1 “成分-靶点-疾病”交互网络的构建
基于数据库构建方法,对丹参治疗CHD的疗效机制进行“成分-靶点-疾病”系统网络构建,发现丹参对CHD的疗效基于其有效成分对多靶点的系统调控,见图1。发现了12个疾病与药物共同直接作用蛋白,见表1;并以此为重点关注的潜在靶标。此外,为更为清楚展现其系统调控网络关系,进一步以上述12个潜在靶标进行次级网络构建,共发现32个与疗效直接相关的活性成分以及47个潜在交互作用蛋白,见图2。通过系统药理学构建丹参治疗CHD作用的交互网络,采用不同形状使其可视化后,可清晰直观地看出药物化学成分与疾病靶点之间的网络关系。其中,三角形为药物化学成分,圆形为药物与疾病的作用蛋白靶标,方形为药物化学成分和疾病共同直接作用的蛋白靶标。

图1 丹参治疗CHD的“成分-靶点-疾病”交互网络Fig 1 The “ingredients-target-disease” interactive network of salvia miltiorrhiza in treatment of coronary heart disease
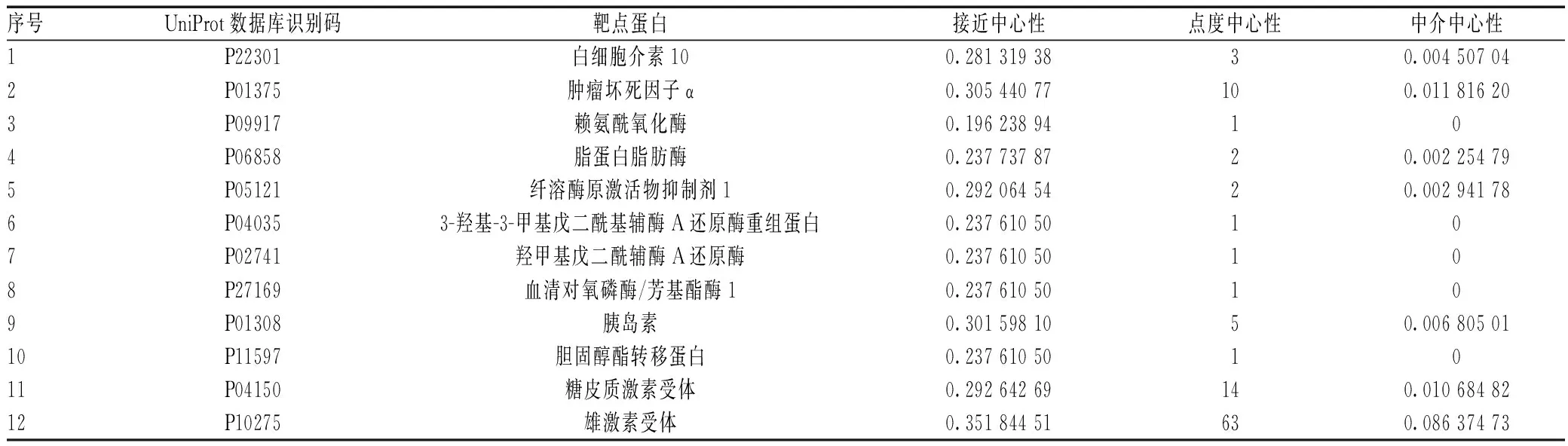
表1 丹参治疗CHD的“成分-靶点-疾病”交互网络中直接作用靶点的拓扑参数分析Tab 1 Topological parameters analysis of direct targets in the “ingredients -target-disease” interactive network of salvia miltiorrhiza in treatment of coronary heart disease

图2 丹参治疗CHD的“成分-靶点-疾病”直接作用次级交互网络Fig 2 The “ingredients-target-disease” secondary interactive network of salvia miltiorrhiza in treatment of coronary heart disease
2.2 KEGG通路富集分析
对二级网络图中的全部潜在靶点进行拓扑参数分析,以中介中心性、点度中心性和接近中心性等3个主要拓扑参数进行相关度分析,并求出拓扑参数中位值分别为0、1和0.260 346 35。以拓扑参数中位值为条件,进行潜在靶点筛选,最终得到相关度最高可能的潜在靶点29个,见表2。采用Array Track v.3.5.0软件进行通路富集分析,根据CHD的特性,挑取出14条相关信号通路,见表3。
2.3 丹参潜在靶点GO分析
为更进一步阐明丹参抗CHD作用的疗效机制,采取生物GO分析对上述通路具体调控的生物过程进行深入分析。结果显示,上述14条通路共参与了62种生物体内调节过程,见图3。对上述生物过程进行统计学分析并按照相关度排列,发现丹参主要通过调控5种生物过程进而发挥对CHD的治疗作用,分别为调节活性氧代谢过程、正调控平滑肌细胞增殖、雄激素受体信号通路、由p53类介导的DNA损伤反应以及积极调节活性氧代谢过程,见图4。此外,通过构建“靶点-生物功效”网络,进一步深入揭示了潜在作用靶标与具体生物过程调控之间的关系,见图5。可以清晰地看到,胰岛素、微囊蛋白1、肿瘤坏死因子α、白细胞介素10、C反应蛋白和3-羟基-3-甲基戊二酰基辅酶A还原酶重组蛋白可以同时调控活性氧代谢和平滑肌细胞增殖过程。
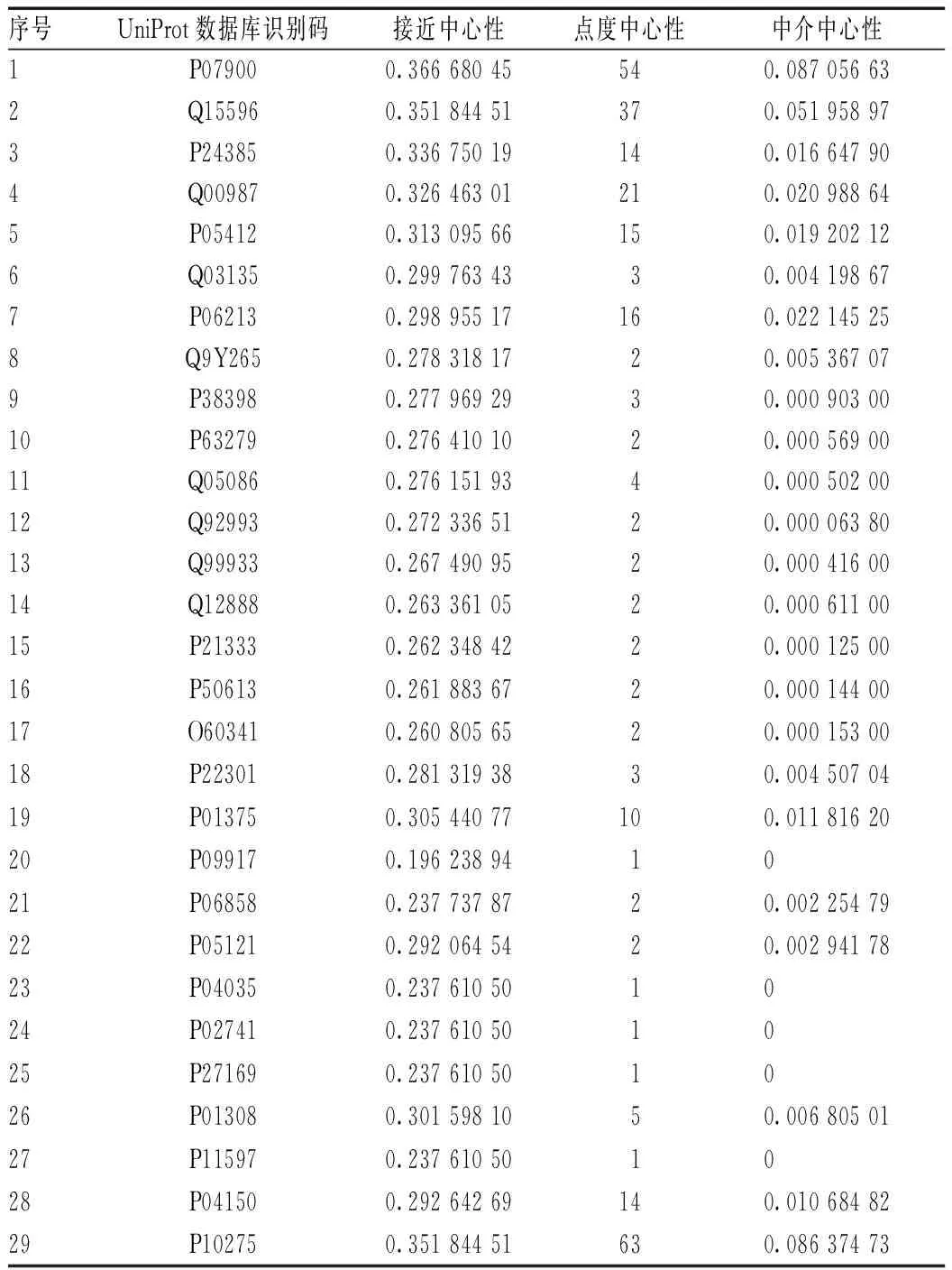
表2 丹参治疗CHD通路蛋白靶点的拓扑参数分析Tab 2 Pathway analysis of protein target of salvia miltiorrhiza in treatment of coronary heart disease

表3 丹参治疗CHD的14条体内通路Tab 3 The 14 internal pathways of salvia miltiorrhiza in treatment of coronary heart disease
3 讨论
丹参的通路富集分析结果显示,丹参多组分所作用的靶点主要富集于磷脂酰肌醇3-激酶-蛋白激酶B信号通路、叉头转录因子信号通路和丝裂原活化蛋白激酶信号通路等,这些信通路可能是未来研究丹参治疗CHD的关键通路。丹参的GO富集分析结果显示,丹参多成分所作用的靶点主要富集于多个与CHD有关的生物过程,主要包括调节活性氧代谢过程、正调控平滑肌细胞增殖、雄激素受体信号通路、由p53类介导的DNA损伤反应以及积极调节活性氧代谢过程等5个方面。目前,关于丹参成分的研究已部分揭示了丹参多组分治疗CHD的功效。研究结果发现,丹参酮ⅡA可调节磷脂酰肌醇3-激酶-蛋白激酶B信号通路进而显著改善大鼠心肌缺血再灌注损伤,显著改善其氧化应激损伤,抑制心肌细胞凋亡[11]。近年来,叉头转录因子信号通路在心血管疾病调控中的作用逐步成为研究热点,其在缓解心脏老化,心肌保护等方面具有重要作用[12-13]。关月等[14]的研究结果表明,丹参素能够通过调节叉头转录因子信号通路参与心脏保护作用。心脏长期处于缺血缺氧状态,可促进心血管新生,进而引起心肌结构重构,而近年来有研究指出,丹参水煎液可激活丝裂原活化蛋白激酶信号通路上调自噬抑制异丙肾上腺素诱导的大鼠心肌重构[15]。上述结果与本研究结果相符。此外,本研究的GO分析所得出的较为相关的5种参与CHD的生物途径更为详细地揭示了丹参对于治疗CHD的疗效机制。有研究指出,CHD模型大鼠存在严重的心肌细胞凋亡、活性氧高表达以及心肌线粒体DNA损伤[16-17]。丹参通过参与上述生物过程的调控或许正是其发挥疗效的作用基础。

图3 生物调节过程分析Fig 3 Analysis of biological regulation process

图4 生物调节过程相关度分析Fig 4 Correlation analysis of biological regulation process
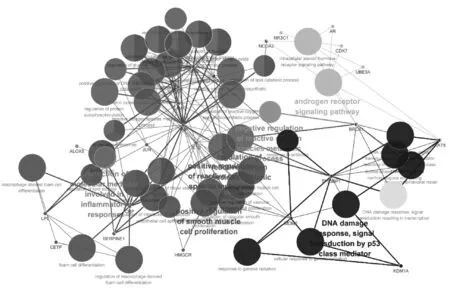
图5 “潜在靶点-生物过程”网络Fig 5 “Potential target-biological process” network
系统药理学是从系统水平研究药物与机体相互作用及其规律和作用机制的一门学科[18],即从分子、网络及细胞到组织、器官等不同水平上研究药物治疗疾病时引起机体功能变化的机制,建立药物对于机体的作用从微观到宏观的各水平之间相互关联的学问。其目的是为了从整体了解系统的行为,而不是了解个体行为。传统中药是多组分、多靶点及其组分间具有协同作用的复杂体系。因此,传统药理学方法难以对其深入研究,而系统药理学则为庞大的中药系统研究提供了新视角和思路。采用系统药理学技术,研究中药活性成分及组合、识别药效成分靶点及其与疾病关系的理论和方法,从而建立系统水平的中药研究理论。
本研究通过系统药理学方法,发现了丹参有效成分,探究其潜在作用靶点,并通过KEGG通路注释和GO富集分析获取丹参治疗CHD的信号通路及生物过程,体现了其作用机制。不仅为丹参治疗CHD的研究提供了基础,同时对其进一步实验研究、临床合理用药以及其他传统中药机制的研究提供了新的范式。
