运动性室性心律失常与临床
2019-02-18鲁端
鲁端
运动性室性心律失常(exercise-induced ventricular arrhythmias,EIVA)系指在运动时和(或)运动后恢复期发生的室性心律失常。自从1927年Bourn首次报道运动时室性期前收缩(PVC)数量改变的临床意义后,EIVA逐渐成为心律失常领域的研究热点之一。近年研究发现,EIVA与患者的临床表现和预后等密切相关,因而倍加关注[1-3]。本文回顾性分析本世纪18项较大样本(>1 000例/项)关于EIVA的研究报道,并对EIVA的临床意义等进行初步探讨。
1 EIVA的类型与发生率[4-21]
由于在心电图分级运动试验时,较规范地监测心电图,故EIVA的类型和发生率均来自该类试验的研究结果。
1.1 EIVA的类型 (1)按心电图表现可分为PVC、非持续性室性心动过速(NSVT)、持续性室性心动过速(SVT)、心室扑动和心室颤动等。其中对PVC的观察和分析居多,且多数研究将PVC负荷>10%者界定为频发PVC,≤10%者界定为非频发PVC。而对SVT、心室扑动和心室颤动观察和分析较少,与发生率较低、部分研究将其作为排除标准之一相关。(2)按室性心律失常出现的时间可分为运动期EIVA和运动后恢复期EIVA。
1.2 EIVA的发生率 在不同研究人群中有较大差异。(1)根据本世纪6项对无症状的无心血管病人群的研究报道(表1),在共计25 636例研究人群中,非频发PVC的发生率约6.61%~23.2%,频发PVC的发生率约0.72%~13.62%,NSVT发生率约0.33%~3.76%。(2)根据本世纪6项对心血管病患者的研究报道(表2),在共计46 817例研究人群中,各种类型的PVC的发生率约48.54%,频发PVC/NSVT的发生率约1.74%~8.10%,严重型/潜在的致命性室性心律失常(potentially life-threatering ventricular arrhythmias,PLVA)的发生率约 0.22%~8.54%。(3)根据本世纪6项对混杂人群(mixed populaion)的研究报道(表3),在共计43 464例研究人群中, PVC的发生率约20.42%,频发PVC的发生率约3.63%~7.40%,不良性/复杂型PVC发生率约 3.10%~3.56%,NSVT发生率约 0.08%~2.18%,运动期PVC的发生率约14.11%~46.12%,运动恢复期PVC的发生率约11.67%~24.58%。从以上研究报道可见,EIVA在3类人群中均有较高的发生率,而在心血管病患者中较易发生运动性严重型/潜在的致命性室性心律失常。但是,由于研究人群、检测方法和诊断标准等互有差异,对EIVA的发生率可产生一定的偏离。

表1 无症状的无心血管病人群EIVA的发生率
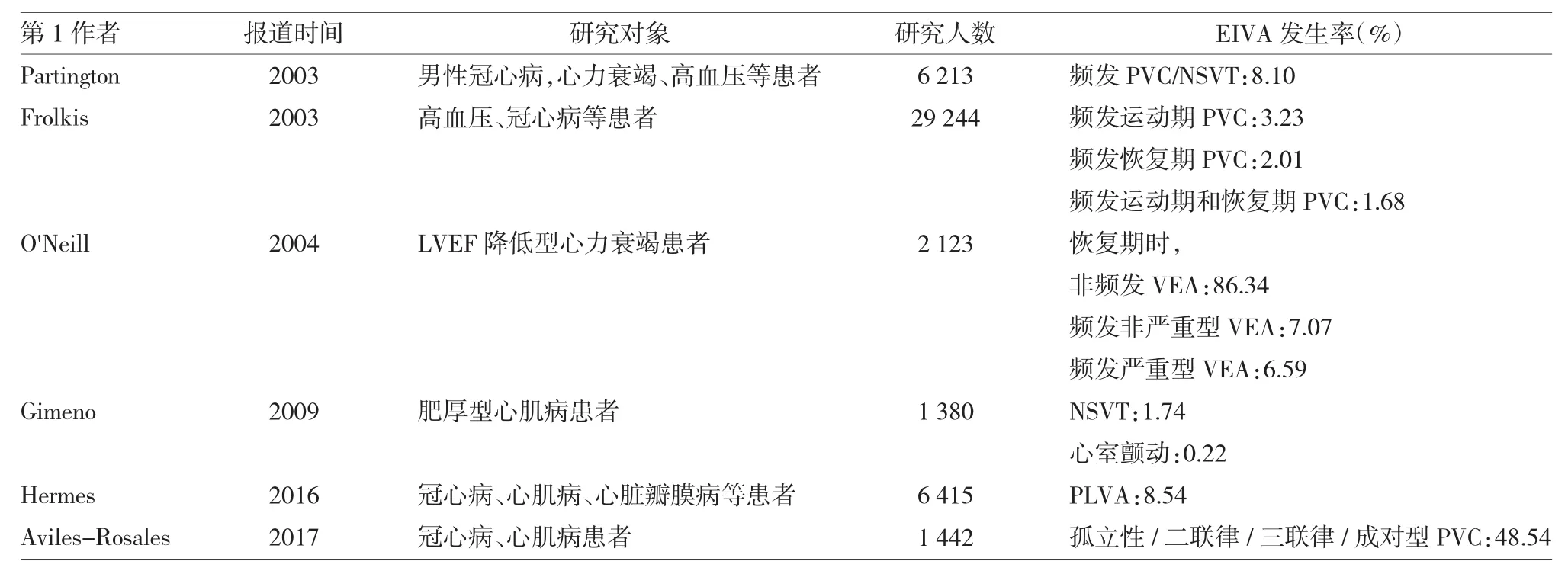
表2 心血管病患者EIVA的发生率

表3 混杂人群EIVA的发生率
2 EIVA 的发生机制和易患因素[2-4,12,20-25]
2.1 自主神经系统功能失调 自主神经系统包括交感神经和迷走神经,主要通过神经末梢释放相应的递质(去甲肾上腺素或乙酰胆碱)作用于心血管受体(β受体或M受体),对心肌细胞的离子通道功能和生物电活动进行调控。当自主神经过度兴奋(激活)和(或)平衡失调时,即可引发室性心律失常等。研究报道显示,健康人群在进行运动试验时,交感神经兴奋性逐渐增高,迷走神经兴奋性逐渐降低。而在运动后恢复期时,迷走神经兴奋性逐渐增高,交感神经兴奋性逐渐降低。
2.1.1 运动期交感神经过度兴奋Michowitz等和Luebbert等报道,当交感神经过度兴奋时,诱发心律失常的机制:(1)心脏内具有自律性的细胞(P细胞、浦肯野纤维、异位节律点)的起搏性If离子流增加和4相自动除极速率增快,阈电位下移,引发自律性增高。(2)心室肌细胞的有效不应期缩短,使其再兴奋的频率增快。(3)心肌内交感神经的递质释放显著不均匀,增加了心肌组织之间的不应期差异,可引发折返激动。(4)交感神经末梢释放的去甲肾上腺素增加,使心肌细胞Ca2+内流和肌浆网Ca2+释放增加,可引发膜电位振荡(后除极振幅增大)和触发活动。Miyakoda等通过冠心病患者与正常(健康)人对比研究,结果显示:在休息和运动试验后即刻时,冠心病组血清正肾上腺素浓度均较正常组增高(P分别为<0.01和<0.05),冠心病伴EIVA者的运动后即刻血清正肾上腺素浓度亦高于无EIVA者(P<0.05)。Dimsdale等亦有相似的报道。同时,Marine等、Partington等和Merine等较多研究显示,在无症状的无心血管病人群、心血管病患者和混杂人群中,伴EIVA(尤其是频发PVC/NSVT)患者的运动时心率峰值和(或)血压峰值均明显高于无EIVA者,P<0.0001~0.05。以上研究均提示,交感神经过度兴奋在各类人群发生运动期的EIVA中具有重要作用。
2.1.2 运动后恢复期迷走神经再兴奋减弱 Perini等、Arai等和Imai等报道,健康人在运动后恢复期增快的心率快速减慢,此中迷走神经的再兴奋具有重要作用。而在慢性心力衰竭的患者,运动后恢复期的心率并不减慢,甚至较运动期更快,与该期的迷走神经再兴奋减弱和交感神经持续兴奋(自主神经功能失调)相关。因为迷走神经再兴奋时,心脏内具有自律性的细胞的起搏性If离子流减少和4相自动除极速率减慢,阈电位上移,可使心率减慢和自律性降低。而在自主神经功能失调时,使心率快速减慢的作用明显减弱和自律性增高。Jouven等、O'Neill等和Meine等研究显示,在对无症状的无心血管病人群、心血管病患者和混杂人群中,均发现运动后恢复期的频发PVC和严重型VEA发生率较高(约2.01%~6.59%),亦提示与自主神经功能失调相关。
2.2 心脏超负荷性损伤 较易发生于已有心血管病的患者。在运动试验时,可导致心力衰竭患者的心脏负荷进一步过度增加、冠心病患者的心肌需血与供血矛盾更趋恶化、心肌病等患者的病变心肌活动异常加重。同时,超负荷运动可引发急性心肌损伤(血肌钙蛋白增高)、心肌纤维化、冠状动脉钙化和心脏病理性重塑等。从而诱发EIVA。Hermes等报道,伴心力衰竭的心血管病患者的EIVA发生率(48%)明显高于无心力衰竭的心血管病患者(26%),P<0.001。Aviles-Rosalse等报道,在冠心病和特发性心肌病患者中,发生EIVA的患者LVEF[(42±14)%]明显低于无EIVA患者[(47±14)%],P<0.001。Partington等报道,在男性心血管病 患者中,EIVA患者伴有运动性心肌缺血的发生率(45%)明显高于无EIVA患者(33%)P<0.001。以上研究结果均提示心脏超负荷性损伤与心血管病患者有较高和较严重的EIVA发生率相关。
2.3 老年人及其他EIVA的易患因素 (1)老年人易伴有较多的心血管病危险因素、心内外疾患和(或)衰老综合征(frailty syndrome)等,心脏结构和功能易发生增龄性病变,如心脏瓣膜退行性变、心肌纤维化、离子通道重构以及缝隙连接蛋白重构等,使心脏的泵储备功能和生物电活动稳定性下降。在运动试验等应激情况下,易诱发心功能不全和EIVA。Marine等报道,在无症状的无心血管病志愿者中,运动诱发NSVT的患者以老年人居多,平均年龄(67±12)岁,明显大于未诱发 NSVT者(51.4±17)岁,P<0.0001。Partington等报道,在男性心血管病患者中,运动诱发频发PVC/NSVT的患者以老年人居多,平均年龄(64±11)岁,明显大于未诱发频发PVC/NSVT的患者(59±11)岁,P<0.001。Beckerman等报道,在男性退役军人中,运动诱发频发PVC/NSVT的患者以老年人居多,平均年龄(63.6±10.2)岁,明显大于未诱发频发PVC/NSVT的患者(58.3±11.2)岁,P=0.01。以上对3类人群的研究结果均提示老年人是EIVA的易患因素之一。(2)在无症状的无心血管病人群中,其EIVA的发生机制除交感神经过度兴奋和心脏负荷过度增加等外,部分人群可能患有潜在的致心律失常基质(underlying generated arrhythmias substrate),如心血管病危险因素(吸烟、酗酒、肥胖、缺乏体力活动等)、心肌纤维化、隐蔽性高血压、隐匿型冠心病、无症状的早期心肌病、严重的心肌桥以及隐匿性遗传性心脏离子通道病(如未发作和未发现的长QT综合征、Brugada综合征等)等。在运动试验时,上述潜在的致心律失常基质可参与EIVA的发生。(3)EIVA的其他易患因素尚有运动能力低下[<5MET(代谢当量)]、运动性高血压以及左心室室壁运动异常等。
3 EIVA 的临床意义[4-21,26]
在20世纪期间,众多学者主要对EIVA的病因进行了较多研究报道。一般认为:(1)运动性PVC的发生率随着年龄增长而增高,在健康人和心脏病患者均较为常见。(2)运动时原有的PVC减少或消失,提示为良性PVC,但不能据此排除患有器质性心脏病。(3)运动时原有的PVC增加,提示患有器质性心脏病,最常见的病因为冠心病。(4)运动时出现频发PVC、多源PVC和(或)连续的PVC时,提示可能患有急性或不稳定性冠心病。(5)在平板运动试验时出现PVC,其临床意义必须结合临床。在外观健康人群不能据此诊断患有器质性心脏病或将来会发生冠状动脉事件。反之,在已患有或怀疑患有心血管病的患者,则支持心脏病的诊断。若发生于胸痛、高血压和(或)有心肌梗死病史患者,则可明确作为将来发生冠状动脉事件的预兆。
在本世纪近20年中,许多学者主要对EIVA患者的预后进行了较多研究报道。(1)在表1的6项对无症状的无心血管病人群研究中,有4项研究结果显示,在总体平均随访16.6(8.1~23)年期间,相关EIVA患者的全因死亡和心血管病死亡风险明显增加,校正后的风险比(HR)或相对危险度(RR)明显增高,P≤0.001~0.003。其余2项研究结果显示,在平均随访10.4(7.4~13.5)年期间,相关EIVA患者的全因死亡、不良事件或患心血管病的风险并未增加。其中Marine等报道的研究结果显示,校正后的HR=1.3,P=0.17(表4)。另一项Verdile等报道的研究结果未列出评估预后风险的相关统计学资料,且其中的36例伴频发PVC和(或)NSVT的运动员在停止运动3~6个月后,复查了运动试验,23例的EIVA有改善,P=0.05。6例EIVA未改善者成功地施行了射频消融治疗。(2)在表2的6项对心血管病患者的研究中,有5项研究结果显示,在总体平均随访6.54(2.9~14.0)年期间,相关EIVA患者全因死亡、心脏性猝死、致命性室性心律失常和(或)植入ICD的风险明显增加,校正后的HR或RR明显增高,P≤0.001~0.02(表 5)。另 1 项 Hermas研究报道未对相关EIVA患者进行预后评估,但通过筛选发现13项临床和测量指标对评估心血管病患者发生EIVA有显著的统计学意义(P<0.001~0.031),并推导出1个预测心血管病患者在运动时发生潜在的致命性室性心律失常风险的复杂计算公式。(3)在表3的6项对混杂人群的研究中,有4项研究结果显示,在总体平均随访4.78(2.7~6.0)年期间,相关EIVA患者的全因死亡、心脏性死亡和(或)新发生冠状动脉事件的风险明显增高,校正后的HR、RR、优势比(OR)、χ2检验或发生率明显增高,P<0.001~0.05。其余1项Meine等的研究结果显示,相关EIVA与全因死亡率无明显相关性,校正后P=0.19,但恢复期PVC与心肌缺血有显著的相关性,校正后OR增高,P=0.017(表6)。另一项Tamkoshi等研究报道,未对相关EIVA患者进行预后评估。值得关注的是在以上3类人群的评估EIVA预后的研究报道中,有13项研究报道(81.3%)的相关性EIVA患者明显较无EIVA患者预后不良,汇总的RR或HR约 2.05(1.50~3.45),P<0.001~0.05,其中心血管病伴相关EIVA的患者预后更差。(4)Lee等于2017年报道,荟萃分析了自1987至2008年的10项关于EIVA的研究报道。其中4项研究对象为无症状的无心脏病患者,在平均随访16年期间,相关EIVA患者(共1 239例),发生心血管事件[非致命性心肌梗死、心绞痛、心源性住院和(或)心脏停搏]、心血管病死亡和全因死亡的风险明显增高,汇总的RR=1.818(95%CI:1.436~2.302),Z值(合并效应量)=4.967,P=0.000。另外 6项研究对象为有症状的心脏病患者,在平均随访5.4年期间,相关EIVA患者(共4 105例)发生相应的心血管事件、心血管病死亡和全因死亡风险明显增高,汇总的RR=1.360(95%CI:1.177~1.571),Z值=4.178,P=0.000。此外,Peng等和Kim等亦有相似的研究报道。总之,以上研究结果均显示,在无心血管病者和心血管病患者中,相关EIVA的患者预后不良。

表4 无症状的无心血管病人群伴EIVA的预后

表5 心血管病伴EIVA患者的预后

表6 混杂人群伴EIVA患者的预后
4 EIVA 的处理策略[2,25-30]
4.1 及时发现和关注EIVA,预防严重型EIVA(1)EIVA不仅可以发生在运动试验中,而且可发生于参加高强度体力劳动、健身运动和(或)体育比赛时。故参与上述运动或活动者(特别是有症状、已有心血管病、老年人群和(或)初次参加高强度运动或活动者),应适时进行心电图运动试验检测,以能及时早发现严重型EIVA,早期干预,改善患者预后。(2)应重视适度的有氧运动在心血管病一级预防和二级预防中的重要作用,而高强度和(或)超负荷的运动发生严重型EIVA和心血管事件的风险明显增高。在日常生活中,推荐循序渐进的中低强度健身运动。在心电图运动试验时,应密切监测生命指标和心电图,严格掌握适应证、禁忌证和终止指标等。对已有心血管病的患者,在运动前应进行危险分层和风险评估,推荐合理的运动方式,避免高强度和(或)超负荷的运动。(3)建议在运动试验报告中,注明EIVA的类型和频率,并予以定期复查。
4.2 紧急救治运动性致命性室性心律失常的患者(1)对于血流动力学不稳定的运动性持续性单形室性心动过速患者,应立即同步直流电复律。(2)对于运动性持续性多形室性心动过速、心室扑动或心室颤动患者,应立即进行徒手心肺复苏(CPR)和非同步电击除颤。继之,对成功复律者实施心肺脑复苏和病因治疗。(3)对于成功紧急救治患者,若患有LVEF<35%的结构性心脏病或非可逆性疾病(如遗传性心脏离子通道病等),预期生存时间>1年,推荐植入ICD。(4)建议对学校体育老师、运动机构工作人员和从事运动试验的心电图医生进行心肺复苏和正确使用体外除颤器的培训,以能及时参与相关的紧急救治工作。
4.3 纠治EIVA的病因与诱因 是处理EIVA的基础。(1)对慢性稳定性心血管病伴EIVA患者,应重新仔细询问病史、详细体格检查和选择无创或有创辅助检查,进一步确定诊断、病程阶段和EIVA相关的病理因素,进行危险分层,加强病因治疗,由医患共同决策优化的药物和非药物治疗要点。(2)对无心血管病的EIVA患者应纠治心血管病的危险因素(如吸烟、酗酒、缺乏体力活动、超重等),并进一步检测有无潜在的致心律失常基质和老年人的增龄性病变,治疗或消除相关诱因。(3)运动时反复发作的单形性NSVT或SVT常起源于右心室流出道或主动脉瓣区,可见于无心血管病人群、心肌病或陈旧性心肌梗死等患者,应予鉴别诊断、经导管射频消融和相关病因治疗。(4)对运动时反复发作的双相/多形性VT患者,若无QTc间期延长、缺血型ST段改变、应用洋地黄类药物和心脏的结构与功能异常(如二尖瓣脱垂等),应首先考虑可能患有遗传性儿茶酚胺敏感性VT,需对其和一级亲属进行遗传咨询和检测有无相关特变基因,确诊后推荐酌情应用β受体阻滞剂、氟卡尼、左心交感神经切除术(left cardiac sympathetic denervation)和(或)植入ICD。
4.4 血流动力学稳定的EIVA的处理 应在纠治EIVA相关病因与诱因的基础上,施行以下处理:(1)对运动性持续性单形VT患者应在生命信息监护下,对无心血管病患者推荐静脉应用β受体阻滞剂、普鲁卡因胺、维拉帕米或氟卡尼。对心血管病患者推荐静脉应用胺碘酮或利多卡因。若药物治疗无效时,推荐经导管消融治疗。消融治疗无效时,推荐对无禁忌证和预计生存时间>1年者植入ICD。(2)对运动性非持续性VT患者,若无心血管病但伴有症状者,推荐服用β受体阻滞剂、非二氢吡啶类钙拮抗剂或Ⅰc类抗心律失常药。对慢性稳定型心血管病患者,推荐进行心电生理检查,其中对诱发持续性VT/心室颤动患者,预计生存时间>1年,推荐植入ICD。未诱发持续性VT/心室颤动患者,推荐服用β受体阻滞剂。(3)对运动性频发PVC患者,若无心血管病但伴有明显相关症状者,推荐短期服用β受体阻滞剂和定期复查。对有心血管病患者应在病因治疗和消除诱因的基础上,推荐服用β受体阻滞剂和(或)参松养心胶囊。对症状持续和药物治疗无效或不能耐受的患者,宜进行动态心电图检查,若伴有高负荷单形性VPC(起源于右心室>10%,起源于左心室>20%),推荐经导管消融治疗。
5 EIVA的启示
5.1 EIVA是一种病理性心电现象,是高强度和(或)超负荷运动时诱发心肌损伤的表现之一,其可发生于无心血管病人群和心血管病患者等。
5.2 适度的规律性有氧运动和活动有益于健康和高血压、糖尿病、肥胖症等疾患的防治,但高强度和(或)超负荷的运动和活动可导致心脏损伤,至今已达成共识。
5.3 心电图运动试验是一项能较好评估心脏负荷能力的常用无创性临床辅助检查,建议从事高强度运动和活动的人群(特别是初次参与者、有症状、老年人或有心血管病患者),应及时进行该项检查,以能尽早发现EIVA等异常征象,施行相关的预防和治疗。
5.4 轻度的EIVA应予以关注和定期复查,严重的EIVA患者预后不良,可以促发心血管事件、心脏性猝死,长期随访时可增加全因死亡和心脏性死亡的风险,必须及时进行相关的预防和救治。
