重组腈水解酶催化合成(S)-3-氰基-5-甲基己酸
2019-02-15李恩杰汤晓玲吴哲明郑仁朝
李恩杰,汤晓玲,吴哲明,郑仁朝
(浙江工业大学 生物工程学院,浙江 杭州 310014)
腈水解酶(nitrilase,EC 3.5.5.1)是一类重要的生物催化剂,能一步催化腈类化合物合成相应的羧酸和氨[1-3]。腈水解酶在自然界中广泛存在于真菌、细菌和植物体中[4],具有反应条件温和、特异性高和立体选择性严格等优点[5-6]。腈水解酶的高立体选择性、高催化活力等特点使其在制备手性羧酸中具有明显优势[7-9],广泛应用于维生素、有机酸、氨基酸等化工产品和医药中间体的生物合成[10-12]。
普瑞巴林(Pregabalin)化学名为(S)-3-氨甲基-5-甲基己酸,是抑制性神经递质γ-氨基丁酸的结构类似物。普瑞巴林为受体激动调节剂,能有效降低电压对钙离子通道的依赖性,从而减少神经递质的释放,对治疗神经痛以及抗癫痫效果良好[13]。由于普瑞巴林良好的治疗效果和适应证的扩大[14-15],自2005年批准上市以来,其销售额逐年递增,2017年全球销售额达到50.65亿美元,列全球最畅销药物榜第13位,已成为“重磅炸弹药物”。
普瑞巴林S型异构体的药理活性是R型异构体的10倍[16]。因此,手性中心的高效构筑是普瑞巴林合成的关键[17]。目前,国内外学者报道了大量普瑞巴林及其中间体的化学合成方法,但存在工艺步骤复杂、拆分试剂昂贵和“三废”排放高等缺陷,限制了其工业化生产。如第一代普瑞巴林合成工艺以等浓度的(S)-扁桃酸为拆分试剂,总收率仅为20%,75%原材料变废弃物[18]。生物催化法因其高立体选择性、高催化效率和环境友好等优点,在手性药物合成中的潜力巨大。如Xie等[19]筛选获得Arabidopsisthaliana腈水解酶AtNit1,能够高选择性水解外消旋异丁基丁二腈(IBSN)合成普瑞巴林关键手性中间体(S)-3-氰基-5-甲基己酸,转化率达到45%,产物对映体过量值(e.e.值)可达97%。但是AtNit1底物耐受性差,且活力较低[20]。Chaudhari等[21]利用腈水解酶水解外消旋3-氨甲基-5-甲基已腈制备普瑞巴林,但该合成路线的底物获得困难,难以规模化应用。因此,挖掘高立体选择性、高活力的生物催化剂对于实现普瑞巴林的生物不对称合成具有重要意义。
本研究以来源于Brassicarapasubsp.的重组腈水解酶BrNit为催化剂,优化其水解IBSN合成(S)-3-氰基-5-甲基己酸的反应条件,以期为普瑞巴林的高效合成奠定基础。
1 材料与方法
1.1 菌种与培养基
腈水解酶基因NIT6,由生工生物工程(上海)有限公司合成;pET28b(+)表达载体,Novagen公司;大肠杆菌BL21(DE3),Invitrogen公司。实验中所用的培养基为LB培养基。
1.2 试剂
蛋白胨、酵母粉、琼脂粉,Oxoid公司;卡那霉素(Kan)、异丙基-β-D-硫代半乳糖苷(IPTG),上海生工生物工程股份有限公司。其他试剂均为市售分析纯。
1.3 重组腈水解酶工程菌BrNit的构建
将表达载体pET28b(+)和合成的腈水解酶基因(源于B.rapasubsp.,登录号:BAG72074.1)分别用XbaⅠ和XhoⅠ进行双酶切,酶切产物用T4连接酶在16 ℃下连接16 h,得到重组表达质粒pET28b(+)-NIT6。将表达载体pET28b(+)-NIT6转化至E.coliBL21(DE3)获得基因工程菌E.coliBL21(DE3)/pET28b(+)-NIT6。
1.4 重组腈水解酶静息细胞的制备
从活化平板上挑取单菌落至装有50 mL LB培养基(含50 μg/mL Kan)的250 mL摇瓶中,在37 ℃、150 r/min下培养7 h。按2.0%的接种量接种至100 mL LB培养基(含50 μg/mL Kan)中,在37 ℃、150 r/min下培养2 h至OD600为0.6左右,加入0.1 mmol/L的 IPTG进行诱导,在28 ℃、150 r/min条件下诱导培养12 h。离心收集菌体(8 000 r/min离心10 min,4 ℃),经0.9%的生理盐水洗涤后,收集菌体存放于-20 ℃冰箱中保存备用。
1.5 pH对水解反应的影响及pH稳定性
研究不同pH对BrNit水解反应的影响,分别为磷酸钠缓冲液(pH 6.0~7.5)、Tris-HCl缓冲液(pH 7.5~9.0)和Gly-NaOH缓冲液(pH 9.0~10.0),浓度都为100 mmol/L。反应体系:10 mL各缓冲液,150 mmol/L IBSN,10 g/L湿菌体,在30 ℃、150 r/min条件下反应30 min,气相色谱法检测转化率和e.e.值。以最高酶活为100%计算。
分别考察在pH 8.0和9.0条件下BrNit的稳定性,取湿菌体重悬于pH 8.0和pH 9.0的Tris-HCl缓冲液中(质量浓度30 g/L),于4 ℃下保存,每隔一定时间取出菌悬液加入到Tris-HCl缓冲液中,使菌体终质量浓度为10 g/L,并调节pH至8.0,加入IBSN至终浓度150 mmol/L,在30 ℃、150 r/min条件下反应30 min,取样进行气相检测。以时间为横坐标、ln(残留酶活)为纵坐标进行线性拟合,计算不同pH下BrNit的失活速率常数(Kd)和半衰期(t1/2),计算见式(1)~(2)。
(1)
(2)
式中:[E]为t时刻的酶活,[E0]为初始酶活,Kd为一级反应失活常数,Xt为时间。
1.6 温度对水解反应的影响及温度稳定性
考察不同温度对BrNit水解反应的影响,反应体系:10 mL的Tris-HCl缓冲液(pH 8.0),湿菌体10 g/L,IBSN浓度150 mmol/L,150 r/min下反应30 min,气相色谱法检测转化率和e.e.值。以最高酶活为100%计算。
分别考察30和35 ℃下BrNit的温度稳定性,取湿菌体悬于Tris-HCl缓冲液(pH 8.0)中(终质量浓度10 g/L),置于30和35 ℃下保温,每隔一定时间取出10 mL菌悬液,加入IBSN至终浓度150 mmol/L,在30 ℃、150 r/min条件下反应30 min,取样进行气相检测。以时间为横坐标、ln(残留酶活)为纵坐标进行线性拟合,计算不同温度下BrNit的失活速率常数(Kd)和半衰期(t1/2)。
1.7 金属离子对水解反应的影响
考察金属离子对BrNit催化IBSN水解的影响。反应体系:10 mL的Tris-HCl缓冲液(pH 8.0),湿菌体10 g/L,IBSN浓度150 mmol/L,加入金属离子至终浓度5 mmol/L,在30 ℃、150 r/min条件下反应3 h,气相色谱法检测转化率和e.e.值。以不添加任何金属离子为参比。
1.8 底物浓度对细胞转化速率的影响
考察底物浓度对BrNit转化速率的影响,反应体系:10 mL的Tris-HCl缓冲液(pH 8.0),湿菌体10 g/L,加入不同浓度的底物至反应体系底物的终浓度为20~200 mmol/L,在30 ℃、150 r/min条件下反应30 min,气相色谱法检测转化率和e.e.值。
1.9 底物、产物分析方法
反应液中底物、产物的光学纯度由气相色谱法测定。气相色谱仪为6890N(Agilent公司),色谱柱为毛细管柱BGB-174(BGB Analytik公司)。载气为高纯He,载气流量1.6 mL/min,分流比为30∶ 1,检测器、进样口的温度为220 ℃。柱温初始温度为120 ℃,保持14 min,再以10 ℃/min升温至170 ℃保持9 min。根据e.e.值计算底物、产物浓度及转化率(c)[22]。
取反应液200 μL,加入50 μL 2 mol/L HCl终止反应,加入800 μL乙酸乙酯萃取,12 000 r/min振荡1 min后离心,取上清液至1.5 mL离心管中,加无水Na2SO4干燥。取有机相,再加入15 μL纯甲醇和30 μL重氮甲烷,进行气相色谱分析。
酶活定义:在30 ℃、pH 8.0条件下,每分钟产生1 μmol 的3-氰基-5-甲基己酸所需的酶量定义为1个酶活单位(U)。
2 结果与讨论
2.1 pH对水解反应的影响及pH稳定性
pH的改变可能会使酶的结构发生改变,从而影响酶分子的催化部位和结合部位,另外,pH的改变还会影响底物分子的解离状态,进而影响底物与酶的结合[23]。在不同缓冲体系下pH对BrNit水解IBSN的影响结果如图1所示。
由图1可知:pH 8.0时活力最高,e.e.值达到98.2%。在pH为7.0~9.0弱碱性环境下,活力变化不明显,表明BrNit比较适合在中性以及弱碱性环境下反应。
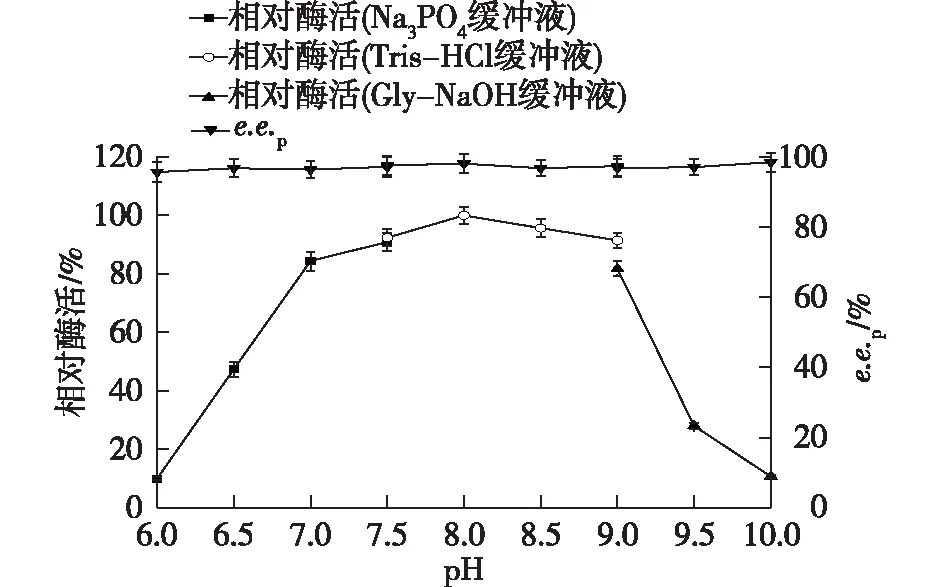
图1 pH对BrNit酶活和立体选择性的影响Fig.1 Effects of pH on activity and enantioselectivityof BrNit
进一步对BrNit在pH 8.0和9.0条件下的稳定性进行研究,结果如图2所示。
由图2可知:BrNit在pH 8.0和9.0条件下的半衰期分别是24.8 h和17.1 h。因此选择pH 8.0为最适pH。
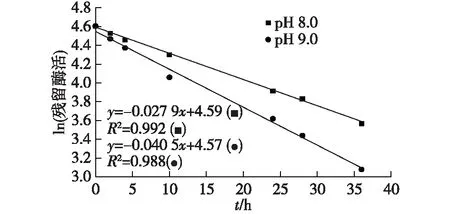
图2 BrNit的pH稳定性Fig.2 pH stability of BrNit
2.2 温度对水解反应的影响及温度稳定性
在一定温度范围内,酶的活力会随着温度的升高而增高,但是当温度高于最适温度时,酶的结构可能会被破坏而使酶的活力下降[24]。因此,笔者研究温度(20~50 ℃)对BrNit水解IBSN的影响,结果如图3所示。
由图3可知:温度对e.e.值几乎没有影响,BrNit在30 ℃时酶活最高,且30 ℃时产物的e.e.值达到98.3%,而35 ℃时的酶活仅为30 ℃时的71%,表明该腈水解酶对温度较为敏感。
进一步对不同温度下BrNit的稳定性进行研究,结果如图4所示。
由图4可知:BrNit在30和35 ℃下的半衰期分别为17.4和13.1 h。由此可知,BrNit在30 ℃下的稳定性较好,30 ℃为最适反应温度。
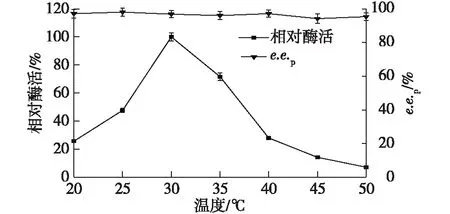
图3 温度对BrNit酶活和立体选择性的影响Fig.3 Effects of temperature on activity andenantioselectivity of BrNit

图4 BrNit的温度稳定性Fig.4 The thermal stability of BrNit

图5 金属离子对BrNit转化率和立体选择性的影响Fig.5 Effects of metal ions on conversion rate andenantioselectivity of BrNit
2.3 金属离子对细胞催化反应的影响
有些金属离子可以起到稳定酶的构象的作用,可参与电子传递从而对催化反应产生影响[25]。笔者考察不同金属离子对BrNit水解IBSN的影响,结果如图5所示。
由图5可知:几乎没有金属离子对BrNit的催化反应有促进作用,Fe3+、Ni2+、Zn2+、Fe2+和Cu2+对其活力有明显抑制作用,其中Zn2+、Fe2+和Cu2+抑制更为严重;Zn2+、Cu2+为巯基结合型金属离子[26],其严重的抑制作用说明巯基对该腈水解酶的水解反应至关重要,所以在后续反应中没添加任何金属离子。
2.4 底物浓度对反应速率的影响
底物耐受性是工业生物催化过程中的重要指标之一。在一定催化剂浓度下,反应速率随着底物浓度的增加而增加,但是底物浓度过高则会使酶的活力下降,甚至对其选择性也会产生影响[27]。笔者考察底物浓度对反应速率(v)的影响,结果如图6所示。
由图6可知,底物浓度的变化对该酶选择性几乎没有影响。当底物从20 mmol/L增至180 mmol/L时,初始反应速率显著增加,从0.3 mmol/(L·h)增加到2.98 mmol/(L·h)。当底物为200 mmol/L时,反应速率下降为2.7 mmol/(L·h),表明高底物浓度对酶活力产生抑制。因此,选择180 mmol/L为最适底物浓度。
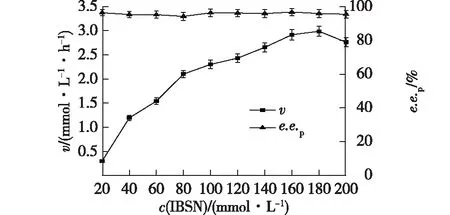
图6 底物浓度对BrNit反应初速率和立体选择性的影响Fig.6 Effects of concentration of IBSN on initial reactionrate and enantioselectivity of BrNit
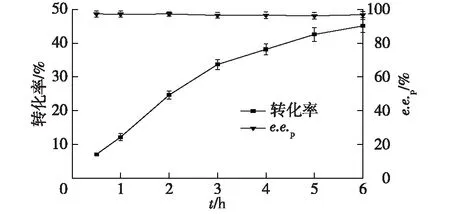
图7 BrNit水解IBSN反应进程Fig.7 Progress of hydrolysis of IBSN by BrNit
2.5 全细胞生物催化选择性水解IBSN反应进程
考察在最适反应条件下,全细胞生物催化选择性水解IBSN的反应进程,结果如图7所示。
由图7可知:随着反应的进行,产物的e.e.值基本保持不变,始终保持在97%以上,反应到6 h时,转化率达到45.1%,e.e.值达到97.9%。
3 结论
利用重组腈水解酶工程菌催化IBSN水解合成(S)-3-氰基-5-甲基己酸,对其反应条件进行了优化。BrNit菌体最适温度为30 ℃,最适pH为8.0,最适底物浓度为180 mmol/L。在此条件下,利用10 g/L湿菌体催化水解180 mmol/L IBSN,反应6 h 转化率可达45.1%,产物(S)-3-氰基-5-甲基己酸的e.e.值达到97.9%。结果表明,重组腈水解酶工程菌BrNit具有较高的立体选择性和催化活性,显示出较好的工业化应用潜力。但是,该腈水解酶的稳定性较差,活力也有进一步提高的空间。因此,后期可以对该腈水解酶进行分子改造,提高其酶活和稳定性。
