不同温度下氧化猪脂和木糖对猪肉蛋白酶解液的热反应特性影响
2019-01-28王天泽肖群飞杜文斌王雅欣谢建春
王天泽,肖群飞,杜文斌,王雅欣,谢建春
(北京食品营养与人类健康高精尖创新中心,食品质量与安全北京实验室,北京市食品添加剂工程技术研究中心,北京工商大学,北京 100048)
热反应肉味香精采用动物及植物蛋白的酶解物、还原糖、氨基酸及脂肪等原料通过热反应制备而成,广泛应用于方便面、火腿肠、速冻水饺、膨化食品等多种食品的增香调味[1]。热反应香精制备中涉及的反应主要包括美拉德反应、脂肪氧化降解反应及其相互作用,这些反应在肉香味形成,以及热反应产物的颜色、滋味等感官特性的形成中有重要作用。有关美拉德反应、脂肪氧化反应对热反应肉香味形成的研究已有较多报道[2-6]。在热反应肉味香精制备中,含硫氨基酸或其肽发生美拉德反应产生2-甲基-3-巯基呋喃、糠硫醇等挥发性含硫化合物,贡献肉的基础香味[7-10]。动物脂肪加热氧化制备的氧化脂肪含有小分子醛、酮、羧酸等含羰基化合物,可赋予热反应肉味香精不同种类肉的特征香气[11]。在脂肪氧化反应与美拉德反应共存的体系中,一方面脂肪氧化对美拉德反应有抑制作用,使含硫氨基酸或其肽的美拉德反应产生的含硫肉香味物质减少[12-15],另一方面还可与含硫氨基酸或其肽的美拉德反应产生的H2S、NH3等小分子作用,生成新的杂环肉香化合物[16-18]。除了以上的挥发性风味方面,近年来人们逐渐开始关注美拉德反应和脂肪氧化反应对形成非(难)挥发性热反应产物的影响,已发现美拉德反应中大豆肽的短肽通过与糖交联,可形成具有滋味增强效应的美拉德肽,从而改善口感[19]。此外,还有报道干鱼片中脂肪氧化产物与蛋白质、肽类等水溶性组分交联形成的一种反应产物,具有增强面汤醇厚感和持续性的优点[20]。
热反应肉味香精制备的主要原料——动物或植物蛋白酶解物,含有游离氨基酸及不同碳链长度的多肽和蛋白质,在热反应产物香气、颜色、滋味等感官特性形成中,涉及的脂肪氧化反应、美拉德反应作用机理极为复杂。本实验以猪肉酶解物为原料,设计“酶解液”(空白)、“酶解液+氧化猪脂”、“酶解液+木糖”、“酶解液+氧化猪脂+木糖”4 个热反应体系,研究不同温度下氧化猪脂及木糖对于热反应产物pH值、褐变、分子质量分布及滋味的影响,并通过动力学模型对各体系反应速率进行比较,从而为热反应肉味香精的制备提供理论基础。
1 材料与方法
1.1 材料与试剂
猪后腿肉 北京美廉美超市;氧化猪脂(过氧化值223 meq/kg;酸值0.65 mg KOH/kg),按照文献[21]制备;复合蛋白酶、风味蛋白酶 诺维信公司;三氟乙酸(色谱纯)、木糖(分析纯) 北京百灵威科技有限公司;乙腈(色谱纯) 飞世尔实验器材有限公司;碘、碘化钾、正己烷(均为分析纯) 国药集团化学试剂有限公司。
1.2 仪器与设备
DF-101S集热式恒温加热磁力搅拌器 河南省予华仪器有限公司;UV2300II紫外分光光度计 上海天美科学仪器有限公司;PHSJ-3F实验室pH计 上海仪电有限公司;3-30K高速离心机 美国Sigma公司;ALPHA 2-4 LSC冷冻干燥机 德国Christ公司;LC1200型高效液相色谱仪 美国Agilent公司。
1.3 方法
1.3.1 猪肉酶解液的制备
猪肉去除可见脂肪,于90 ℃水漂烫3 min,绞成肉糜。按料液比1∶1(m/m)将一定量的肉糜、水加入到烧瓶中,加入质量分数0.4%的复合蛋白酶,于55 ℃水浴酶解3 h;再加入0.3%风味蛋白酶,酶解1 h;升温至85 ℃,灭酶10 min。酶解液20 000 r/min离心15 min,取上清液,与正己烷混合(1∶1,V/V)萃取除脂,冻干待用。
1.3.2 热反应
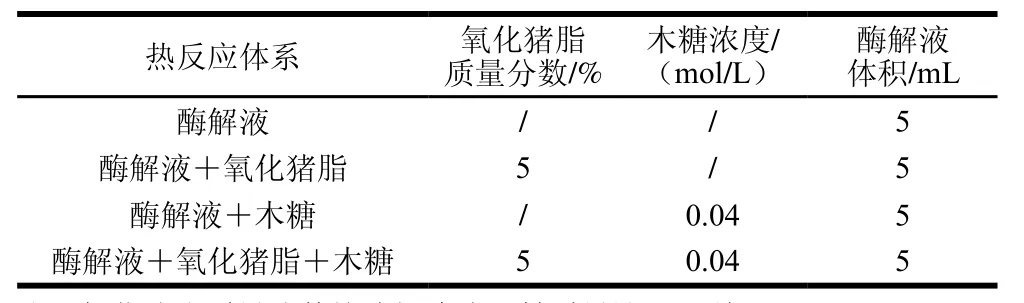
表1 热反应所用原料Table1 Formulation of thermal reaction systems
取0.5 g除脂冻干粉,加水5 mL复溶酶解液,置于15 mL耐压管中。基于本课题组前期研究[11],按表1设计4 个反应体系“酶解液”、“酶解液+氧化猪脂”、“酶解液+木糖”、“酶解液+氧化猪脂+木糖”,在120、130、140 ℃分别反应20、40、60、80、100、120 min进行分析。其中120 ℃反应120 min的样品进行滋味评价。
1.3.3 指标的测定
吸光度:反应产物经0.45 μm聚醚砜膜过滤,用超纯水稀释一定倍数,在294 nm和420 nm波长处测定吸光度(A)。结果=测定值×稀释倍数。重复测定2 次。
色度值:参照SB/T 10323—1999《色度测定法》[22]。取1.000 g碘颗粒,溶于碘化钾溶液中,用100 mL容量瓶定容,配制成1 g/100 mL碘液,再进一步稀释10、20、…、100 倍,加入4 g碘化钾配制成不同质量浓度的标准色液。将反应产物与标准色液进行比较,其中与标准色液颜色最一致的碘液质量浓度,记录为该反应产物的色度值。
pH值:用pH计测定。重复测定2 次,结果取平均值。
1.3.4 高效凝胶液相色谱分子质量分布的测定
测定4 个体系于120 ℃反应120 min反应产物分子质量分布。反应液用超纯水稀释10 倍,经0.22 μm聚醚砜膜过滤,采用高效凝胶液相色谱分析;色谱柱TSK gel G2000 SWXL(300 mm×7.8 mm,5 μm),流动相:0.1%三氟乙酸溶液-乙腈(80∶20,V/V);流速0.5 mL/min;柱温30 ℃;二极管阵列检测器;检测波长220 nm;进样量10 μL。
分子质量校正曲线所用标准品:乙氨酸-乙氨酸-乙氨酸(189 Da)、乙氨酸-乙氨酸-酪氨酸-精氨酸(451 Da)、杆菌酶(1 450 Da)、抑肽酶(6 500 Da)、细胞色素(12 500 Da)。标准曲线方程:lgy=-0.227 6x+7.155 4,R2=0.977 9(y为分子质量/Da,x为保留时间/min)。
参照文献[19]将4 种体系测定的分子质量分布结果分为>5 kDa,3~5 kDa,1~3 kDa和<1 kDa。其中>5 kDa组分主要为大分子无滋味产物,3~5 kDa和1~3 kDa组分主要为呈味多肽,<1 kDa组分为短肽和氨基酸等小分子物质。计算4 种体系以上分子质量分布范围的相对含量,以探究各体系反应产物特性的差异。
1.3.5 感官评价
感官评价前将样品水浴加热至60 ℃,样品质量浓度10 mg/mL。评价小组包括5 名人员,为本实验室参照文献[23]进行培训后筛选出的具有感官分析经验的成员,年龄在21~26 周岁之间,其中男性2 名,女性3 名。对120 ℃反应120 min的各体系反应产物滋味进行评价,描述词为鲜味、肉味、醇厚感、持续性、苦味、咸味。滋味强度按a、b、c和d四档打分,其中a代表滋味最强,b、c、d滋味强度依次递减。
1.4 数据统计及图像处理
图像采用Microsoft Excel 2017软件绘制,pH值、A294nm、A420nm、色度值和分子质量分布等数据采用SPSS 19.0统计分析软件分析,差异分析采用单因素方差分析。P<0.05,为差异显著。
2 结果与分析
2.1 热反应产物pH值比较
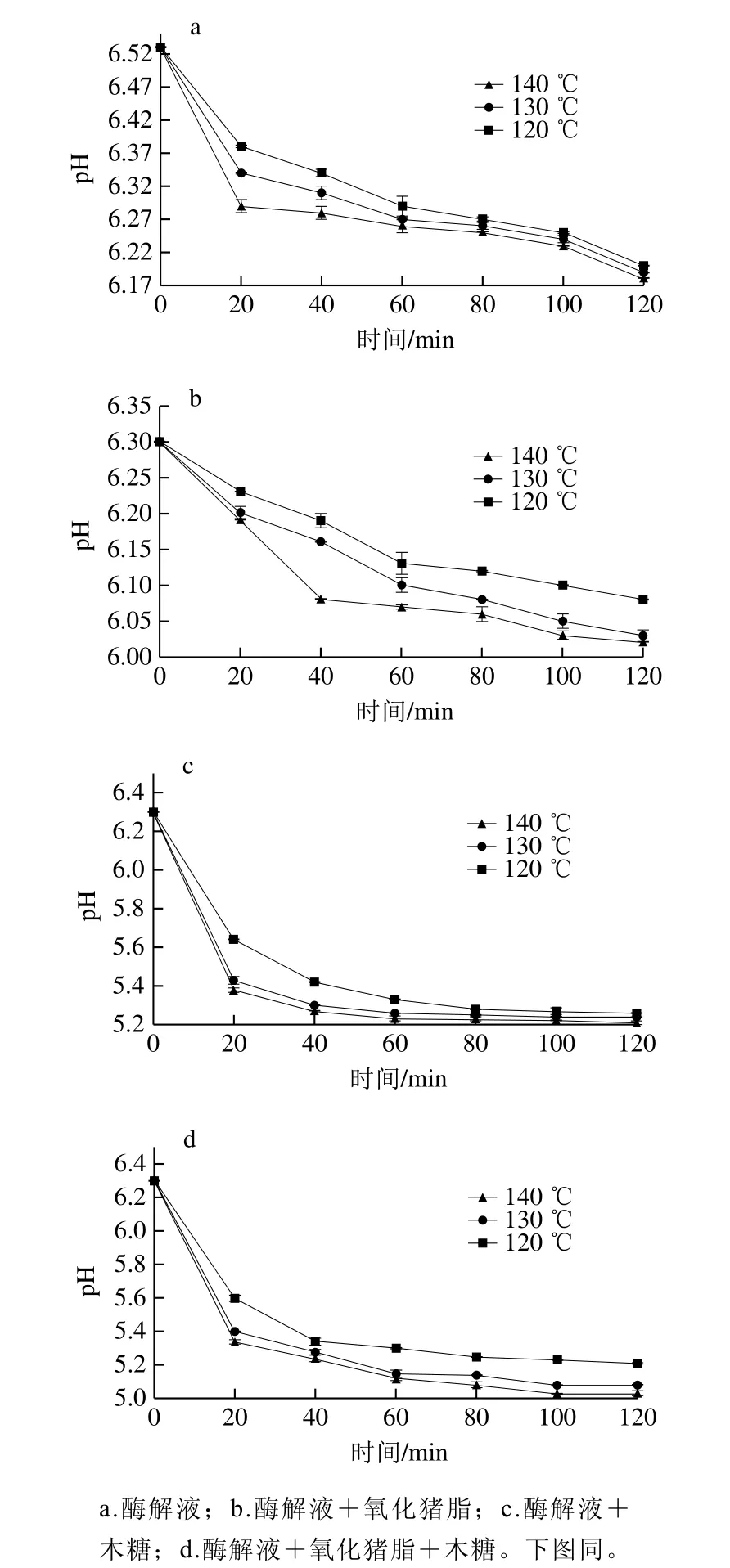
图1 各体系不同温度下热反应产物pH值变化趋势图Fig.1 Change in pH of reaction products from four systems heated at different temperatures
由图1可知,在120、130、140 ℃条件下,4 个反应体系pH值均呈下降趋势。“酶解液+氧化猪脂”体系在反应时间0~40 min,pH值下降明显,另外3 个体系反应时间为0~20 min时,pH值下降明显;在相同反应时间时,温度升高,由于反应加快,4 个体系pH值均降低;相同温度及相同反应时间下,4 个体系pH值下降量由高到低为“酶解液+氧化猪脂+木糖”体系、“酶解液+木糖”体系、“酶解液”体系、“酶解液+氧化猪脂”体系。随着美拉德反应进行,由于氨基被消耗并生成有机酸,pH值将下降[24],pH值下降程度是反映美拉德反应进行程度的一个重要指标。“酶解液+氧化猪脂”体系的pH值变化量很小,可能由于氧化猪脂与酶解液反应过程中不能生成有机酸。
2.2 热反应产物A294 nm比较
A294nm可代表美拉德反应中期阶段形成的无色中间产物(如双羰基化合物)含量[25-26]。由图2可知,在120、130、140 ℃条件下,随着时间延长,4 个体系A294nm均呈上升趋势;与pH值变化趋势类似,“酶解液+氧化猪脂”体系在反应时间0~40 min时A294nm上升明显,另外3 个体系在反应时间0~20 min时A294nm上升明显,而后变化趋于平稳。相同反应时间,温度升高时,由于反应加快,4 个体系A294nm均增大。相同反应温度下,反应时间小于20 min时,4 个体系的A294nm由大到小顺序为“酶解液+木糖”、“酶解液+氧化猪脂+木糖”、“酶解液+氧化猪脂”、“酶解液”体系;反应时间大于20 min后,4 个体系的A294nm吸光度由大到小顺序变为“酶解液+氧化猪脂+木糖”、“酶解液+木糖”、“酶解液+氧化猪脂”、“酶解液”体系。
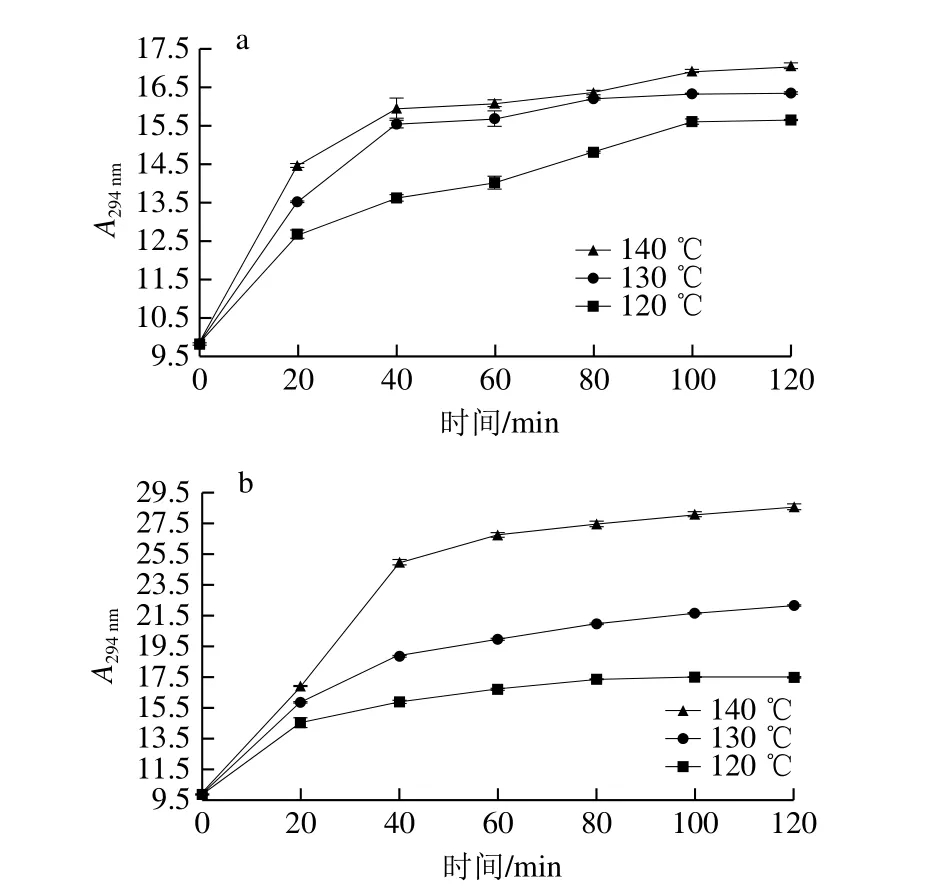
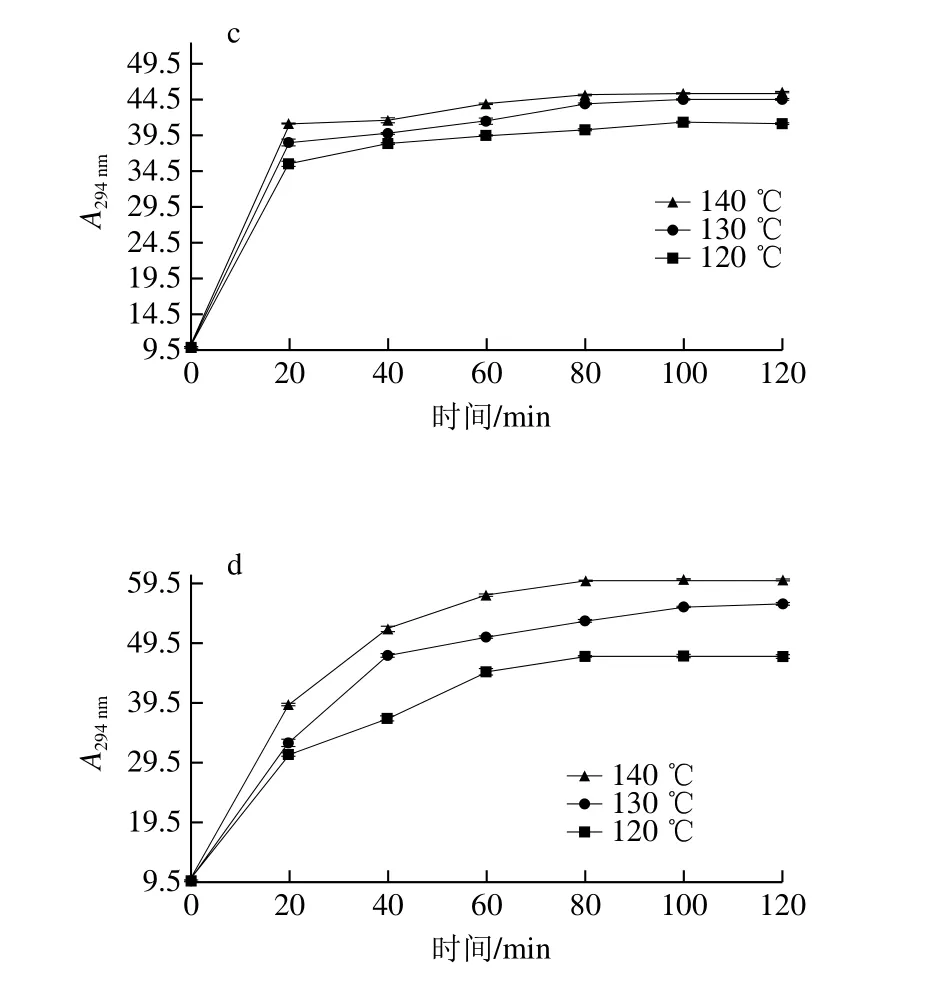
图2 各体系不同温度下热反应产物A294 nm变化趋势图Fig.2 Change in absorbance 294 nm of reaction products from four systems heated at different temperatures
2.3 热反应产物A420 nm比较
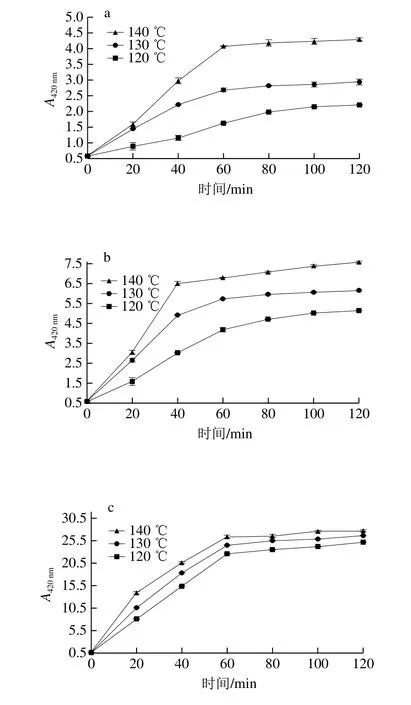
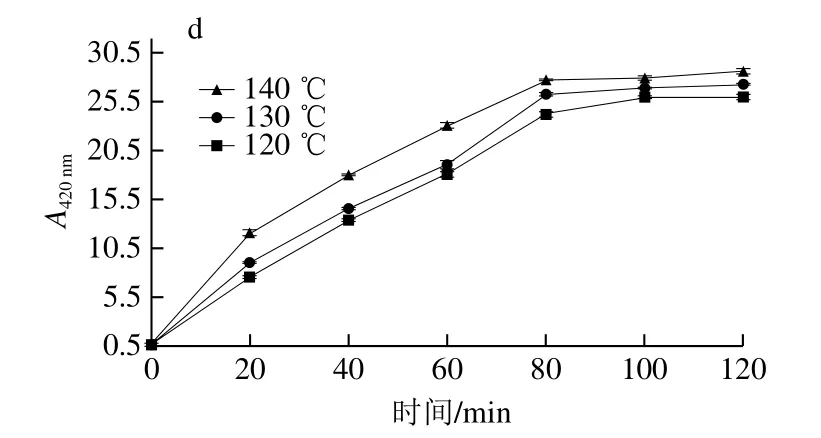
图3 各体系不同温度下热反应产物A420 nm变化趋势图Fig.3 Change in absorbance 420 nm of reaction products from four systems heated at different temperatures
A420nm代表美拉德反应在末期阶段反应形成的类黑精物质[27-28]。由图3可知,在120、130、140 ℃条件下,随着时间延长,4 个体系吸光度均呈上升趋势;其中“酶解液+氧化猪脂”体系在反应时间0~40 min时吸光度上升明显,“酶解液+氧化猪脂+木糖”体系在反应时间0~80 min时吸光度上升明显,另外2 个体系在反应时间0~60 min时吸光度上升明显,然后趋于平缓;相同反应时间,温度升高时,由于反应加快,4 个体系A420nm均增大;相同反应温度下,比较4 个体系,反应时间小于60 min时,4 个体系A420nm由大到小顺序为“酶解液+木糖”、“酶解液+氧化猪脂+木糖”、“酶解液+氧化猪脂”、“酶解液”体系;反应时间大于60 min时,4 个体系A420nm由大到小顺序为“酶解液+氧化猪脂+木糖”、“酶解液+木糖”、“酶解液+氧化猪脂”、“酶解液”体系。
2.4 热反应产物色度比较
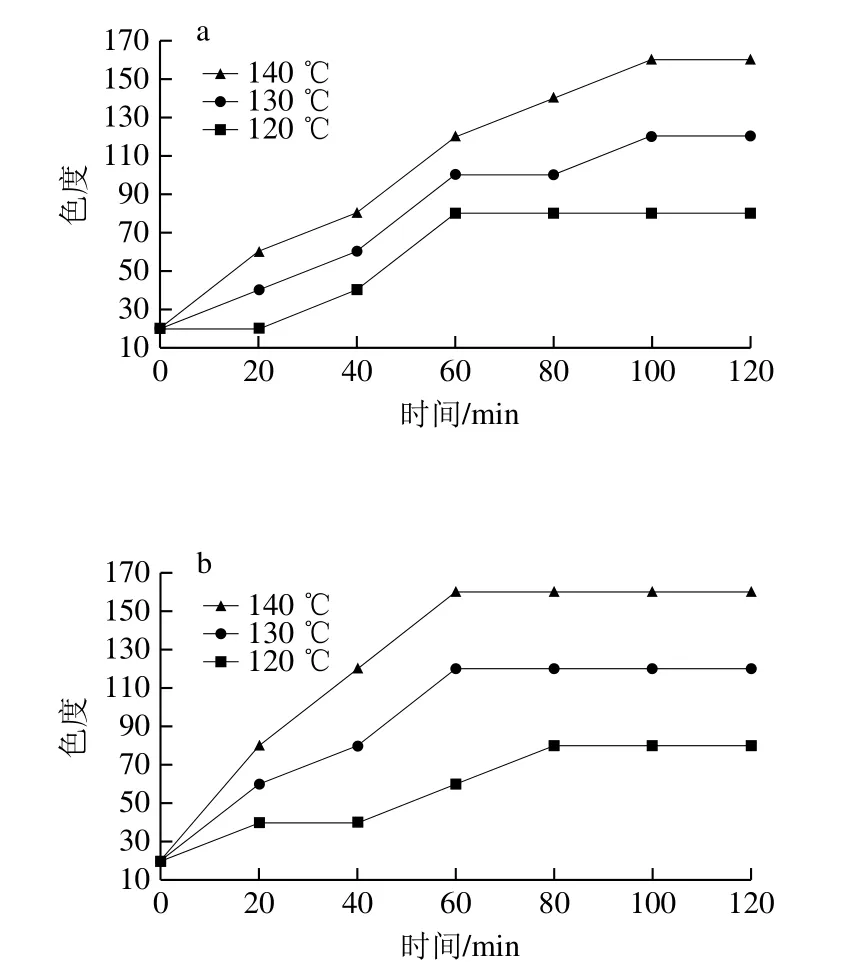
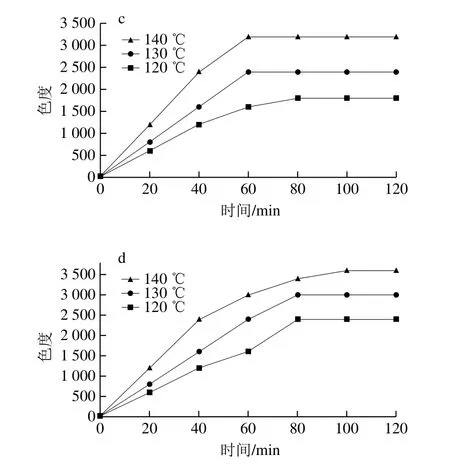
图4 各体系不同温度下热反应产物色度变化趋势图Fig.4 Change in chroma of reaction products from four systems heated at different temperatures
由图4可知,在120、130、140 ℃条件下,随着时间延长,4 个体系色度值均呈上升趋势,“酶解液+氧化猪脂+木糖”体系在反应时间0~80 min,另外3 个体系在反应时间0~60 min内上升幅度较大,然后趋于平缓。相同反应时间,温度升高时,由于反应加快,4 个体系色度值均增大。相同反应温度下,比较4 个体系,反应时间小于60 min时4 个体系色度值由大到小顺序为“酶解液+木糖”体系、“酶解液+氧化猪脂+木糖”体系、“酶解液+氧化猪脂”体系、“酶解液”体系;反应时间大于60 min时,4 个体系色度值由大到小顺序为“酶解液+氧化猪脂+木糖”、“酶解液+木糖”、“酶解液+氧化猪脂”、“酶解液”体系。色度值代表反应液的褐变颜色深浅程度。色度值除与生成类黑精有关外,还与其他有颜色的物质有关,如Hofmann[29]发现戊酸与丙氨酸发生美拉德反应会形成有吡咯和吡咯啉酮结构的有色化合物。
2.5 热反应产物动力学分析
由上述可知,4 种体系的A294nm均在前20或40 min迅速上升后,就已趋于平缓,数据点较少,而4种体系A420nm和“酶解液+木糖”、“酶解液+氧化猪脂+木糖”2 种体系色度值在反应60~80 min时才趋于平缓,数据点足以进行动力学研究,为此仅对4 种体系A420nm和“酶解液+木糖”、“酶解液+氧化猪脂+木糖”2 种体系色度值按零级动力学模型进行拟合,再根据Arrhenius方程对-lnk-1/T进行线性拟合,计算后得到各体系的活化能,结果如表2所示。
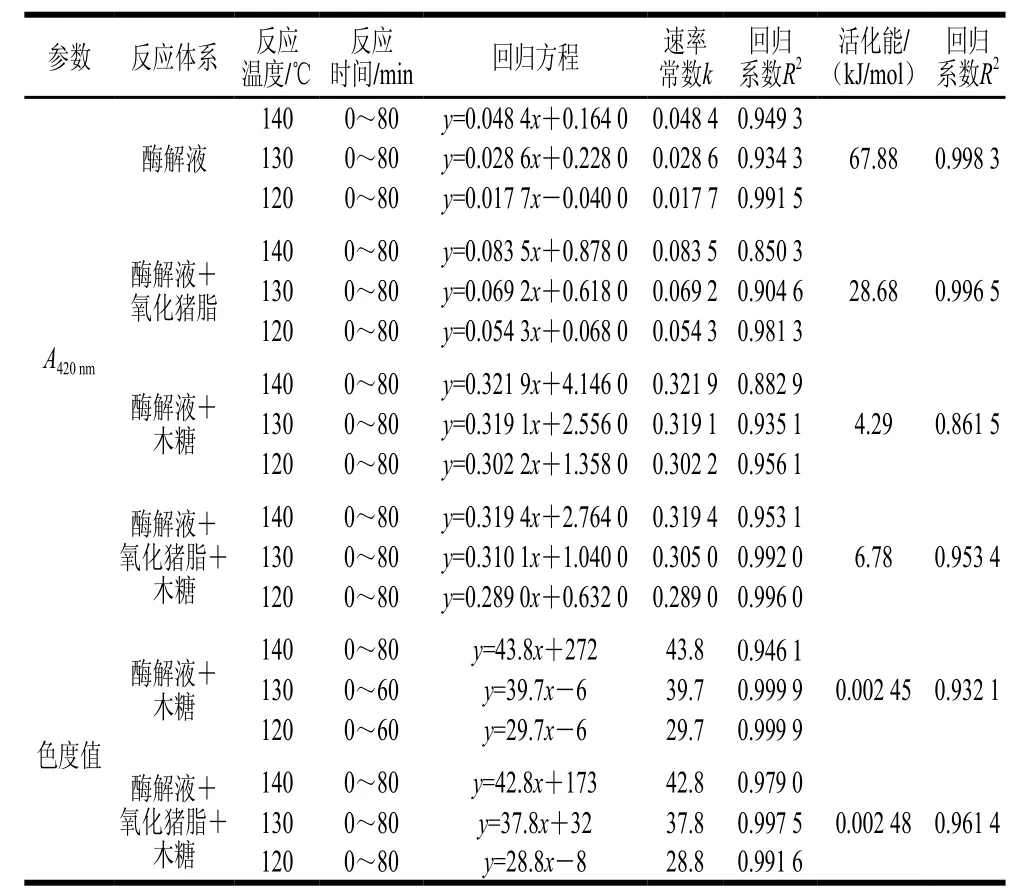
表2 A420 nm和色度值拟合动力学方程及活化能Table2 Fitted kinetic equations and activation energy for absorbance at 420 nm and chroma
由表2可知,各体系回归方程的回归系数R2均大于0.85,多数大于0.95,说明各体系A420nm及色度值和反应时间均表现出良好的线性关系。随着温度升高,4 个体系速率常数k均增大。反应温度相同时,4 个体系A420nm反应速率常数由大到小顺序为“酶解液+木糖”、“酶解液+氧化猪脂+木糖”、“酶解液+氧化猪脂”、“酶解液”体系,色度值反应速率常数大小为“酶解液+木糖”体系大于“酶解液+氧化猪脂+木糖”体系,说明反应初期酶解液中单独加入木糖反应速率最快,单独加入氧化猪脂速率也有一定加快,同时加入氧化猪脂和木糖时,氧化猪脂抑制“酶解液-木糖”反应,使“酶解液+氧化猪脂+木糖”体系反应速率小于“酶解液+木糖”体系。反应活化能低,表明反应容易进行。“酶解液+氧化猪脂+木糖”体系活化能大于“酶解液+木糖”体系,进一步证明此现象。
2.6 分子质量分布及滋味比较
反应温度120 ℃是制备肉味香精的常用温度,在此温度下反应120 min 4 个体系所得热反应产物的滋味均最佳。因此测定此反应产物分子质量分布及进行滋味感官评价,结果如表3所示。
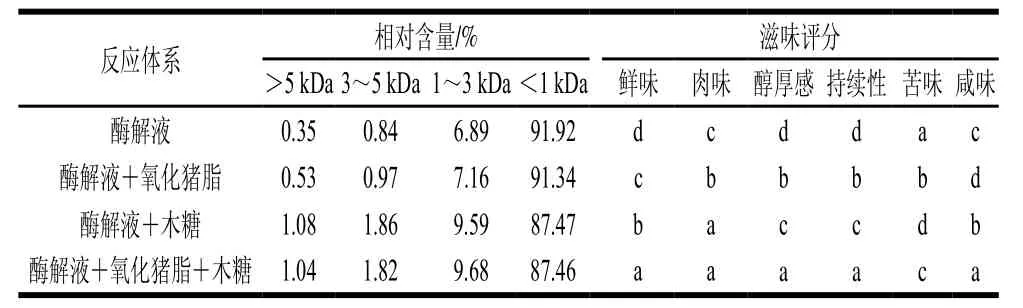
表3 120 ℃反应120 min各体系分子质量分布和滋味评分Table3 Molecular mass distribution and sensory taste scores of reaction products from four systems heated at 120 ℃ for 120 min
由表3可知,4 个体系反应产物主要为分子质量<1 kDa的组分,可达85%以上,其次为分子质量1~3 kDa的组分,而分子质量3~5 kDa和>5 kDa的组分含量很少。与“酶解液”体系相比,加入木糖的体系分子质量<1 kDa组分相对含量减少,随之1~3 kDa、3~5 kDa和>5 kDa的组分相对含量增加;而加入氧化猪脂分子质量仅有较小变化。<1 kDa组分相对含量减少由大到小排序为:“酶解液+氧化猪脂+木糖”、“酶解液+木糖”、“酶解液+氧化猪脂”体系。
比较4 个体系滋味变化,鲜味、肉味从强到弱顺序为“酶解液+氧化猪脂+木糖”、“酶解液+木糖”、“酶解液+氧化猪脂”、“酶解液”体系;醇厚感、持续性从强到弱顺序为“酶解液+氧化猪脂+木糖”、“酶解液+氧化猪脂”、“酶解液+木糖”、“酶解液”体系;苦味从强到弱顺序为“酶解液”、“酶解液+氧化猪脂”、“酶解液+氧化猪脂+木糖”、“酶解液+木糖”体系。说明与“酶解液”体系相比,同时加入氧化猪脂和木糖所得产物的鲜味、肉味、醇厚感、持续性、咸味均明显增强;加入木糖后产物鲜味、肉味和咸味增强;加入氧化猪脂后产物醇厚感和持续性明显增强。
3 讨论与结论
原料酶解液经除脂处理,主要含有蛋白质、多肽、氨基酸和少量还原糖。在加热条件下,“酶解液”(空白)体系仅可发生轻度的美拉德反应;“酶解液+氧化猪脂”体系中,除轻度的美拉德反应,还包括氧化猪脂所含的醛类、酮类等脂肪氧化降解产物与氨基酸、多肽、蛋白质等含氨基化合物的反应;“酶解液+木糖”体系主要为蛋白质、多肽、氨基酸和木糖的美拉德反应;“酶解液+氧化猪脂+木糖”体系包含上述体系所有反应,以及脂肪氧化反应与美拉德反应的相互作用。氧化脂肪中醛类、酮类等脂肪氧化产物与蛋白质、多肽、氨基酸的作用,也属于“羰-氨”反应,即属于美拉德反应范畴。
A294nm代表美拉德反应中期阶段形成的双羰基类中间产物,A420nm及色度值代表美拉德反应末期阶段产物,因此与A294nm变化相比,反应初期A420nm及色度值的显著变化存在滞后性。反应时间为0~20 min时,pH值和A294nm变化明显,是由于反应初期原料的浓度高、反应快造成;而随后因原料逐渐被消耗,pH值和A294nm变化减缓。随着反应进行,4 个体系A294nm、A420nm及色度值均呈上升趋势,表明A294nm代表的无色中间产物不断反应生成高级美拉德反应产物,从而反应液褐变加深。
相同温度下4 个体系最终反应液的A420nm、色度值由高到低的顺序均为“酶解液+氧化猪脂+木糖”、“酶解液+木糖”、“酶解液+氧化猪脂”、“酶解液”体系,表明木糖或氧化猪脂均可提升酶解液的美拉德反应程度。加入木糖比加入氧化猪脂提升幅度大,表明加入木糖的“羰-氨”反应速率大于加入氧化猪脂。与“酶解液+木糖”、“酶解液+氧化猪脂”体系相比,“酶解液+氧化猪脂+木糖”体系反应程度最高,是因氧化猪脂中的羰基类脂肪氧化产物及木糖二者与氨基化合物共同作用造成。
反应初期酶解液中单独加入木糖反应速率最快,单独加入氧化猪脂速率也有一定加快。但与加入木糖相比,同时加入氧化猪脂和木糖时,反应速率却有所下降,这是由于在反应初期,氧化猪脂的醛类脂肪氧化产物与木糖竞争性地与氨基化合物作用,从而表现为抑制酶解液与木糖间的美拉德反应。这与先前研究发现的现象脂肪醛可抑制美拉德反应一致[14]。随着反应进行,“酶解液+氧化猪脂+木糖”体系反应程度逐渐大于“酶解液+木糖”体系,最终造成“酶解液+木糖+氧化猪脂”体系反应程度最高,这与后期羰基类脂肪氧化成分可参与终期美拉德反应有关。
与“酶解液”体系相比,加入木糖使分子质量低于1 kDa组分相对含量减少,大于1 kDa组分相对含量相对增加,这可能因木糖与酶解液中短肽发生交联反应造成。另外,美拉德反应末期产物如类黑精等褐色物质也为大分子质量化合物,这些化合物也会导致分子质量大的组分相对含量上升。而加入氧化猪脂分子质量小于1 kDa组分百分比减少得很小,总体分子质量变化不大,这很可能因为氧化脂肪中的醛、酮等化合物本身分子质量较小,即使与酶解液中肽组分缩合也对分子质量分布影响很小。同时加入氧化猪脂和木糖时,小于1 kDa组分相对含量减少最大,总体分子质量增大,是因木糖及氧化脂肪中的醛、酮等化合物共同与肽类组分作用造成。
由于未加热时,加入木糖或氧化猪脂并未观察到滋味变化(表3),因此滋味的变化是由于热反应产物分子质量分布的变化造成。美拉德肽具有风味增强作用,其分子质量在1~5 kDa之间[30-31]。加入木糖所得产物的滋味变化,与木糖与低于1 kDa的短肽发生交联反应形成具有风味增强作用的美拉德肽,使得质量分数高于1 kDa组分百分比升高有关[23]。加入氧化猪脂所得产物的滋味变化,可能与氧化脂肪所含的醛类羰基化合物与酶解液中的氨基化合物交联有关[20]。同时加入氧化猪脂和木糖所得产物的滋味变化最明显,是因为木糖及氧化猪脂中脂质氧化成分均与酶解液中肽组分作用造成。此外,与“酶解液”体系相比,3 个体系反应产物的苦味均下降,说明加入木糖或氧化猪脂均具有一定的减弱反应物苦味的作用,这可能由于酶解液中苦味氨基酸或肽参与了美拉德反应被消耗所致。
综上所述,本实验设计4 个反应体系,检测不同温度下随反应时间反应液的pH值、A294nm和A420nm、色度值变化,建立A420nm和色度值的动力学模型,并在此基础上测定较佳反应产物的分子质量分布和滋味特性变化,得出以下结论:与“酶解液”体系相比,添加木糖或氧化猪脂均可使最终反应液的褐变程度提高;相比之下,添加木糖比添加氧化猪脂褐变反应程度高,同时添加木糖和氧化猪脂时褐变反应程度最高。反应初期,由于脂肪氧化产物中的醛类成分与木糖存在竞争,同时添加木糖和氧化猪脂的褐变反应速率反而低于单独添加木糖。木糖或氧化猪脂可与酶解液中低于1 kDa的短肽发生交联反应,从而可改善反应产物的滋味特性,但由于脂肪氧化生成的醛类组分本身分子质量较小,其与肽交联后对反应产物的分子质量分布影响不大。而木糖与酶解液中肽组分发生反应的机理,以及氧化猪脂中羰基类脂质氧化成分与肽组分发生作用情况等,还有待于进一步研究。
