基底细胞癌诊治的研究进展
2019-01-24邢天娇李东霞
邢天娇,李东霞
(内蒙古医科大学附属医院皮肤科,呼和浩特 010050)
基底细胞癌(basal cell carcinoma,BCC)又称基底细胞上皮瘤,是源自表皮或其附属器的皮肤恶性肿瘤,由Kropecher于1903年首次发现报道,为皮肤恶性肿瘤中最常见的组织类型(占65%~75%)[1]。BCC多发生在中老年人,单发,偶有多发,大多数病变位于头部、面部和颈部,而在躯干和背侧则较少,提示紫外线可能是诱发BCC的重要因素。有相关研究表明,长期紫外线照射会对氧化的DNA造成间接损伤,诱导DNA突变和错误表达,从而触发致癌机制[2]。BCC临床表现多样,且起病隐匿,一般自觉症状轻微或无自觉症状,生长速度缓慢,极少转移,预后较好。但近年来BCC在各国的发病率越来越高[3]。其主要治疗方法首选手术治疗,治愈率高,平均治愈率为90%~91%[4]。目前新兴技术如 Mohs显微外科手术(Mohs microsurgery,MMS)、氨基酮戊酸光动力疗法、联合治疗逐渐应用于临床,可以增加治愈率,避免复发,提高美容度[5]。不同部位、不同治疗方法的BCC预后不同。现对BCC的诊治研究进展予以综述。
1 BCC的诊断
临床医师通过患者的临床表现进行经验诊断,再行皮肤镜等专科检查给予初步诊断,后行病理及免疫组织化学可确诊。诊断后,必要时可行磁共振成像、CT、正电子发射计算机断层扫描、皮损部位淋巴结彩色多普勒超声等确定是否出现浸润及转移。
1.1发病情况与临床特征 BCC发病隐匿,一般自觉症状轻微或无自觉症状。据欧美学家统计,BCC以40岁以上的中老年人较20岁左右的人群多见,单发,多发相对少见,病灶大多位于头部、面部、颈部等暴露部位[6-7]。早期病变多为皮肤色或红色圆形或椭圆形斑块,表面光亮,可附着鳞屑,少数伴有扩张的毛细血管或色素沉着,其典型特征为边缘具有卷曲的“珍珠样”半透明小结节。本病呈慢性进行性发展,久而久之中心坏死可向深部组织扩展蔓延,甚至深达软组织和骨组织,呈大片状侵袭性坏死,又名侵袭性溃疡。上述特征性表现及皮肤癌家族史、砷剂接触史、器官移植等病史可考虑临床诊断为BCC。
1.2电子皮肤镜 BCC在皮肤镜下具有特征性表现,国外报道BCC的诊断标准如下[8]:①皮损血管模式分为不规则且弥漫分布的散在血管模式和皮损内无血管的无血管模式。②局部皮肤镜特征表现为15项,分别是蓝灰色卵圆形巢;多发性蓝灰色小球或小点;枫叶状结构;轮辐样结构;出血溃疡;分支状血管;毛细血管扩张;逗号样血管;螺旋状血管;不典型血管;无结构区;红白背景下无结构区;色素减退区;乳红色小球;乳红色小点。皮肤镜作为无创性初筛技术可显著提高BCC的诊断率, 对无条件做病理诊断的基层单位及合理选择治疗方法有一定意义[9-10]。
1.3共聚焦显微镜 共聚焦显微镜又称皮肤CT,具有动态、快速、适时、无创、可重复操作等特点,能够较好地区别良恶性肿瘤[11]。BCC在共聚焦显微镜下的表现与组织病理具有相似性,可见表皮细胞排列紊乱及单个核的癌细胞形成癌细胞肿瘤团块,其拉长的细胞核呈轮辐状排列出现细胞极性,中央间杂折光度较低的间质为黏蛋白,还可见扩张的毛细血管及炎细胞浸润。其中表皮和(或)真皮内折光的肿瘤细胞团块及轮辐状排列的肿瘤细胞具有特征性,被认为是BCC的诊断依据[12]。共聚焦显微镜对BCC的诊断具有较高的敏感性和特异性,灵敏度可高达100%,特异度为89%,但因其检查的深度仅限于真皮浅层,常用于BCC的早期筛查及术后随访,明确诊断还需结合组织病理学检查[13]。
1.4组织病理学诊断 皮肤镜、共聚焦显微镜等新兴检查方法最大的特点具有无创性,在临床中逐渐应用,但仍具有一定的假阴性,而组织病理学检查为BCC诊断的金标准。组织病理典型特点为嗜碱性基底样细胞肿瘤团块。边缘细胞呈栅栏状排列,边界清楚,肿瘤与周围组织出现明显的收缩间隙,可见核分裂,异型性明显。病理分型分为8型[14],分别是实体型、角化型、纤维上皮瘤型、腺样型、色素型、硬班病样型、浅表型和囊肿型。各种类型有其各自的特点,其中硬斑病样型BCC恶性程度相对较强,结节溃疡型破坏性较大。
1.5鉴别诊断 BCC临床表现多样化,需要与以下疾病鉴别:①脂溢性角化。脂溢性角化是一种良性疾病,病理上基底细胞呈乳头状增生,常见假角囊肿形成,细胞无异型性,但激惹型脂溢性角化部分细胞可见异型性。②鳞状细胞癌。鳞状细胞肿瘤团块不规则增生,向真皮内浸润,核分裂象明显,癌巢周围无收缩间隙。高分化的鳞状细胞癌可见角珠、鳞状涡。③Bowen病。表皮角化过度伴角化不全,表皮增厚,全层细胞排列紊乱,极性消失,不典型细胞多见,个别角化不良细胞,基底完整。④毛母细胞瘤。起源于基底样细胞,与BCC形态学相似。毛母细胞瘤位于真皮及皮下组织内,不与表皮相连,边界清楚。肿瘤团块由实性毛母细胞团构成,分布均匀对称,部分可见毛球、毛乳头结构。两者免疫表型的表达程度不同,有资料报道,雄激素受体、趋化因子7、Ki-67在BCC中呈阳性、弱阳性或高表达,毛母细胞瘤中大部分为阴性或低表达。Bcl-2在BCC中广泛弥漫表达,毛母细胞瘤则弱阳性[15]。此外,CD10在毛母细胞瘤间质中呈强阳性,瘤细胞呈阴性,在BCC中的基底样细胞呈阳性,而无间质表达情况[16]。
2 BCC的治疗
BCC的治疗主要分为手术治疗、非手术治疗和联合治疗3种。根据BCC不同部位、肿瘤直径的大小、患者对美容的要求及浸润程度选择相应的治疗方案。
2.1手术治疗
2.1.1标准手术治疗 近年来一些新兴治疗技术发展迅速,但早期手术仍是BCC的首选治疗方法。手术治疗原则以原发病灶的安全切缘前提下的完全切除为目的。手术切缘范围未统一,欧洲指南上指出,BCC手术切除主要依据皮损直径的大小,BCC肿瘤直径<2 mm,切缘延长至4 mm,然而肿瘤的切缘还取决于肿瘤的类型,原发或复发及肿瘤的嗜神经性等[17]。王炜主编的《整形外科学》中提到的BCC直径4~10 mm安全手术切缘被国内公认,3 mm的切除率为100%,随访71个月无复发[18]。对于个别生长隐匿或免疫缺陷的患者,切除范围需10 mm以上。皮肤BCC恶性程度低于其他皮肤恶性肿瘤,转移率约0.1%[19],如有转移应给予手术治疗、相应骨组织切除术、淋巴结清扫术及植皮术。
2.1.2局部皮瓣转移修复 当肿瘤位于特殊部位如眼睑、鼻尖等,因局限,范围缩小,美观要求较高,此时可采用局部皮瓣转移修复术。其原则为由近及远,由简单到复杂。在治疗的同时,取得良好的美观度,根据创面的大小、深度、结合肿瘤外科、整形外科基本原理及手术医师个人对皮瓣操作娴熟程度选择合适的皮瓣。常见有V-Y推进皮瓣、A-T滑行推进皮瓣、“风筝”皮瓣、菱形皮瓣等。外科医师最常用菱形皮瓣,其较简单实用且能减少手术面积。特殊皮瓣如A-T皮瓣是一个双推进皮瓣,适用于局部头面部或某些特定的位置。额部皮瓣因其无张力、血供丰富的特点适用于鼻部或缺损直径较大的BCC[20]。当较大缺损或供区不能直接关闭的皮损时选择多瓣联合。游离皮瓣多用于皮肤薄(如耳廓)部位的中小缺损的修复。
2.1.3游离植皮术 皮损直径≥5 cm[21]或老年患者对美观要求不高时可选用游离植皮术。其优点是修复各种形状的创面,取材方便,一般选用耳后或侧颈部较隐蔽的部位,范围选择性足够大,利于手术的操作,但影响美观、局部易复发。头颅部位的大型皮损,方法包括联合多种皮瓣转移和游离植皮技术、人工真皮联合刃厚皮片移植的方法修复、吻合血管游离皮瓣技术,也有帽状腱膜下筋膜瓣加植皮成功 Ⅰ 期修复头皮大面积缺损伴颅骨外露的报道[22-23]。
2.1.4MMS MMS是一种皮肤外科技术和特殊治疗冷冻组织切片相结合的治疗方法。在显微镜下观察阳性的肿瘤边缘进行手术,逐步切除到安全切缘。这种方法根据创面的形状、大小、深度进行。值得提出的是,肿瘤生长并非圆形生长,MMS能选择性切除BCC,避免非选择性切除引起的不必要创伤。适用于大面积非圆形和有复发趋势的皮损,对BCC治愈率高达96%~99%[24],并基于临床不断操作,切缘略小于推荐范围(3 mm)时,可为直接缝合和选择推进皮瓣提供更多空间,此时愈合率较高[25]。即使手术扩大切除后进行病理检查也不能完全确定是否完整切除了肿瘤组织时可采用MMS。MMS可以较精细地确定肿瘤的边缘,避免了这种误差。MMS需要较高的设备需求,费时且费用高,但由于其治愈率较高,临床上逐渐应用推广,被认为是目前最理想、最科学、最可靠的手术方式。
2.2非手术治疗
2.2.1冷冻治疗 冷冻治疗的原理为温度下降到0 ℃以下,细胞内、外的组织液形成冰晶,冰晶数量大小达到一定程度,超过细胞承受能力,达到冰晶撑破细胞的效果以破坏肿瘤细胞。冷冻疗法还可以增强细胞免疫,抗原呈递细胞(如树突状细胞)将其呈递给T细胞产生效应,促进全身特异性细胞免疫[26]。在临床上适用于社区医院或医疗条件差的地区,同样适用于不适合手术、患者年龄较大及肿瘤直径<3 cm的患者。冷冻范围控制在超出肿瘤边缘1~2 mm,至少3个冻融周期。当皮损较深或范围较大时,可适当增加冷冻次数及范围。当皮损直径>3 cm或侵犯鼻软骨时,不适合选择此治疗方法[27]。
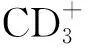
BCC对化疗药物不敏感。但少数药物如Vismodegib[29]、Odomzo[30]、伊曲康唑[31]通过影响Hh信号通路对控制BCC起关键性作用。新型靶向药物Hedgehog抑制剂Vismodegib可以缩小肿瘤大小,甚至完全消失,有报道指出,其适应证为眼睑BCC、高龄并具有多个并发症及不宜手术治疗的患者[32]。
2.2.35-盐酸氨酮戊酸光动力疗法 近年来5-盐酸氨酮戊酸光动力疗法广泛应用于临床,被视为局部无创或微创治疗皮肤恶性肿瘤的一种快速有效的方法。基本原理是将光敏剂带入人体,在一定时间后,用特定波长照射病变组织,激活内源性、外源性化学物质而产生光动力作用,并使肿瘤细胞发生不可逆损伤,以达到治疗目的。当光敏剂进入人体时,它对肿瘤细胞有很高的亲和力,肿瘤细胞中光敏剂的含量是正常组织的12倍,这使得5-盐酸氨酮戊酸光动力疗法对正常组织起到的作用较小,具有对病变组织进行选择性吸收,而对正常组织无杀伤作用的特点。不良反应有少量皮肤发红、烧灼感、刺痛,但不影响治疗效果。5-盐酸氨酮戊酸光动力疗法浸润深度仅为1.0 cm左右。因而对浅表型BCC可以完全缓解,适合老年患者。对于色素型预后相对较差,单独使用易复发[33]。当肿瘤为隆起性皮损时可采用钬激光联合光动力疗法。钬激光联合光动力疗法治疗BCC的优势在于钬激光将头面部BCC的逐层清理,再用光敏剂封包,这种处理后的残存肿瘤细胞能更好地吸收光敏剂,得到很好的消除[34]。
2.2.4其他治疗方法 ①激光治疗:常用为CO2激光及氦氖激光治疗,适用于早期、表浅、皮损小(直径<2 cm)分化良好的BCC[35]。优点是患者痛苦小、对美容影响较小、操作简单易行等特点。但有一定的局限性,范围不易掌握,易复发。②放射线疗法:放射性疗法可用于单独放射性治疗或外科手术的辅助治疗。BCC对放射性敏感度较高,常用有软X线、超软X线等。其中重离子加速器是利用碳离子束流进行照射的一种放射线疗法,它是未来放疗趋势的代表性技术,对于肿瘤的治疗有较好的应用前景,具有较常规放疗时间缩短的优势,适用于各年龄阶段的人群,不留瘢痕[36]。③基因治疗指向有功能缺陷的细胞导入具有相应功能的外源基因,以纠正或补偿其基因缺陷而达到治疗目的。BCC的发生与多基因突变有关,包括 H-ras、N-myc、nm-23、C-erb2、Ptch1、smo等。有相关报道指出,BCC的发展和转移与明胶酶、金属蛋白酶2表达呈正相关[37]。关于BCC的基因治疗已开展了大量实验研究,期待进一步的研究进展。
2.3联合治疗 BCC皮损多样化、局部破坏性强,且多位于曝光部位,严重影响患者的美观度及生活质量,因此制订联合治疗方案显得尤为重要。常用小范围外科手术联合光动力疗法,适用于BCC直径>3 cm特殊部位的皮损,效果明显。联合治疗除光动力联合咪喹莫特软膏、钬激光联合光动力治疗外,还包括外科手术联合咪喹莫特软膏、光动力联合高频电灼、外科手术联合药物或放射线治疗,5-盐酸氨酮戊酸光动力疗法、手术治疗及咪喹莫特软膏三联疗法等[38]。有报道指出手术联合光动力疗法治疗硬斑病样BCC不易复发,且美观度较好[39]。
3 展 望
BCC进展缓慢趋近于良性肿瘤,多数患者预后良好。BCC的预后主要取决于多种因素,如部位、大小、治疗是否及时或得当。由于BCC发病率高,多发生于曝光部位,早期不予重视会引起不可逆损容性损伤。为了避免紫外线照射,外出时可使用遮光剂。对长期接触化学致癌物质的人群应定期随访观察。同时加强BCC科普知识的宣教,提高人群对BCC的认识,严格监测、防晒、皮肤镜检查等无创初筛手段以做到早预防、早诊断、早治疗。
