活血消瘿方标准汤剂质量评价研究*
2019-01-18叶利春肖静霞郑国华石召华王桂红
叶利春,肖静霞,柳 畅,郑国华,石召华,王桂红**
(1. 湖北中医药大学药学院 武汉 430065;2. 武汉爱民制药股份有限公司 鄂州 436070;3. 湖北李时珍药物研究院 鄂州 436070)
结节性甲状腺肿(简称结甲)是临床最为常见的甲状腺疾病的一种,西医针对结甲的治疗方法有手术、甲状腺激素抑制等,手术治疗存在意外如损伤喉部神经而导致音哑等风险和并发症,且术后复发率较高,临床上针对治疗结甲的药物多为化学激素类,该类药物副作用大,且容易复发[1-4]。节甲从中医学角度为“瘿病”[5,6],主要病机是气滞痰凝血瘀,而引起的患者颈部肿大,肿块坚韧疼痛,口黏多痰等症,其形成缓慢且时间较久。故主要以活血消瘿,兼疏肝理气、清热解毒为治疗方法[7],活血消瘿方为湖北省名老中医陈如泉教授多年研究治疗结甲临床经验方,方中由柴胡、王不留行、桃仁、莪术、蜣螂虫、土鳖虫、蜈蚣、猫爪草8 味入药,具有活血化瘀、软坚化痰、散结消肿的功效[8,9]。已作为医院制剂活血消瘿片在临床上使用近20 年,疗效显著,深受广大结甲患者欢迎。现有医院制剂活血消瘿片将柴胡、王不留行、桃仁、莪术、蜣螂虫、猫爪草6 味药按《医疗机构中药煎药室管理规范》煎煮,将土鳖虫和蜈蚣两味药打粉过筛后压片包衣成药。拟对医院制剂活血消瘿片进行新药开发实现商业化生产,保证其质量疗效一致情况下,降低患者用药成本,作为治疗结甲专用药广泛推广临床使用。
中药复方是多味药组方而成,其关键难点在于复杂的化学物质基础研究及过程质量控制,目前大部分的中药质量控制仅依靠终端标准检验或个别化学成分控制,存在很大的局限性,2016 年国家药品监督管理部门发布了《中药配方颗粒质量控制与标准制定技术要求(征求意见稿)》和2017 年发布的《中药经典名方复方制剂简化注册审批管理规定(征求意见稿)》中提出了“标准汤剂”的概念,即标准汤剂是在中医药理论指导下,按照临床汤剂煎煮流程的规范化操作,固液分离,经适当浓缩的方法干燥制得;以古代医籍中记载的经典名方制备方法为依据制备的浓缩浸膏或冻干品[10]。而这两个概念表述的质量控制理念相似,均表示在传统中药大生产过程中,标准汤剂是作为参照物的作用。日本汉方药多来源于中国古代经典名方,其中对内服制剂提出了标准汤剂的概念,要求制定标准汤剂化学与生物学的基准。对于中间体及成品应提供化学、生物学上与标准汤剂具有统一性的研究资料,确保化学成分及药效作用与标准汤剂具有一致性[11]。针对标准汤剂中“标准”研究,主要是将中药材的产地、基源、提取工艺的统一性及质控等建立标准。本研究遵循“原处方、原工艺,原用法”[12,13],通过对标准汤剂的指标成分含量测定、指纹图谱研究[14-17],建立活血消瘿片商业化生产的中药材、制备工艺、规格等的标准体系,旨在建立评价工业化生产的工艺和质量控制可控、有效的质量体系,保证其与传统的医院制剂的一致性,保证其疗效。
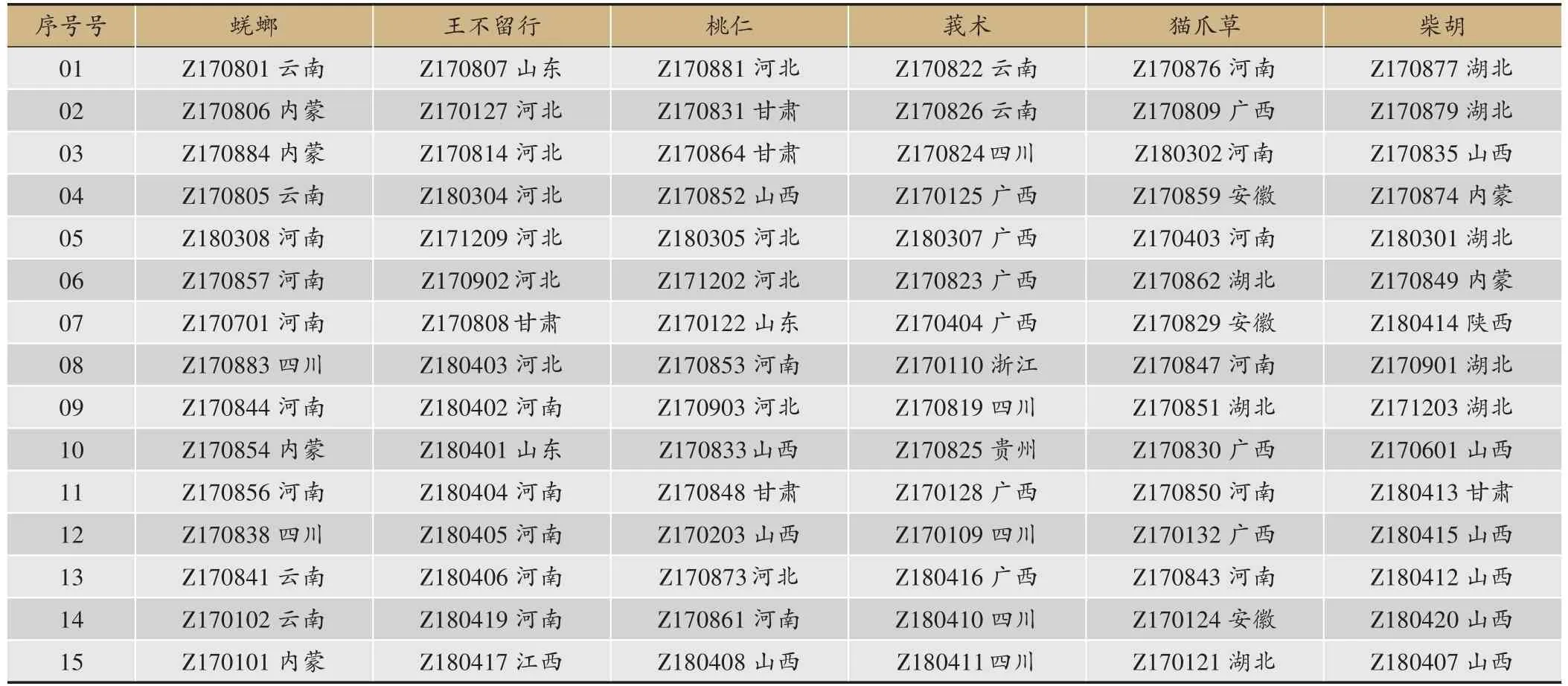
表1 15批样品中各味药材来源及批号
1 材料
1.1 仪器
沃特世e2695 型高效液相色谱仪(美国沃特世公司,2489型紫外检测器);安捷伦1260Infinity 型高效液相色谱仪(美国安捷伦公司,G1329B 型自动进样系统,G1316A 型柱温箱,G4212B 型DAD 检测器),色谱柱:Waters XSelect ® HSS T3(4.6×250 mm,5 μm);XSE 205 型电子分析天平(METTLER TOLEDO);HHZK 6 型恒温水浴锅(巩义市予华仪器有限责任公司);TD 5A-WS 型台式低速离心机(上海维尔康湘鹰离心机);KQ-500B 型超声波清洗器(昆山市超声仪器有限公司)。
1.2 材料
苦杏仁苷对照品(含量以90.7%计,批号110820-201607,购自中国药品生物制品检定院)、王不留行黄酮苷对照品(含量以92.6%计,批号111853-201303,购自中国食品药品检定研究院)去甲氧基姜黄素对照品(批号112003-201501,购自中国食品药品检定研究院)、双去甲氧基姜黄素对照品(批号112004-201501,购自中国食品药品检定研究院)、柴胡皂苷B1 对照品(批号18042831,购自同田生物)、柴胡皂苷B2 对照品(批号18042531,购自同田生物)、刺桐碱(18042532,同田生物)、吉马酮(批号MUST-15051913,成都曼思特生物科技有限公司)甲醇、乙腈为色谱纯(TEDIA 公司),实验室自制超纯水,其他试剂为分析纯。活血消瘿颗粒是由武汉爱民制药股份有限公司研发中试验证车间生产所得(批号分别为H170527、H170528、H170530)。
蜣螂、王不留行、桃仁、莪术、猫爪草、柴胡6 味药材分别采自主产区、道地产区及GAP 基地,湖北、河南、河北、甘肃等地,包括符合《中国药典》要求的不同商品规格等级。药材来源及批号见表1。经湖北中医药大学陈科力教授鉴定,研究样品分别为金龟子科昆虫屎壳螂Catharsiusmolossus Linnaeus的干燥体(蜣螂)、石竹科植物麦蓝菜Vaccaria segetalis(Neck.)Garcke 的干燥成熟种子(炒王不留行)、蔷薇科植物桃Prunus persica(L.)Batsch的干燥成熟种子(燀桃仁)、姜科植物广西莪术Curcuma kwangsiensisS.G.Lee et C.F.Liang 的干燥根茎(莪术)、毛茛科植物小毛茛Ranunculus ternatusThunb.的干燥块根(猫爪草)、伞形科植物柴胡Bupleurum chinenseDC.的干燥根(柴胡)。
1.3 标准汤剂的制备
按活血消瘿方处方分别称取各味药材共15批,每个处方量药材850 g,分别加8 倍量水浸泡30 min,加热煎煮30 min,100 目滤布过滤,药渣再加6 倍量水加热煎煮30 min,100 目滤布,合并滤液,滤液采用4 000 r·min-1离心5 min,取上清液,低温浓缩至约1 000 mL,置1 000 mL 容量瓶中,加水定容至刻度,得标准汤剂。取本品摇匀,精密量取6 mL,加24 mL 甲醇溶解,置4 000 r·min-1离心5 min,取上清液置蒸发皿中,水浴蒸至约2 mL,转移至5 mL 容量瓶中,加甲醇定容至刻度,0.45 μm 滤膜过滤,取续滤液,即得标准汤剂供试品溶液(编号HXXYP-01-HXXYP-15)
1.4 饮片供试品溶液的制备
1.4.1 桃仁
精密称取本品粗粉约0.3 g置具塞锥形瓶中,加石油醚(60-90℃)50 mL,加热回流1 h,冷却至室温,滤过,弃去石油醚液,药渣及滤纸挥干溶剂,放入原锥形瓶中,加入70%甲醇50 mL,精密量取,称定重量,加热回流1 h,冷却至室温后称定重量,用70%甲醇补足减失的重量,摇匀,滤过。精密量取续滤液5 mL,置10 mL量瓶中,加70%甲醇至刻度,摇匀,即得。
1.4.2 王不留行
精密称取本品粉末(过三号筛)约1.2 g 置具塞锥形瓶中,精密加入70%甲醇50 mL,称定重量,超声处理30 min,冷却至室温后称定重量,用70%甲醇补足减失的重量,摇匀,滤过,取续滤液,即得。
1.5 浸膏供试品溶液的制备
称取活血消瘿浸膏适量,精密称定,置50 mL容量瓶中,加25%甲醇水溶液,称定重量,超声20 min(功率300 W,频率为40 kHz),放冷至室温,再称定重量,用25%甲醇溶液补足减失重量。置4 000 r·min-1离心5 min,取上清液置蒸发皿中,水浴蒸至约2 mL,转移至5 mL容量瓶中,加甲醇定容至刻度,0.45 μm滤膜过滤,取续滤液,即得。
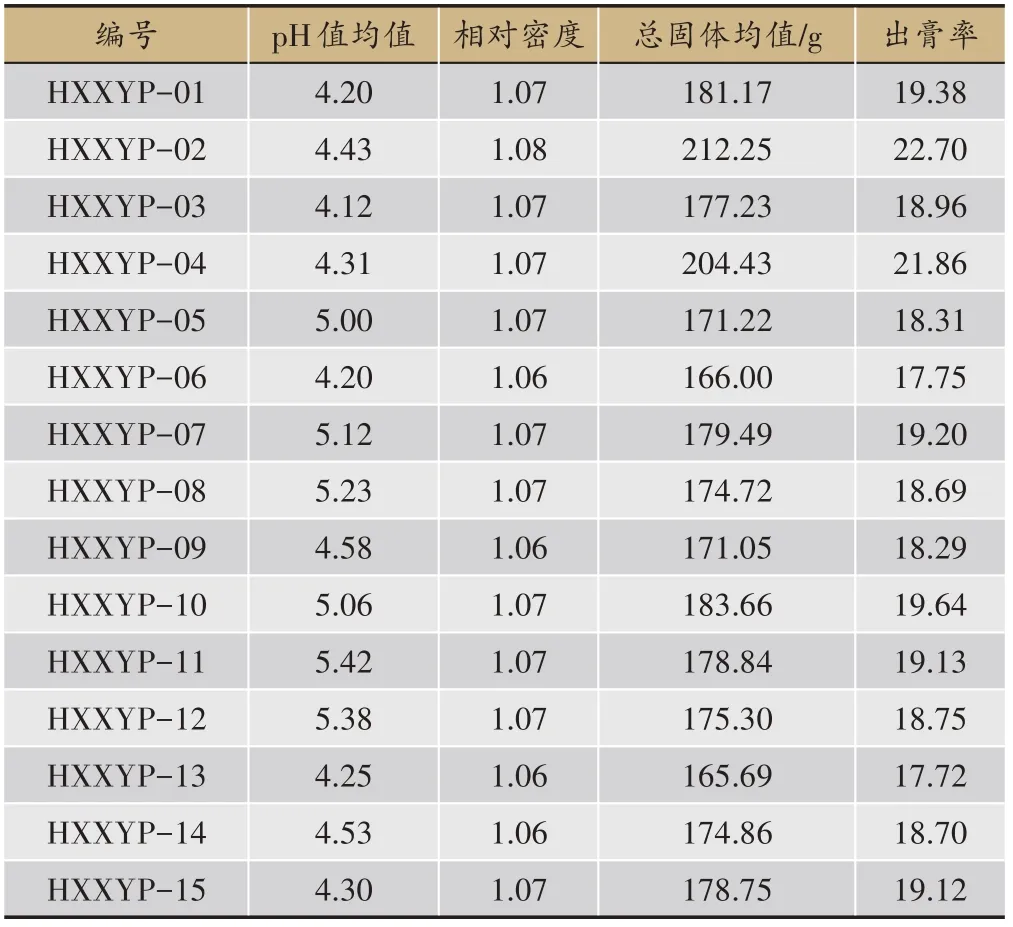
表2 15标准汤剂各检查项结果

表3 含量测定梯度洗脱条件
2 方法及结果
2.1 pH及相对密度的测定
分别取混合均匀的HXXYP01-HXXYP15 标准汤剂30-50 mL,用pH 计测定pH 值,15 批的标准汤剂pH值在4.12-5.42 内。用比重瓶法测定相对密度,15 批次的标准汤剂相对密度应为1.06-1.08(表2)。
2.2 总固体及出膏率测定
分别精密吸取混合均匀的HXXYP01-HXXYP15标准汤剂50 mL,置已干燥至恒重的蒸发皿中,在105℃干燥3 h,蒸干溶剂后移至干燥器中,冷却30 min,迅速称定重量,即得。15 批次的标准汤剂总固体为165.69-212.25,出膏率为17.72-22.70。总固体结果及出膏率结果见表2。3 批中试验证生产的活血消瘿方提取液的pH 分别为4.57、4.63、4.60,相对密度分别为1.07、1.06、1.07,总 固 体 为185.79g、186.23g、185.81g,出膏率为19.84%、19.95%、19.79%。结果表明活血消瘿方生产工艺稳定,工艺研究放大可重复性良好。
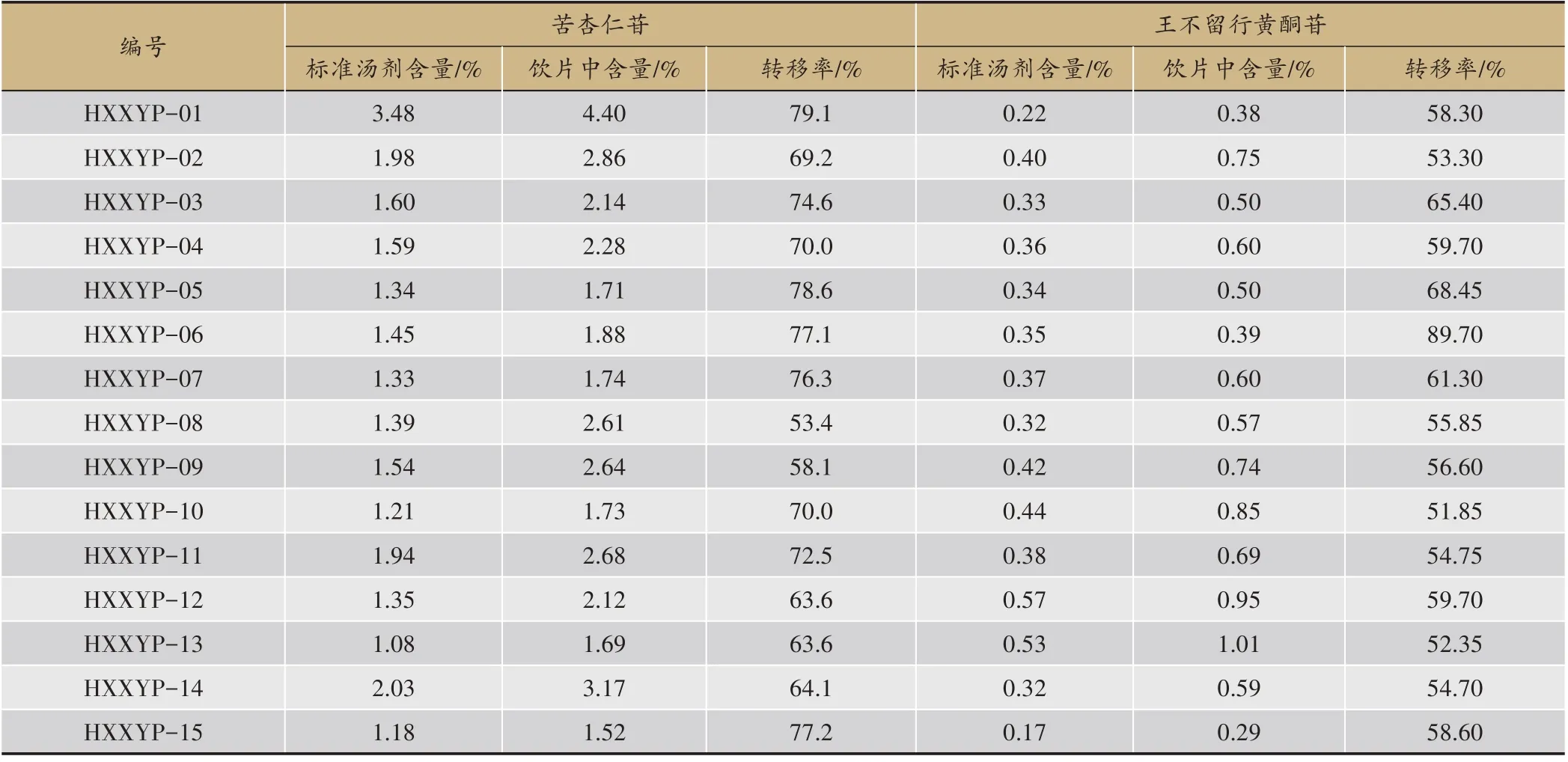
表4 2种成分的含量及转移率结果
2.3 样品含量测定
2.3.1 色谱条件
色谱柱为Waters XSelect®HSS T3(4.6×250 mm,5 μm);以甲醇为流动相A,以0.3%磷酸溶液为流动相B,按表3 的规定进行梯度洗脱;检测波长为210 nm;柱温为30℃;进样量为10 μL;流速为1 mL·min-1。理论塔板数按苦杏仁苷峰及王不留行黄酮苷峰计算均应不低于3 000。
2.3.2 饮片对照品溶液的制备
分别取苦杏仁苷、王不留行黄酮苷对照品适量,精密称定,分别置于10 mL容量瓶中,加70%甲醇制成每1 mL 含苦杏仁苷80 μg、含王不留行黄酮苷0.1 mg的溶液,即得。
2.3.3 标准汤剂对照品溶液的制备
取苦杏仁苷、王不留行黄酮苷对照品适量,精密称定,置于10 mL 容量瓶中,加甲醇制成每1 mL 含苦杏仁苷2.59 mg、王不留行黄酮苷0.65 mg 的溶液,即得。
2.3.4 线性关系考察
精密量取“2.3.2 项下”对照品溶液,配制成6 个梯度的质量浓度注入液相色谱系统,测定色谱峰面积。分别以苦杏仁苷和王不留行黄酮苷峰面积积分值为纵坐标(Y),以对照品浓度(mg·mL-1)为横坐标(X),绘制标准曲线,苦杏仁苷及王不留行黄酮苷的线性回归方程分别为Y=9 844 472X+709 345,Y=12 679 639X-124 246,相关系数分别为0.999 6,0.994,线性范围分别为0.129-2.59 mg·mL-1,0.032 5-0.65 mg·mL-1,表明在各自的浓度范围内,线性关系良好。
2.3.5 精密度试验
精密量取“2.3.2项下”对照品溶液,连续进样6针,按“2.3.1”项下条件进行测定,计算苦杏仁苷和王不留行黄酮苷色谱峰面积RSD 分别为0.68%、0.75%,保留时间RSD 分别为0.55%、0.62%,表明该仪器精密度良好。
2.3.6 重复性试验
取相同批号样品(批号为HXXYP-15),按照“1.3”项下方法分别处理6份,按“2.3.1”项下色谱条件测定,测得苦杏仁苷和王不留行黄酮苷含量分别为1.77 mg·mL-1、0.26 mg·mL-1,RSD 分别为0.78%、0.95%,表明该方法的重复性良好。
2.3.7 稳定性试验
取“1.3”项下的样品(批号为HXXYP-15),室温放置,分别于0、2、4、8、16、24 h 取样,按“2.3.1”项色谱条件测定,进样量为10 μL,测得苦杏仁苷和王不留行黄酮苷含量的RSD 分别为1.02%、0.97%,表明供试品溶液室温放置24 h内稳定。
2.3.8 回收率
精密称取已知含量的样品(批号为HXXYP-15),按照2.2.1 项下方法制备,分别加入80%、100%、120%定量的苦杏仁苷和王不留行黄酮苷对照品溶液,测定3 次,测得苦杏仁苷和王不留行黄酮苷加样回收率分别为98.3%和99.9%,RSD分别为1.5%和1.2%。
2.3.9 含量测定
取对照品溶液和供试品溶液各10 μL,精密量取,注入高效液相色谱仪,按照“2.3.1”条件检测,15 批的检验结果见表4,得到苦杏仁苷和王不留行黄酮苷含量范围在1.08%-3.48%,0.17%-0.57%,转移率范围分别是53.4%-79.1%,51.85%-89.70%。3 批中试验证生产的活血消瘿方浸膏的苦杏仁苷和王不留行的黄酮苷的含量及转移率在以上标准汤剂的范围内。
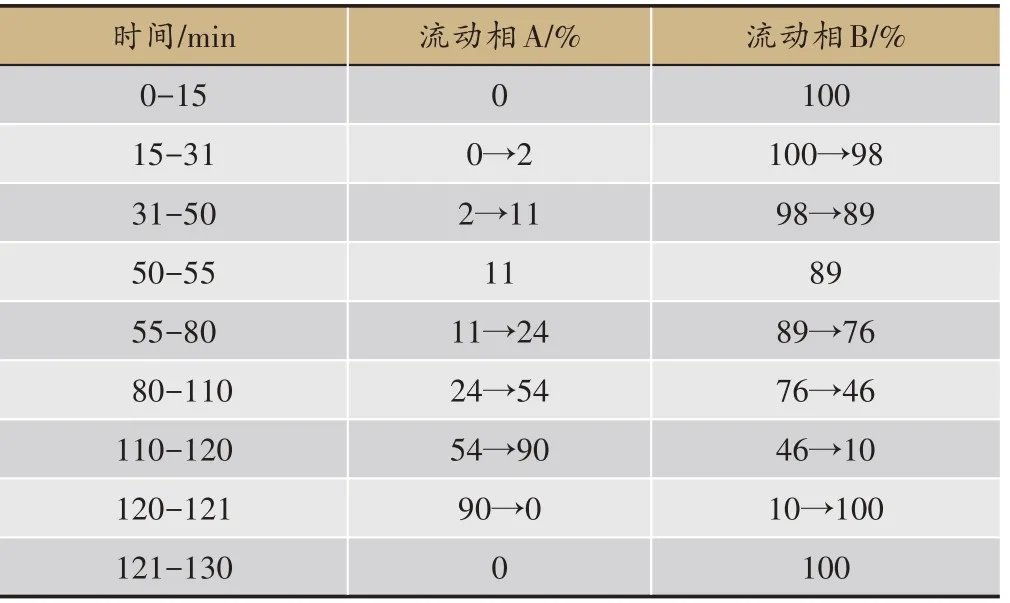
表5 指纹图谱梯度洗脱条件
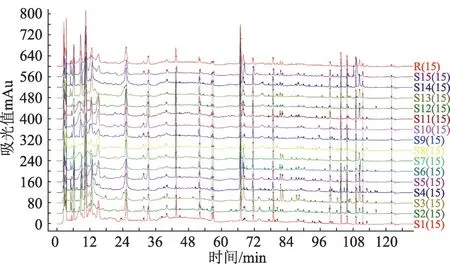
图1 15批次标准汤剂指纹图谱
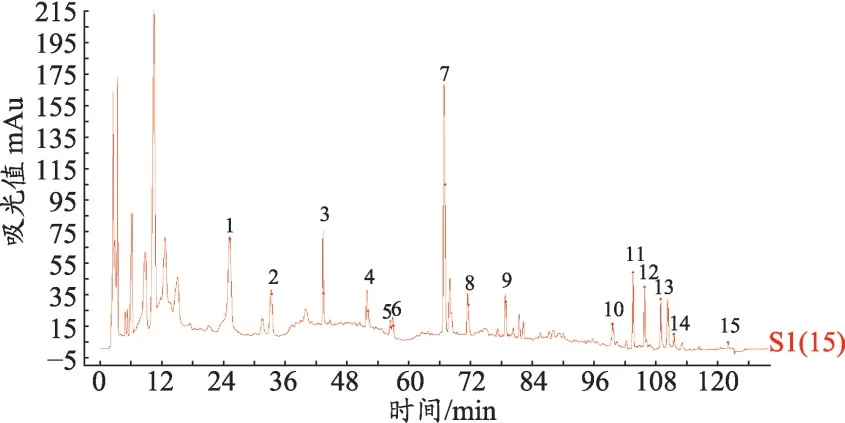
图2 对照特征图谱及共有峰的确认
2.4 指纹图谱研究
2.4.1 色谱条件
色谱柱为Waters XSelect®HSS T3(4.6×250 mm,5 μm);以乙腈为流动相A,以纯水为流动相B,按表5的规定进行梯度洗脱;检测波长为250 nm;柱温为30℃;进样量为10 μL;流速为1 mL·min-1。理论塔板数按苦杏仁苷峰及王不留行黄酮苷峰计算均应不低于3 000。
2.4.2 标准汤剂定位对照品溶液制备
取刺桐碱、苦杏仁苷、王不留行黄酮苷、柴胡皂苷B1、柴胡皂苷B2、双去甲氧基姜黄素、去甲氧基姜黄素、吉马酮对照品适量,精密称定,分别加甲醇制成每1 mL含取刺桐碱0.22 mg、苦杏仁苷2.51 mg、王不留行黄酮苷0.60 mg、柴胡皂苷B10.56 mg、柴胡皂苷B20.26 mg、双去甲氧基姜黄素0.29 mg、去甲氧基姜黄素0.15 mg、吉马酮1.27 mg的溶液,即得。
2.4.3 精密度考察
取HXXYP-15 标准汤剂,按供试品方法制样,连续进样6次,按“2.4.1”项色谱条件进行测定,计算各特征色谱峰的相对峰面积和相对保留时间的RSD 值,结果分别为0.16%-2.07%、0.04%-0.28%,表明该仪器精密度良好(以7号峰王不留行黄酮苷为参比峰)。
2.4.4 稳定性考察
取HXXYP-15 标准汤剂,按供试品方法制样,按“2.4.1”项色谱条件测定,分别在0 h、2 h、4 h、8 h、16 h、24 h 内检测,计算各特征色谱峰的相对峰面积和相对保留时间的RSD 值,结果分别为0.32%-2.98%、0.04%-0.21%,表明室温放置24 h,供试品溶液稳定性良好(以7号峰王不留行黄酮苷为参比峰)。
2.4.5 重复性考察
取HXXYP-15 标准汤剂6 份,按供试品的制备方法制,按“2.4.1”项下色谱条件测定,计算各特征色谱峰的相对峰面积和相对保留时间的RSD 值,结果分别为0.39%-2.54%、0.05%-0.25%,表明该方法的重复性良好(以7号峰王不留行黄酮苷为参比峰)。
2.4.6 特征图谱的建立及共有峰的标定
按2.4.1 下色谱条件,分别吸取15 批标准汤剂供试品溶液各10 μL,精密量取,注入高效液相色谱仪,15 批次的标准汤剂的特征图谱见图1,其中R 为生成的对照图谱,生成的对照特征图谱见图2,其中共有峰15个,指认出8个色谱峰。以峰7为参照峰,统计共有峰峰面积及保留时间,计算其他共有色谱峰的相对峰面积和相对保留时间(表6)。

表6 各共有峰的相对保留时间与相对峰面积结果
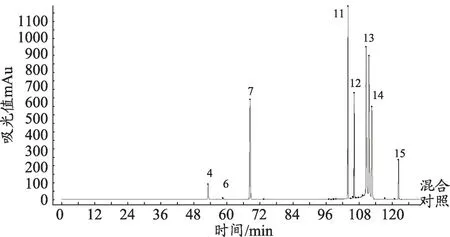
图3 混合对照品溶液色谱图
2.4.7 相似度评价
用《中药色谱指纹图谱相似度评价系统》(2012 年版本),对15批次的标准汤剂的实验结果进行评价,根据软件匹配确定15 个共有峰,因7 号峰(王不留行黄酮苷)的分离度良好,峰面积所占总峰面积比例适中,故选用其作为参考峰。15 批次活血消瘿方标准汤剂的指纹图谱相似度计算结果见表7,15 批标准汤剂中各批次的指纹图谱与生成对照指纹图谱的相似度分别 为0.968、0.930、0.965、0.960、0.967、0.968、0.948、0.983、0.978、0.969、0.969、0.951、0.975、0.904、0.998,均大于0.90。将三批中试验证生产的活血消瘿方浸膏与标准汤剂的对照指纹图谱的相似度分别为0.992、0.994、0.994,均大于0.9,表明工业化生产样品与传统方法重复性良好。
3 讨论
3.1 研究批次及药材来源选择
中药材多来源于动植物,种质资源、土壤、气候、栽培和加工技术等因素均会对其质量影响[18-19],不同的药材产地、采收期、产地加工等因素都有可能产生质量风险[20-22],为降低药材产生的影响,应考虑不少于3个产地的不少于15批次药材的质量属性进行分析研究,本研究中各味药材分别采用全国5 个产区的药材共15 批次研究,结果表明,以桃仁及王不留行药材到标准汤剂中指标成分含量可看出,不同产地的桃仁及王不留行指标成分的差异较大,且药材的指标成分含量高,相应的标准汤剂中的成分较高,后续产业化过程中,应当选择各味药材指标成分较高的产区,选用上好的药材,保证其成品药的质量。
3.2 煎煮参数的选择
中药标准汤剂的制备工艺包括煎煮、固液分离、浓缩、干燥步骤等。对于保证中药的化学成分起着关键作用[23]。在煎煮药材,选用口径较小陶瓷材质煎药器具,较好的保留挥发性成分及水分,可提高效率以及保证药物疗效。不同的药物质地和药性不同,加水量和煎煮时间也会对其产生较大影响,部分药物的化学成分会随着煎煮时间的延长而破坏[24],易挥发的物质会挥发而损失[25],药效也会影响,故本研究参照《医疗机构中药煎药室管理规范》中对中药煎煮的要求,选择第1 次煎煮加8 倍量水浸泡30 min,加热煎煮30 min,第2次煎煮加6倍量水加热煎煮30 min。
3.3 活血消瘿方标准汤剂的应用
本研究通过对15 批活血消瘿方标准汤剂的研究,计算其pH 范围4.12-5.42,密度为1.06-1.08,出膏率范围在17.22%-22.70%,采用HPLC 法测定的标准汤剂的苦杏仁苷和王不留行黄酮苷含量范围在1.08%-3.48%,0.17%-0.57%,转移率分别在53.4%-79.1%,51.85%-89.70%。又采用HPLC 法建立了活血消瘿方标准汤剂的特征图谱,系统整体地反映标准汤剂中的各组分情况。通过对活血效应方的标准汤剂的研究,构建活血消瘿方产业化过程中中间体的质量控制体系,充分体现了质量源于设计的理念,该研究结果可为活血消瘿方的工业化生产中间体质量标准和过程质量控制提供科学的数据支撑。
