石墨烯负载花球状二氧化锰复合材料制备及其电容性能研究
2019-01-16燕绍九南文争彭思侃戴圣龙
陈 翔,燕绍九,南文争,王 楠,彭思侃,王 晨,戴圣龙
(中国航发北京航空材料研究院 石墨烯及应用研究中心,北京 100095)
电化学超级电容器因其超长使用寿命、支持快速充放电和相对传统电容器较高的储能密度等特性,在新能源储能领域有着巨大的应用潜力。二氧化锰由于来源广泛、价格低廉、环境友好、理论电容性能优异等诸多优点[1],已被视为超级电容器的理想电极材料,并受到广泛关注。
二氧化锰在结构上是由锰氧八面体通过共角或者共棱的方式连接构成的[2]。作为一类典型的变价过渡金属氧化物,锰的化合价通常在三价/四价之间相互转化,加上晶体中往往存在各种缺陷,催生了二氧化锰晶型和形貌的多样性[3],目前已经有大量文献报道了二氧化锰的晶型控制、形貌调控以及电容性能测试等相关的研究工作。Devaraj等[4]和Brousse等[5]系统地研究了二氧化锰晶型对其比电容的影响,发现比电容按照α≈δ>γ>λ>β的顺序逐次递减。基于Turner等[6]对二氧化锰隧道结构的研究,目前普遍认为α和δ相之所以电容性能更加优异,是因为其内部存在较大尺寸的隧道结构,有助于电解液阳离子在其间快速嵌入/脱出。此外,二氧化锰的微观形貌会影响电解液离子向电极表面迁移和同时也会影响材料表面氧化还原反应活性位点的数量,从而对电容性能产生显著的影响。选择合适的制备工艺,并调整二氧化锰的合成工艺参数就能够实现对其微观形貌的适度调控。Ragupathy等[7]在室温下采用乙二醇还原高锰酸钾得到纳米δ-MnO2颗粒,材料的比表面积可达230m2·g-1,比容量可达250F·g-1。Xu等[8]通过水热法合成了空心海胆结构的α-MnO2,材料比表面积可调,在5mV·s-1扫速下比电容可达147F·g-1。Subramanian等[9]通过调整水热工艺合成了一种片状形态的MnO2纳米柱,在中性电解液中比电容可达168F·g-1。Yu等[10]采用微波乳化工艺,利用油酸还原高锰酸钾得到了一维结构的δ-MnO2,在0.2mA·cm-2电流下测得材料比电容可达277F·g-1。然而纯二氧化锰材料倍率性能普遍较差,无法匹配超级电容器快速充放电(10-1~102s)的实际使用环境。MnO2的电导率非常低,仅有10-6~10-3S·cm-1[11],从而导致MnO2的电容性能在高速充放电条件下急剧衰减。此外,低的活性材料电导率还会引起等效串联电阻过高,导致电容器功率密度不足。
针对MnO2电导率低的问题,最常用的解决办法就是通过引入纳米导电材料与MnO2形成复合材料。常见的纳米导电材料主要为碳材料,包括:碳纳米管、碳气凝胶、有序介孔碳和石墨烯等。通过化学共沉积、热分解、电沉积、原位合成等工艺能够成功实现MnO2在碳材料表面负载或者包覆。Ren等[12]利用化学共沉积法在生物质碳气凝胶上包覆MnO2,通过优化工艺最终实现123.5F·g-1的比电容。He等[13]在三维柔性石墨烯上电沉积MnO2,负载量高达9.8mg·cm-2,MnO2占整个电极比重高达92.9%。在2mV·s-1扫速下,面积比电容高达1.42F·cm-2,通过优化MnO2的负载量能够实现最大质量比电容为130F·g-1。Li等[14]通过化学还原法在碳纳米管表面包覆一层约50nm厚的MnO2,得到的复合材料在1A·g-1电流密度下比容量可达201F·g-1,20A·g-1下电容保持率可达70%,具有较好的倍率性能和循环性能。对于一些MnO2负载量较低的复合材料,基于MnO2含量的比电容甚至可以高达1061F·g-1[15],接近MnO2的理论比电容。研究表明MnO2与导电碳材料形成的复合材料往往具有丰富的孔结构和良好的导电性,有助于MnO2与电解液的充分接触,同时能够促进可逆电容反应过程中电荷的转移,因此在倍率性能和循环性能上通常会有较大的改善。
石墨烯具有优异的导电性能和丰富的比表面积,是一种优异的MnO2载体材料。石墨烯本身容易相互堆叠甚至团聚,同时表现为憎水性,难以在水系溶液中分散。大部分石墨烯/MnO2复合材料都是以氧化石墨烯/MnO2为前驱体,通过还原处理得到。氧化石墨烯分子结构中存在大量的羟基、羧基和环氧基等亲水基团,使其表现出良好的亲水性,极易在水中分散。然而含氧官能团的引入会破坏石墨烯的(键结构,使得氧化石墨烯表现为电子绝缘性,即使后期经过还原处理仍然难以完全修复。为了充分发挥石墨烯的导电性能,在石墨烯上直接负载/包覆MnO2才是石墨烯/MnO2复合材料未来发展的重要方向,目前直接在石墨烯上负载MnO2并获得优异性能的文献报道还比较少。
本工作采用化学气相沉积多孔石墨烯为原料,通过表面吸附乙醇改善其在水溶液中的润湿性,随后利用高锰酸钾溶液与乙醇之间的氧化还原反应,在多孔石墨烯表面原位合成MnO2纳米花球,得到石墨烯/MnO2复合材料。该方法工艺简单、条件温和,得到的复合材料具有优异电化学性能。多孔石墨烯与MnO2纳米花球复合(质量比1∶1),能够显著改善纳米二氧化锰花球的倍率性能和循环性能,同时基于MnO2质量的比容量提高了近一倍,高达590F·g-1(2mV·s-1扫描速率下)。
1 实验材料与方法
1.1 石墨烯/MnO2复合材料的合成
石墨烯/MnO2复合材料是通过高锰酸钾与无水乙醇的氧化还原反应,在多孔石墨烯表面沉积负载纳米MnO2花球而得到。多孔石墨烯由北京北方国能科技有限公司提供,其余试剂均由北京国药集团提供,纯度为99.5%。制备过程如下:首先称取1g高锰酸钾粉末溶于500mL去离子水中,滴加1mL冰乙酸调节pH值为3,得到酸性高锰酸钾紫色溶液。称取0.55g多孔石墨烯并逐滴加入1mL乙醇溶液,用玻璃棒搅拌石墨烯使其充分吸附乙醇,随后加入500mL去离子水并置于超声池中处理30min(37kHz,200W)。在持续磁力搅拌作用下(800r/min)加入酸性高锰酸钾溶液充分反应6h,然后通过抽滤将固体沉淀物滤出。先后用去离子水和乙醇将固体沉淀物反复清洗、抽滤,得到的产物置于80℃恒温箱中干燥12h,得到黑色石墨烯/MnO2复合材料粉体。对照组纳米MnO2花球也是采用相同的反应条件并通过类似处理过程得到,区别在于制备过程中不添加多孔石墨烯。
1.2 材料表征
X射线衍射仪的型号为D8 advance,采用铜靶Kα射线,波长为0.15406nm。扫描电镜的型号为NanoSEM 450,工作电压20kV。比表面积测试仪型号为Kubo-X1000,吸附气体为氮气。Raman光谱分析仪的型号为LabRAM HR800,测试温度为室温。热重分析仪的型号为STA 449 F1,测试气氛为空气。
1.3 电化学性能表征
工作电极由电极材料、导电炭黑(SP)、羟甲基纤维素钠(CMC)和丁苯橡胶(SBR)按照7∶2∶0.5∶1的质量比组成。将电极浆料滴于抛光后的玻碳电极表面并干燥,得到工作电极。将工作电极、Ag/AgCl参比电极与铂丝电极组成三电极系统,浸入0.5mol/L K2SO4电解液中形成开放的电化学池进行CV循环性能测试。
2 结果与分析
2.1 微观形貌观察
图1为多孔石墨烯、纳米MnO2花球和石墨烯负载花球状二氧化锰复合材料的微观形貌。多孔石墨烯微观上表现为不规则多孔聚集体颗粒形态,是由片状石墨烯堆积而成。在不添加多孔石墨烯的情况下,酸性高锰酸钾与乙醇反应形成纳米MnO2花球(如图1(b)所示)。纳米花球尺寸分布较宽,最大在700nm左右,最小在200nm上下,纳米MnO2花球的次级结构为MnO2纳米片。在添加多孔石墨烯的情况下,酸性高锰酸钾与乙醇反应生成的纳米MnO2花球均匀地负载于多孔石墨烯表面。形成的纳米花球尺寸较一致,直径约为400nm。从微观形貌上不难看出,多孔石墨烯的加入显然有助于得到尺寸一致的纳米MnO2花球,而且有利于细化纳米花球,同时纳米MnO2花球在石墨烯表面负载有助于改善MnO2的电子传导,这些对于纳米花球电化学性能的发挥都有着积极的作用。可以认为一方面基于乙醇对多孔石墨烯良好的亲和性,在石墨烯表面处会发生乙醇分子的偏聚,加上石墨烯中sp2杂化碳原子形成的大π键能够提供电子对,可造成缺电子的H+质子在石墨烯表面富集[16]。由于多孔石墨烯表面处高锰酸钾的反应活性更强且反应物乙醇的浓度更高,因此纳米MnO2花球将按照反应方程(1)优先在多孔石墨烯表面处发生形核与生长。

图1 多孔石墨烯(a)、纳米MnO2花球(b)和石墨烯负载花球状二氧化锰复合材料(c),(d)的微观形貌Fig.1 Morphology of porous graphene(a), globular MnO2 nanoflowers(b)and MnO2 flowers anchoredgraphene composites (c), (d)
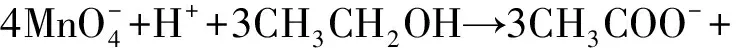
(1)
另一方面,多孔石墨烯的存在为MnO2花球的形核与生长提供丰富的异质形核中心,能够有效降低MnO2花球形核和生长能垒,有助于纳米MnO2花球在多孔石墨烯表面均匀形核与生长,因此得到的纳米MnO2花球尺寸更一致。
2.2 组织结构表征
图2为多孔石墨烯、纳米MnO2花球以及石墨烯负载花球MnO2复合材料的XRD图谱、Raman图谱和热重曲线。多孔石墨烯、纳米MnO2花球以及纳米MnO2花球负载石墨烯复合材料的XRD图谱呈现纳米材料常有的宽化峰型,根据峰型的宽化程度可以推测对应纳米晶畴的尺寸。多孔石墨烯XRD图谱上出现的峰位与层状石墨的(002),(011) 峰位一致,具有层状石墨相似的密排六方晶体结构,而通过(002)峰半峰宽可以估算出石墨烯的层数大概在4层,属于少层石墨烯范畴[17]。纳米MnO2花球的衍射峰位与K-birnessite[18]的(001),(002),(110),(020)晶面的位置相符,晶体结构属于C心单斜晶系。石墨烯/MnO2复合电极材料既出现了纳米MnO2花球的特征峰,同时在20o~30o之间出现类似石墨烯中的宽峰。该位置的峰由纳米MnO2花球的(020)晶面与多孔石墨烯的(020)晶面衍射共同叠加形成。进一步分析确认了石墨烯上负载的MnO2与未添加石墨烯时生成的纳米MnO2花球属于同样的晶体结构。

图2 多孔石墨烯、纳米MnO2花球以及石墨烯负载花球MnO2复合材料的XRD图谱(a)、Raman图谱(b)和热重曲线(c)Fig.2 XRD patterns(a), Raman spectra(b) and TG curves (c) of porous graphene, globular MnO2 nanoflowers and MnO2 flowers anchored graphene composites
多孔石墨烯的拉曼图谱呈现少层石墨烯特征峰:1338cm-1D峰、1588cm-1G峰及2664cm-12D峰。其中D峰由sp2杂化碳原子混排(或缺陷)引起,G峰代表sp2杂化碳原子的伸缩振动,2D峰则是所有sp2杂化碳原子的二阶拉曼峰的叠加[19-20]。根据D峰强度较高的特征,可推断多孔石墨烯中碳原子六边形结构存在一定的混乱度[21]。纳米MnO2花球则分别在566cm-1和651cm-1处出现拉曼峰,它们分别代表层状氧化锰的层间伸缩振动ν3(Mn-O)和锰氧八面体的对称伸缩振动ν2(Mn-O)[22-23]。石墨烯/MnO2复合材料出现了石墨烯和二氧化锰的特征拉曼峰,印证了复合材料是由这两种组元构成。另一方面,相对于多孔石墨烯,复合材料的D峰、G峰、2D峰以及峰强比(ID∶IG)均没有改变。可见在合成纳米MnO2花球过程中,高锰酸钾并未破坏多孔石墨烯的结构。从而印证了高锰酸钾会优先氧化乙醇,且过量的乙醇能够避免高锰酸钾对多孔石墨烯的破坏,起到保护多孔石墨烯的作用。
多孔石墨烯、纳米MnO2花球以及纳米MnO2花球负载石墨烯在空气中加热后均出现不同程度的失重。多孔石墨烯在100℃附近失去吸附水,在300~500℃发生氧化,最终800℃处理后失重率为98.4%。纳米MnO2花球在200℃附近失去结晶水,在600℃以上发生热分解(形成Mn2O3或Mn3O4)[23],最终800℃处理后失重率为14.7%。复合材料是由纳米MnO2花球和多孔石墨烯组成的,其实验曲线位于两种材料失重曲线之间,这与理论结果一致。此外根据800℃处理后复合材料的失重率(56.6%)还可以推算出复合材料中两种组元的质量分数。经过计算,得到MnO2的质量分数为49.9%,与设计值50%非常接近。
图3为多孔石墨烯、纳米MnO2花球以及石墨烯负载花球MnO2复合材料的氮气等温吸附脱附曲线与孔径分布图。CVD法制备的多孔石墨烯表现出超高的比表面积,具有典型的Ⅳ型等温线特征。吸附脱附曲线组成H3型的磁滞环,这与多孔石墨烯的片状微观形貌特征是一致的。多点BET法测试表明该材料比表面积高达1452m2·g-1,高于氧化还原法、物理剥离法制备的石墨烯比表面积。由脱附曲线得出的BJH孔径分布曲线可以看出多孔石墨烯材料主要由介孔构成,孔径分布在2~16nm之间。纳米MnO2花球具有和多孔石墨烯相似的等温吸附脱附曲线特征,表明了MnO2花球在微观上也具有片状形貌特征。纳米MnO2花球的多点BET比表面积可达120.5m2·g-1,孔径分布较窄,在3~8nm之间。负载纳米MnO2花球的石墨烯复合材料比表面积位于二者之间,多点BET法测得为741m2·g-1。据此可推测复合材料中纳米MnO2花球的质量分数为53.4%,与TG测试的结果基本一致。

图3 多孔石墨烯(a)、纳米MnO2花球(b)以及石墨烯负载花球MnO2复合材料(c)氮气等温吸附脱附曲线与孔径分布图Fig.3 Nitrogen adsorption-desorption isotherms and pore size distribution of porous graphene(a), globular MnO2 nanoflowers(b) and MnO2 flowers anchored graphene composites(c)
2.3 电化学性能分析
图4(a),(b)给出了三电极体系在10,20,50,100mV·s-1扫速下纳米MnO2花球与石墨烯/MnO2电极材料的CV曲线,电解液采用0.5mol/L的K2SO4溶液(通过稀的氢氧化钾和醋酸溶液将pH调为10),扫描范围为0~0.8V (vs. Ag/AgCl)。纳米MnO2花球电极材料的CV曲线在低扫速条件下接近矩形形状,增加扫速后曲线形状保持良好但是曲线整体发生明显倾斜。这种曲线整体倾斜的行为表明纳米MnO2花球电极电阻较大,导电性能较差。石墨烯/MnO2电极材料的CV曲线则在整个扫速范围内均接近矩形形状,非常接近理想双电层电容器的曲线形状。扫速增加后曲线面积相应增大,同时曲线形状得到良好的保持。与纳米MnO2花球电极材料不同,石墨烯/MnO2电极材料的CV曲线不呈现显著的电阻特征。这表明在多孔石墨烯表面负载纳米MnO2花球后,整体材料的电子传导行为得到相应改善,这对于纳米MnO2花球电容性能(尤其是在高扫速下的电容性能)的充分发挥是非常有益的。
图4(d)给出了两种电极材料在100mV·s-1扫速下的电容的循环保持率变化曲线。纳米MnO2花球电极材料的比电容在前20次循环衰减明显,保持率仅为89%;200次循环后保持率为80%,1000次循环后比容量仅剩余70.5%。石墨烯/MnO2电极材料在循环初期发生活化,比电容前期略有上升,后期几乎保持不变。在石墨烯/MnO2电极材料中,MnO2花球弥散地负载在多孔石墨烯表面有助于电化学过程中的电子传导和电解液传输,而MnO2花球均匀的尺寸能够有效避免电极副反应的发生。1000次循环后石墨烯/MnO2电极材料的电容损失率仅有3.7%,表明该材料具有优异的电化学稳定性。

图4 纳米MnO2花球与石墨烯/MnO2电极材料的电化学性能(a)纳米MnO2花球的CV曲线;(b)石墨烯/MnO2复合材料的CV曲线;(c)倍率曲线;(d)循环衰减曲线Fig.4 Electrochemical performance of globular MnO2 nanoflowers and MnO2 flowers/graphene composites electrode materials(a)CV curves of globular MnO2 nanoflowers;(b)CV curves of globular MnO2 flowers anchored graphene composites;(c)rating curves;(d)cycling curves
3 结论
(1)多孔石墨烯的引入有助于纳米MnO2花球在多孔石墨烯表面均匀形核与生长,得到的纳米MnO2花球尺寸更一致。
(2)MnO2花球属于C心单斜晶系的K-birnessite相,是由片层结构的MnO2组装形成,具有较高的比表面积,可达120m2·g-1。
(3)多孔石墨烯负载花球二氧化锰这种独特的材料结构赋予复合电极材料优异的电子传导和电解液离子传输性能,有助于提高MnO2的电化学利用率和倍率性能,从而获得优异的电化学性能。
(4)复合电极材料在2mV·s-1扫速下的比电容高达295F·g-1,在1000mV·s-1扫速下,比电容仍然可达102F·g-1。1000次循环后,复合电极材料相对于初始电容的衰减率只有3.7%,表现出优异的电化学稳定性。表明石墨烯负载花球状二氧化锰材料是一种极具潜力的超级电容器电极材料。
