丹参提取物中脂溶性成分检测及体外溶出行为考察*
2019-01-16高秀容许小红杨恒博张旭李望汪少
高秀容,许小红,杨恒博,张旭,李望,汪少
(成都医学院药学院,成都 610083)
丹参(RadixetRhizomaSalviae Miltiorrhiza)为唇型科植物丹参的干燥根及根茎,作为活血化瘀药有悠久的临床应用历史,具有祛疲止痛、活血通经、清心除烦的功效[1]。大量研究证实,丹参主要含有脂溶性和水溶性两大类成分,隐丹参酮、丹参酮Ⅰ及丹参酮ⅡA为脂溶性成分,是丹参中含量最高也是最具代表性的主要成分,丹参药材中丹参酮ⅡA含量较高,为0.1%~0.9%,因而丹参酮ⅡA曾经一直作为丹参有效成分的质量控制指标,在《中华人民共和国药典》2015年版中也以丹参酮ⅡA为丹参药材和丹参注射液的定性定量控制标准[2-3]。
目前,以脂溶性有效成分为主入药的丹参口服制剂品种有复方丹参滴丸、丹参酮片、丹参酮胶囊、丹参酮油、丹参舒心胶囊、丹参舒心片和精制冠心片等[4]。体外溶出行为是口服制剂处方工艺筛选的重要指标,也是有效控制制剂质量的重要指标。而丹参脂溶性成分的低水溶性是影响口服固体制剂溶出度的一个重要因素,从而影响丹参口服生物利用度[5-8],笔者以丹参酮Ⅰ、丹参酮ⅡA及隐丹参酮为指标成分,建立了高效液相色谱(HPLC)法同时测定丹参提取物中丹参酮Ⅰ、丹参酮ⅡA及隐丹参酮含量的方法,考察了丹参脂溶性成分的体外溶出行为,筛选其体外溶出条件,以期为丹参脂溶性成分口服制剂的研究开发提供参考。
1 仪器与试药
1.1仪器 戴安高效液相色谱仪(美国,Dionex UltiMate3000,包括四元高压液相泵、自动进样器、紫外检测器);色谱软件(戴安液相层析仪软件Chromeleon 7.1);电子天平(德国 Sartorius,型号:BS 224S,感量:0.01 mg);离心机(上海安亭科学仪器厂,型号:TGL-16G);超声清洗器(天津市奥特赛斯仪器有限公司,型号:AS5150BD);纯水仪(优普超纯科技公司,型号:UPT);电热鼓风干燥箱(上海一恒科学仪器有限公司,型号:DHG-9013A);溶出仪(天津市国铭医药设备有限公司,型号:RC-6)。
1.2试药 丹参酮Ⅰ对照品(中国食品药品检定研究院,含量:99.0%,批号:110867-201607);丹参酮ⅡA对照品(中国食品药品检定研究院,含量:99.0%,批号:110766-201520);隐丹参酮对照品(中国食品药品检定研究院,含量:99.0%,批号:110852-200806);丹参提取物(陕西慈缘生物技术有限公司,批号:20140401,20140402,20140413);十二烷基硫酸钠(SDS,成都市科龙化工试剂厂,分析纯);磷酸二氢钾(成都市科龙化工试剂厂,分析纯);甲醇(迪马公司,色谱纯);乙腈(迪马公司,色谱纯);无水甲酸(天津市科密欧化学试剂有限公司,色谱纯);其他试剂为分析纯,水为超纯水。
2 方法与结果
2.1色谱条件 采用Agilent HC-C18(4.6 mm×250 mm,5 μm)色谱柱;流动相:A(0.1%甲酸),B(乙腈),采用梯度洗脱,洗脱顺序为:0~30 min,5%→55% B;>30~40 min,55%→75% B;>40~50 min,75% B;>50~55 min,75%→5% B;流速1.0 mL·min-1;检测波长286 nm;柱温30 ℃;进样体积10 μL。
2.2对照品溶液的制备 分别精密称取干燥至恒重的各对照品适量于5 mL棕色量瓶,甲醇定容,得到贮备液备用。取各储备液适量于25 mL量瓶,甲醇定容得到各对照品的混合标准溶液,其中各对照品浓度分别为丹参酮Ⅰ93.00 μg· mL-1,丹参酮ⅡA 82.50 μg· mL-1,隐丹参酮57.50 μg· mL-1,冷藏、避光备用。
2.3供试品溶液的制备 精密称取一定量丹参提取物至10 mL 量瓶内,加入一定量甲醇,超声使其完全溶解,10 000 r·min-1(r=8.0 cm)离心5 min以除去不溶物,甲醇定容后,上清液经孔径0.22 μm 微孔滤膜滤过后进样。
2.4方法学考察
2.4.1方法专属性考察 按“2.1”项色谱条件,分别取空白甲醇溶液、对照品溶液和供试品溶液,记录色谱图(图1),丹参酮Ⅰ、丹参酮ⅡA和隐丹参酮保留时间分别约为39,40和46 min,丹参酮Ⅰ和丹参酮ⅡA分离度为1.2,隐丹参酮分离度大于1.5。可见,空白溶液对各成分无干扰,各成分与杂质峰分离度较好。
2.4.2线性关系考察 取“2.2”项配制的混合标准溶液,用甲醇依次稀释,得以下混合标准品的标准曲线溶液:丹参酮Ⅰ标准曲线浓度为93.00,46.50,23.25,11.63,5.81,2.91,1.45 μg· mL-1,丹参酮ⅡA标准曲线浓度为82.50,41.25,20.63,10.31,5.16,2.58,1.29 μg· mL-1,隐丹参酮标准曲线浓度为57.50,28.75,14.38,7.19,3.59,1.80,0.90 μg· mL-1。 按“2.1”项色谱条件进样20 μL,以色谱峰面积(Y) 对药物浓度(X)进行线性回归,绘制标准曲线。
丹参酮Ⅰ回归方程为Y=0.202 3X+0.296 7(R2=0.999 2),线性范围1.45~93.00 μg· mL-1;丹参酮ⅡA回归方程为Y=0.445 6X+0.527 2(R2=0.999 4),线性范围1.29~82.50 μg· mL-1;隐丹参酮回归方程为Y=0.131 8X+0.000 2(R2=1.000),线性范围0.90~57.50 μg· mL-1。结果表明各标准品在考察浓度范围内线性关系良好。
2.4.3精密度实验 取高、中、低浓度混合对照品溶液,其中丹参酮Ⅰ高、中、低浓度分别为46.50,11.63,2.91 μg· mL-1,丹参酮ⅡA高中低浓度分别为41.25,10.31,2.58 μg· mL-1,隐丹参酮高、中、低浓度分别为28.75,7.19,1.80 μg· mL-1,在上述色谱条件下,连续进样5次,记录峰面积,分别计算峰面积的RSD。 结果丹参酮Ⅰ高、中、低浓度的峰积RSD分别为0.36%,0.54%,0.55%;丹参酮ⅡA高中低浓度的峰面积RSD分别为0.50%,0.14%,0.32%;隐丹参酮高中低浓度的峰面积RSD 分别为0.66%,0.28%,0.45%;说明各成分精密度良好。

A.空白甲醇溶液;B.对照品溶液;C.供试品溶液;1.丹参酮Ⅰ;2.丹参酮ⅡA;3.隐丹参酮
图13种溶液的HPLC图谱
A.methanol solution;B.reference solution ;C.sample solution;1.tanshinoneⅠ;2 tanshinonⅡA;3.cryptotanshinone
Fig.1HPLCchromatogramsofthreekindsofsolution
2.4.4稳定性实验 取两种浓度混合对照品溶液,其中丹参酮Ⅰ高、低浓度分别为46.50,2.91 μg· mL-1,丹参酮ⅡA高、低浓度分别为41.25,2.58 μg· mL-1,隐丹参酮高、低浓度分别为28.75,1.80 μg· mL-1,将该混合对照品溶液置于37 ℃恒温水浴锅中,于0,2,4,6,8,12,24,36 h取样,在上述色谱条件下进样,记录峰面积。结果丹参酮Ⅰ高、低浓度RSD分别为1.15%,1.02%;丹参酮ⅡA高、低浓度RSD分别为1.01%,0.66%;隐丹参酮高、低浓度RSD分别为0.65%,1.16%,可见,各成分在37 ℃下36 h稳定。
2.4.5加样回收率实验 取已知含量的提取物,精密称定27份,分成9组,每组3份。分别加入高、中、低浓度的混合对照品溶液,其中丹参酮Ⅰ高、中、低浓度分别为46.50,11.63,2.91 μg· mL-1,丹参酮ⅡA高、中、低浓度分别为41.25,10.31,2.58 μg· mL-1,隐丹参酮高、中、低浓度分别为28.75,7.19,1.80 μg· mL-1,按“2.3”项下方法处理,在上述色谱条件下测定。结果丹参酮Ⅰ高、中、低浓度平均加样回收率为(99.85±0.034)%(n=3),丹参酮ⅡA高、中、低浓度平均加样回收率为(100.35±0.019)%(n=3),隐丹参酮高、中、低浓度平均加样回收率为(100.74±0.026)%(n=3),符合要求。
2.5丹参提取物中各成分含量测定 取3个批号丹参提取物,每个批号分别按“2.3”项下方法平行制备3个样品,进行含量测定,在上述色谱条件下测定,记录色谱峰面积,按外标法计算各成分的含量,结果见表1。
表1丹参提取物中各成分含量测定结果
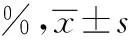

提取物批号丹参酮Ⅰ丹参酮ⅡA隐丹参酮201404010.332±0.0540.954±0.0680.544±0.010201404020.345±0.0330.886±0.0740.532±0.021201404130.310±0.0120.827±0.0510.478±0.038
2.6提取物中各成分体外溶出行为考察 溶出条件:由于丹参脂溶性成分均为水难溶性成分,故选择《中华人民共和国药典》收载的第三法(小杯法)进行溶出实验。释放介质体积为250 mL,为纯水或不同pH值缓冲液,溶出温度为(37.0±0.5)℃,取样时间点为0,2,4,6,8,10,12 h,每次吸取溶出液3 mL,取出后及时补加新鲜空白溶出介质3 mL,溶出液以孔径0.45 μm滤膜过滤,续滤液用HPLC法进行测定。
2.6.1SDS对丹参提取物成分溶出行为的影响 对于水溶性较差的药物,可在释放介质中加入表面活性剂促进药物溶出[5],故本实验考察了0.0%,0.3%,0.5%,0.7%和0.9% SDS对丹参脂溶性成分丹参酮Ⅰ、丹参酮ⅡA和隐丹参酮溶出行为的影响。释放介质为pH值6.8磷酸盐缓冲液,转速75 r·min-1,实验结果见图2~4。
由图2~4可知,当溶出液中不加入SDS时(即SDS浓度0.0%),溶出液中未能检测上述3种成分;随着溶出液中SDS浓度增加,3种脂溶性成分溶出度逐渐增加,可见SDS对上述3种成分溶出行为有显著影响。由于一般要求溶出介质中SDS浓度<0.5%,故在后续实验中选择SDS浓度为0.5%继续进行考察。

图2 不同浓度SDS对丹参酮Ⅰ溶出行为的影响
Fig.2EffectofdifferentconcentrationsofSDSonthedissolutionbehavioroftanshinoneⅠ

图3 不同浓度SDS对丹参酮ⅡA溶出行为的影响
Fig.3EffectofdifferentconcentrationsofSDSonthedissolutionbehavioroftanshinonⅡA

图4 不同浓度SDS对隐丹参酮溶出行为的影响
Fig.4EffectofdifferentconcentrationsofSDSonthedissolutionbehaviorofcryptotanshinone
2.6.2不同pH值对丹参提取物溶出行为的影响 考察丹参酮Ⅰ、丹参酮ⅡA和隐丹参酮在纯化水、pH值4.0、pH值6.8和pH值7.4磷酸盐缓冲液中的溶出行为。释放介质SDS浓度为0.5%、转速75 r·min-1时实验结果见图5~7。
由图5~7可知,溶出介质的pH值对丹参酮Ⅰ、丹参酮ⅡA和隐丹参酮的溶出行为无显著影响,美国食品药品管理局(FDA)规定,以pH值6.8与人体肠液相似,此pH值更符合药物经口服后的体内环境[9],故在后续实验中采用pH值6.8磷酸盐缓冲液为溶出介质。

图5 不同pH值溶出液对丹参酮Ⅰ溶出行为的影响
Fig.5EffectofdifferentpHsolutiononthedissolutionbehavioroftanshinoneⅠ

图6 不同pH值溶出液对丹参酮ⅡA溶出行为的影响
Fig.6EffectofdifferentpHsolutiononthedissolutionbehavioroftanshinonⅡA

图7 不同pH值溶出液对隐丹参酮溶出行为的影响
Fig.7EffectofdifferentpHsolutiononthedissolutionbehaviorofcryptotanshinone
2.6.3转速的影响 由于丹参脂溶性成分均为水难溶性成分,本实验采用提高溶出仪转速的方法提高其溶出度,分别考察3种成分在50,75和100 r·min-1条件下的溶出行为,结果见图8~10。
由图8~10可知,溶出仪转速对丹参酮Ⅰ、丹参酮ⅡA和隐丹参酮的溶出行为无显著影响,说明这3种成分的溶出特性受释放介质流动状态影响较小。
3 讨论
由于丹参3种脂溶性成分结构相似,尤其是隐丹参酮和丹参酮,所以HPLC很难将二者达到基线分离,所以本实验采用梯度洗脱的方法,最终分离度良好,成功对三者进行分析。

图8 不同转速对丹参酮Ⅰ溶出行为的影响
Fig.8EffectofdifferentrotationalspeedonthedissolutionbehavioroftanshinoneⅠ

图9 不同转速对丹参酮ⅡA溶出行为的影响
Fig.9EffectofdifferentrotationalspeedonthedissolutionbehavioroftanshinonⅡA
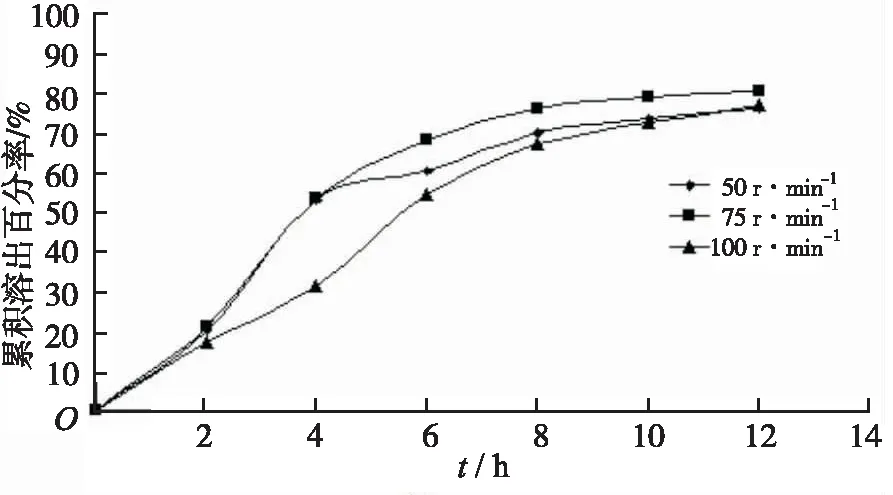
图10 不同转速对隐丹参酮溶出行为的影响
Fig.10Effectofdifferentrotationalspeedonthedissolutionbehaviorofcryptotanshinone
由于丹参脂溶性成分均为水难溶性成分,在溶出介质中浓度较低,故选择《中华人民共和国药典》2015年版收载的第三法——小杯法进行溶出实验,实验结果显示,该方法适宜作为丹参脂溶性成分溶出行为的研究。
在实验中,曾考察除SDS之外的其他表面活性剂对丹参3种脂溶性成分的溶出行为的影响,如聚山梨酯-80,结果显示聚山梨酯-80对3种成分溶出行为无影响(数据未列出),最终筛选出SDS为作为溶出介质。
本实验以丹参酮Ⅰ、丹参酮ⅡA及隐丹参酮为丹参脂溶性成分的指标成分,成功建立了HPLC方法同时测定丹参提取物中丹参酮Ⅰ、丹参酮ⅡA及隐丹参酮含量,考察了丹参脂溶性成分的体外溶出行为,筛选其体外溶出条件,为丹参脂溶性成分口服制剂的研究开发提供研究基础。
