外切型蛋白酶法制备高档医用骨明胶工艺研究*
2018-12-28
(济宁医学院生物科学学院,日照 276826)
骨明胶是一种高分子量的聚合物,主要从部分水解的骨头胶原物质中提取获得[1-2],广泛应用于食品及医药行业,可用于心脏瓣膜、角膜、肌腱等软组织的替代物[3-4]。目前骨明胶的制备工艺主要有传统的浸灰工艺和现代生物酶法工艺。传统的浸灰工艺因存在好胶率低、能耗大、耗水量大等缺点,逐渐被淘汰[5]。与传统浸灰工艺相比,生物酶法工艺因具有明胶质量高、生产周期短(2~3d)、吨明胶耗水量低等优势,备受青睐[6]。
影响生物酶法制备骨明胶的关键因素为生物酶的种类,已报道的生物酶法工艺中多采用内切型蛋白酶[7-8]。但该酶作用于骨素(骨粉浸酸脱除矿物质后的物质)时,酶解速度过快,酶解终点不易判定,导致所获骨明胶黏度较低[9]。
本文拟采用以外切型蛋白酶为主的复合型蛋白酶对骨粉进行酶解,并对骨明胶制备过程中的浸酸终点pH、复合酶蛋白酶配方、酶解时间进行优化,确定优质骨明胶的制备方法,以期解决生物酶法制备骨明胶过程中存在的缺陷和不足,实现高档医用骨明胶的清洁生产。
1 材料和方法
1.1 材料
1.1.1原料与试剂 30~150目骨粉购于漯河市五龙明胶有限公司;外切型蛋白酶(风味蛋白酶,2万U/g)购于诺维信(中国)生物技术有限公司;内切型蛋白酶(2709蛋白酶,2万U/g)购于无锡杰仁生物科技有限公司。
1.1.2仪器 搅拌器(上海析域仪器设备有限公司);明胶冻力测试仪(天津创兴电子设备制造有限公司);明胶勃式黏度测试仪(天津创兴电子设备制造有限公司);明胶透明度测试仪(天津创兴电子设备制造有限公司);LC-20AD高效液相色谱仪(日本岛津公司);TSK-GEL G2000 SWXL色谱柱(300mm×7.8mm,5μm)(上海东曹生物科技有限公司)。
1.2 方法
1.2.1骨粉浸酸终点pH优化 骨粉与水按质量比1∶5混合,搅拌至悬浮状态,将质量分数为15%的盐酸以缓慢滴加的方式加入骨粉悬浊液中。第1次浸酸,pH控制在3.5~4.0,浸酸后清洗;第2次浸酸,pH控制在3.0~3.5,浸酸后清洗;第3浸酸pH(浸酸终点)分别控制在pH 0.5(3% HCl)、1.0、1.5、2.0、2.5、3.0,测定Ca2+残留率和明胶黏度,优化浸酸终点pH控制。整个梯段滴滤浸酸过程中,水温控制为20 ℃。对照组亦为3次浸酸,每次按骨粉与3%盐酸质量比1∶5混合,搅拌作用2 h后清洗,再进行下一次浸酸。
1.2.2复合蛋白酶配方优化 将骨素(浸酸脱矿后的骨粉)按照质量比1∶2 加水,调节pH 10.0,分别加入0.2%的不同组分的复合蛋白酶(风味蛋白酶、2709蛋白酶质量比分别为9∶1、8∶2、7∶3),于22 ℃酶解22 h,后调节pH 2.0,维持3h完成灭酶。清洗后按照质量比1∶2加水,70 ℃水浴提胶3 h,测定所获骨明胶的黏度、冻力、提交率。
1.2.3酶解时间优化 将浸酸脱矿后的骨粉按照质量比1∶2加水,调节pH 10.0,添加0.2%优化后的最佳复合蛋白酶,于22 ℃分别酶解16、18、20、22、14、30、36 h,后调节pH 2.0,维持3h完成灭酶。清洗后按照质量比1∶2 加水,70 ℃水浴提胶3 h,测定所获骨明胶的黏度、冻力、提交率。
1.2.4明胶的絮凝澄清 在连续搅拌将的条件下,将0.1%阳离子聚丙烯酰胺溶液加入至(65±1)℃的明胶溶液中,直至明胶溶液清澈。
1.2.5干明胶的制备 将明胶溶液置于4 ℃冰箱,待其凝固成型后,切成细条状,于-20 ℃冷冻过夜,后将其浸没于95 %乙醇溶液中,30 min后取出拧干,转移至30 ℃烘箱内干燥5~6 h,得到水分小于14 %的干明胶。
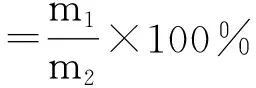
m1为干明胶质量;m2为骨粉的总质量。
1.2.6分析方法 1)明胶相对分子质量测定。色谱柱TSK-GEL G2000 SWXL(300 mm×7.8 mm,5 μm);流动相为乙腈、水和三氟乙酸(15∶85∶0.1,V/V);流速0.6 ml/min;柱温30 ℃;进样体积20 μl;检测波长220 nm。2)明胶冻力、勃式黏度、透明度测定参照医用明胶轻工部行业标准(QB2354-2005)。3)酶解中氨基酸测定[10]。4)Ca2+残余率的测定。分别称取一定质量的骨粉和完成梯度滴滤浸酸的骨粉,清洗数次,按照重量1∶5加入10%浓盐酸,浸泡24 h,按GB/T 7476-1987钙离子EDTA滴定法测定溶液中Ca2+的浓度,并计算Ca2+的残余率。
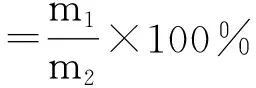
m1为完成浸酸后骨粉含有的Ca2+的质量;m2为浸酸前骨粉含有的Ca2+的质量。
2 结果和讨论
2.1 梯度滴滤浸酸终点pH对骨粉脱矿效果以及明胶黏度的影响
采用骨粉替代2~5cm骨粒,结合梯度滴滤浸酸的工艺,探讨较高pH环境下是否可以完成骨粉的浸酸脱矿物质(Ca2+),以期减少低pH条件下对骨粉中胶原分子的破坏,提高明胶黏度。
对照组中骨素Ca2+残余率为4.94%;梯度滴滤浸酸终点pH<2.0时,骨素中Ca2+残余率随浸酸终点pH变化较小;梯度滴滤浸酸终点pH>2.0时,骨素中Ca2+残余率则大幅增加。对不同pH下浸酸获得的骨素进行酶解后提胶,浸酸终点pH<2.0时,明胶黏度随浸酸终点pH的升高而大幅提高;浸酸终点pH>2.0时,明胶黏度随着浸酸终点pH的升高而差异较小。综合考虑骨粉脱矿效率及所提明胶黏度差异,选择梯度滴滤浸酸最佳终点pH2.0。见图1。
图1 浸酸终点pH对骨粉脱矿效率及明胶黏度的影响
2.2 不同组分的复合蛋白酶对明胶质量的影响
使用外切型风味蛋白酶对骨素进行酶解,测定酶解过程中氨基酸含量和pH值的变化。见图2。
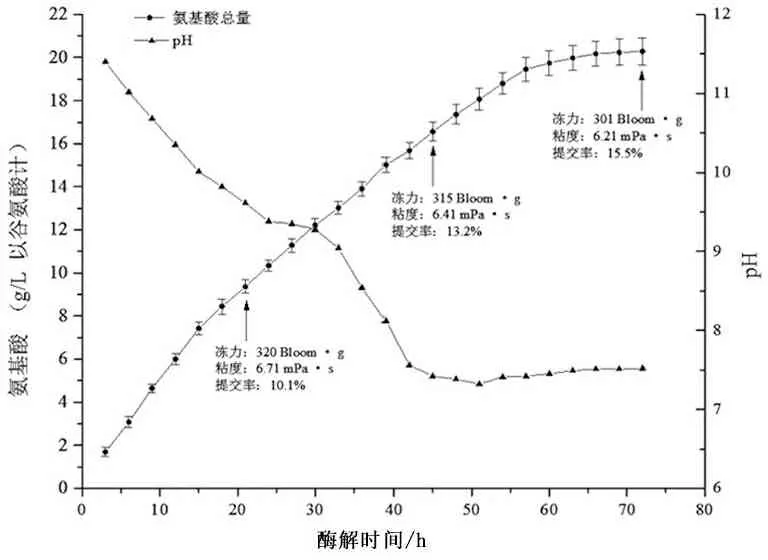
图2 酶解过程中pH和氨基酸含量变化过程
随着酶解的进行,溶液中氨基酸总量不断增加,当氨基酸含量达到最大值时,提胶率达到最高,酶解液中氨基酸的含量可作为判断酶解程度的重要依据(图2)。单纯采用风味蛋白酶酶解骨素,酶解速度较慢,耗时较长(约70 h)。同时,当酶解至30 h时,酶解液中开始滋生微生物,有异味,酶解液 pH随之急剧下降。而通过增加风味蛋白酶的用量并不能有效地缩短酶解时间。见图3。

图3 不同组分的复合蛋白酶对明胶提取质量的影响
风味蛋白酶中添加少量内切型2709蛋白酶构成复合型蛋白酶,于22 ℃酶解骨素22 h。随着2709蛋白酶添加比例的增加,制备的明胶冻力差别较小,提胶率小幅降低,而明胶黏度显著降低,风味蛋白酶与2709蛋白酶质量比为8∶2时所提明胶的综合质量最佳,该条件下所提明胶的冻力和黏度均不低于单独使用外切型风味蛋白酶时的结果,且酶解时间由原来的70h缩短为22h。见图3。
2.3 酶解时间对明胶质量的影响
测定不同酶解时间下所提明胶的冻力、黏度、提胶率。见表1。
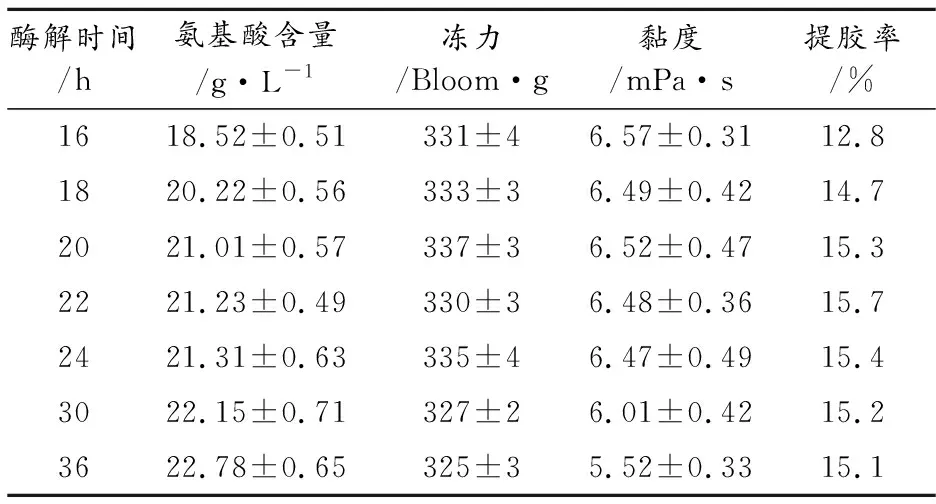
表1 酶解时间对明胶质量的影响
酶解20 h时,明胶的冻力、黏度最佳;酶解24 h时,明胶的冻力、黏度降幅均在1%以内,差异不大。20 h时的提交率也仅比22 h最高时降低2.5%。酶解时间超过30 h时,明胶的冻力、黏度及提胶率均降低。综合考虑明胶质量及生产成本因素,后续实验选择酶解时间为20 h。
2.4 所提明胶的相对分子质量分布
经工艺优化后,所提明胶的透明度>400mm,对其相对分子质量分布进行测定。见表2。
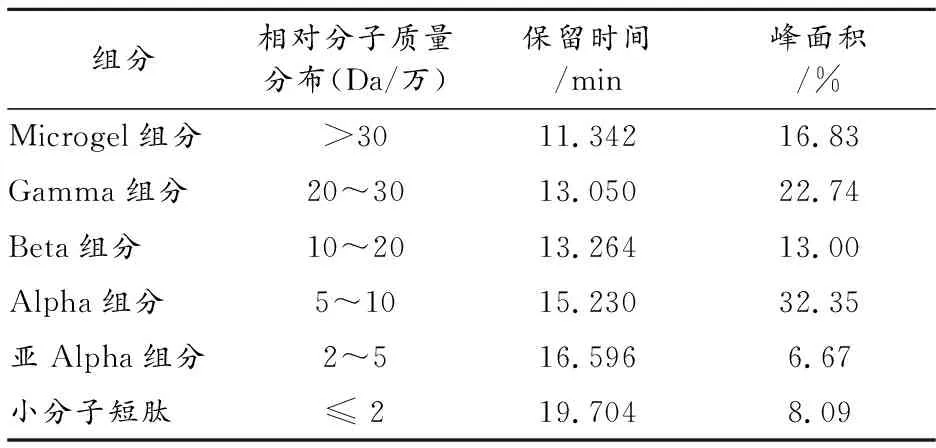
表2 所提明胶的相对分子质量分布
实验结果显示,所制备的明胶分子中Alpha组分占32.35%,为主要组分。相对分子质量>10万的组分,占52.57%,而相对分子质量<5万的亚Alpha和小分子短肽组分比例较小,仅占14.76%。由此可知,该法制备明胶的过程中,复合蛋白酶没有过度降解骨素,克服了所提明胶相对分子质量偏低、黏度不高的缺陷。
3 结论
外切型蛋白酶从胶原纤维肽链外端逐一切除氨基酸,在具备较强的水解胶原纤维之间交联键能力的同时,对胶原纤维内部纤维肽键的损伤亦较小,可弥补内切型蛋白酶酶解速度过快而导致所提骨明胶黏度低的难题。本文采用骨粉代替骨粒进行梯度滴滤浸酸,能有效地将浸酸终点pH提高至2.0,所提骨明胶的黏度提高了90.4%,避免了低pH对胶原的破坏。组合使用外切型风味蛋白酶与内切型2709蛋白酶酶解骨素,在可保持明胶高黏度的条件下,有效地将酶解时间缩短为20 h。最佳工艺条件下,所提明胶的冻力337 Bloom·g,黏度6.52 mPa·S,提交率为15.3%,透明度>400 mm,相对分子质量>10万的组分占52.57%,明胶质量达到高档医用骨明胶国家标准,为后续生物酶法制备高档骨明胶的工业化应用奠定基础。
