木兰科喙木兰属3种植物的叶挥发油成分及其系统分类学意义
2018-12-27司马永康马惠芬徐涛杨冀寅张达
司马永康,马惠芬,徐涛,杨冀寅,张达
(1.云南省森林植物培育与开发利用重点实验室,国家林业和草原局开放性重点实验室云南珍稀濒特森林植物保护和繁育实验室,云南省林业科学院,云南 昆明650201;2.云南大学生命科学学院,云南 昆明650091)
喙木兰属(LiriantheSpach)植物是一类在木兰科(Magnoliaceae)中主干大多不明显至明显的常绿木本资源植物[1-6],具有十分重要的实际利用价值,是举世闻名的园林观赏、工业用材、药材和香原料树种[7-11],分布于亚洲南部和东南部的热带和亚热带地区[2-4,6]。由于营养器官形态十分相似,在没有果实的情况下,是常常不能区分喙木兰属中的盖裂类和非盖裂类的[12]。但在野外工作中,经验丰富的当地人常用揉叶嗅味的方法,精确分辨喙木兰属中的一些种类。这表明,叶气味的不同和浓淡,具有一定的种类鉴别意义[13]。
根据司马永康[3]的分类学研究,山玉兰〔Lirianthedelavayi(Franchet)N.H.Xia & C.Y.Wu〕又名优昙花、波萝花、山波萝、土厚朴、野玉兰、大菠萝叶、云南玉兰、野厚朴、大棚棚叶,为喙木兰属优昙花亚组(Lirianthesubsect.YoutaniaSima & S.G.Lu)常绿灌木、小乔木或乔木,小枝密被淡黄褐色平伏柔毛,花直立,不下垂,花被片9,乳白色、淡黄白色或粉红色,心皮疏被毛,每心皮胚珠2-7枚,分布于贵州、四川和云南,生于海拔1 100-2 800m的石灰岩山地阔叶林中或箐边较潮湿的坡地[1,3,14]。馨香木兰[Liriantheodoratissima(Y.W.Law & R.Z.Zhou)N.H.Xia & C.Y.Wu],又名馨香玉兰、馨香喙木兰、董马木兰、调羹花或夜来香,为喙木兰属喙木兰亚组(Lirianthesubsect.LiriantheSpach)常绿灌木或小乔木,小枝密被白色或淡黄白色长毛,花不直立,多少下垂,花被片9,白色,心皮密被毛,每心皮胚珠2枚,分布于云南东南部,越南也有分布,生于海拔1 100-1 600m的阔叶林中[1-3,14-16]。夜香木兰[Lirianthecoco(Loureiro)N.H.Xia & C.Y.Wu]又名夜合花,为喙木兰属喙木兰亚组常绿灌木或小乔木,小枝无毛,花不直立,多少下垂,花被片9,白色,心皮无毛,每心皮胚珠2枚,分布于福建、广东、广西、台湾、云南和浙江,越南也有分布,生于海拔20-1 000m的阔叶林下[1,3,14]。
目前,虽然除山玉兰外,馨香木兰和夜香木兰2种植物的叶挥发物化学成分已有报道[17-19],但尚未见结合挥发物化学成分而开展其系统分类学价值的探讨。本文通过对山玉兰、馨香木兰和夜香木兰3种植物叶挥发油化学成分的分析,开展其系统分类学意义的探讨,旨在探明该3种植物叶挥发油化学成分的系统分类学价值,为喙木兰属植物的种类鉴定和困难类群的分类修订提供一定的参考,并为该类香原料植物的开发利用提供基本的科学资料。
1 材料与方法
1.1 主要仪器、材料和试剂
山玉兰、馨香木兰和夜香木兰3种喙木兰属植物的研究材料叶片采自云南省昆明树木园,经作者鉴定种类后,其原植物凭证标本(司马永康和余鸿98096、司马永康98300、司马永康和蒋宏97202)则保存于国家林业和草原局开放性重点实验室云南珍稀濒特森林植物保护和繁育实验室标本馆(YCP)。分析过程中采用的溶剂为北京百灵威公司生产色谱纯正己烷,挥发油化学成分的分析仪器为Trace 1310-ISQ气相色谱-质谱联用仪(美国赛默飞公司)。
1.2 挥发油的提取
将山玉兰、馨香木兰和夜香木兰剪碎的鲜叶各100g,分别放入1 000mL圆底烧瓶,加500mL蒸馏水,接同时蒸馏萃取(SDE)装置的一端,用电热套加热至沸腾;装置另一端接装有40mL正己烷的200mL平底烧瓶以50℃水浴加热;接通循环冷却水。蒸馏萃取1.5h,取下正己烷瓶,倒入分液漏斗静置冷却0.5h后,分离后的正己烷溶液加入10%左右的无水硫酸钠,静置,过滤除去硫酸钠,所得溶液供试验所用。
1.3 气相色谱-质谱测定条件和方法
GC条件 TR-1 MS石英毛细管柱(30mm×0.25mm×0.25μm);程序升温40℃保留3min,以5℃/min的升温速率升至180℃,保留5min,再以10℃/min的升温速率升至250℃,保留5min。溶剂切割时间为4min;柱流量为1.5mL/min;进样口温度200℃;柱前压100kPa,进样量2μL;分流比50︰1;载气为高纯氦气。
MS条件 电离方式EI,电压1.5kV,传输线温度280℃,离子源温度230℃,质量范围40-300,采用NIST 标准谱库检索定性。
将经SDE装置提取得到的挥发油经GC-MS进行分析和质谱数据库(NIST标准谱库)检索,结合谱图人工解析,查对有关质谱资料,对挥发性成分进行定性,并采用面积归一化法计算各组分的相对百分含量。
1.4 相似性分析
根据挥发油化学成分组成的特点,选用司马永康等[20]的方法和评价标准,计算物种间的组分多度相似百分率,并进行相似性比较评价。其计算公式为SP={1-∑[|Xi-Yi|÷(Xi+Yi)]÷n}×100,其中,SP为组分多度相似百分率,n为X物种和Y物种挥发油所组成的化学成分数,Xi和Yi为X物种和Y物种挥发油组成的第i个化合物的相对含量。
1.5 聚类分析
利用SPSS(PASW Statistics 18)软件,以喙木兰属3种植物为分类单位(Operational Taxonomic Unit,简写为OUT),以叶挥发油化学成分有无二态编码数据或相对含量全距0-1标准化数据为分类特性,以欧氏距离为度量指标,采用Ward系统聚类法进行聚类分析,绘制树状谱系图,分析探讨喙木兰属叶挥发油化学成分的系统分类学意义。
2 结果与分析
2.1 叶挥发油GC-MS色谱图
从叶挥发油GC-MS色谱图(图1)看,山玉兰、馨香木兰和夜香木兰3种植物均含有低沸点的芳香性物质,同时又含有高沸点的芳香性物质,芳香度饱满而持久,挥发性成分出峰时间主要集中在15-30min和40-55min。而山玉兰叶挥发油在36-38min的位置,出现了一个明显有别于馨香木兰和夜香木兰的特征峰(黄樟油精)。据此特征峰,可以很容易地将山玉兰从另外两种喙木兰属植物中鉴别出来。
2.2 叶挥发油化学成分
从叶挥发油化学成分及其相对百分含量(表1)看,山玉兰、馨香木兰和夜香木兰3种喙木兰属植物共分离鉴定出38种挥发性化合物。其中,山玉兰有30种,馨香木兰有29种,夜香木兰有22种,分别占挥发性物质总含量的86.98%、97.74%和78.97%。
在喙木兰属3种植物的38种挥发性化合物中,山玉兰的主要挥发性化学成分有-月桂烯(28.82%)、三环烯(8.84%)、3-侧柏烯(6.63%)、α-水芹烯(4.9%)、α-蒎烯(4.24%)等30种化合物,其中独有成分有-月桂烯(28.82%)、三环烯(8.34%)、3-侧柏烯(6.63%)、黄樟油精(4.13%)、Cyclohexane,2-ethenyl-1,1-dimethyl-3-methylene-(1.97%)和.gama.-桉叶醇(0.88%)6种化合物,合计含量达50.77%。馨香木兰的主要挥发性化学成分有α-水芹烯(36.68%)、α-蒎烯(7.05%)、1,3-Benzodioxole,4-Methoxy-6-(2-propenyl)-(6.72%),4(10)-侧柏烯(5.26%)、4(10)-侧柏烯(4.55%)、1(10),4-杜松二烯(4.54%)等29种化合物,其中独有成分有3-蒈烯(3.13%)和P-4(8)-薄荷二烯(0.92%)2种化合物,合计含量为4.05%。夜香木兰的主要挥发性化学成分有2-侧柏烯(33.81%)、1,3-Benzodioxole,4-Methoxy-6-(2-propenyl)-(7.84%)、1(10),4-杜松二烯(5.42%)、α-蒎烯(3.19%)、匙叶桉油醇(2.92%)、α-杜松醇(2.66%)等22种化合物,其中独有成分只有长叶烯(2.03%)1种化合物,合计含量仅2.03%。从独有化合物看,山玉兰有最多和最大量的独有化合物,其挥发油组成明显与馨香木兰和夜香木兰不同。
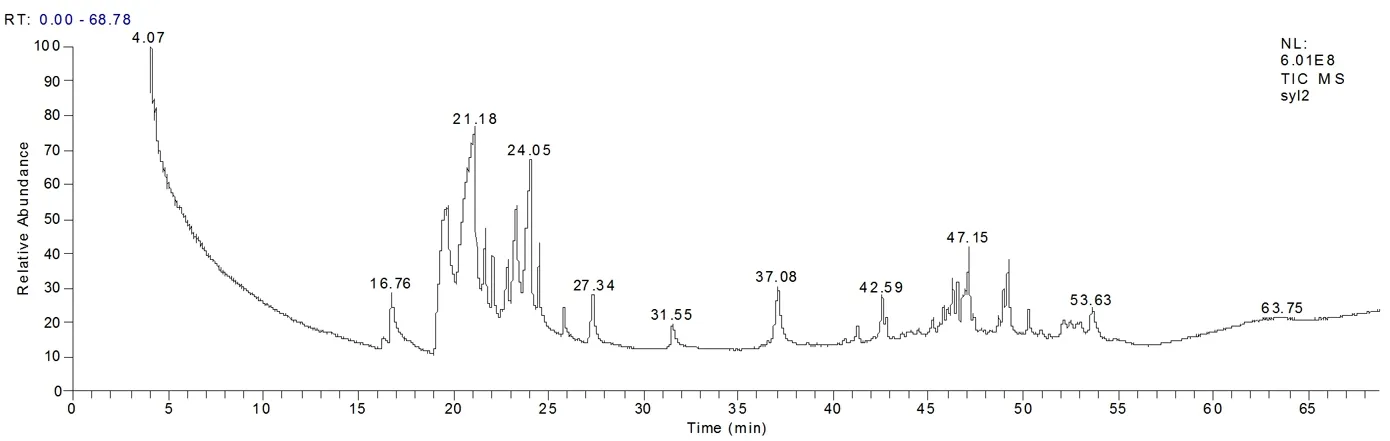
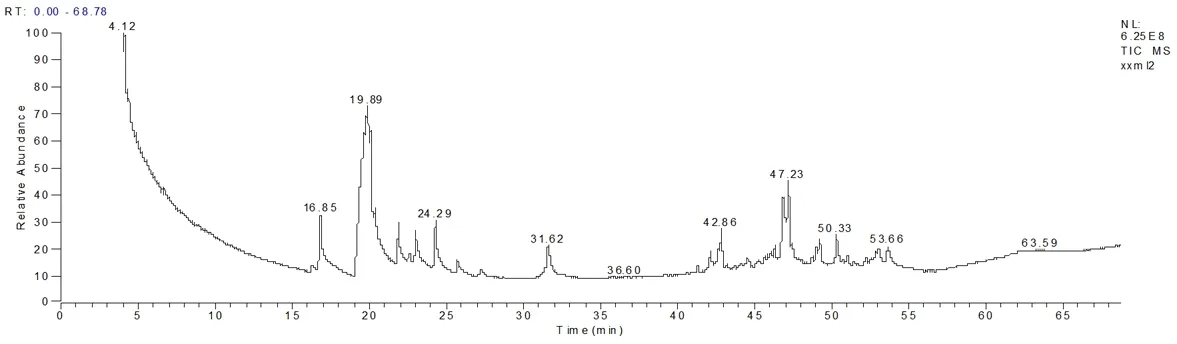

图1 山玉兰、馨香木兰和夜香木兰的叶挥发油GC-MS谱图

序号保留时间/min化合物峰面积百分比/%山玉兰馨香木兰夜香木兰116.98α-蒎烯α-Pinene4.247.053.19219.34α-水芹烯α-Phellandrene4.936.68319.53三环烯Tricyclene 8.34420.394(10)-侧柏烯4(10)-Thujene5.261.62521.17-月桂烯-Myrcene28.82621.592-侧柏烯2-Thujene2.4533.81722.433-蒈烯3-Carene3.13
续表1
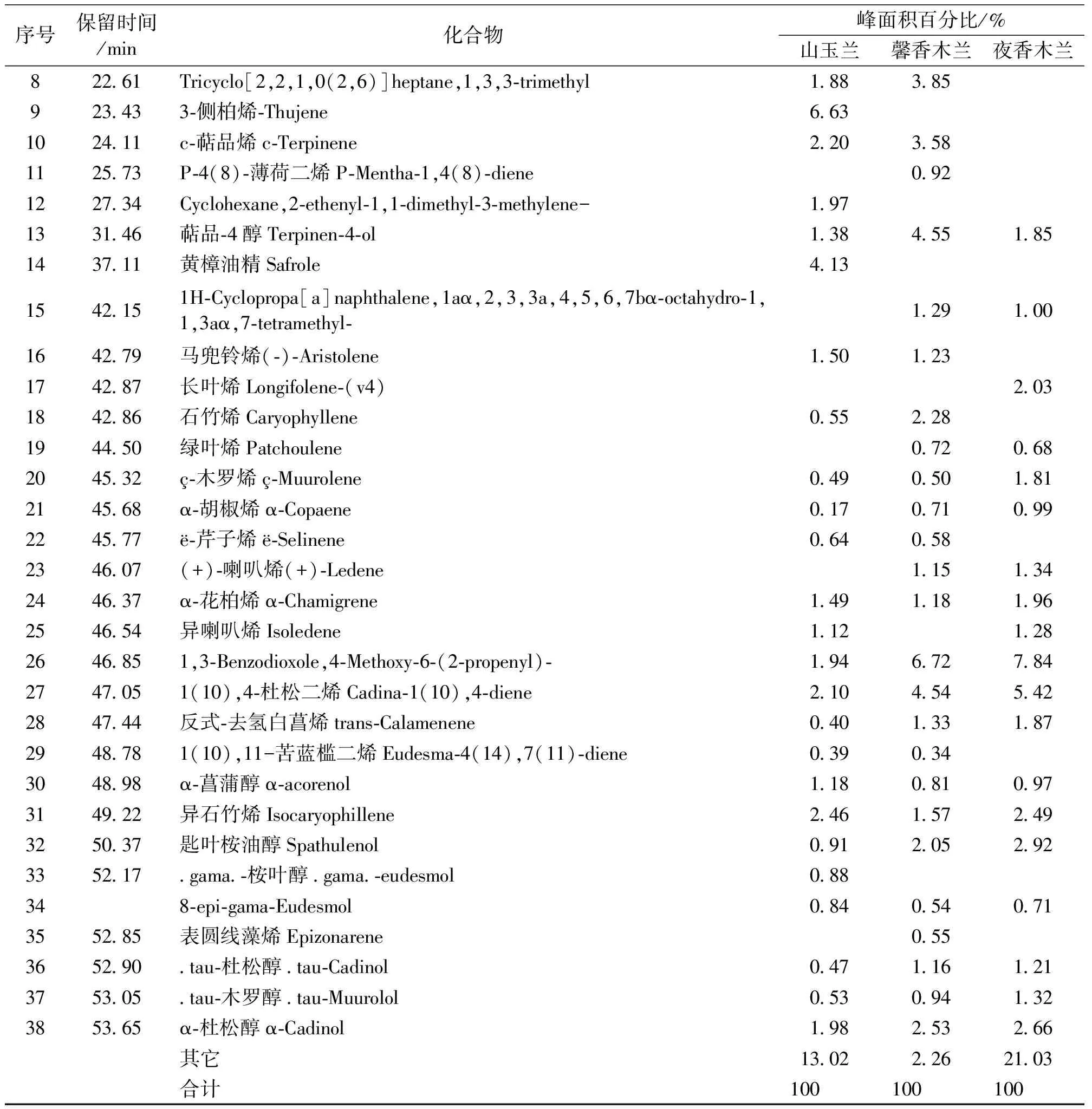
序号保留时间/min化合物峰面积百分比/%山玉兰馨香木兰夜香木兰822.61Tricyclo[2,2,1,0(2,6)]heptane,1,3,3-trimethyl1.883.85923.433-侧柏烯-Thujene6.631024.11c-萜品烯c-Terpinene2.203.581125.73P-4(8)-薄荷二烯P-Mentha-1,4(8)-diene0.921227.34Cyclohexane,2-ethenyl-1,1-dimethyl-3-methylene-1.971331.46萜品-4醇Terpinen-4-ol1.384.551.851437.11黄樟油精Safrole4.131542.151H-Cyclopropa[a]naphthalene,1aα,2,3,3a,4,5,6,7bα-octahydro-1,1,3aα,7-tetramethyl-1.291.001642.79马兜铃烯(-)-Aristolene1.501.231742.87长叶烯Longifolene-(v4)2.031842.86石竹烯Caryophyllene0.552.281944.50绿叶烯Patchoulene0.720.682045.32ç-木罗烯ç-Muurolene0.490.501.812145.68α-胡椒烯α-Copaene0.170.710.992245.77ë-芹子烯ë-Selinene0.640.582346.07(+)-喇叭烯(+)-Ledene1.151.342446.37α-花柏烯α-Chamigrene1.491.181.962546.54异喇叭烯Isoledene1.121.282646.851,3-Benzodioxole,4-Methoxy-6-(2-propenyl)-1.946.727.842747.051(10),4-杜松二烯Cadina-1(10),4-diene2.104.545.422847.44反式-去氢白菖烯trans-Calamenene0.401.331.872948.781(10),11-苦蓝槛二烯Eudesma-4(14),7(11)-diene0.390.343048.98α-菖蒲醇α-acorenol1.180.810.973149.22异石竹烯Isocaryophillene2.461.572.493250.37匙叶桉油醇Spathulenol0.912.052.923352.17.gama.-桉叶醇.gama.-eudesmol0.88348-epi-gama-Eudesmol0.840.540.713552.85表圆线藻烯Epizonarene 0.553652.90.tau-杜松醇.tau-Cadinol0.471.161.213753.05.tau-木罗醇.tau-Muurolol0.530.941.323853.65α-杜松醇α-Cadinol1.982.532.66其它13.022.2621.03合计100100100
注:山玉兰(Lirianthedelavayi)、馨香木兰(Liriantheodoratissima)、夜香木兰(Lirianthecoco)。
从已鉴定出的挥发油化学成分的类型(表2)看,主要成分为单萜类(40.47%-65.02%)、倍半萜类(18.10%-29.66%)和苯系芳香族类(6.07%-8.84%)等化合物。其中,只有单萜类和倍半萜类化合物来源于相同的生物合成途径,单萜类化合物是初始合成分支的产物而倍半萜类化合物是终极合成分支的产物。在喙木兰属3种植物中,单萜类化合物的含量在40.47%-65.02%之间,明显高于倍半萜类化合物(18.10%-29.66%)的含量。
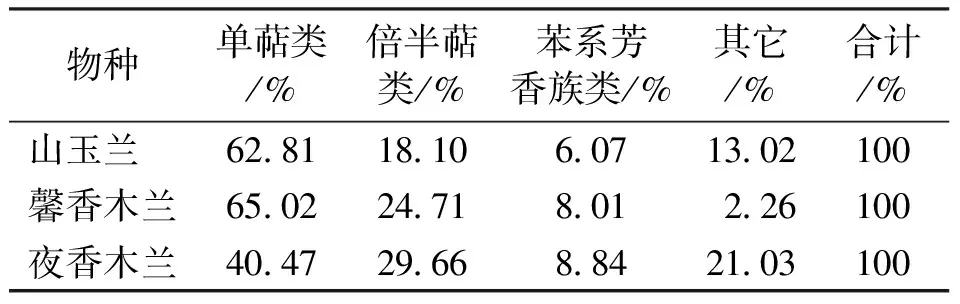
表2 喙木兰属3种植物的叶挥发油成分的主要类型及含量
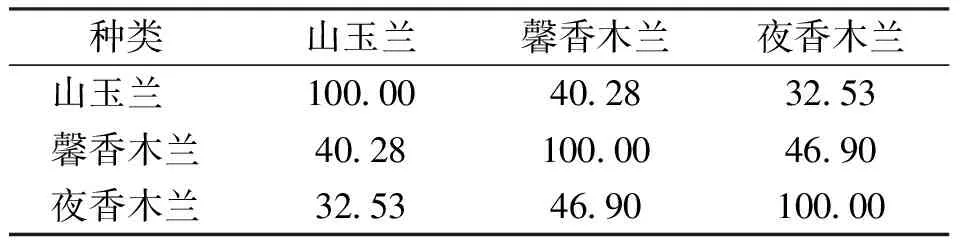
表3 喙木兰属3种植物的叶挥发油化学成分组分多度相似百分率
2.3 种的相似性
从喙木兰属3种植物叶挥发油成分的组分多度相似百分率(表3)看,馨香木兰与夜香木兰最相似,组分多度相似百分率为46.90%,而它们与山玉兰的相似程度较低,组分多度相似百分率分别为40.28%和32.53%。
2.4 种的聚类
经种的聚类分析发现,无论以叶挥发油化学成分有无二态编码数据或相对含量全距0-1标准化数据为分类特性,均得到一致的聚类树状谱系图。从聚类树状谱系图(图2)看,在0-1距离范围,即结合距离约为1-0=1时,将喙木兰属植物(OUT)分为3类,每类各含1种,即可以将喙木兰属植物的3个种区分开;而在1-25距离范围,即结合距离为25-1=24时,将喙木兰属植物(OUT)分为两类,一类包括馨香木兰和夜香木兰姊妹群,另一类仅包括山玉兰。
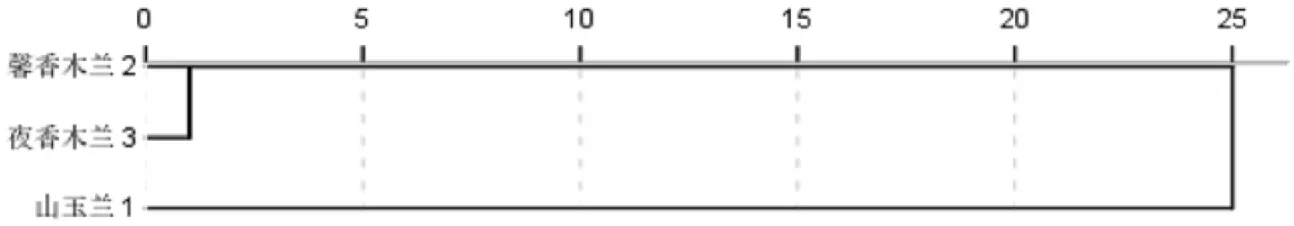
图2 喙木兰属3种植物的聚类树状谱系图
3 讨论
根据本文的研究结果,从叶挥发油GC-MS色谱图(图1)看,山玉兰、馨香木兰和夜香木兰3种喙木兰属植物均含有低沸点的芳香性物质,同时又含有高沸点的芳香性物质,芳香度饱满而持久,是值得开发的天然香料,可用于高、中档化妆品及香精中[19]。其中,优昙花亚组的山玉兰有明显区别于喙木兰亚组的馨香木兰和夜香木兰的特征峰(黄樟油精),表明叶挥发油GC-MS色谱图具有一定鉴别喙木兰属种类甚至亚组的系统分类学价值,而此特征峰是否就是山玉兰或优昙花亚组的指纹特征峰,还需要在更多的类群中开展实验研究,仔细比较确定。
山玉兰、馨香木兰和夜香木兰3种喙木兰属植物叶挥发油共分离鉴定出38种挥发性化合物,其中山玉兰30种,馨香木兰29种,夜香木兰22种,分别占挥发性物质总含量的86.98%、97.94%和78.97%。3种植物叶挥发油化学成分组成各有异同,共有的化合物有α-蒎烯、萜品-4醇、-木罗烯、α-胡椒烯、α-花柏烯、1,3-Benzodioxole,4-Methoxy-6-(2-propenyl)-、1(10),4-杜松二烯、反式-去氢白菖烯、α-菖蒲醇、异石竹烯、匙叶桉油醇、8-epi-gama-Eudesmol、.tau-杜松醇、.tau-木罗醇和α-杜松醇15种,而只有馨香木兰和夜香木兰共有的化合物有4(10)-侧柏烯、1H-Cyclopropa[a] naphthalene,1aα,2,3,3a,4,5,6,7bα-octahydro-1,1,3aα,7-tetramethyl-、绿叶烯和(+)-喇叭烯4种。山玉兰有-月桂烯、三环烯、3-侧柏烯、黄樟油精、Cyclohexane,2-ethenyl-1,1-dimethyl-3-methylene-和.gama.-桉叶醇6种独有化合物。馨香木兰有3-蒈烯和P-4(8)-薄荷二烯2种独有化合物。夜香木兰只有长叶烯1种独有化合物。
喙木兰属3种植物叶挥发油化学成分的类型相似,主要成分为单萜类(40.47%-65.02%)、倍半萜类(18.10%-29.66%)和苯系芳香族类(6.07%-8.84%)等化合物,而且单萜类化合物的含量明显高于倍半萜类和和苯系芳香族类等化合物的含量。
山玉兰的叶挥发油化学成分在此为首次报道,其共有化合物用途与其它种类的相同,而在其独有化合物中,-月桂烯和黄樟油精是合成香料的重要天然原料,而.gama.-桉叶醇则是重要的天然定香剂。比较前人对馨香木兰[18-19]和夜香木兰(夜合花)[17]叶挥发油化学成分的研究,其结果与本文结果在化合物种类和相对含量上虽略有差异,但在化合物种类上绝大多数是一致的。这种差异的造成,与实验材料、实验条件和实验人员等因素的差异有关。其中,最常见的差异是由于实验材料的采集地点和采集时期等不同造成的。例如,馨香木兰实验材料,芮和恺等[18]采自云南省广南县的野生居群,李玉媛等[19]采自云南省文山州林业局苗圃的栽培居群,均与本文采自云南省昆明树木园的栽培居群不同。至于夜香木兰(夜合花)实验材料,虽然芮和恺等[17]与本文均采自昆明树木园(云南省林业科学院植物园),但采集时期明显不同。
为了保证有高的可比性,本文的实验材料叶在同一天内采自同一地点即昆明树木园的栽培居群,最大可能地排除了环境因子和时期对叶挥发油化学成分的影响。因此,可以认为本文研究的不同种之间叶挥发油化学成分及其含量的差别是植物本身的生物学特性即遗传性的不同所造成,而叶挥发油化学成分的相似性在一定程度上反映了这些种之间亲缘关系的远近[21]。喙木兰属3种植物叶挥发油化学成分组成特征各有异同,既有含量在种间不同的共有化合物,也有各种独有的化合物。在叶挥发油化学成分的相似性上,3种植物间的组分多度百分率从大到小的排序是馨香木兰与夜香木兰(46.90%)>馨香木兰与山玉兰(40.28%)>夜香木兰与山玉兰(32.53%),结合司马永康等[20]的12级相似等级标准看,馨香木兰与夜香木兰和馨香木兰与山玉兰的组分多度百分率处于极近似水平,它们的叶挥发油化学成分组成亲缘关系很密切,其中尤以馨香木兰与夜香木兰的亲缘关系最为密切,而夜香木兰与山玉兰的组分多度百分率处于很近似水平,其叶挥发油化学成分组成亲缘关系较为疏远。从聚类分析的树状谱系图(图2)看,可将喙木兰属的这3种植物分为两大类,一类就包括亲缘关系最为密切的馨香木兰和夜香木兰姊妹群,而另一类仅包括与馨香木兰和夜香木兰亲缘关系都较为疏远的山玉兰。这一结果与司马永康[3]将馨香木兰和夜香木兰与山玉兰划分为两类的分类方案一致,在一定程度上支持司马永康[3]有关喙木兰亚组(包括馨香木兰和夜香木兰)和优昙花亚组(包括山玉兰)的划分。显然,叶挥发油化学成分及其含量差异对木兰科植物种和种上等级具有一定的系统分类学意义。前人在木兰科其它类群中有关叶[22-24]、花[25-29]或茎皮[30]等化学成分的研究,也得到类似的结论。
Fujita[31]认为在植物体中精油化合物的形成过程是不可逆的。如果真是这样,那么可以假定在形成过程中处于起始地位的化合物要比处于终端的化合物来得原始些[21]。萜类(单萜和倍半萜)化合物通过甲羟戊酸途径(mevalonic pathway)合成[25,32],但单萜类化合物是初始合成(牻牛儿基焦磷酸geranyl pyrophosphate)分支的产物而倍半萜类化合物是终极合成(法尼基焦磷酸farnesyl pyrophosphate)分支的产物。因此,单萜类化合物是原始的,倍半萜类化合物是进化的。基于普遍即原始的系统发育原理,在喙木兰属3种植物中,单萜类化合物的含量在40.47%-65.02%之间,明显大大地高于倍半萜类化合物的含量(18.10%-29.66%),也可推断出单萜类化合物原始而倍半萜类化合物进化的结论。从两类化合物含量的差值上看,显然喙木兰属三种植物从原始到进化的排序是山玉兰(44.71%)>馨香木兰(40.31%)>夜香木兰(10.81%)。其中,山玉兰是最原始的种,而夜香木兰是最进化的种。从形态上看,木兰科植物的形态性状演化规律[3-4,33-35]是乔木→灌木,植物体密被毛→无毛,花序梗粗壮而直立→纤细而向下弯垂,花型大→小,花色多变→单一,每心皮胚珠多数而不稳定→2枚而稳定。山玉兰多为乔木,小枝、花短枝和叶背密被毛,花序梗粗壮直立,花型大而颜色多变、从白色、淡黄色白色到粉红色,每心皮胚珠2-7枚,具有较多的原始性状,花形态和花色变化与原始的木莲属(ManglietiaLinnaeus)植物相似[2],是最为原始的种类。馨香木兰多为小乔木,小枝、花短枝和叶背密被或疏被毛,花序梗较细而多少向下弯垂,花型较小而颜色为白色,每心皮胚珠2枚,具有较少的原始性状,是较山玉兰进化的种类。夜香木兰多为灌木,小枝、花短枝和叶背几无毛或无毛,花序梗较细而向下弯垂,花型较小而颜色为白色,每心皮胚珠2枚,具有最少的原始性状,是最进化的种类。以上分析表明,喙木兰属3种植物利用叶挥发油化学成分组成特征所推导的从原始到进化的排序结果与根据形态性状所推导的结果一致,并以化学性状的形式从分子水平进一步揭示了喙木兰属3种植物之间的系统发育关系。
综上所述,喙木兰属3种植物叶挥发油化学成分组成特征各有异同,既有含量在种间不同的共有化合物,也有各种独有的化合物。叶挥发油化学成分及其含量差异明显具有一定的种及种上等级的系统分类学价值,因此从科学上很好地解释了,为什么在野外工作中,经验丰富的当地人常用揉叶嗅味的方法,依据其气味的不同和浓淡,精确地分辨营养器官形态十分相似的喙木兰属中的一些种类。另外,叶挥发油化学成分的组成相似性在一定程度上可作为判断物种间亲疏关系的依据,而其不同类型化合物间的演化关系也可在一定程度上以化学性状的形式从分子水平揭示了物种间的系统发育关系。然而,就其独有化合物而言,这些独有化合物能否作为各自的指纹化合物?在其共有化合物中,有多少种化合物为喙木兰属及其亚组的指纹特征化合物或是否存在喙木兰属及其亚组的指纹特征化合物?其不同类型化合物间的演化关系是否都能揭示喙木兰属甚至木兰科所有物种间的系统发育关系?对这些问题的解答,还需要在更大范围的种类中开展更多的实验研究,经进一步仔细比较确定和验证。
