Ki-67与脑膜瘤分级及复发的相关性分析
2018-12-27王文阳卢珍玲林晓宁杨修
王文阳 卢珍玲 林晓宁 杨修
脑膜瘤是中枢神经系统中发病率位于第2位的原发性肿瘤。脑膜瘤WHOⅠ级为良性肿瘤,生长缓慢,但术后仍可见复发[1],WHOⅡ级介于良性和恶性之间,WHOⅢ级为恶性,侵袭性较强,极易复发。肿瘤细胞免疫组化染色中Ki-67为常用的免疫组化标志物,作为一个细胞增殖的标志物,能够较好地评估某一细胞群增殖比例,可用来评估脑膜瘤的分级、良恶性和复发风险[2]。本文对近年来脑膜瘤手术患者临床资料和病理资料进行回顾性分析,旨在探讨Ki-67阳性率与脑膜瘤分级及复发的相关性。
1 材料与方法
1.1 材料
经医院伦理委员会审核批准,收集2005年1月—2013年5月脑外科脑膜瘤手术治疗患者172例,均为初次手术患者,手术后均经影像学显示全切,并经病理证实为脑膜瘤。其中男63例,女109例,年龄27~78岁,平均年龄(52.5±13.3)岁,病程1个月~17年。肿瘤发生部位依次是大脑凸面88例,窦旁34例,镰旁20例,鞍区18例,桥小脑角6例,其它6例。主要以头晕、头痛、肢体乏力、癫痫等症状就诊,部分患者出现视力、视野、嗅觉或听觉障碍,部分患者无临床症状,体检偶然发现。
入选标准:临床症状、体征、影像学检查符合脑膜瘤的诊断标准;初次手术患者;术后经影像学显示全切;术后经病理确诊;性别不限;术前未接受放化疗;术后配合进行随访;签署书面知情同意书。排除标准:严重凝血功能障碍;并发严重心、肝、肾功能异常等系统性疾病;其他原因不能耐受手术。
1.2 试剂与方法
病理标本用10%福尔马林固定后石蜡包埋连续切片,显微镜下观察脑膜瘤的分级及分型。采用鼠抗人Ki-67单克隆抗体做免疫组化(福州迈新生物技术有限公司),具体操作严格按照试剂盒说明书。
病理标本均由2名病理科医生采用双盲法同时阅片,Ki-67以肿瘤细胞核内有棕褐色染色颗粒为阳性。在×400高倍镜下,根据肿瘤切片的大小选择10个高倍视野(包括阳性细胞最高区域)各计数1 000个肿瘤细胞,Ki-67染色阳性细胞占计数总细胞的百分数表示,取2人计数的平均数作为Ki-67的阳性率。
1.3 患者随访
对术后患者每年复查颅脑磁共振平扫+增强,随访5年,观察脑膜瘤患者术后复发情况。
1.4 统计学处理
利用Excel表建立患者临床资料数据库,采用SPSS 21.0软件对数据进行统计分析,计量资料用(x-±s)表示,不同级别脑膜瘤Ki-67阳性率比较、复发和非复发患者ki-67阳性率比较采用非参数秩和检验,以P<0.05为差异有统计学意义。
2 结果
2.1 WHO脑膜瘤病理分级及分型
172例脑膜瘤中,Ⅰ级脑膜瘤128例(74.4%),其中脑膜上皮型66例,过渡型34例,纤维型18例,血管瘤型6例,砂粒体型4例。Ⅱ级脑膜瘤32例(18.6%),其中非典型性18例,脊索瘤样型10例,透明细胞4例。Ⅲ级脑膜瘤12例(7.0%),均为间变性。
2.2 不同级别脑膜瘤Ki-67阳性率的表达情况
172例脑膜瘤组织中Ki-67均为阳性表达,Ⅰ、Ⅱ、Ⅲ级脑膜瘤患者的Ki-67阳性率逐渐增高,非参数秩和检验结果显示,三组患者Ki-67阳性率差异有统计学意义(Z=79.474,P<0.05),不同级别脑膜瘤Ki-67表达差异,见表1。
2.3 术后随访
对术后患者门诊复查或电话随访,时间为7个月~5年,平均(27.19±15.84)个月,MRI影像学检查证实脑膜瘤复发32例。32例复发患者中,Ⅰ级脑膜瘤8例,其中脑膜上皮型4例,过渡型2例,血管瘤型2例。Ⅱ级脑膜瘤12例,其中非典型性6例,透明细胞型4例,脊索瘤样型2例。Ⅲ级脑膜瘤12例,均为间变性。术后5年内,Ⅰ级脑膜瘤复发率6.25%,Ⅱ级脑膜瘤复发率37.5%,Ⅲ级脑膜瘤复发率100%。
2.4 复发和非复发患者Ki-67阳性率的比较
32例复发患者Ki-67阳性率(10.94±12.25)%,140例非复发患者Ki-67阳性率(2.30±2.34)%,差异有统计学意义(Z=3.958,P<0.05)。提示Ki-67阳性率与脑膜瘤的预后存在相关性。
3 讨论
脑膜瘤好发于中老年人,女性发病率高于男性,本研究显示,男女发病率比值为1∶ 1.73,在印度某城市男女发病率比值为1 ∶ 1.5[3],发病率接近。脑膜瘤主要起源于蛛网膜上皮细胞,好发部位与蛛网膜上皮细胞的分布一致,所以常发生在大脑凸面、矢状窦-大脑镰旁、鞍区等部位。
根据WHO(2016年)中枢神经系统肿瘤病理分级及分型标准[4],脑膜瘤分为WHOⅠ、Ⅱ、Ⅲ级和15种亚型。Ⅰ级有9种亚型,包括脑膜上皮型、纤维型、过渡型、砂粒体型、血管瘤型、微囊型、分泌型、富于淋巴细胞-浆细胞型和化生型;Ⅱ级有3种亚型,包括脊索瘤样型、透明细胞型、非典型性脑膜瘤;Ⅲ级有3种亚型,包括乳头型、横纹肌样型和间变性脑膜瘤。分级对于临床治疗方案的制定具有指导意义。
外科手术切除是脑膜瘤最主要的治疗方法,手术原则是在安全的范围内最大限度切除肿瘤,但是部分脑膜瘤术后易复发,尤其是肿瘤位置深位于重要功能区周围或肿瘤级别高呈浸润性生长易造成手术切除困难、无法全切。复发可能与肿瘤发生部位、手术切除是否彻底、肿瘤细胞在手术过程中播散、影像学特征、组织病理学分级与分型等有关。脑膜瘤的WHO分级单纯依靠临床症状和体征不能鉴别,MRI能够明确病变向邻近脑实质侵犯的程度和范围,但难以明确脑膜瘤的级别及亚型[5],明确分级及诊断最终仍然需要依靠术后病理诊断。病理诊断根据肿瘤表现的形态特征判断亚型,属于定性标准,每个医生的经验不同,可能存在误诊。免疫组化从分子水平进行诊断,是有力的辅助手段,有助于脑膜瘤分级和判断预后。
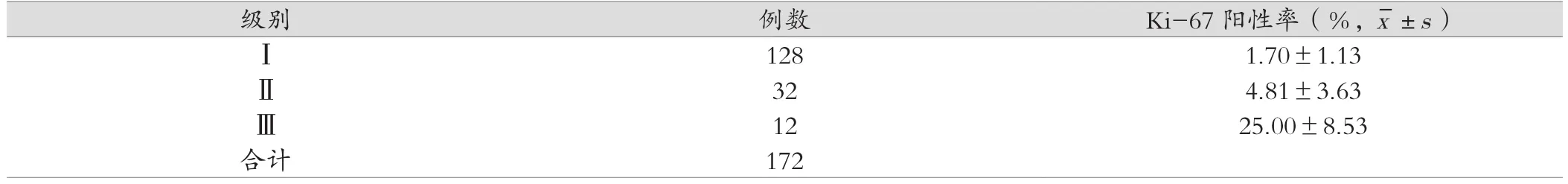
表1 不同级别脑膜瘤Ki-67阳性率表达差异
Ki-67是表达于所有G0期以外细胞的一种细胞增殖抗原,与细胞增殖及组织分化关系密切,如果处于增殖期的细胞越多,组织分化越差,Ki-67表达越高。Ki-67可作为评估脑膜瘤良恶性的指标。谢韬等[6]研究表明,Ki-67和脑膜瘤生长的生物学行为和恶性程度相关,脑膜瘤WHO分级越高,Ki-67表达越高,Ki-67表达高的脑膜瘤有很高的复发率。蒋春秀等[7]研究显示Ki-67与肿瘤的恶性程度、增殖指数及生物学行为密切相关。王力军等[8]研究显示Ki-67≥8%的WHOⅡ级脑膜瘤患者,术后复发率高。本研究中,Ⅲ级脑膜瘤患者的Ki-67阳性率高于Ⅰ级和Ⅱ级脑膜瘤患者,复发患者Ki-67阳性率高于非复发患者。上述研究结果提示,Ki-67与病理分级有关,可作为判断脑膜瘤恶性度,预测脑膜瘤复发的重要指标。但同一级别脑膜瘤Ki-67阳性率并非一致,不能仅依靠Ki-67对脑膜瘤患者进行分级。Ki-67与患者的年龄、性别、肿瘤大小、是否出现“脑膜尾征”无相关性[9]。
脑膜瘤复发率与分级有关,WHO Ⅲ级脑膜瘤具有很高的侵袭性和复发性,尿激酶型纤溶酶原激活物(u PA)及其受体(u PAR)对恶性脑膜瘤细胞有促侵袭作用[10]。本研究中,12例间变型脑膜瘤全部复发,有7例一开始即为恶性生长的间变型,有5例由Ⅰ级和Ⅱ级脑膜瘤演变而来,提示脑膜瘤可以在一开始就表现为恶性,也可以从良性逐步恶变。间变型脑膜瘤中男性10例,女性2例,提示男性可能也是复发的一个危险因素。男性脑膜瘤患者的级别往往更高,生物学行为更具侵袭性,更易复发,临床转归不良,与类似文献报道一致[11]。对于易复发的WHOⅢ级脑膜瘤患者,生存期短,放射治疗有利于延长术后无进展生存期[12]
综上所述,Ki-67阳性率为脑膜瘤临床病理分级的客观指标之一,与脑膜瘤术后复发密切相关,具有重要的临床价值,Ki-67表达高的脑膜瘤患者出院后尤其应密切随访,以便尽早采取有效的辅助治疗措施,延长生存期。
