吉西他滨与培美曲塞分别联合顺铂治疗非小细胞肺癌的临床效果
2018-12-26薛英杰赵美芝薛英超
薛英杰,贾 靖,吴 杨,邵 董,赵美芝,薛英超
肺癌是临床常见的肺部恶性肿瘤,其发病率和病死率在世界范围内有逐年升高的趋势,发病率也位于癌症患者的首位[1]。肺癌患者中80%~85%为非小细胞肺癌(NSCLC),多数NSCLC患者就诊时即为晚期,手术治愈率低,只能接受化疗[2-3]。基质金属蛋白酶(MMP)是细胞外基质重构的主要酶,可能影响并参与恶性肿瘤的发生、发展等过程[4]。肿瘤标志物可以对癌症患者化疗效果进行监测,并用于判断患者预后和制定后续治疗方案。本研究观察了吉西他滨与培美曲塞分别联合顺铂治疗NSCLC的临床效果及对相关指标的影响,以期为临床治疗方案的制定提供参考。
1 资料与方法
1.1一般资料 选择2015年10月—2016年12月定州市人民医院收治的NSCLC患者120例进行回顾性分析。①纳入标准:均经CT、MRI检查及肺活检后确诊为NSCLC,并符合相关诊断标准;生存期>3个月;病变未侵袭胸膜,且无胸腔积液;无脑转移且未合并其他器官病变。②排除标准:其他脏器功能不全者;对化疗药物不耐受者;合并其他恶性肿瘤的患者。根据化疗药物不同分为观察组65例和对照组55例。观察组男36例,女29例;年龄(51.07±2.35)岁;病理类型:腺癌40例,鳞癌25例;肿瘤分期:ⅢA期18例,ⅢB期20例,Ⅳ期27例。对照组男30例,女25例;年龄(50.96±2.02)岁;病理类型:腺癌35例,鳞癌20例;肿瘤分期:ⅢA期15例,ⅢB期18例,Ⅳ期22例。两组的性别、年龄、肿瘤分期及病理类型比较差异均无统计学意义(P>0.05),具有可比性。
1.2化疗方法 两组均给予地塞米松、维生素B12及叶酸等基础治疗。对照组给予吉西他滨联合顺铂治疗,于第1、8天给予吉西他滨900 mg/m2溶入5%葡萄糖注射液250 ml静脉滴注,顺铂75 mg/m2静脉滴注。观察组给予培美曲塞联合顺铂治疗,于第1天给予培美曲塞500 mg/m2溶入于生理盐水100 ml静脉滴注,顺铂75 mg/m2静脉滴注。21 d为1个周期,两组均给予2个周期治疗后观察疗效。
1.3观察指标
1.3.1近期疗效观察:根据RECIST实体瘤疗效评价标准进行判定。①完全缓解:可见病灶完全消失并维持1个月以上,相关肿瘤标志物恢复正常;②部分缓解:肿瘤最大直径与最大垂直直径乘积缩小>50%,相关肿瘤标志物下降;③疾病稳定:肿瘤最大直径与最大垂直直径的乘积增大不超过25%,缩小<50%。④疾病进展:出现1个或多个病灶肿瘤最大直径与最大垂直直径的乘积增大>25%。总有效率=(完全缓解+部分缓解+疾病稳定)/总例数×100%。
1.3.2血清肿瘤标志物检测:化疗前后抽取患者空腹静脉血2~3 ml,分离血清,采用化学微粒子免疫系统检测血清抗原125(CA125)、癌胚抗原(CEA),电化学发光免疫分析检测神经元特异性烯醇化酶(NSE)。
1.3.3其他化学指标:化疗前后抽取患者空腹静脉血3 ml,离心10 min取上清液,-20℃待检。放射免疫法检测白介素-27(IL-27)、酶联免疫法检测转化生长因子-β1(TGF-β1)和MMP-2。
1.3.4毒副反应观察:化疗期间密切检测患者血常规、肝肾功等,并采用WHO抗癌药物毒副反应分级标准评定药物毒副反应。
2 结果
2.1近期疗效 两组化疗的总有效率比较差异无统计学意义(P>0.05)。见表1。

表1 两组非小细胞肺癌患者化疗的近期疗效比较(例)
2.2IL-27、TGF-β1和MMP-2水平比较 化疗前,两组IL-27、TGF-β1、MMP-2水平比较差异均无统计学意义(P>0.05)。化疗后,两组TGF-β1、MMP-2均低于化疗前,且观察组低于对照组(P<0.05)。化疗后,两组IL-27水平高于化疗前,且观察组高于对照组(P<0.05)。见表2。
2.3肿瘤标志物比较 化疗前,两组CA125、CEA和NSE水平比较差异无统计学意义(P>0.05)。化疗后,两组CA125、CEA和NSE水平低于化疗前,且观察组均低于对照组(P<0.05)。见表3。
2.4毒副反应发生情况 两组化疗药物毒副反应发生情况比较差异均无统计学意义(P>0.05)。见表4。
表2 两组非小细胞肺癌患者化疗前后IL-27、TGF-β1和MMP-2水平比较
表3 两组非小细胞肺癌患者化疗前后肿瘤标志物水平比较
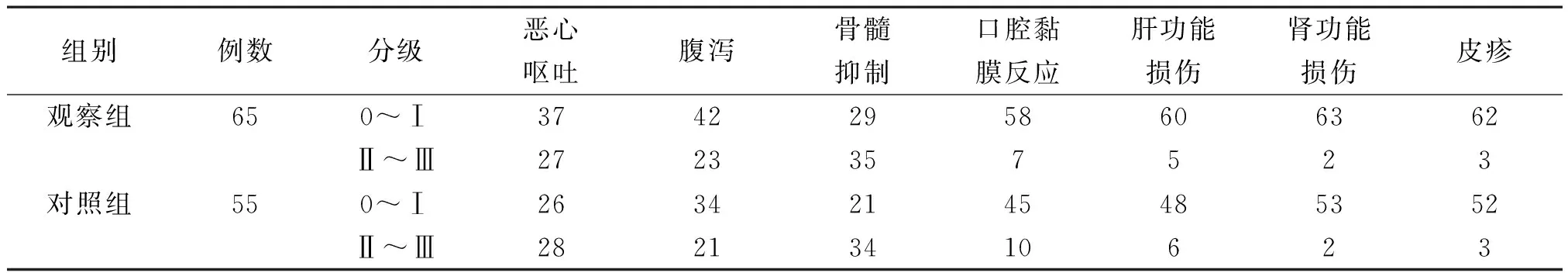
表4 两组非小细胞肺癌患者化疗药物毒副反应发生情况(例)
3 讨论
目前,临床治疗NSCLC主要以手术联合放化疗的方式。NSCLC发病人群多为中老年人,患者身体机能、抵抗力及免疫能力均大幅下降,同时可伴有其他组织器官的器质性病变,使其治疗更加困难。由于年龄偏大的肺癌患者对疾病及手术治疗耐受性差,骨髓造血功能也出现退化和减弱,免疫能力明显降低,很容易发生强烈的应激反应[5]。晚期NSCLC患者往往失去最佳的手术时机,放化疗是唯一途径。有研究指出,根据NSCLC患者病情合理选择化疗药物可延长患者的生存时间,并能改善生活质量[6-9]。因此,针对晚期肺癌患者生存率低的情况,早期诊断和合理选择药物是治疗的关键。
在临床上培美曲塞、吉西他滨、多西塔塞等联合顺铂是晚期NSCLC患者的一线化疗方案。长期应用铂类药物的肿瘤患者可能出现一定程度的耐药性,癌细胞对药物敏感性逐渐降低,推测发生原因可能与癌细胞对铂类药物的解毒作用日渐增强,同时抑制细胞凋亡和修复DNA能力增强有关[10]。顺铂是广谱抗癌药,抗癌作用明显,且具备较高的抗癌活性,对实体瘤和一般化疗不敏感的患者均有明显的治疗效果。顺铂毒副反应与其他药物有所不同,可以与其他抗癌药物配伍,进而逆转联合化疗的毒副反应,同时与这些药物产生协同,并无交叉耐药现象,因此常用于联合化疗方案[11-12]。
吉西他滨是一种二氟核苷类抗代谢肿瘤药物,具有破坏细胞复制的作用,也是核糖核苷酸还原酶的抑制性酶替代物。对于NSCLC有明显的治疗效果,联合顺铂化疗也是临床常用的治疗方案。吉西他滨虽然能够促进癌细胞凋亡并抑制细胞分裂,但有研究指出其缓解率为30%~40%,远期疗效不佳,并有明显的毒副反应,包括骨髓抑制、白细胞异常与神经毒性等[13]。培美曲塞是Ⅰ类抗代谢抗癌药物,能够有效抑制多个叶酸依赖性代谢途径参与酶,该药可通过运载叶酸载体及叶酸结合蛋白的运输系统进入肿瘤细胞,阻碍嘧啶和嘌呤的合成,从而使细胞在分裂间期发生停滞,由此加速细胞凋亡,抑制肿瘤生长[14]。多数文献报道,培美曲塞联合顺铂治疗NSCLC可取得明显效果[13-15]。本研究结果发现,两组的化疗总有效率比较无明显差异,说明两者对NSCLC近期疗效均有明显作用,而本文未对其远期疗效进行观察。本研究结果还发现,两组药物毒副反应发生情况也无明显差异,与相关报道不同[12,16-17],可能与本研究的样本选择和患者耐受性有关。
肿瘤组织可产生大量肿瘤标志物,存在于病变组织、血液与其他液体中。检测血清肿瘤标志物具有简单快捷的特点,可迅速对患者的病情及疗效进行判定[18-19]。本研究结果发现,培美曲塞联合顺铂化疗更能改善患者肿瘤标志物指标,提示其对患者预后可能产生影响。TGF-β1是一种免疫细胞产生的多肽,可调节NSCLC细胞上皮间质转化,从而促进肿瘤浸润和转移;MMP-2在NSCLC肿瘤中的作用体现在促进肿瘤血管生成与生长方面,并表达于浸润肿瘤细胞;IL-27在肿瘤免疫治疗中发挥重要作用,可促进细胞Th1/Tc1免疫应答,从而发挥免疫调节功能[15-18]。以上指标均与NSCLC的病情发展及治疗效果有密切联系。本研究对上述指标进行观察,发现培美曲塞联合顺铂化疗的改善情况均优于吉西他滨联合顺铂化疗,提示培美曲塞联合顺铂有更强的抑制肿瘤细胞增殖、促进细胞凋亡作用,并可进一步增强机体免疫能力。但由于本文观察的样本量有限,且由于随访时限原因,未对远期效果进一步评估,还需增加样本量和研究时间进行深入探讨,以达到化疗药物选择的合理化和个体化。
