Dupilumab治疗常年性变应性鼻炎并发哮喘患者的疗效和安全性
2018-12-22StevenWeinsteinMDRohitKatialMDShyamalieJayawardenaPhDGianlucaPirozziMDHeribertStaudingerMDLaurentEckertPhDVijayJoishPhDNikhilAminMDJamanMaroniMDPaulRoweMDNeilGrahamMDandArielTeperMD
Steven F. Weinstein, MD,Rohit Katial, MD, Shyamalie Jayawardena, PhD, Gianluca Pirozzi, MD, Heribert Staudinger, MD, Laurent Eckert, PhD, Vijay N. Joish, PhD, Nikhil Amin, MD, Jaman Maroni, MD,Paul Rowe, MD, Neil M. H. Graham, MD, and Ariel Teper, MD
控制不佳的持续性哮喘患者通常生活质量明显下降,且发生疾病加重、住院和死亡的风险较高[1-3]。 这些患者普遍合并有其他2型免疫疾病,其中变应性鼻炎(allergic rhinitis,AR)最为常见[4]。与哮喘并发其他2型免疫疾病包括鼻息肉(nasal polyposis,NP)、鼻窦炎、特应性皮炎(atopic dermatitis,AD)和食物过敏[5]。大约75%~80%的哮喘患者并发AR,这些患者几乎100%都属于特应性或过敏性哮喘[6-8]。由于地理位置和过敏原的不同,变应性鼻炎可以季节性或常年性发生[6,9]。季节性变应性鼻炎通常由花粉引起,而常年性变应性鼻炎(perennial allergic rhinitis,PAR)通常由室内过敏原[如尘螨、霉菌(如果不是季节性的话)和动物皮屑]引起[6]。在这两种鼻炎中,PAR通常更难治疗,且即使给予最佳治疗,患者仍然有症状的出现[10]。PAR患者发展成哮喘的风险也更大。流行病学证据表明,并发AR是难控制或严重哮喘的标志[8,11-13]。这两种疾病的同时发生还伴随着哮喘住院次数的增加、生活质量的降低和每年总医疗费用的增加[8,14-16]。AR和哮喘的2型免疫炎症非常相似。“联合呼吸道疾病”或“同一气道,同一疾病”的假说得到了广泛的认同,并且有流行病学、病理生理学和临床研究的证据支持[17-19]。尽管有相似之处,AR和哮喘这两种疾病是独立的实体,管理应该要以症状为中心,尤其在两种疾病并存时,症状可能出现恶化。目前,存在一种令人兴奋的可能性,采用单一的药物同时治疗这两种疾病,这样的治疗方式也符合同一气道的假说。
2型细胞因子IL-4、IL-5、IL-13在哮喘和其他2型/ IgE介导的免疫疾病的发病机制中发挥重要作用[20-23]。近年来,针对这些靶点的以抗体为基础的治疗方法在疾病治疗方面取得了重大进展[23]。
Dupilumab是一种以IL-4受体alpha亚基(IL-4Rα)为靶点的全人单克隆抗体,可以阻断IL-4和IL-13的信号转导(因为IL-13共享有IL-4α链);IL-13和IL-4都是2型免疫疾病(如变应性/过敏性疾病)的关键驱动因子。在最近一项关于确定剂量范围的2b期临床研究(ClinicalTrials.gov注册号:NCT01854047)中,针对使用了中高剂量吸入激素(ICSs)并发长效β2受体激动剂(LABAs)仍控制不佳的持续性哮喘患者,dupilumab可降低哮喘重度急性发作的发生,改善肺功能和生活质量,且耐受性良好。这些发现既适用于总体人群,也适用于以基线嗜酸性粒细胞计数高或低分组(定义:≥300或<300个细胞/μL)的亚组人群[5]。
Dupilumab被美国食品和药物管理局批准用于治疗中重度特应性皮炎的患者:这些患者的皮炎不能通过局部药物控制,或不推荐局部疗法时,dupilumab可以单独使用也可以与局部激素联合使用。Dupilumab还获得了欧盟欧洲药品管理局的批准,用于患有中重度特应性皮炎且需要接受系统性激素治疗的成年人。Dupilumab目前正在进行研究可否用于哮喘、慢性鼻-鼻窦炎(chronic rhinosinusitis,CRS)合并鼻息肉病(chronic rhinosinusitis with nasal polyposis,CRSwNP)和嗜酸粒细胞性食管炎的治疗[5,24,25]。使用选择性免疫调节剂(如dupilumab)进行系统性治疗,有可能同时兼顾经常并发存在的多种特应性/变态反应性疾病。
在本次2b期临床研究的亚组分析中,我们主要探究dupilumab在哮喘并发PAR患者中的疗效和安全性。
1 方法
1.1 研究设计与处理
NCT01854047研究是一项在全球范围内174个研究中心进行的随机、双盲、安慰剂对照、平行分组的2b期临床试验,此前已分别作过报道[5]。 本次析因分析主要研究的是哮喘并发PAR这一亚组人群。
PAR定义为在研究开始时对下列任何一种抗原出现IgE ≥ 0.35 Ku/L的抗体反应,每种抗原均可导致PAR:烟曲霉、猫皮屑、尘螨(粉尘螨和屋尘螨)、狗毛屑、德国蟑螂或东方蟑螂。这个阈值提供了一个对受试者过敏致敏的适当的保守估计,故而为其他研究人员使用[26]。
正如在之前的文章中所描述的[5],所有纳入患者均需接受中高剂量ICS联合LABA治疗。患者按照1∶1∶1∶1∶1的比例进行随机分配,接受24周附加的治疗——每2周(q2w)或每4周(q4w)皮下注射一次dupilumab 200或300 mg,或安慰剂。在本次分析中,只报告了接受安慰剂或每两周注射200或300 mg dupilumab的意向治疗人群的数据;这部分剂量的dupilumab目前正在进行3期临床研究(NCT02414854)。
研究期间允许的合并用药包括抗组胺剂和访视1前30 d使用稳定剂量的鼻内激素,除非用于治疗哮喘的急性发作,不得使用全身性(口服或注射)皮质激素,不得使用以下药物:茶碱类(如茶碱和氨茶碱);脂氧合酶抑制剂(如齐留通);色酮;抗IgE治疗(如omalizumab);生物治疗;甲氨蝶呤;访视前3个月开始的过敏原免疫治疗;静脉注射免疫球蛋白治疗。
1.2 研究结果及过程
在之前的文章里已经描述并报道了全部研究患者的主要终点指标和次要终点指标[5]。
在这次分析中,我们使用22项鼻腔鼻窦指标测试(22-item Sino-Nasal Outcome Test,SNOT-22)来评估dupilumab对鼻炎相关症状的影响。SNOT-22是一项已经经过验证的患者自评结果的工具,用于测评鼻窦疾病的存在和严重程度以及这些疾病对健康相关生活质量的影响;评分包括了22项症状的严重程度和发生的频率[26]。 每项症状的评分是6分制,得分越高,表示病情越重(例如,0=“没问题”,5 =“病情很严重”)。总分是22项评分的总分,表明鼻窦总体健康的状况(范围0~110)。在SNOT-22的22项评分中,以下症状通常是与AR相关的典型症状:鼻后分泌物、鼻塞、流鼻涕和打喷嚏[12]。
本研究主要终点指标是检测在并发及无并发PAR的哮喘患者中,从基线到24周治疗结束后SNOT-22的总分变化及与AR相关的典型症状的评分变化。其他终点指标包括dupilumab 对从基线到24周治疗结束后FEV1(L)变化的影响,以及24周治疗期间哮喘重度急性发作的折合年率。哮喘的重度急性发作定义为哮喘恶化需要使用全身糖皮质激素至少3天,或住院或需要使用全身糖皮质激素治疗的急诊就诊。
因为SNOT-22已经在慢性鼻-鼻窦炎患者中得到验证,而在鼻息肉患者中还未得到验证,过去有鼻息肉病史或现在患有鼻息肉的患者被排除在分析之外,以避免任何可能的混杂效应[26]。鼻息肉的病理基础与PAR无关,合并鼻息肉的患者可能对PAR的评估产生影响。
1.3 统计分析
在本次析因分析中,没有对I型错误进行控制。治疗后P≤ 0.05被认为有统计学意义。
连续终点变量(第24周治疗的SNOT-22和FEV1) 采用重复测量方法的混合效应模型进行分析。该模型包括从基线到第24周的变化作为反应变量,以及治疗的因素(固定效应),基线血嗜酸性粒细胞的水平,国家/地区,随访次数,逐次治疗的相互作用,基线值和逐次治疗与基线的相互作用。缺失的数据没有被计算在内。
全身性糖皮质激素(口服或注射)仅可用于哮喘急性发作的治疗。在这种情况下,任何在激素使用过程中收集到的FEV1 或者SNOT-22都被排除在数据分析之外,以减少全身性糖皮质激素的混杂效应。
以第一次给药日期至最后一次给药日期加上14天之间发生重度急性发作事件的总数作为反应变量,使用负二项回归模型得出24周治疗期间发生的哮喘重度急性发作事件的年发生率。以治疗组、基线嗜酸性粒细胞水平、国家或地区、研究前一年哮喘急性加重事件的数量作为协变量,以治疗时间的对数作为位移变量。
在安全集中研究治疗中出现的突发不良事件(treatment-emergent adverse events,TEAEs)。安全集定义为:患者被随机分配接受1种或1种以上的剂量或部分剂量临床研究药物,最终根据实际接受的药物的情况进行分析,这部分实际接受了临床研究药物治疗的人群为安全集。
所有分析均使用SAS 9.2版本(SAS Institute Inc, Cary, NC)。
2 结果
2.1 基线人口统计学和临床特征
从2013年6月到2014年6月,776名患者被随机分配到NCT01854047研究的5个分组中。在这些患者中,465名患者被分配到每两周dupilumab治疗组(200 mg,n=150;300 mg,n=157)或对照组(n=158)(图1)。共有73名有鼻息肉病史或目前患有鼻息肉的患者被排除在分析之外,以排除重叠症状造成的混杂效应。
根据对常见PAR变应原的IgE抗体阳性反应,241例(61.5%)患者被确定为并发有PAR。结果分析的总人数为392例(并发PAR的患者有241例,无PAR的患者有151例)(图1)。
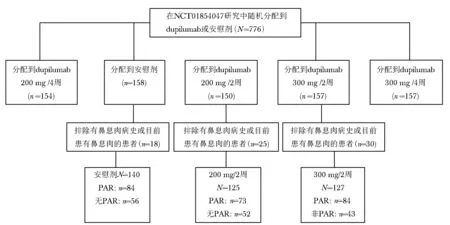
图 1 CONSORT图
是否并发PAR的患者基线特征见表1。总体而言,在意向治疗人群中哮喘患者多为女性(68%);然而,男性患者中并发PAR的比例更高。与无PAR组相比,PAR组中亚洲人、黑人或非洲裔美国人的比例更高,尽管每个亚组的人数都较少; PAR组中并发AR的人数更多;PAR组患者的哮喘确诊时间相对更晚。SNOT-22总分在PAR组中低于无PAR组,这可能是因为SNOT-22评估的项目中还包括与AR无关的项目。两组患者之间没有观察到其他有意义的差异。总体研究人群的基线特征(包括采用每4周治疗一次的治疗方案的患者)在之前的文章中已经报道过了[5]。
2.2 疗效
与安慰剂相比,每两周300 mg dupilumab在治疗的第24周显著改善了PAR患者的SNOT-22总分(最小二乘平均差,-5.98;95%CI,-10.45~-1.51;P=0.0088;图2;参见本文在线存储库www.jacionline.org中的表E1)。每两周200 mg dupi-lumab治疗后,SNOT-22总分有改善但下降的幅度不如300 mg组明显,与安慰剂相比差异无统计学意义(P=0.4426)。在无PAR的患者中,不同剂量每两周dupilumab治疗后的SNOT-22总分与安慰剂相比无差异。
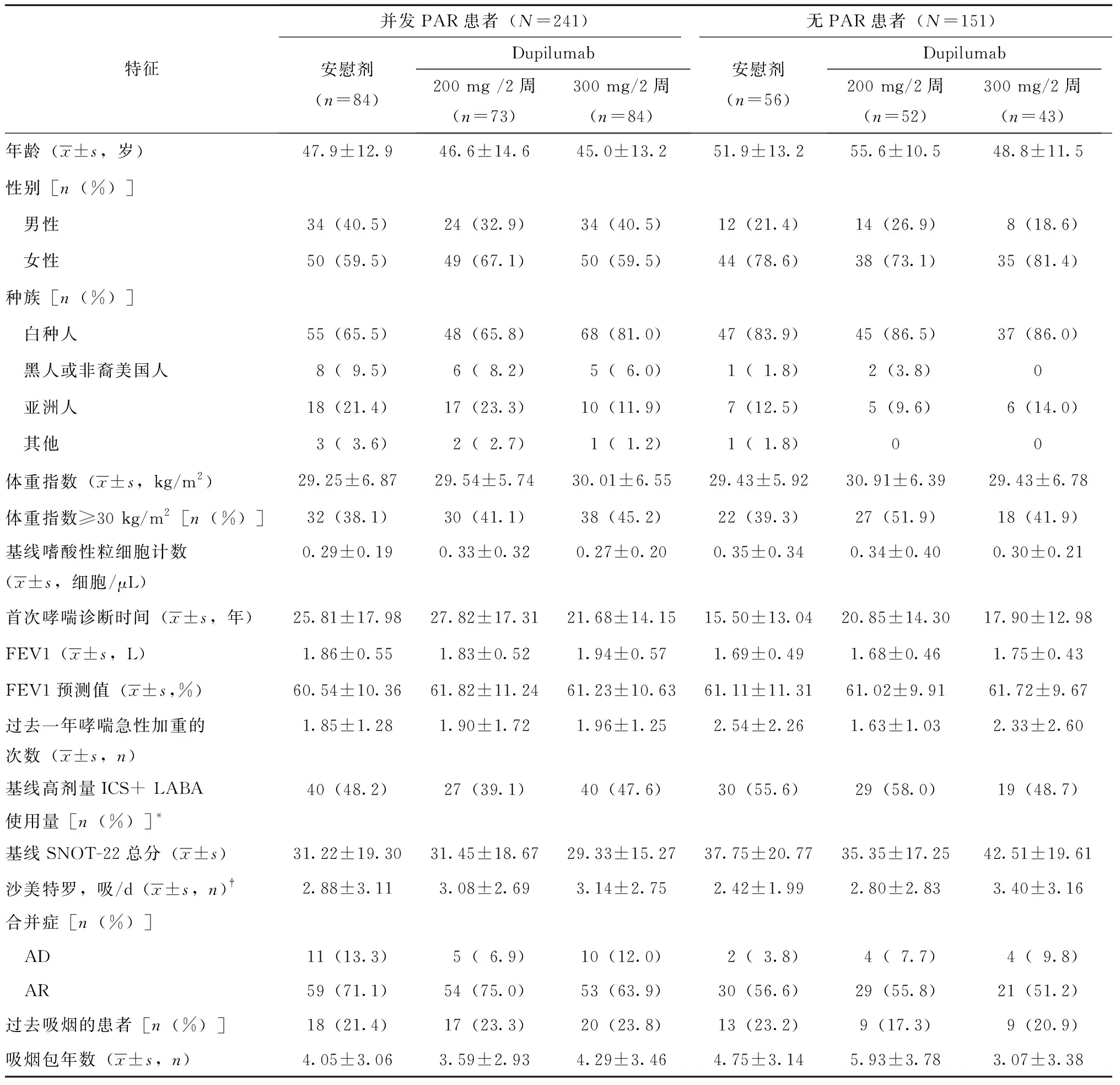
表1 按PAR分组的基线特征
与安慰剂相比,每两周300 mg dupilumab治疗后显著改善了PAR患者的4项AR相关的SNOT-22的评分(所有4项的P值均<0.01)(图2,表E1)。与安慰剂相比,24周治疗后的鼻塞症状评分改善了-0.60 (95%CI, -0.96~-0.25)(比基线降低48.5%),流涕症状评分改善了-0.67 (95%CI,-1.04~-0.31)(比基线降低57.1%),喷嚏症状评分改善了-0.55 (95%CI, -0.89~-0.21)(比基线减少46.5%),鼻后分泌物症状评分改善了-0.49 (95%CI, -0.83~ -0.16)(比基线减少52.2%)(图2;表E1)。在接受每两周200 mg dupilumab治疗的患者中,4项症状的评分都没有观察到明显的改善。在无PAR的患者中,dupilumab治疗后与AR相关的4项症状评分与安慰剂相比无差异。
在肺功能方面,每两周300 mg dupilumab治疗24周后,PAR患者中FEV1预计值比基线提高了12.9%,FEV1绝对值比安慰剂组明显提高了平均0.13L (95%CI, 0.01~ 0.25;P=0.0337)(表2)。每两周200 mg dupilumab治疗后也同样观察到FEV1绝对值的升高 (0.10 L;95%CI,-0.03~0.22;P=0 .1256)(表2),但与安慰剂比较无统计学意义。每两周200 mg dupilumab治疗24周后,无PAR患者中FEV1预计值比基线显著提高了19.0%,FEV1绝对值比安慰剂增加0.15 L (95%CI,0.01~0.30) (P=0.0403)(表2)。在每两周300 mg dupilumab治疗后的无PAR的患者中,FEV1与安慰剂相比无明显差异(0.08 L;95%CI,-0.08~0.23;P=0.3310)(表2)。
在24周治疗期间,与安慰剂相比,每两周dupilumab 300 mg治疗显著降低了PAR患者哮喘重度急性发作的折合年率(风险降低51.7%;P=0.0373)。每两周200 mg dupilumab治疗也同样降低了患者重度急性发作的风险,但无统计学意义 (风险降低51.5%;P=0.0506)(表3)。在无PAR的患者中,每两周200和300 mg dupilumab治疗后与安慰剂相比显著降低了哮喘重度急性发作的折合年率(每两周200 mg组风险降低:83.0%,P=0.0002;每两周300 mg组风险降低:76.8%,P=0.0012)(表3)。
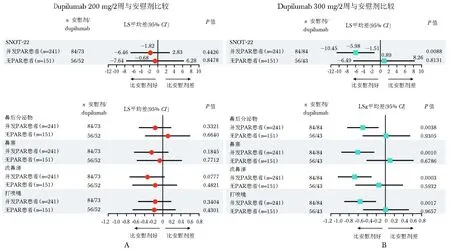
图 2 无论是否合并PAR的哮喘患者,在第24周SNOT-22总分和与PAR相关的症状评分的最小二乘平均值和95% CI,每两周200 mg dupilumab与安慰剂相比(A)和每两周 300 mg dupilumab与安慰剂相比(B);负值表示鼻部症状有更好的改善;LS,最小二乘法
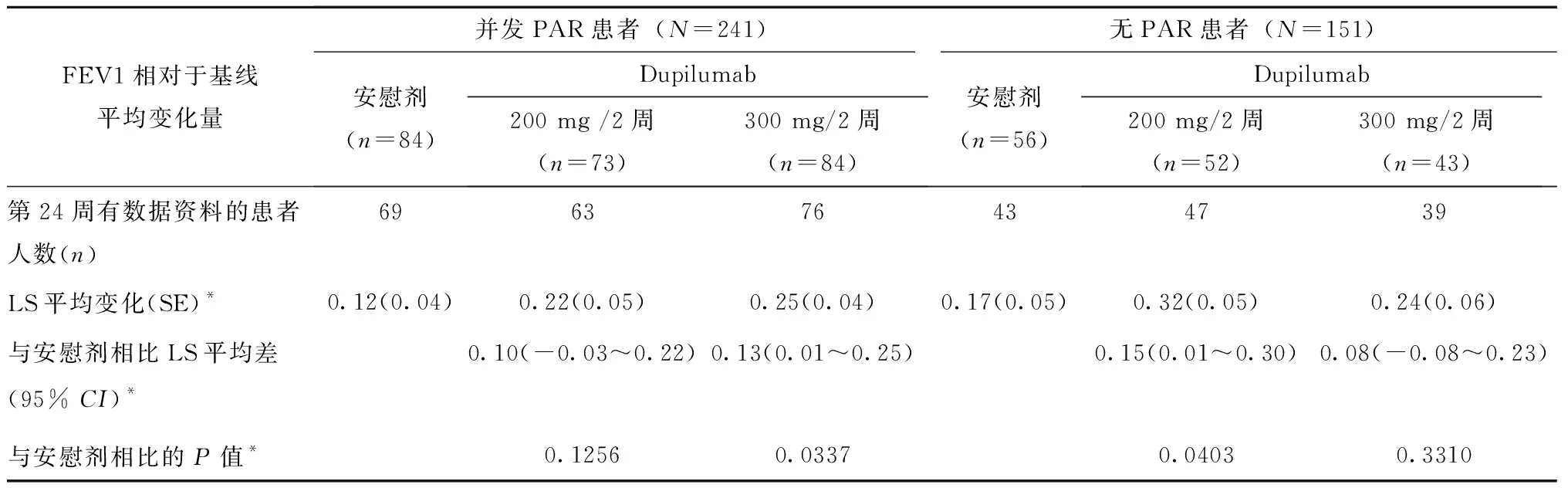
表2 并发或无PAR的哮喘患者FEV1在第24周相对于基线水平的变化
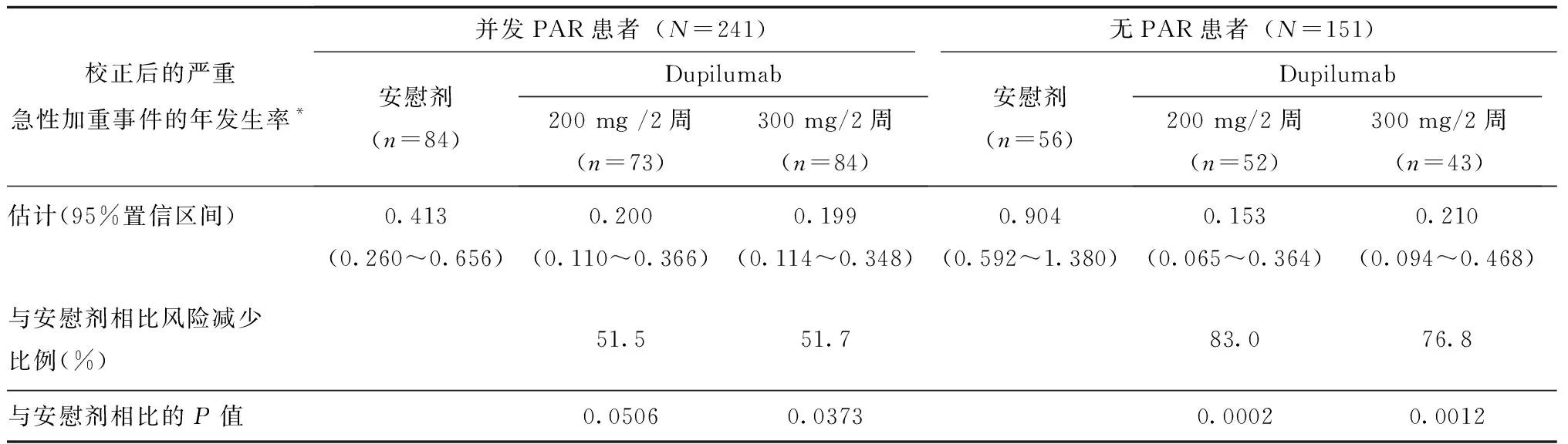
表3 按有无PAR分组的哮喘重度急性加重事件的年折合率
2.3 安全性
之前的文章已经报道了总体研究人群的安全数据[5];简而言之,dupilumab的耐受性普遍很好,不同治疗组TEAEs的发生率基本相似(dupilumab 治疗组75%~ 83%,安慰剂75%)。
在本次分析中,无论有无PAR,不同治疗组的患者TEAEs的发生率相似(表4)。TEAEs (首选术语)中发生在10%或以上的PAR患者,且相较于安慰剂更频繁地发生在接受每两周dupilumab治疗的安全人群中的症状为:头痛(dupilumab,9.5%~16.4%;安慰剂,7.1%)和注射部位红疹(dupilumab,17.8%~20.2%;安慰剂,8.3%)。TEAEs发生在10%或以上的无PAR患者,且相较于安慰剂更频繁地发生在接受每两周dupilumab治疗的安全人群中的症状为:注射部位红疹(dupilumab,10.0%~26.2%;安慰剂,8.9%)。根据有无PAR进行分组,注射部位反应(高级术语)发生的比率列于表4。
3 讨论
我们的数据是基于提出的假设进行分析的, 在持续性控制不佳哮喘合并PAR的患者中,中高剂量ICS+LABA 加用每两周300 mg dupilumab治疗显著改善了PAR的症状 (SNOT-22中鼻炎相关的症状得分和SNOT-22总分)。这是一项重要的发现, 因为合并AR会恶化整体哮喘的控制[8,27]。
此前尚无dupilumab治疗合并PAR的哮喘患者的数据。在此之前,抗IgE抗体omalizumab的治疗已被证实可以有效预防哮喘加重,并改善过敏性哮喘合并持续性AR患者的生活质量[28]。 Dupilumab已经被证实在其他的两种2型免疫介导疾病中的有效性:过敏性皮炎(AD)[24](已获得批准)和慢性鼻-鼻窦炎合并鼻息肉(CRSwNP)(在基于概念验证的研究中得到证实)[25]。本次dupilumab治疗后析因分析的研究结果(即PAR患者疗效的证据),以及AD和CRSwNP患者的疗效证据,支持这一理念,即以整体方式识别和治疗2型免疫疾病患者。
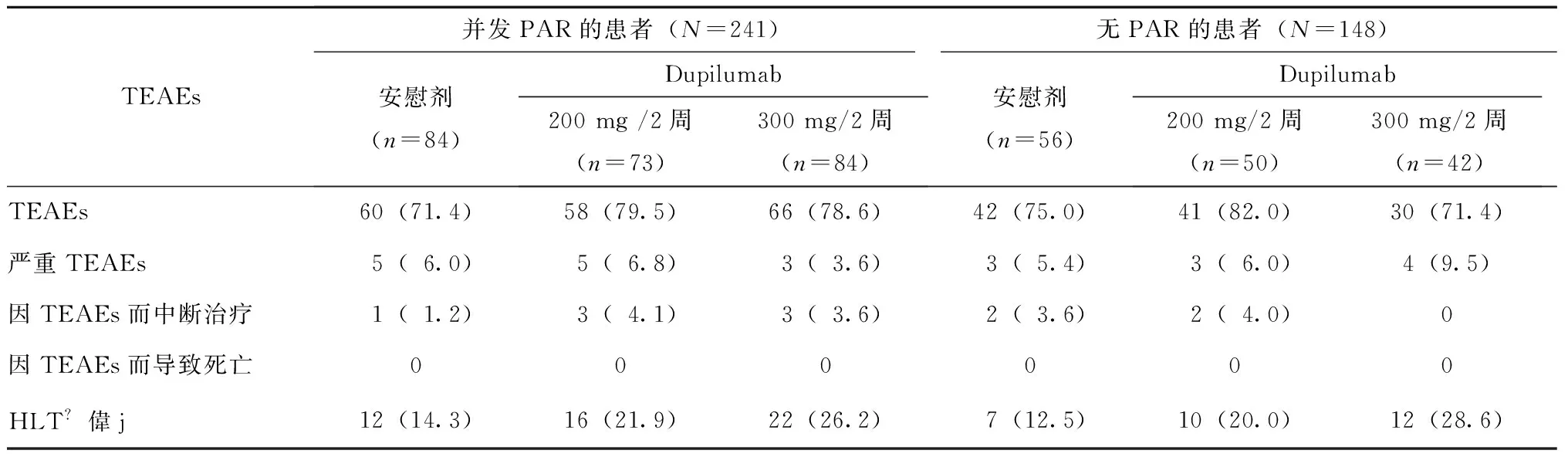
表4 安全集TEAEs概况[n(%)]
另外,dupilumab改善了PAR和无PAR患者的肺功能,且降低了哮喘急性发作的发生率。这些发现与之前报道的总体研究人群的研究结果一致[5]。
意料之中的是,AR相关症状评分在无PAR的患者中与安慰剂相比无差异。这是可以预料的,因为通常缺乏这种并发症的患者不大可能出现治疗后PAR典型症状的明显差异。甚至,这些发现从内部进一步证实总体的结果因为治疗(在每两周300 mg治疗下)后PAR患者在AR症状方面改善的效果比无PAR患者更好。这些数据表明,dupilumab通过双重阻断2型炎症的关键驱动因子,可能有利于治疗哮喘患者并发PAR——哮喘最常见的2型相关并发症之一[4]。的确,哮喘并发症的治疗应当得到更多的关注。
在最大剂量dupilumab (即每两周300 mg)治疗后鼻部症状得到持续且显著地改善,而在200 mg治疗下没有观察到与安慰剂组的差异。这表明,至少在并发PAR的患者中,每两周300 mg 是最有效的剂量。
与安慰剂相比,每两周300 mg dupilumab 也显著改善了PAR患者的肺功能(FEV1),并减少了哮喘重度急性发作的发生。这些发现与每两周治疗后显著改善了肺功能和哮喘急性发作的发生率这一结果相一致,在整体研究人群和亚组(基线嗜酸性粒细胞≥300/μL或<300/μL)中都观察到了这一结果[5]。如前所述,这些改善在两组患者的24周治疗期间都得到了维持,进一步证实了dupilumab同时对IL-4和IL-13信号的抑制在治疗效果不佳的持续性哮喘中发挥了重要作用,无论患者是否并发有PAR。
在本研究中,392名接受dupilumab(每两周200或300 mg)或安慰剂治疗的患者中,有241例(61%)患者并发有PAR。此前有报道估计75%~100%的哮喘患者并发有AR[6-8];实际上,讨论组认为哮喘并发AR的患者仍诊断不足,提议患有两者中任何一种疾病的患者都应该评估是否并发另一种疾病[6]。
以往的研究表明,哮喘并发AR的患者的预后比无AR的患者更差,对医疗资源的占用率也更高[29]。这部分并发AR的哮喘患者代表了一个亚群,他们对于除了ICS+LABA方案基础上的附加治疗的需求未得到满足。
与总体研究人群中观察到的情况一致,治疗后TEAEs的发生率在并发PAR与无PAR的患者中相似,表明dupilumab在这些患者中耐受性良好,安全性可接受。
本次研究有一些局限性。这项研究是事后的析因分析。PAR在研究开始时被定义为对典型的常年抗原有特异性应答(IgE ≥0.35 Ku/L),严格来说,这项定义指出的是过敏原致敏而不是PAR本身的存在。此外,基于以上PAR和无PAR的定义,季节性AR患者可能会包含在PAR患者或无PAR患者中(~50%按照本次分析定义为无PAR的患者,在并发病史中提及有AR)。本研究未对鼻内使用皮质类固醇或抗组胺药物进行系统监测,因此这些药物使用对结果的影响尚不清楚。SNOT-22评分在慢性鼻-鼻窦炎(CRS)患者中已经得到验证[30],然而在哮喘并发PAR的患者中并未得到验证,因此,在PAR患者中该评分有临床意义的最小分值差异尚不清楚。另外,少数CRS患者包括在亚组分析中(PAR患者:安慰剂,n=11;每两周200 mg dupilumab,n=9;每两周300 mg dupilumab,n=10。无PAR患者:安慰剂,n=3;每两周200 mg dupilumab,n=5;每两周300 mg dupilumab,n=6)。然而,考虑到涉及的人数很少,如果排除这部分患者,结果也不太可能有明显的不同。SNOT-22评分并不是评估AR症状控制的有效工具;然而,其中部分项目的评分评估的是AR的典型症状。因此,本文可以作为未来大样本的前瞻性研究的基础。目前,正在控制不佳的持续性哮喘患者中进行每两周不同剂量dupilumab的3期临床试验(NCT02414854)。
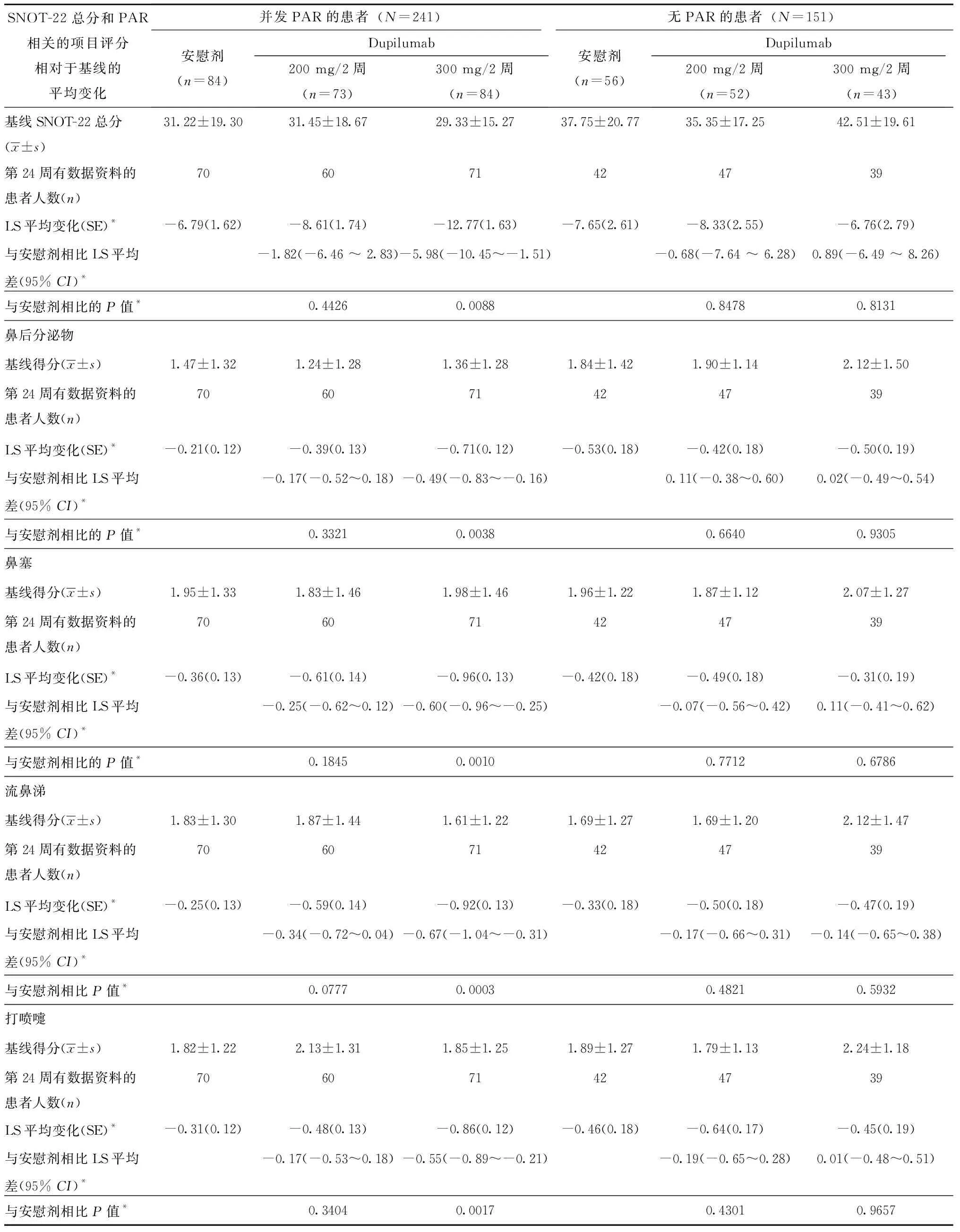
表E1 在并发或无PAR的哮喘患者中,在第24周的SNOT-22总分和与PAR相关的项目评分相对于基线的变化
结论
AR是一种常见且经常治疗不足的疾病,常并发哮喘且有可能加重哮喘症状。在本次分析中,ICS+LABA联合每两周300 mg dupilumab治疗通过显著改善控制不佳的持续性哮喘并发PAR患者的鼻部症状而表现出潜在的优势。每两周300 mg dupilumab治疗也明显改善了4项与AR相关的症状评分:鼻后分泌物,鼻塞,流鼻涕,打喷嚏。然而在每两周200 mg dupilumab治疗后的患者中,与安慰剂相比未观察到评分的差异。
与之前的报道一致,dupilumab作为中高剂量ICS+LABA的附加治疗,在改善控制不佳的持续性哮喘并发PAR患者的肺功能(FEV1)的同时,减少了哮喘重度急性发作的发生率,且改善了上呼吸道 (鼻部)的症状。
这些数据表明,dupilumab(每两周300 mg)作为中高剂量 ICS +LABA的附加疗法可能在控制不佳的持续性哮喘并发PAR患者中起到缓解鼻部症状的作用。未来需要更多研究调查dupilumab在这组患者人群中的作用。
临床意义
在哮喘并发鼻炎的患者,一种选择性的免疫调节剂全身治疗可以同时改善过敏性鼻炎和未控制的持续性哮喘。
参考文献请见原文:
J Allergy Clin Immunol,2018,142:171-177.
专家点评
刘春涛四川大学华西医院呼吸内科
赛诺菲和再生元制药公司研发的抗IL-4受体α亚基的单克隆抗体dupilumab通过拮抗IL-4/IL-13,抑制Th2介导的变应性哮喘。一项在大剂量ICS/LABA哮喘患者中进行的2b期临床研究(NCT01854047)取得了良好的临床疗效,其结果已经发表。本文是对这项研究的数据进行事后分析,评估dupilumab在哮喘患者并发常年性变应性鼻炎(PAR)亚组中的疗效。入选的776例患者,随机按1∶1∶1∶1∶1分到dupilumab组(200 mg、300 mg,每两周一次、每四周一次)和安慰剂。本文仅分析了每两周dupilumab组和安慰剂组的区别。主要终点指标是治疗24周后,与安慰剂相比,22项鼻腔鼻窦指标测试(SNOT-22)的总分及其中变应性鼻炎症状评分的改善情况。SNOT-22总分在PAR患者中改善情况,dupilumab 200 mg、dupilumab 300 mg中分别为-1.82和-5.98。鼻炎症状评分在300 mg dupilumab后的改善情况,鼻塞、流鼻涕、打喷嚏、鼻后分泌物分别为-0.60、-0.67、-0.55、-0.49。鼻炎症状评分在200 mg dupilumab后的改善情况不如300 mg的治疗。在无PAR的患者中,dupilumab与安慰剂治疗后在这些评分上无差异。次要指标之一为肺功能的改善情况,FEV1在PAR+200 mg dupilumab、PAR+300 mg dupilumab、无PAR+200 mg dupilumab、无PAR+300 mg dupilumab组中分别升高0.10、0.13、0.15、0.08 L。另一次要指标为哮喘重度急性加重风险,在PAR+200 mg dupilumab、PAR+300 mg dupilumab、无PAR+200 mg dupilumab、无PAR+300 mg dupilumab组中分别降低51.5%、51.7%、83.0%、76.8%。dupilumab的耐受性良好。PAR+dupilumab组最常见的不适症状是头痛和注射部位红疹;而在无PAR+dupilumab组是注射部位红疹。本文分析提示,鉴于过敏性哮喘患者并发过敏性鼻炎非常常见(可高达80%),而哮喘和鼻炎又存在共同的免疫学机制,因此凡是阻断Th2反应的生物制剂,在治疗重度过敏性哮喘的同时,对过敏性鼻炎也会产生额外的获益,而在选择dupilumab治疗对象时,并发常年性过敏性鼻炎的重度哮喘可作为优先考虑。

刘春涛
四川大学华西医院呼吸内科教授,主任医师,博士研究生导师,呼吸内科医疗副主任,四川省学术与技术带头人,中国呼吸医师协会副会长、医学人文工委会主任,中国变态反应医师协会副会长,中华医学会变态反应分会常委、呼吸学组组长,中华医学会呼吸病学分会哮喘学组成员,四川省呼吸医师协会会长,四川省医学会呼吸专委会副主任委员 哮喘学组组长,中国基层呼吸防治联盟副主席,四川省哮喘联盟主席,四川省基层呼吸防治联盟主席,《中国呼吸与危重监护杂志》主编。研究方向:呼吸系统变态反应性疾病
