氢化物发生原子荧光光谱法测定绿豆中砷的测量不确定度评定
2018-12-14
(西安海关(原陕西出入境检验检疫局),西安 710068)
1 概述
砷是一种类金属元素,具有较高的生物毒性,以化合物形式广泛存在于地表、土壤、水、大气、食物及生物体内[1,2]。2017年9月发布实施的《GB 2762—2017食品安全国家标准食品中污染物限量》要求,谷物及其制品中总砷限量为0.5 mg/kg[3]。对其含量进行准确测定在食品检测中很重要。目前,对食品中总砷的测定主要有电感耦合等离子体质谱法、氢化物发生原子荧光光谱法、银盐法等[4]。其中,《GB 5009.11—2014食品安全国家标准食品中总砷及无机砷的测定》中总砷的测定第二法即采用氢化物发生原子荧光光谱法。氢化物发生原子荧光光谱法测定微量砷含量的分析方法具有灵敏度高、重现性好、简便易操作的特点,是砷含量分析的主要方法[5]。
在实验室检测过程中,分析结果往往具有误差而不能得到真值。为评价测定结果的质量,衡量测定条件和方法是否可靠,实验室需要找出影响测定结果质量的因素。测量不确定度(Measurement uncertainty)是根据所用到的信息,表征合理地赋予被测量之值的分散性,与测量结果相联系的非负参数[6,7]。目前,测量不确定度已经作为一个主要的指标和项目要求,被中国实验室认可委员会列入检测能力认可的指标之中[8]。
本文选取绿豆做样品,根据《JJF1059.1—2012测量不确定度评定与表示》[9],对氢化物发生原子荧光光谱法测定砷含量的各个环节和影响因素进行了考察,分析评估测量不确定度,找出影响其测量不确定度的主次因素,改善测量过程,有效减小误差,提高检测技术质量。
2 实验部分
2.1 砷测定依据
《GB5009.11—2014食品安全国家标准食品中总砷及无机砷的测定》第一篇总砷的测定第二法氢化物发生原子荧光光谱法。
2.2 仪器耗材
2.2.1 仪器
AFS-9130双道原子荧光光度计,由北京吉天仪器有限公司制造;电子天平:感量为0.1mg;控温电热板:50℃~200℃;高速粉碎机。
2.2. 2主要试剂耗材
砷标准储备液(1000mg/L,北京神州科创生物科技有限公司);硝酸(优级纯);高氯酸(优级纯);硫酸(优级纯);硼氢化钾(优级纯);硫脲(分析纯);抗坏血酸(优级纯)。
2.3 测定方法
2.3.1 样品制备
根据《GB/T 5009.1—2003食品卫生检验方法理化部分总则》[10]规定,制取绿豆样品,将均匀的绿豆随机取样磨粉。依据《GB 5009.11—2014食品安全国家标准食品中总砷及无机砷的测定》第一篇总砷的测定第二法氢化物发生原子荧光光谱法进行试验。
称取试样1.0g~1.2g(精确至0.001g),置于50mL锥形瓶中,同时做两份试剂空白。加硝酸20 mL,高氯酸4mL,硫酸1.25 mL,摇匀后放置过夜。置于电热板上加热消解。若消解液处理至1mL左右时仍有未分解物质或色泽变深,取下放冷,补加硝酸5~10 mL,再消解至2mL左右观察,如此反复两三次,注意避免炭化。继续加热至消解完全后,再持续蒸发至高氯酸的白烟散尽,硫酸的白烟开始冒出。冷却,加水25 mL,再蒸发至冒硫酸白烟。冷却,用水将内溶物转入25 mL容量瓶或比色管中,加入硫脲+抗坏血酸2mL,补水至刻度并混匀,放置30min,备测。按同一操作方法作空白。
2.3.2 仪器条件
负高压:260V;砷空心阴极灯电流60mA;载气:氩气;载气流速:400mL/min;屏蔽气:氩气,屏蔽气流速:800 mL/min;测量方式:荧光强度;读数方式:峰面积。
2.3.3 测量样品
以硼氢化钾为还原剂,将样品导入原子荧光光度计中,根据标准系列进行定量。
2.3.4 标准溶液制备
用1000μL可调移液器吸取1mL砷标准储备液(1000mg/L),逐级稀释定容到25mL容量瓶,制成50ng/mL砷标准工作液(标准系列仪器根据配制的50ng/mL砷标准工作液自动稀释)。
2.3.5 比较定量
待测样品与标准系列比较定量。
3 测量不确定度识别、分析及量化
3.1 建立数学模型
根据《GB 5009.11—2014食品安全国家标准食品中总砷及无机砷的测定》第一篇总砷的测定第二法氢化物发生原子荧光光谱法中总砷含量计算公式建立数学模型如下:
(1)
式中:
X:试样中总砷的含量,单位为毫克每千克(mg/kg)或毫克每升(mg/L);
C0:试样被测液扣除试剂空白消化液后总砷的浓度,单位为纳克每毫升(ng/mL);
V:试样消化液总体积,单位为毫升(mL);
m: 试样质量 (或体积) ,单位为克(g)或毫升(mL);
1000:换算系数。
3.2 测量不确定度识别
按照数学模型(1)以及方法概要,分析不确定来源主要有以下8个方面:
1)测量重复性引入的标准不确定度u0;
2)试样被测液扣除试剂空白消化液后总砷的浓度测定引入的标准不确定度u1(即校准曲线校准引入的不确定度);
3)试样定容引入的标准不确定度u2;
4)样品的质量测量不准引入的标准不确定度u3;
5)总砷标准储备液引入的标准不确定度u4;
6)稀释过程引入的标准不确定度u5;
7)取样引入的标准不确定度u6;
8)试剂空白引入的标准不确定度u7。
3.3测量重复性引入的标准不确定度u0
按照2实验部分方法对同一样品进行6次重复试验(表1),结果分别为:

表1 绿豆中砷含量的重复测定值
平均值为:As(mg/kg)=0.031 mg/kg
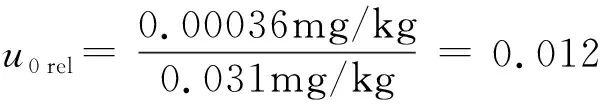
3.4 校准曲线校准引入的标准不确定度u1
制备5个不同浓度砷标准溶液,每个浓度用原子荧光光度计测3次,得到相应的荧光强度值A,用最小二乘法拟合,获得直线方程A=b×c+a及线性相关系数r,列于表2。
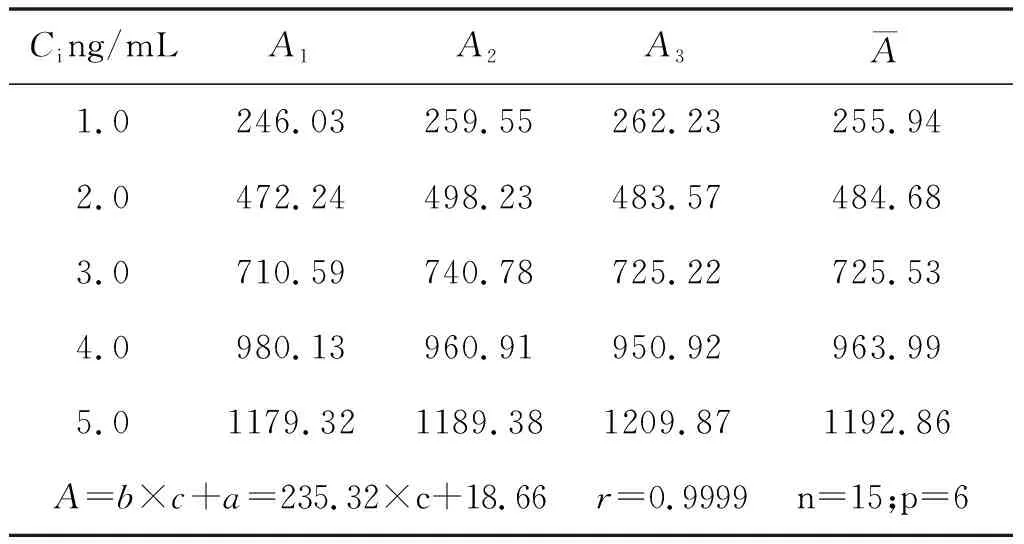
表2 总砷标准溶液c和荧光强度值A以及最小二乘法拟合直线
按照2 实验部分方法对样品测定液测量6次(p=6);其平均荧光强度值A为310.46,代入直线方程的样品浓度C0=1.24ng/mL,所需计算数据见表3。

表3 评估校准曲线校准引入的标准不确定度u1所需计算数据
校准曲线校准引入的标准不确定度
u1:从标准曲线求校准曲线校准引入的不确定度;
s1:标准溶液吸光度残差的标准差(贝塞尔公式);
p:样品溶液测定次数;
n:标准系列测定次数;
a:标准曲线的截距;
b:标准曲线斜率;
C0:试样被测液扣除试剂空白消化液后总砷的浓度,单位为纳克每毫升(ng/mL);

ci:标准溶液系列总砷的浓度,单位为纳克每毫升(ng/mL);
Ai:标准系列溶液的荧光强度测定值。
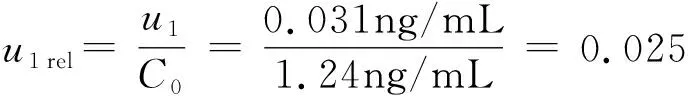
3.5 试样定容引入的标准不确定度u2

本实验在20℃进行,温度对体积的影响可忽略。
3.6 样品的质量测量不准引入的标准不确定度u3

≈0.00289
3.7 砷标准储备液引入的标准不确定度u4
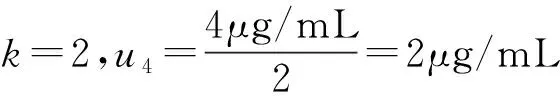
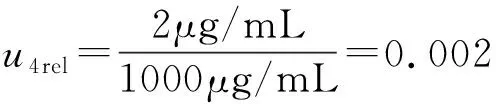
3.8 稀释过程引入的标准不确定度u5
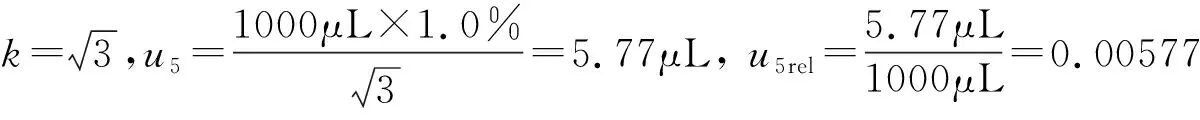
3.9 取样引入的标准不确定度u6
绿豆样品的制取符合《GB/T 5009.1—2003食品卫生检验方法理化部分总则》规定,将均匀的绿豆随机取样磨粉,取样不确定度可忽略。
3.10 试剂空白引入的标准不确定度u7
使用优级纯硝酸,符合《GB 5009.11—2014食品安全国家标准食品中总砷及无机砷的测定》的要求,因此,扣除空白导致的总砷的微小变化产生的影响可忽略。
3.11 计算合成标准不确定度uc
各不确定度分量值见表4。
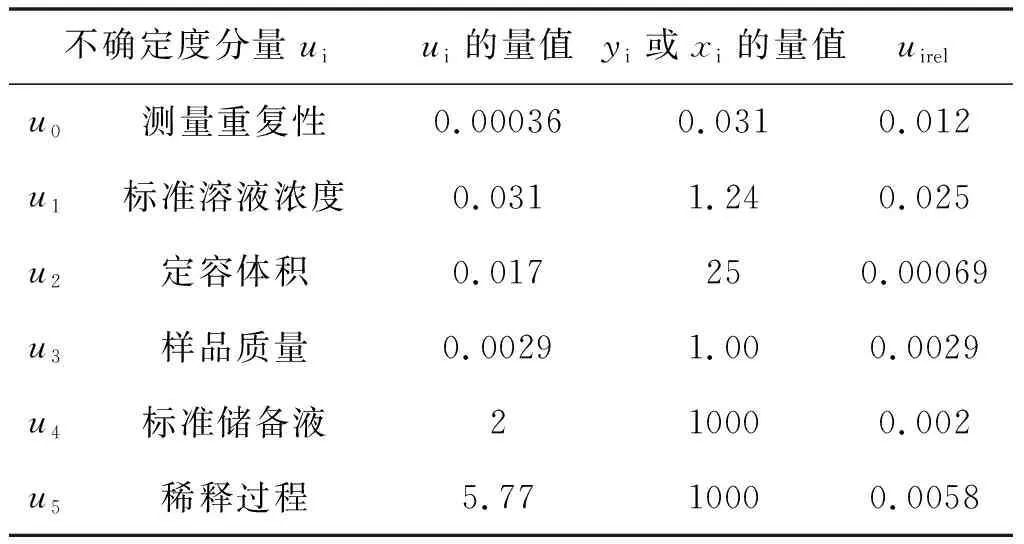
表4 各不确定度分量值
uc=0.031 mg/kg×0.029=0.00090 mg/kg
3.12 计算扩展不确定度U
根据《JJF 1059.1—2012 测量不确定度评定与表示》, 在一般情况下, 取k=2, 置信水平为0.95, 计算扩展不确定度:
U=k×uc=2×0.00090 mg/kg=0.0018 mg/kg
3.13 结果表示
X=0.031mg/kg,U=0.002mg/kg,k=2。
4 结论
综上,影响氢化物发生原子荧光光谱法测定绿豆中砷的测量不确定度的主要因素是原子荧光强度,其它如样品称量、标准物质的配制、量器精确度等是对其测定不确定度的影响是次要的。
