副猪嗜血杆菌高密度发酵工艺研究
2018-12-10耿笑林张浩浩翟路峰李向东黄玉欣田克恭
耿笑林,张 翼,刘 鹏,张浩浩,翟路峰,李向东,黄玉欣,田克恭
(国家兽用药品工程技术研究中心,河南 洛阳 471003)
副猪嗜血杆菌病又称多发性纤维素性浆膜炎和关节炎,也称格拉泽氏病,是由副猪嗜血杆菌引起的一种严重危害各年龄猪群的细菌性传染病[1]。按照常规血清分型方法,可以将副猪嗜血杆菌分为 15 种血清型, 其中 1、5、10、12、13 型毒力最强,我国以血清4型和血清5型流行为主[2]。采用我国普遍流行血清型菌株(4、5型)研制的灭活疫苗是预防和控制该病的最有效方法[3]。目前,国内副猪嗜血杆菌疫苗还是采用传统的分离病原菌菌株,通过固体平板培养、灭活制备,该方法获得的疫苗价格较为昂贵,产量低,成本高[4],而采用液体发酵培养技术能很好地解决该问题[5]。由于副猪嗜血杆菌比较脆弱,对营养要求严格,在体外培养容易死亡,因此,其在体外培养时,培养基的营养成分、培养时间和保存方式等是开展副猪嗜血杆菌相关试验的关键因素[6]。
高密度发酵可有效提高抗原产量和培养基的利用率,大幅度降低生产成本,显著缩短生产周期,降低劳动强度,提高生产效率[7],为副猪嗜血杆菌灭活疫苗的生产提供了一种新的有效可行的抗原制备工艺。该研究通过利用高密度发酵技术,培养副猪嗜血杆菌血清4型JS株和血清5型ZJ株,并制备二价灭活苗抗原,以期为国内副猪嗜血杆菌流行菌株血清4型和5型二价灭活疫苗的规模化生产提供理论依据。
1 材料与方法
1.1 试验材料
1.1.1 主要试剂及设备:TSA培养基 (BD公司),TSB 培养基(BD 公司),BHI培养基(BD 公司),酵母提取物(OXOID),胰蛋白胨(OXOID),NaCl(天津凯通),葡萄糖(国药试剂),辅酶Ⅰ(NAD,上海生工),维生素(上海生工),新生牛血清(浙江杭州四季青),204 消泡剂(Sigma),微量元素,HCl、NaOH。
IC222 EXCELLA恒温培养箱购自德国Medcenter Einrichtungen公司,E24R恒温培养振荡器购自NBS公司,6132核酸蛋白测定仪购自德国Eppendort,10JS-7000C型发酵罐购自上海保兴生物工程有限公司,1 000 L发酵设备购自上海迪沃信生物工程有限公司。
1.1.2 试验菌株:副猪嗜血杆菌血清4型JS株和血清5型ZJ株冻干菌种由普莱柯生物工程股份有限公司国家兽用药品工程技术研究中心分离、鉴定、保存[8]。
1.1.3 培养基及试剂配制:TSA固体培养基、TSB液体培养基、BHI培养基、LB培养基,其他液体培养基及试剂按实验室常规方法进行制备。
1.2 试验方法
1.2.1 副猪嗜血杆菌生产用种子液的制备:取副猪嗜血杆菌血清4型JS株和血清5型ZJ株冻干菌种,分别用含0.05%的NAD和10%新生牛血清的TSB培养基溶解,划线接种于含0.05%的NAD和10%新生牛血清的TSA平板上,37℃培养24 h,挑选典型菌落,接种于含0.05%的NAD和10%新生牛血清的TSB培养基,37℃振荡培养12 h,取样经纯净检验合格后作为生产用种子。
1.2.2 不同培养基的筛选:对不同培养基TSB、BHI、LB在10 L发酵罐中进行发酵试验,按4%的接种量进行发酵罐接种,并添加10%血清和0.05%的NAD。设定搅拌速度为100~500 r/min,pH值通过添加HCl和NaOH控制在7.2~7.4,培养14 h。在培养 8、10、12、14 h 时取样进行活菌计数,测定不同培养基配方菌液中的活菌数和菌体密度(OD600nm值)。
1.2.3 TSB培养基的优化:在TSB培养基的基础上通过添加葡萄糖、大豆蛋白胨等对与副猪嗜血杆菌代谢相关的碳源、氮源进行优化。按4%的接种量进行发酵罐接种,添加10%血清和0.05%的NAD。设定搅拌速度为100~500 r/min,pH值通过添加HCl和NaOH控制在7.2~7.4,37℃培养14 h。在培养 8、10、12、14 h 时取样进行活菌计数,测定不同培养基配方菌液中的活菌数和菌体密度(OD600nm值)。
1.2.4 血清添加量的优化:对优化TSB培养基的血清添加量按照2%、5%、8%、10%进行调整,并通过批次添加和流加相结合的方式增加补料工艺,补料培养基成分为葡萄糖、血清、TSB、NAD、维生素、微量元素等。按4%的接种量进行发酵罐接种,并添加0.05%的NAD。设定搅拌速度为100~500 r/min,pH值通过 HCl和 NaOH控制在 7.2~7.4,37℃培养14 h收获,测定不同血清添加量情况下菌液中的活菌数和菌体密度(OD600nm值)。
1.2.5 副猪嗜血杆菌在1 000 L发酵罐中的培养:根据上述试验的测定结果,按照最优发酵工艺进行1 000 L发酵试验。按4%的接种量进行发酵罐接种,并添加5%血清和0.05%的NAD。设定搅拌速度为 100~500 r/min,pH值通过添加 HCl和NaOH控制在7.2~7.4,37℃培养14 h收获,测定不同血清添加量情况下菌液中的活菌数和菌体密度(OD600nm值)。连续3批次副猪嗜血杆菌血清4型 JS株发酵抗原编号为 K1809001、K1809002、K1809003,连续3批次副猪嗜血杆菌血清5型JS株发酵抗原编号为K1809004、K1809005、K1809006。
1.2.6 副猪嗜血杆菌二价灭活疫苗的制备:用自制水性佐剂按10%的比例与不同批次副猪嗜血杆菌血清4型JS株和5型ZJ株灭活抗原充分搅拌混匀[9],制成3批副猪嗜血杆菌二价灭活疫苗,具体见表1。3批疫苗中副猪嗜血杆菌血清4型JS株和5型ZJ株抗原含量均为2.0×109CFU/mL。
1.2.7 副猪嗜血杆菌二价灭活疫苗效力评价试验:将40只5~7周龄豚鼠随机分为4组,每组10只。第1~3组分别免疫3批副猪嗜血杆菌二价灭活疫苗,后腿肌肉注射,0.5 mL/只,另外设1个空白对照组。首免后21 d,按相同途径、相同剂量进行二免,二免后14 d采血。采用微量凝集方法检测二免后14 d豚鼠血清中副猪嗜血杆菌血清4型和5型抗体效价。判定标准如下:免疫组10只豚鼠血清中副猪嗜血杆菌血清4型抗体几何均值不低于1∶16,血清5型抗体几何均值不低于1∶32判为合格,否则判为不合格。

表1 不同批号疫苗的抗原组成及佐剂含量
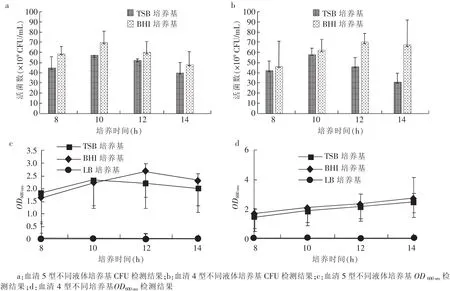
图1 不同液体培养基中副猪嗜血杆菌生长情况检测结果
1.2.8 检测方法
1.2.8.1 菌体浓度测定:利用6132核酸蛋白测定仪在600 nm处测定其吸光度。
1.2.8.2 发酵液活菌计数:按《中华人民共和国兽药典(2010年版)》进行发酵液活菌计数,计算菌落形成单位(CFU)。
1.2.8.3 发酵液纯粹检验:培养结束后取样,根据《中华人民共和国兽药典(2010年版)》附录对样品进行纯粹检验,结果应为纯粹。
2 结果与分析
2.1 不同液体培养基对副猪嗜血杆菌生长情况的影响结果
培养结果表明,副猪嗜血杆菌在LB培养基中不生长,在TSB和BHI培养基中均可生长,差异不显著(见图1)。考虑到BHI培养基的价格明显高于TSB培养基,因此,选定TSB培养基作为后续优化用基础培养基。
2.2 优化TSB培养基对副猪嗜血杆菌生长情况的影响结果
通过对TSB培养基添加葡萄糖、大豆蛋白胨等进行优化,结果表明,副猪嗜血杆菌在优化后的TSB培养基中的生长情况显著由于优化前 (见图2),因此,选定优化TSB培养基作为后续发酵用培养基。
2.3 不同血清添加量对副猪嗜血杆菌生长情况的影响结果
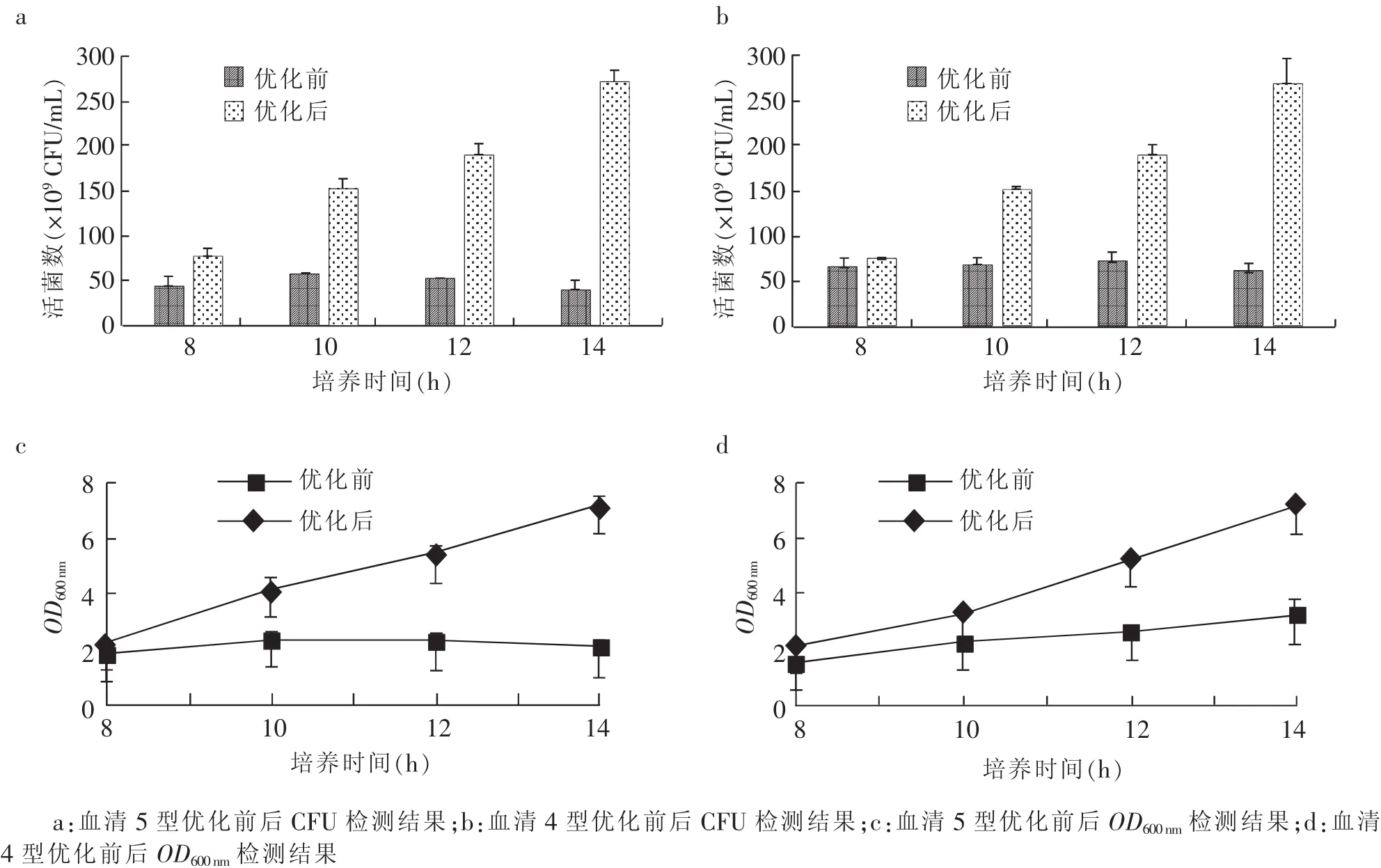
图2 TSB培养基优化前后副猪嗜血杆菌生长情况检测结果
血清在副猪嗜血杆菌抗原生产中占主要成本,优化血清的添加量可以显著降低副猪嗜血杆菌抗原生产成本。通过补料工艺优化,结果表明,副猪嗜血杆菌在血清添加量为5%、8%、10%的情况下活菌数差异不显著,当血清的添加量降低至2%时活菌数显著降低(见图3),因此,选择5%的血清添加量作为后续发酵添加量。
2.4 最优培养条件下副猪嗜血杆菌连续3批次的1 000 L发酵结果
根据上述最优的发酵工艺,对副猪嗜血杆菌进行1 000 L生产规模的发酵试验,结果表明,血清4型JS株和血清5型ZJ株的活菌数和菌体密度OD600nm与10 L发酵罐结果差异不显著 (见图4),提示可进行生产规模放大,用于二价灭活苗的抗原发酵。
2.5 副猪嗜血杆菌二价灭活疫苗效力评价试验结果
利用微量凝集方法检测二免后14 d豚鼠血清中的副猪嗜血杆菌血清4型和5型抗体效价。由表2和表3可知,3批疫苗免疫组 (第1~3组)二免后14 d豚鼠血清中的副猪嗜血杆菌血清4型抗体几何均值均大于1∶16,血清5型抗体几何均值均大于1∶32,表明3批疫苗均判为合格。
3 讨论
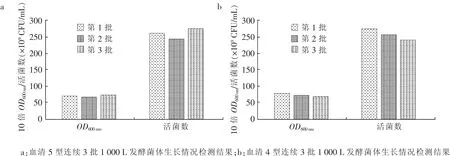
图4 1 000 L规模发酵放大试验结果

表2 3批1 000 L发酵血清4型抗原所配疫苗效力检验结果

表3 3批1 000 L发酵血清5型抗原所配疫苗效力检验结果
高密度发酵在细菌培养及重组蛋白高效表达方面显示出独有的优势[10-11]。付强等[12]通过不同的培养方式对副猪嗜血杆菌进行高密度发酵,使发酵液菌体抗原含量由最初的4.0×109CFU/mL提高到1.6×1010CFU/mL。该研究通过对不同培养基培养副猪嗜血杆菌过程进行分析,寻找对代谢限制的核心营养源碳源和氮源,并通过代谢调控技术对关键营养单元物质生长因子、微量元素和维生素的优化实现最佳代谢流调控,在1 000 L发酵罐中进行高密度发酵工艺优化,副猪嗜血杆菌血清4型JS株和5型ZJ株的活菌数均达到2.5×1010CFU/mL。
副猪嗜血杆菌生长中需要动物血清中的生长因子、微量元素、维生素等,因此,血清浓度的高低与成本关系比较密切[6]。通过批次添加和流加相结合的方式增加补料工艺,在补料培养基中添加葡萄糖、血清、TSB、NAD、维生素、微量元素等,使关键成本血清的使用量降低了1/2,解决了业内发酵成本普遍偏高的问题。最终成功地在1 000 L发酵规模上实现放大,完成了产业化。通过对3批次的1 000 L发酵规模抗原进行疫苗制备,并利用替代动物豚鼠进行动物实验,结果表明所用抗原均合格。
