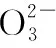Cu元素氧化态的稳定性探析
2018-12-06河北韩万中
河北 韩万中
一、问题的提出

【例1】(2017年全国卷Ⅲ·13题)在湿法炼锌的电解循环溶液中,较高浓度的Cl-会腐蚀阳极板而增大电解能耗。可向溶液中同时加入Cu和CuSO4,生成CuCl沉淀从而除去Cl-。根据溶液中平衡时相关离子浓度的关系图,下列说法错误的是
( )
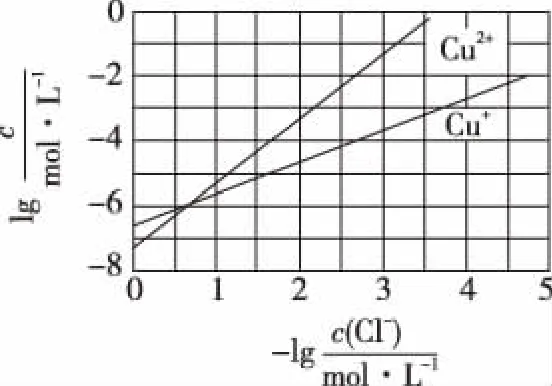
A.Ksp(CuCl)的数量级为10-7

C.加入Cu越多,Cu+浓度越高,除Cl-效果越好

本题以电解液中杂质离子的除去原理为背景,体现化学学科的应用性和实践性。Cl-对阳极有害,如果考查Cl-的去除方法是本题的明线,那么考查Cu的价态转化则是暗线。引人注目的是题目中出现的CuCl沉淀,与熟悉的CuCl2形成了鲜明的对比,学生普遍感到陌生却又新奇。
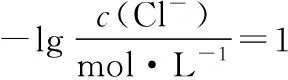
上述解析,从氧化还原反应原理角度解释了Cu(Ⅱ)与Cu(Ⅰ)的相互转化;从求导溶度积常数、化学平衡常数出发,剖析了溶液中平衡时相关离子浓度的关系……凡此种种理解,仅仅局限在中学能力层级,没有更多的深究和理论支撑。

二、理论探析
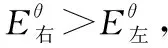


三、思维进阶
当学习选修3《物质结构与性质》时,物质结构观念不断强化,教师有责任引导学生从物质结构上分析铜元素两种氧化态存在的合理性。
【例2】(2016年四川卷·9题节选)CuCl广泛应用于化工和印染等行业。某研究性学习小组拟热分解 CuCl2·2H2O 制备CuCl,并进行相关探究。
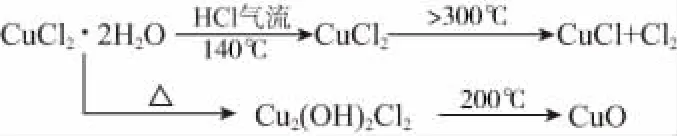
问题略。
【解析】阅读题目中所列出的“资料查阅”,我们先不管CuCl2·2H2O的分解,只把目光聚焦在CuCl2的热分解上,可以发现CuCl2加热到300℃以上时,生成稳定的CuCl。
我们可以从Cu的电离能数据找到依据:


这说明在较高温度下,Cu+比Cu2+稳定,符合洪特规则。
类似的事实还有:CuO加热到1 000℃时分解生成红色的Cu2O,Cu2O十分稳定,在1 235℃熔化但不分解。

所以,在有水的情况下Cu2+是稳定的,这就是我们通常接触到的铜的化合物是Cu(Ⅱ)的缘故。
【例3】(2015年全国卷Ⅰ·36题节选)氯化亚铜(CuCl)广泛应用于化工、印染、电镀等行业。CuCl难溶于醇和水,可溶于氯离子浓度较大的体系,在潮湿空气中易水解氧化。以海绵铜(主要成分是Cu和少量CuO)为原料,采用硝酸铵氧化分解技术生产CuCl的工艺过程如下:
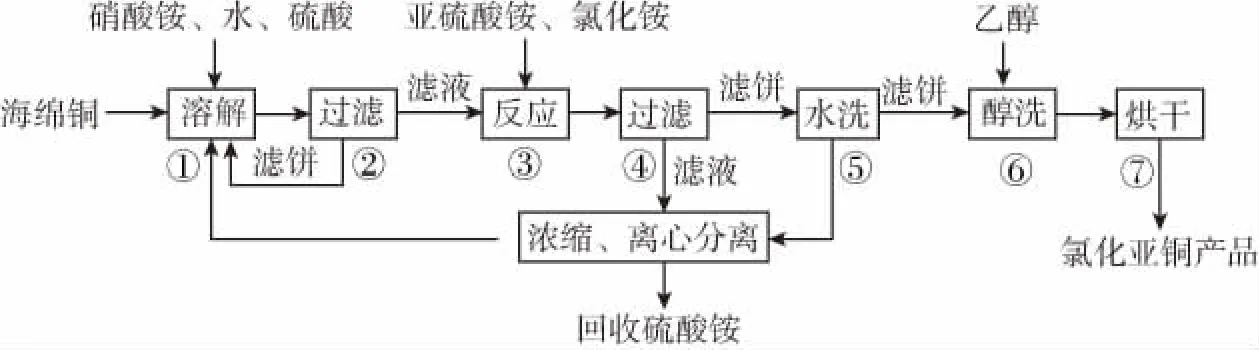
写出步骤③中主要反应的离子方程式___________。
上述工艺中,步骤⑥不能省略,理由是__________。