顽固性咯血患者肺叶切除术前行动脉栓塞介入治疗的价值
2018-12-04朱建坤刘大伟金锋赵彬王成张运曾乔高锋杨秀珍
朱建坤 刘大伟 金锋 赵彬 王成 张运曾 乔高锋 杨秀珍
咯血为临床常见的急症,原因以肺结核、支气管扩张、肺癌及曲菌感染等多见[1]。虽然选择性支气管动脉栓塞术(bronchial artery embolization,BAE)在咯血治疗上广泛应用并取得很好疗效,但仍有约10%~20%的患者咯血不能控制[2-4]。手术可以通过清除感染病灶、切除肿瘤及毁损肺叶等方式,达到彻底止血的目的;但同时存在操作困难、术中出血多、并发症发生率高等风险。我院自2013年始,对顽固性咯血患者在肺叶切除术术前先采用数字减影血管造影(DSA)引导下超选择性经导管动脉栓塞介入治疗(简称“介入栓塞治疗”),2~3 d后行肺叶切除的方式治疗20例患者,获得满意疗效,总结报告如下。
资料和方法
一、临床资料
搜集我院自 2013年1月至2018年1月收住的因顽固性咯血入院而施行肺叶切除的患者共45例,其中男32例,女13例;平均年龄(45.0±6.7)岁;病史9个月至15年,平均7.8±1.9年;曾行BAE治疗42例。原发疾病:肺结核性毁损15例,支气管扩张17例,肺空洞并曲菌球8例,肺结核并发脓胸5例。少量咯血30例,中量咯血11例,大量咯血4例。
二、方法

结 果
观察组20例患者均有病理性非支气管性体动脉(NBSA)侧支循环形成。DSA 检查发现出血责任血管共 57支,其中支气管动脉(BA)12支,NBSA侧支循环 42支,肺动脉(PA) 3支。结核性毁损肺7例,肺空洞并发曲菌球4例,NBSA侧支循环以肋间动脉(11支)、锁骨下动脉(11支)及腋下动脉(7支)为主;支气管扩张9例,NBSA侧支循环以食管固有动脉(9支)、膈下动脉(4支)为主。栓塞后即刻止血13例,咯血减少7例(表1)。
研究组中行肺叶切除9例,行肺叶切除加胸膜剥脱6例,全肺叶切除5例;对照组行肺叶切除13例,行肺叶切除加胸膜剥脱5例,全肺叶切除7例,均恢复良好。研究组术中出血量平均为(600±155) ml,对照组术中出血量平均为(850±210) ml;研究组手术时间平均为(150±35) min,对照组手术时间平均为(180±40) min;两组间术中出血量与手术时间比较,差异均有统计学意义(表2)。
讨 论
顽固性咯血是指咯血反复发作1年以上,大咯血发生1次以上并经过积极治疗再次反复发生者[2]。BAE为治疗急性大咯血的有效手段,但由于支气管扩张,以及肺结核及肺肿瘤等基础病变的进展、NBSA参与供血及侧支循环形成等原因,咯血复发率高达10.9%~41.8%[5-6]。有研究报道,当胸膜厚度达3 mm或胸膜下病灶长期炎症刺激,NBSA侧支循环血管成为咯血的责任血管[7]。本研究观察组患者术前DSA检查发现,20例全部有病理性NBSA侧支循环形成,为咯血的主要责任血管或共同责任血管。其中,结核性毁损肺及肺空洞并发曲菌球11例患者以肋间动脉、锁骨下动脉及腋下动脉为主,与其上述病灶位于邻近后上胸膜的上叶尖后段和下叶背段、并有相邻胸膜肥厚有关;支气管扩张9例,病理性NBSA侧支循环以食管固有动脉、膈下动脉为主,与病灶位于邻近纵隔、膈胸膜的中叶、舌段及下叶基底段有关。本组患者入院前均有行BAE止血的手术史,此次肺叶切除术术前行介入栓塞治疗,即刻止血率为65.0%(13/20),另外7例咯血减轻;低于文献报道采用BAE后的77%~98%的即刻止血率[5]。原因与肺毁损使得责任血管代偿、增生形成复杂血管网,行姑息性近端栓塞疗效不佳,以及由肿瘤、感染引起的弥散性出血,对血管的末梢栓塞效果差等因素有关。由于原发病灶的存在,咯血复发在所难免,故经导管动脉栓塞介入治疗仅能减轻患者咯血症状,为患者赢得进一步治疗时机,但不能完全代替外科手术。

表1 观察组20例介入栓塞治疗患者责任血管分布及栓塞效果
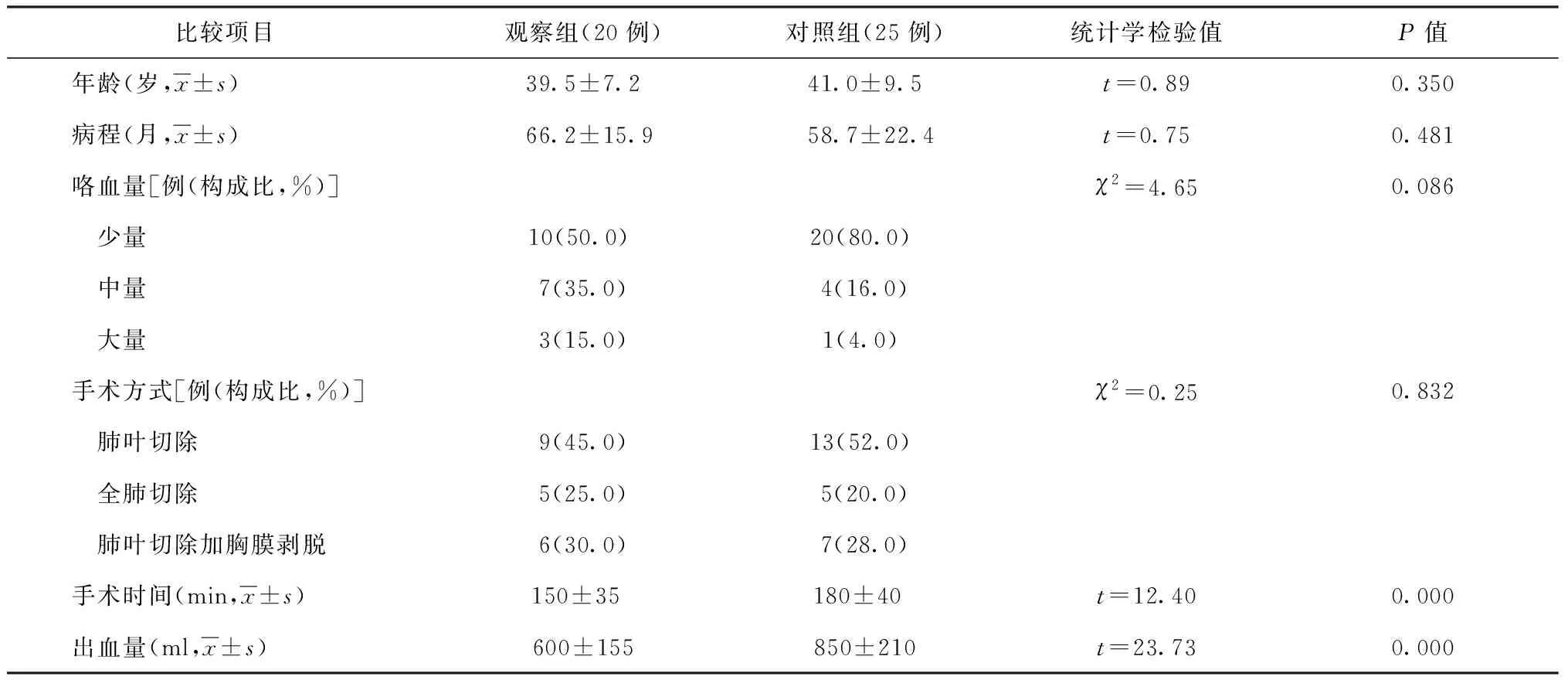
表2 不同比较项目在观察组与对照组患者中的统计与分析对比
纤维支气管镜检查被认为是确定出血部位的金标准[8],可在直视下看到出血肺叶、肺段开口或出血点;但对于毁损肺及长期慢性感染的支气管扩张患者,肺组织硬化、固缩等,或肺段、肺裂发育不全、支气管的变形等因素将影响手术部位的确定,尤其是支气管扩张病变可累及多个肺叶,切除不全易再发咯血。于大平和段勇[9]报道53例因大咯血行急诊肺切除的肺结核并发支气管扩张的患者,有7例不能完全切除扩张部位,其中1例再发大咯血而死亡,另6例出现少量咯血而再次行BAE治疗后好转。术前行DSA检查可显示出血责任血管,联合纤维支气管镜检查将更有助于病变部位的确定及手术方式的选择。另外,隐源性咯血在临床发生率约为7%~25%[10],即虽将病变肺组织切除仍有咯血症状、甚至有加重的情况,要求临床医师必须在术前行DSA检查,以排除隐源性咯血的存在。
咯血患者行急诊手术因其危险性高、并发症多[11],使得众多外科医生心存顾忌。毁损肺则往往与上纵隔增厚的壁层胸膜粘连紧密,使得锁骨下血管、无名静脉与肺组织的解剖关系不清,强行分离会导致难以控制的出血及组织损伤。尤其是长期的慢性炎症刺激导致粘连处产生广泛的血管增生、侧支循环形成,分离粘连时会导致出血增加及术后渗血增多。术前行DSA检查可全面了解出血责任血管,通过显示血管走行及出血部位,对出血及高危血管予以栓塞,可为后期手术创造良好的手术条件。贺继刚等[12]曾提出,对病变与胸壁严重粘连,并已经形成侧支循环者,应用阻断肋间动脉以按需控制胸廓区域的血流,再切除胸内严重粘连病变获得成功;但由于术前未做DSA检查,不能提供客观的影像学依据。目前,胸部CT血管造影(CTA)被广泛应用,有助于发现肺外体循环供血支对肺内病变的供血。徐旭东等[13]报道,对结核性毁损肺患者行胸膜全肺切除术前应用DSA引导下经导管动脉栓塞术,然后行胸膜全肺切除术的术中、术后出血量为(810±125) ml,平均输血400 ml,明显少于对照组。同时手术时间由平均(143±62) min降至(105±45) min,认为术前栓塞可明显减少术中出血,操作相对便捷。本研究观察组患者的手术出血量平均为(600±155) ml,对照组术中出血量平均为(850±210) ml;观察组手术时间平均为(150±35) min,对照组手术时间平均为 (180±40) min;平均手术出血量、手术时间两组间比较,差异均有统计学意义,与文献报道相似;进一步证实了肺叶切除术前行介入栓塞治疗在控制术中出血及缩短手术时间方面的有效性。笔者认为,介入栓塞治疗后行肺叶切除的时机以2~3 d 为宜,此时病灶侧支循环尚未建立、患者临床症状改善,故可较好地耐受手术。
肺叶切除术术前行介入栓塞治疗相对增加了患者费用,并具有脊髓缺血、腹腔器官血管梗塞等风险[14]。但是,由于其一方面能控制咯血为患者贏得进一步治疗的宝贵时间;另一方面有助于明确手术部位、确定手术方式,并能控制术中出血、降低手术风险等;综合考虑,总体上利大于弊。本研究由于样本量较少,所以尚需进行大样本、多中心研究,以进一步证实上述观点。
