溶剂顺序及配比对常压制备SiO2气凝胶的影响
2018-11-20隋学叶周长灵韩乃红刘福田
孙 达 ,隋学叶 ,周长灵 ,李 魁 ,韩乃红 ,刘福田
(1. 济南大学 材料科学与工程学院,山东 济南 250022;2. 山东工业陶瓷研究设计院有限公司,山东 淄博 255000)
0 引 言
SiO2气凝胶是一种纳米多孔非晶态材料,具有连续的三维网络结构,低密度、低导热系数、高孔隙率、高比表面积等特点[1]。1931年美国斯坦福大学的Kistler通过水解水玻璃的方法制得了SiO2气凝胶,自此,各国学者对二氧化硅气凝胶展开了广泛的研究。其具体应用涵盖科研、工业、国防等保温隔热领域,尤其是航空航天和航海领域,同时,还可用于工业和民用的多种领域,如隔热玻璃、隔热墙体、衣物保暖、冰箱隔热、管道保温、吸声降噪,乃至提高太阳能集热器的效率等[2-5]。
在之前的研究中,超临界干燥是制备气凝胶最常用的干燥方式。目前,常压干燥技术越来越受到研究者的重视。Shlyakhtina等[6]以正硅酸乙酯为硅源,凝胶经溶剂交换和表面修饰后,在常压条件下干燥得到二氧化硅气凝胶。刘光武[7]等采用廉价的水玻璃为硅源,通过乙醇溶剂替换及盐酸和六甲基二硅醚混合液[n(HCl) : n(HMDSO) = 0.8]对凝胶的表面基团改性,经过常压干燥,制备出疏水介孔的 SiO2气凝胶。赵大方[8]等以硅溶胶为原料,通过三甲基氯硅烷/六甲基二硅氧烷(TMCS/HMDSO)混合液对制得的凝胶直接进行表面改性,当改性剂n(TMCS)/n(H2O)摩尔比大于0.1时,经过常压干燥得到了疏水的SiO2气凝胶。毕江海[9]等以正硅酸乙酯为硅源,通过酸碱两步溶胶-凝胶法,利用常压干燥的方法制备了疏水SiO2气凝胶,研究了两种改性剂(三甲基氯硅烷、六甲基二硅氮烷)对二氧化硅气凝胶结构和性能的影响,结论是采用三甲基氯硅烷进行改性制备得到的SiO2气凝胶综合性能更加优异。上述研究者都考虑到了常压干燥过程中的溶剂替换和表面基团改性环节,但是都没有具体到溶剂的顺序及比例对SiO2气凝胶的影响。
不同的液体具有不同的表面张力。20 ℃条件下,水的表面张力为72.7 mN/m,乙醇的表面张力为22.3 mN/m,正己烷的表面张力为18.4 mN/m,是水的近1/4倍。溶剂替换完全后可大幅度降低由于溶剂表面张力造成的毛细管力。但是,凝胶状态下孔洞内残留的水与三甲基氯硅烷较易反应,阻碍三甲基氯硅烷对凝胶表面的改性,干燥时容易造成凝胶骨架坍塌,因而先采用乙醇进行溶剂完全替换,再用正己烷与三甲基氯硅烷进行替换和改性。或者用一定比例的乙醇、正己烷与三甲基氯硅烷的混合液直接对凝胶进行替换和改性。乙醇和水可以任意比互溶、价格相对低廉和安全性较高。表面改性过程如(1)式[10]所示:

凝胶的表面存在着大量的羟基基团,在常压干燥过程中会发生脱水缩合的不可逆反应,因而要对其进行表面改性。改性后,Si原子表面-OH中的H会和Cl-Si(CH3)3的Cl反应生成HCl,避免了-OH之间的脱水缩合反应而引起的结构坍塌。
本文以硅溶胶为硅源,用氨水作为调凝剂,硅溶胶经氨水调凝后得到凝胶,分别采用乙醇、正己烷、三甲基氯硅烷对凝胶中的水进行替换以及对凝胶表面的基团进行改性,研究乙醇、正己烷、三甲基氯硅烷的加入顺序和体积比对常压干燥制备SiO2气凝胶的影响。
1 实 验
1.1 制备方案

图1 二氧化硅气凝胶制备流程图Fig.1 The flow chart of silica aerogel preparation
分别将质量分数为20%的硅溶胶等量置于6个烧杯中,每个烧杯中的硅溶胶用氨水调节pH值到6.5。在80 ℃水浴条件下硅溶胶变为凝胶。按照表1 配制的溶剂对凝胶进行溶剂替换和改性,其中,由于正己烷与水不能互溶,所以对1号和2号凝胶先用乙醇进行替换,时间为48 h,然后再分别用正己烷和三甲基氯硅烷各自浸泡48 h。按所示比例的混合溶剂分别对3、4、5、6号凝胶浸泡144 h。上述6组凝胶均需要12h更换一次溶液。替换结束后,常压下将6组凝胶同时放在60℃条件下干燥12 h,80 ℃条件下干燥12 h,120 ℃条件下干燥8 h。最终得到SiO2气凝胶试样。
1.2 表征技术
利用荷兰FEI公司的 Sirion 2000扫描电镜观察气凝胶的微观形貌。采用美国Micromeritic Instruments公司的全自动Gemini Ⅶ2390比表面积和孔径分析仪测定样品的比表面积、孔容和孔半径分布。采用瑞士Mettler Toledo公司的TGA/DSC1型同步热分析仪测试样品的热稳定性。
2 结果与讨论
2.1 气凝胶微观结构
图2分别为六组二氧化硅气凝胶的扫描电镜照片。由图2可知,虽然六组气凝胶的微观形貌各不相同,但是六组照片均表现为多孔结构,均为连续网络结构的多孔纳米材料。但图(2)中气凝胶孔结构最不明显,这是因为凝胶表面的Si-OH并未被完全改性,干燥时-OH之间发生脱水缩合反应,这种反应产生的压力差超过了凝胶网络结构所能承受的最大压力,导致样品的网络状结构明显遭到破坏,样品出现了明显的致密化,宏观上表现为凝胶破碎和体积收缩,性质上表现为密度大、比表面积低、孔容小等。图(5)具有最好的三维网络结构,其网络是由硅氧四面体通过无规则的排列而构成的,颗粒和孔结构较为均匀。图(1)与图(3)结构相近,颗粒尺寸较小,但是孔结构不明显。图(4)与图(6)气凝胶颗粒尺寸较大,颗粒之间的团聚现象更为明显,但仍具有明显的多孔结构。

表1 溶剂顺序及配比Tab.1 The solvent sequence and ratio

图2 二氧化硅气凝胶SEM照片Fig.2 SEM images of silica aerogels

表2 溶剂顺序及配比对气凝胶性质的影响Tab.2 The effect of solvent sequence and ratio on the parameters of aerogels
2.2 气凝胶的基本性质
SiO2气凝胶的密度由质量体积比得到。孔隙率P可由(2)式[11]得到,
其中,ρb是样品的密度,ρs是SiO2的理论密度,为2.2 g/cm3。
从表 2可看出,溶剂的顺序及配比对气凝胶比表面积、密度等性质的影响较为明显。按照EtOH→n-hexane→TMCS的顺序进行溶剂替换和改性得到的气凝胶比按EtOH→TMCS→n-hexane顺序得到的气凝胶具有更好的基本性质。这是因为乙醇替换完成后,少量的水残留在孔隙中,再用正己烷能一定程度上替换掉孔隙中剩余的水,最后用三甲基氯硅烷能对Si-OH完全改性。如果乙醇替换完成就用三甲基氯硅烷改性,三甲基氯硅烷会跟孔隙中剩余的水反应,影响改性效果。表2反映出,当EtOH,n-hexane与TMCS的混合比为10 : 10 : 1时,得到基本性质较好的气凝胶。图3中,SiO2气凝胶的孔径分布图表明,孔径分布较为集中,孔径集中分布在10 nm-30 nm,都是典型的介孔材料。

图3 SiO2气凝胶的孔径分布图Fig.3 Pore diameter distribution of SiO2 aerogels
2.3 气凝胶的热稳定性分析
图4是SiO2气凝胶的TG-DSC曲线。在图(a)中,样品在100 ℃前失重比较明显,这是由气凝胶表面上的吸附水和残余溶剂的迅速挥发引起的,在250 ℃-300 ℃之间样品失重最为明显,大约为1.8%,这主要是由于气凝胶孔内以及气凝胶表面吸附的有机物被氧化所致。100 ℃下的DSC曲线的宽吸热峰是由于吸附水及残余溶剂的挥发所致,在260 ℃附近有一个较强的放热峰,这主要是气凝胶孔隙内有机物的氧化所致,在350 ℃-550 ℃之间有一个较宽的放热峰,这主要是由于-CH3基团氧化所致,此温度下不明显的失重曲线也说明了-CH3基团较少,进而说明了改性不完全。在图(b)中,样品同样在100 ℃前失重比较明显,此过程主要发生的是吸附水及残余溶剂的挥发和氧化,由于吸附水及残余溶剂的量比(a)少,所以没有较多的失重,而明显的失重现象发生在了400 ℃-500 ℃之间,失重3%左右,这主要是-CH3基团氧化所致,较强的放热峰说明-CH3基团较多,改性较好。在400 ℃-450 ℃之间有一个较大的放热峰,在450 ℃-500 ℃之间有一个较小的放热峰,主要是因为改性剂的结构式以及甲基的排列位置不同,而且键长的轻微变化也会导致甲基分解温度的差异。
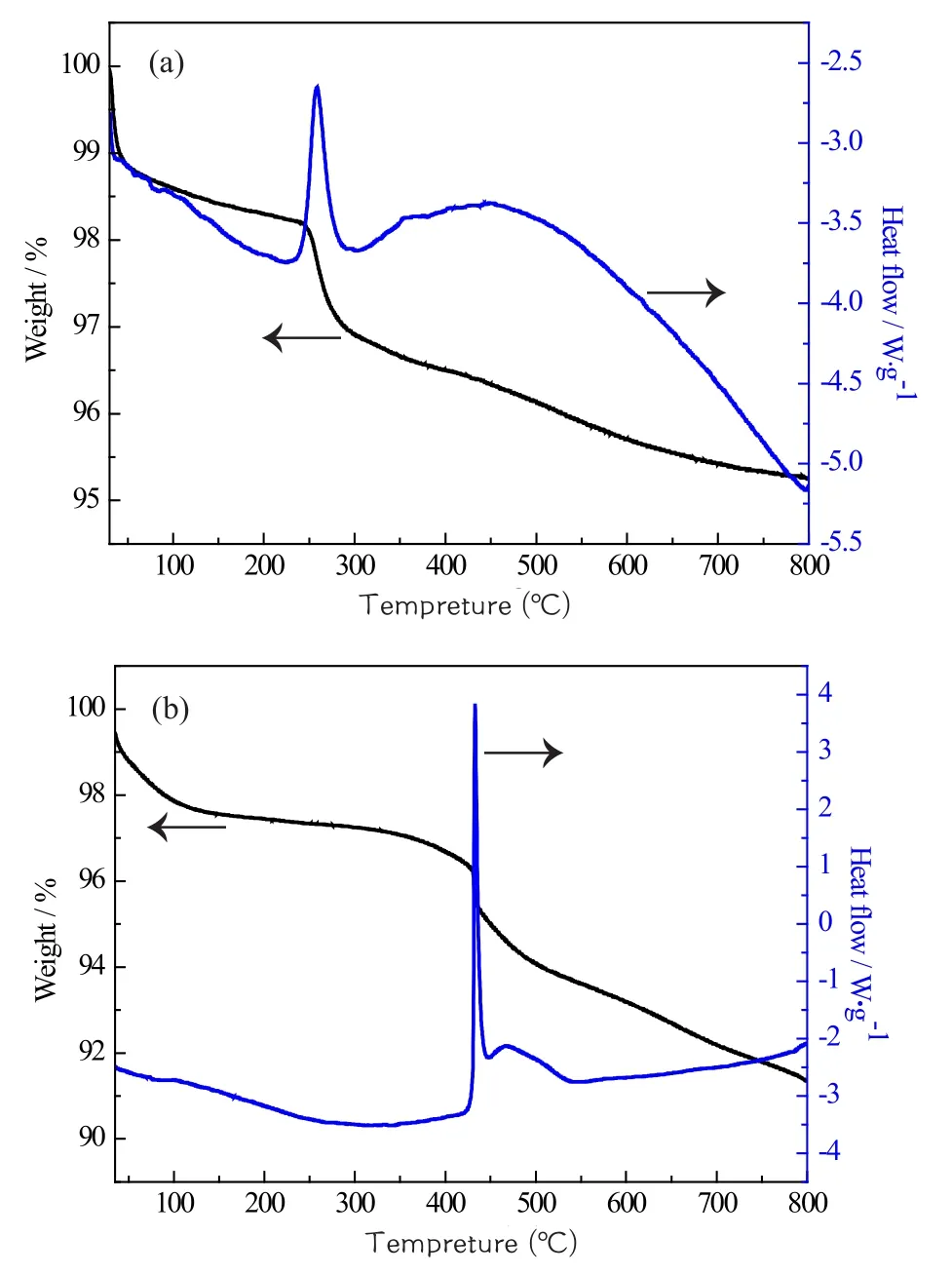
图4 SiO2 气凝胶的TG-DSC曲线(a: EtOH→n-hexane→TMCS;b: EtOH/ n-hexane TMCS=10:10:1)Fig.4 TG-DSC curves of SiO2 aerogels(a: EtOH→n-hexane→TMCS; b: EtOH/n-hexane/TMCS= 10 : 10 : 1)
3 结 论
本文以硅溶胶为硅源,以氨水为催化剂,在80 ℃水浴条件下使硅溶胶凝胶,分别采用不同顺序和不同配比的溶剂对凝胶进行溶剂替换和改性,最后利用常压干燥工艺制备得到了SiO2气凝胶。通过对样品进行扫描电镜分析,比表面积及孔径分析和综合热分析得到如下结论:
(1)按照EtOH→n-hexane→TMCS的顺序进行溶剂替换和改性得到的气凝胶比按EtOH→TMCS→n-hexane顺序得到的气凝胶具有更好的微观结构和性质。
(2)溶剂EtOH/ n-hexane/ TMCS为10 : 10 : 1时,气凝胶具有最均匀的三维结构,最优的比表面积、密度等性质,其中,比表面积为460.86 m2/g,密度为0.287 g/cm3,孔隙率为86.89%,孔容为1.87 cm3/g。
(3)以溶剂EtOH/ n-hexane/ TMCS为10 : 10 : 1得到的气凝胶要比按EtOH→n-hexane→TMCS的顺序得到的气凝胶具有更好的热稳定性。
