抗虫绿豆晋绿7号对小鼠食用的安全性评价
2018-11-19成小芳王金明赵阳飞李妍妍张耀文张仙红
成小芳 王金明 赵阳飞 李妍妍 张耀文 张仙红
(山西农业大学农学院1,太谷 030801)
(山西农业大学文理学院2,太谷 030801)
(山西农业大学动物科技学院3,太谷 030801)
(山西省农业科学院作物研究所4,太原 030000)
绿豆(Vigna radiata L.)在我国广泛种植,其栽培面积、总产量和出口量均居世界前列,作为我国传统主要食用豆类广泛应用于食品、酿造和医药等工业[1]。但在绿豆储藏期极易受到绿豆象(Callosobruchus chinensis L.)的危害,严重影响其产量和质量[2]。随着杂交技术和转基因工程技术的发展,国内外学者成功的将野生种的抗虫成分或外源抗虫基因转入栽培种以减少昆虫侵害,已成为一项广泛应用的技术[3]。我国学者将来源于广西野生稻的抗褐飞虱基因利用杂交转育的方法培育出抗虫水稻品种[4-5];将抗虫基因苏云金芽杆菌(Bacillus thuringiensis,Bt)转入水稻、玉米等作物中以减少病虫的危害[6-7]。其中晋绿豆7号是通过山西省品种审定委员会认定以抗豆象的野生绿豆资源TC 1966为亲本培育的高抗豆象品种[8],主要是通过抑制绿豆象幼虫体内消化酶、保护酶及解毒酶的活力从而起到抗绿豆象的作用[9]。但是要进行广泛种植并食用或进入商业市场必须进行安全性评价。
具有抗虫作用的晋绿7号绿豆是否会对人类的健康造成威胁尚不明确。目前,GB 15193—2014《食品安全性毒理学评价程序和方法》中应用小鼠亚慢性毒理学实验是国内外对食用作物安全性评价的主要方法。故本研究以不同比例的抗绿豆象绿豆晋绿7号和感绿豆象绿豆潍绿2117作为小鼠饲料,对昆明小鼠进行60 d的喂养实验。观察食用抗绿豆象绿豆后对小鼠生长性状、血常规、血生化指标及组织结构变化并应用RT-PCR技术检测肝脏、肾脏中与细胞凋亡相关基因的表达,评价其对小鼠的亚慢性毒性,旨在为抗虫绿豆晋绿7号的食用安全性和商业前景提供参考。
1 材料与方法
1.1 材料
1.1.1 供试绿豆
抗虫绿豆晋绿7号、感虫绿豆潍绿2117均由山西省农业科学院作物研究所提供。该实验中抗虫绿豆晋绿7号是 VC1973A与 TC1966杂交后代[8],具有高抗绿豆象的特性,主产于山西省晋中市,5月中旬播种,8月下旬采收,自然风干密封后4℃冰箱保存备用。
1.1.2 主要试剂及仪器
TRIZOL试剂:大连宝生物工程有限公司;SYBR®PrimeScriptTM RT-PCR Kit试剂盒、DNA ladder maker:TaKaRa公司;Diethyl Pyrocarbonate(DEPC)、溴酚蓝:Sigma公司;其余试剂均为国产分析纯。
旋转切片机:美国Thermo公司;生物显微镜:日本Olympus公司;Varioskan Flash全波长多功能酶标仪:美国Thermo公司;D-375高速冷冻离心机:德国Sigma公司;核酸蛋白测定仪:德国EP公司;凝胶成像系统:美国Bio-Rad公司;DYY-7型转移电泳仪:北京市六一仪器厂;MX3000P荧光定量PCR仪:美国Stratagene公司。
1.1.3 实验动物
选择21日龄断奶昆明小鼠90只,购自山西医科大学动物饲养中心(动物合格证号SCXK(晋)2009-0001),雌雄各半,体重18~24 g,适应1周后按照体重随机分为5组,每组18只。动物饲养管理严格按照中华人民共和国科技部实验动物管理规范,实验期间所有小鼠采用自由采食和自由饮水的方式饲养,光周期12 L∶12 D,温度22~25℃,湿度55% ~60%,定期更换垫料,保证良好的饲养环境,每天定量饲喂,确保每组小鼠采食量一致,每天饲喂3次,每3 d测定一次体重,实验周期为15、30、60 d,按照3R原则给予人道的关怀。
1.1.4 饲料
实验小鼠按体重随机分为5组,分别为空白对照组(BK)、对照组(CK)、低剂量组(JL)、中剂量组(JM)和高剂量组(JH)。BK组饲料为普通饲料,由山西医科大学动物饲养中心提供;CK组饲料为60%普通饲料添加40%的感虫绿豆潍绿2117,JL、JM和JH组的饲料分别为在普通饲料中分别添加抗虫绿豆晋绿7号10%、20%、40%。将饲料按照表1配好后加水制作成颗粒饲料,烘干箱中烘干后按照每天5 g/只的标准进行饲喂小鼠。

表1 实验小鼠日粮配方
1.2 方法
1.2.1 实验动物小鼠生长状况
饲养期间每天观察实验小鼠的精神状态、生长发育情况和采食饮水状况,小鼠体重每3 d称量一次。
1.2.2 样品的采集及前处理
小鼠分别于实验第15、30、60天时禁食禁水24 h,每组随机抽取6只(3雌、3雄)小鼠,摘眼球取血,3 000 r/min离心15 min分离血清并分装在1.5 mL的EP管中 -20℃保存,用于血液生化指标测定。取血后迅速处死,取肝脏、肾脏放入液氮罐,最后统一放入超低温冰箱-80℃保存,用于提取RNA并进行细胞凋亡分析。其余2只(1雌、1雄)进行心脏灌流,同时快速取肝脏、肾脏、脾脏、空肠置于10%的中性福尔马林固定液固定,用于组织形态学检查。
1.2.3 血清生化指标测定
血清中血钙、碱性磷酸酶、白蛋白、甘油三酯、总胆固醇、谷丙转氨酶、谷草转氨酶、尿酸、尿素氮、肌酐、血糖、总蛋白含量测定均严格按照试剂盒说明书进行操作,采用Varioskan Flash全波长多功能酶标仪读取吸光度计算含量。
1.2.4 器官指数

1.2.5 组织形态学观察
将饲养30 d的小鼠麻醉处死,取各组小鼠肝脏、肾脏、脾脏和空肠用10%的甲醛固定后,用不同梯度的酒精脱水,二甲苯透明2次,浸蜡过夜,石蜡包埋,置于旋转切片机上连续切片,切片厚度为5 μm,然后用温水展片、捞片,烤干,苏木精伊红(HE)染色。生物显微镜下观察其形态结构及病理情况。
1.2.6 晋绿7号绿豆对小鼠肝脏、肾脏凋亡相关基因的mRNA表达
1.2.6.1 总RNA的提取、cDNA的合成及质量鉴定
利用TRIZOL试剂提取肝脏、肾脏中的总RNA,采用0.8%琼脂糖凝胶电泳和核酸蛋白测定仪对RNA进行检测。置于 -82℃超低温冰箱保存备用。1.2.6.2 荧光定量 RT-PCR引物设计与合成:由美国国立生物信息技术中心(NCBI)和Primer 3 Plus软件设计小鼠 bax、bcl-2、Caspase-3和 cyt-c的基因序列和引物,同时以β-肌动蛋白(β-actin,Gen-Bank登录号 NM_031144.3)为内参基因检测和比较各RNA样品的完整性及其反转录效率之间的差别,引物序列及大小见表2。
1.2.6.3 QRT-PCR反应体系及扩增条件的建立及数据处理
所有实验RNA样品的目的基因和内参基因扩增进行实时荧光定量PCR反应,使用两步法进行,第一步为 RNA反转录为 cDNA(20 μL体系):Prime Script TM Buffer(5×),4μL;总 RNA,2μL;RNase and Free dH20,14 μL。反转录条件:37.5 ℃ 10 min,90℃ 5 s。第二步为RT-PCR扩增(20 μL体系):SYBR Premix Ex TaqTM(2 × ),10 μL;PCR Forward Primer,0.8 μL;PCR Reverse Primer,0.8 μL;ROX Reference DyeⅡ(50 × ),0.4 μL;cDNA,2 μL;去离子水,6 μL。QRT-PCR 扩增条件:95℃ 10 s预变性;95℃ 5 s,60℃ 15 s,72℃ 5 s PCR 反应;95℃ 60 s,55℃ 30 s,95℃ 30 s溶解曲线绘制,QRT-PCR反应在MX3000P荧光定量PCR仪上进行,反应结束后软件将自动进行数据分析,调整基线,计算出Threshold cycle(Ct值)。

表2 实验中合成的引物序列
数据处理采用相对定量标准曲线法,根据Ct值计算目的基因在CK组和各实验组的基因初始浓度,然后以β-actin为内参基因,计算其在CK组和各实验组的基因初始浓度;相对表达量=(待测样品目的基因初始浓度/待测样品内参基因初始浓度)/(对照样品目的基因初始浓度/对照样品内参基因初始浓度),以此公式计算实验组目的基因相对于CK组的表达差异倍数。
1.2.7 数据统计分析
采用GraphPad Prism 5.0软件进行各组间ANOVA差异显著性分析,Dunnett's(P<0.05)多重比较进行检验,数值用平均值±标准差表示。
2 结果与分析
2.1 小鼠生长状况观察
实验期间BK组、CK组及实验组小鼠均无死亡和中毒的临床症状,食欲正常,生长发育良好,精神活泼反应灵敏,皮毛正常有光泽,尿液正常清亮,粪便颜色呈灰褐色颗粒。表明在受试期内抗虫绿豆晋绿7号对小鼠的生长发育未受到影响。
2.2 抗虫绿豆晋绿7号对小鼠体重的影响
抗虫绿豆晋绿7号对小鼠体重的影响见图1,各组小鼠体重随实验时间的延长均呈上升趋势。与BK组相比,在整个实验期小鼠CK组及JL组体重有所升高,但均差异不显著,表明在饲料中不添加绿豆或少量添加绿豆不会显著改变小鼠体重。与CK相比,JM与JH组小鼠体重在实验前期(前30 d)体重显著降低,但实验后期(后30 d)体重变化不显著,表明短时间采食中、高剂量抗虫晋绿7号绿豆对小鼠的体重增长有一定的抑制作用。
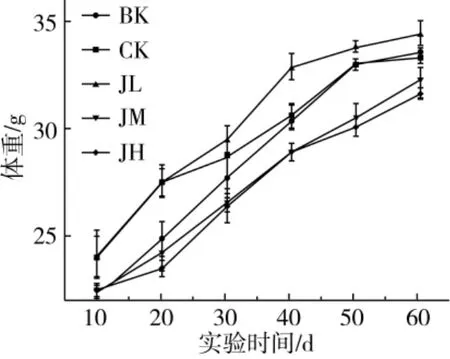
图1 抗虫绿豆晋绿7号对小鼠体重的影响
2.3 抗虫绿豆晋绿7号对小鼠血清生化指标的影响
表3为抗虫绿豆晋绿7号对小鼠血清生化指标的影响。从小鼠血清总蛋白(TP)、白蛋白(ALB)、碱性磷酸酶(ALP)、血清谷丙转氨酶和谷草转氨酶、血清钙、葡萄糖、血清尿素氮和肌酐含量在实验期内各实验组均无显著变化(P>0.05),表明抗虫绿豆晋绿7号在受试剂量下对小鼠未发现明显的肝脏、肾脏的毒性作用。
在实验15 d时,各组小鼠甘油三酯浓度无显著变化(P>0.05);30 d时,BK组、JL组、JM组小鼠甘油三酯浓度与CK组相比均无显著性差异,但JH组小鼠的甘油三酯浓度显著降低(P<0.05);60 d时,BK组、JL组与CK组相比均无显著差异(P>0.05),JM组和JH组的甘油三酯浓度显著低于CK组(P<0.05)。小鼠血清总胆固醇浓度在整个实验期与血清甘油三酯浓度呈一致的变化趋势,与CK组相比,15 d时,只有JH组总胆固醇浓度显著降低(P<0.05);实验30 d和60 d时,BK组、JL组的均无显著变化,但JM组和JH组显著低于CK组(P<0.05)。可见,抗虫绿豆晋绿7号在一定程度上可降低小鼠血液中甘油三酯和总胆固醇浓度,表明晋绿7号抗虫绿豆对小鼠有一定的降脂作用。

表3 晋绿7号对小鼠血液生化指标的影响(n=6)
2.4 抗虫绿豆晋绿7号对小鼠器官发育的影响
实验30 d时分别对小鼠6个实质性组织器官的外形进行观察,未发现实质性组织器官的变形和病变,并对器官进行称重计算器官指数(见表4),与CK组相比,心、肝、脾、肾、肺、脑器官指数在JL、JM和JH组均无显著变化(P>0.05),可见在实验期抗虫绿豆晋绿7号对小鼠心、肝、脾、肾、肺、脑的发育未产生不良影响。
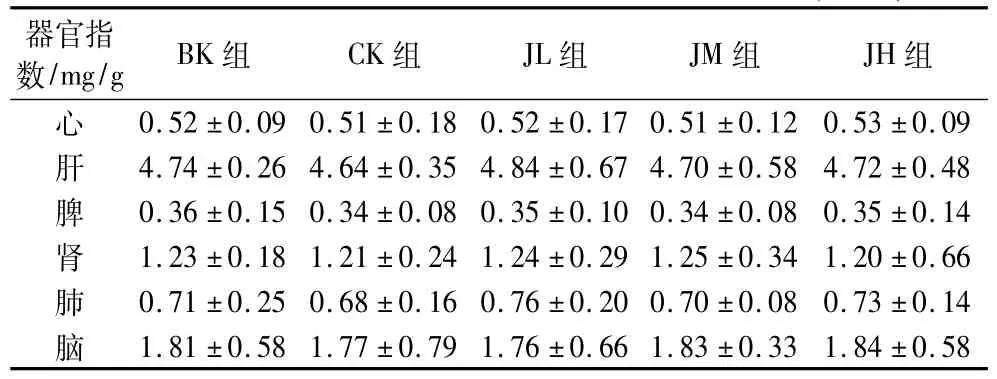
表4 实验30 d后晋绿7号对小鼠器官指数的影响(n=6)
2.5 组织形态学观察
实验60 d时小鼠肝脏、脾脏、肾脏、空肠组织切片HE染色结果见图2。CK组小鼠肝小叶结构完整,肝细胞索和肝窦排列规则清晰,以中央静脉为中心向周围呈放射状排列,肝细胞核仁大而圆,其他实验组肝组织切片细胞分布均匀,细胞核完整,未见异常现象。在脾脏组织中,CK组红髓与白髓之间界限清晰,白髓内的淋巴小结结构清晰完整,生发中心明显可见,而其他实验组中脾脏组织结构同样完整,淋巴细胞清晰可见,数量及结构未发现明显改变。CK组小鼠肾脏组织结构正常,肾小管上皮细胞排列整齐有序,肾小球数量正常,结构清晰;其他实验组小鼠肾脏结构未发生明显的病理学改变,未看到肾小管管腔发生变窄及上皮细胞脱落等现象。表明抗虫绿豆晋绿7号没有导致小鼠肝、脾、肾组织发生病理学改变。
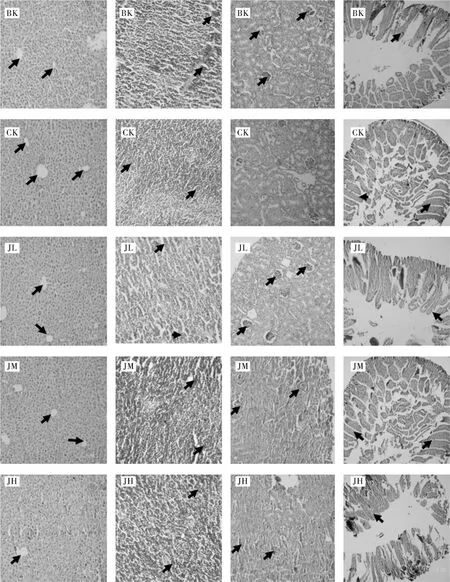
图2 实验60 d小鼠肝脏、脾脏、肾脏、空肠组织切片HE染色
从实验60 d小鼠空肠组织切片可见,CK组小鼠空肠结构完整,隐窝深度及小肠绒毛长短正常,未发生肠腺细胞增生性病变;其他实验组小鼠的空肠黏膜表面的纹状缘结构层次清晰,肠绒毛排列整齐,细胞衣较厚,肠黏膜上皮细胞形状规则,排列紧密,细胞核与细胞浆染色对比鲜明。表明晋绿7号未对小鼠肠道结构发生病理改变。
2.6 晋绿7号绿豆对小鼠肝脏、肾脏凋亡相关基因mRNA的表达
荧光定量PCR检测肝脏、肾脏结果见图3和图4,实验60 d时小鼠肝脏和肾脏凋亡相关基因bax、bcl-2、cyt-c及Caspase-3均无显著差异,说明在实验期内实验剂量的晋绿7号对小鼠肝脏细胞和肾脏细胞的凋亡无促进作用。
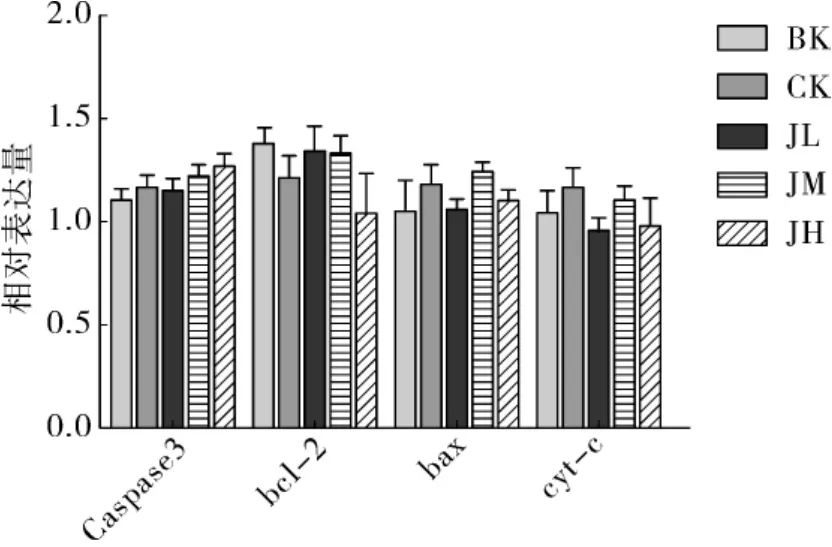
图3 肝脏凋亡相关基因表达水平测定结果
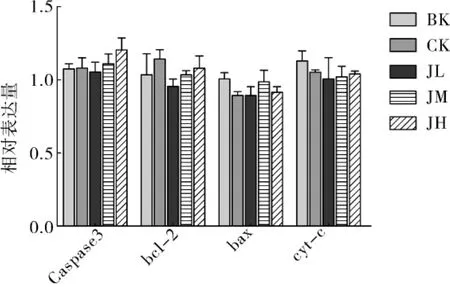
图4 肾脏凋亡相关基因表达水平测定结果
3 讨论
3.1 晋绿7号绿豆对小鼠生长发育的影响
在本实验中,从肉眼观察小鼠外观及临床表现各实验组均正常,只有采食含抗虫绿豆晋绿7号绿豆20%和40%的饲料前30 d的小鼠,其体重比CK组有所下降。而导致体重减轻的原因是多方面的,可能与抗虫绿豆降低血液中胆固醇及甘油三酯的结果相关,这一结果与Chukwudebe等[10]报道大鼠采食含有33%的CV127大豆在实验70 d和77 d时体重下降的结果相一致(其血糖在同期也显著下降)。但Yao等[11]报道大鼠采含有65%的抗虫绿豆90 d中体重无显著变化(同期其血液生化指标均无改变)。具体导致小鼠体重下将的原因及机制尚不清楚,有待进一步深入探讨。
3.2 晋绿7号绿豆对小鼠血液生化指标的影响
血清总蛋白是判定肝细胞合成蛋白质功能的有效指标,也是检测肾脏重吸收功能的重要参考依据,血清白蛋白是肝脏合成的一种免疫球蛋白,二者是反映肝、肾功能的有效指标。本实验血清总蛋白和白蛋白在所有实验组中均没有发生显著改变,说明抗虫绿豆晋绿7号没有影响小鼠肝脏合成总蛋白及白蛋白的功能,但是否影响了肝脏及肾脏的其他功能还需结合血液学的其他生化指标综合判定。本实验中各实验组小鼠的ALP没有发生显著变化,表明晋绿7号绿豆本身对骨骼生长没有促进或抑制作用。但在实验15 d时,各实验组小鼠的碱性磷酸酶均高于30 d和60 d,这可能与小鼠在实验前期生长发育较快,引起骨骼较快生长有关。这一结果分别与用转基因稻谷[6]、CV127 大豆[10]、抗虫绿豆[11]和转基因玉米[12]饲喂大鼠的结果相一致,对小鼠骨骼、肝脏、肠道等组织器官没有毒害作用。
本实验结果表明,采食抗虫绿豆的小鼠在实验期血清ALT和AST浓度与对照相比均无显著差异(P>0.05),表明抗虫绿豆晋绿7号对小鼠肝脏功能没有损伤。这与用转基因稻谷[6]和抗虫绿豆中绿3号、4号、5号、6号[11]饲喂小鼠90 d后血清 ALT和AST也没有发生变化相一致。
甘油三酯和胆固醇是体内能量的主要来源。在血液中,甘油三酯以脂蛋白的形式运输,胆固醇主要与脂肪酸合成胆固醇酯存在于脂蛋白中。据报道,在十二指肠内pH为6.3时,绿豆可以结合胆汁酸和增加粪便分泌物的排泄来降低胆固醇[13-15];研究表明用70%的绿豆粉混合于家兔饲料中饲喂家兔,既有预防和治疗高血脂症的作用,又有减轻冠状动脉粥样病变的功效[16];将绿豆提取物混于饲料中喂养小鼠和大鼠7 d,发现绿豆具有明显降低血清胆固醇的作用[17]。本实验JM组和JH组的小鼠TG浓度和胆固醇浓度与对照相比均显著下降(P<0.05),这可能是由于绿豆中所含的植物甾醇与胆固醇可同时竞争酯化酶,使之不能酯化而减少肠道对胆固醇的吸收有关。在本实验中,添加不同剂量的抗虫绿豆晋绿7号并未对小鼠的血钙产生影响,这也印证了其他生化指标未变化的合理性。同时本研究发现,抗虫绿豆晋绿7号未对小鼠血糖产生影响,表明对肝脏合成和分解肝糖原不产生影响,对消化系统吸收碳水化合物提供血糖不产生负面影响,不会引起糖异生。这与前人对转基因稻谷[6]、转基因玉米[7,12]及转基因大豆[10]的安全性评价结果相一致。
本实验中,处理组小鼠血清尿素氮和肌酐含量均未发生显著变化。这与用转基因稻谷[6]和用抗虫绿豆[11]饲喂小鼠后尿素氮和肌酐没有发生改变的研究结果一致。表明抗虫绿豆晋绿7号对小鼠肾小球的滤过功能没有影响,不会造成肾脏功能的损伤。
3.3 晋绿7号绿豆对小鼠脏器发育及组织形态的影响
本实验中抗虫绿豆晋绿7号对小鼠心、肝、脾、肺、肾、脑的器官指数无显著影响(P>0.05)。这一结果与 Chukwudebe等[10]及 Yao等[11]分别用含有33%的CV127大豆饲喂大鼠及用抗绿豆象的中绿3号饲喂小鼠90 d后,心、肝、脑、脾、肾、胸腺等脏器系数均无显著变化。表明小鼠脏器并不会由于食入含有抗虫绿豆晋绿7号的饲料而发生改变。
张珍誉[6]采用检查组织病理学方法对转基因稻谷对小鼠的安全性进行评价,朱元招[18]用转基因稻谷和大豆饲喂小鼠进行过组织病理学检查均未发现组织器官发生病理学改变。本实验选取处理组和CK组小鼠空肠、肝脏、肾脏和脾脏器官进行组织结构观察比较,发现采食晋绿7号绿豆的小鼠空肠结构完整,肠绒毛排列整齐,空肠上皮细胞清晰可见,肝脏细胞排列整齐,结构完整,肾小球大小正常,脾脏淋巴细胞数量和形态均未见明显变化,表明在实验期内抗虫绿豆晋绿7号没有影响小鼠组织器官的结构及功能。这一结果也与血液生化指标的结果相符,与 CV127 大豆[10]、抗虫绿豆[11]、转基因稻谷[12]饲喂大鼠实验中脏器的检查结果相一致。
3.4 晋绿7号绿豆对小鼠肝脏、肾脏凋亡相关基因的影响
线粒体通路是目前被公认的动物细胞凋亡的主要机制之一。Anuradha等[19]指出,线粒体通路中bcl-2家族促凋亡蛋白bax、bcl-2会诱导线粒体膜间质凋亡蛋白(如细胞色素C,cyt-C)的释放,与凋亡酶启动子结合,活化凋亡酶启动子后会进一步活化Caspase-3作为凋亡通路中效应型Caspases执行细胞的凋亡,所以检测Caspase-3的表达对线粒体凋亡通路至关重要。目前鲜有关于从组织器官的分子水平进行检测食品安全性的研究。因此,本实验从采食抗虫绿豆小鼠线粒体通路中选择肝脏、肾脏凋亡的相关基因进行检测,结果显示,采食晋绿7号绿豆的小鼠,其肝脏和肾脏中 bax、bcl-2、cyt-c及Caspase-3的基因表达均未发生改变,表明抗虫绿豆晋绿7号对小鼠基因表达未产生影响,因此从分子水平上看对小鼠肝脏、肾脏也是安全的。
4 结论
采食晋绿7号抗虫绿豆不会对小鼠生长发育、血液学指标及组织器官产生毒性作用,作为食用性食物可能不会对人类及动物造成危害,同时为晋绿7号的商业种植及食品安全性提供参考。
