胚胎单基因病诊断患者辅助生殖累积妊娠率低的原因初探
2018-11-15王珺陈书强张亨德黄剑磊李博
王珺,陈书强,张亨德,黄剑磊,李博
(空军军医大学唐都医院妇产科生殖医学中心,西安 710038)
单基因遗传病是一类由1个或1对等位基因的突变引起的疾病,符合孟德尔遗传规律。虽然每种单基因遗传病的发病率较低,但是因为其种类繁多,总体患病率并不低。目前已发现的单基因遗传病有7 000多种,涉及基因3 000多个。目前大多数单基因遗传病还缺乏有效的治疗方法,致死率、致残率均很高[1-2]。胚胎植入前单基因病检测(preimplantation genetic test for monogenetic,PGT-M)是一种与辅助生殖(ART)相结合的遗传学诊断技术[3],即在胚胎植入前进行特定的遗传诊断,从而避免单基因病患儿出生。这为单基因病受累家庭带来了新的希望,但通过临床观察发现PGT-M技术的累积妊娠率并不高,本文将针对这一现象做初步探讨,为PGT-M临床遗传咨询提供参考。
材料与方法
一、研究对象
收集我中心2016年7月至2017年6月期间接诊的PGT-M患者,共31个促排卵周期、102枚胚胎。患者平均年龄(32.4±4.1)岁。其中常染色体隐性遗传(AR)8个周期,常染色体显性遗传(AD)7个周期,X连锁隐性遗传(XR)15个周期,X连锁显性遗传(XD)1个周期。
同时收集我中心2016年7月至2017年6月期间进行胚胎植入前染色体非整倍性检测(preimplantation genetic test for aneuploidies,PGT-A)患者[3],90个周期,350枚胚胎。患者平均年龄(31.9±4.2)岁。
患者纳入标准:PGT-A:(1)复发性流产(≥3次);(2)反复胚胎种植失败(≥3次);(3)不良孕产史;(4)严重男性不育。PGT-M:有明确单基因病致病风险。患者排除标准:(1)不符合上述入选标准者;(2)中途放弃检测,导致无实验结果者。
二、研究方法
1.胚胎活检:PGT患者,体外受精后116~144 h,待胚胎发育到囊胚期(D5-D6),并达到活检标准时(4B-C+以上胚胎),在内细胞团对侧使用激光在透明带上打一直径6~10 μm的孔,继续培养4~6 h,待滋养外胚层细胞形成疝,激光法活检5~10个细胞,PBS洗涤后,装入预先准备好的0.2 ml EP管内。
2.胚胎扩增:使用Qiagen REPLI-g single cell kit(212768,RUBICON GENOMICS,美国)提取试剂盒,对胚胎活检细胞进行裂解、DNA提取、全基因组预扩增及扩增。然后用QubitdsDNA HS Assay Kit(ZYKW-KY-002-2,嘉宝仁和)对全基因组DNA产物进行定量检测。
3.胚胎植入前遗传学检测:本研究所有PGT检测,均是以高通量测序技术(Next Generation Sequencing,NGS)为基础,采用Ion PROTON进行检测。对于PGT-A患者,采用胚胎植入前染色体非整倍体检测试剂盒(ZYKW-X-013,嘉宝仁和)行染色体非整倍性检测。对PGT-M患者,采用S-PGDM法:胚胎植入前染色体非整倍体检测试剂盒/胚胎植入前单基因病检测试剂盒(ZYKW-X-013/ZYKW-X-016,嘉宝仁和)进行染色体非整倍性及单基因异常检测。
三、统计学处理

结 果
一、两组基本情况比较
PGT-M患者与PGT-A患者相比,在女方平均年龄、平均Gn使用量、平均Gn使用天数、平均获卵数等方面差异均无统计学意义(P>0.05),PGT-M患者染色体非整倍性胚胎占比与PGT-A患者相比无显著性差异(P>0.05),患者平均内膜厚度无显著性差异(P>0.05)(表1)。
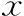
表1 PGT-M患者与PGT-A患者的基本情况比较[(-±s),n(%)]
二、两组患者的促排卵结果
PGT-M患者31个促排卵周期,共计获得卵母细胞434枚,成熟卵母细胞351枚(80.88%),形成胚胎271枚(62.44%),最终获得可行遗传学诊断的囊胚102枚(23.50%)。PGT-A患者,90个促排卵周期,共计获得卵母细胞1 393枚,成熟卵母细胞1 132枚(81.26%),形成胚胎871枚(62.53%),最终获得可行遗传学诊断的囊胚350枚(25.13%)。
三、胚胎染色体非整倍性检测结果
本研究用于PGT-M检测的102枚胚胎,其中94枚进行了染色体非整倍性及结构异常NGS检测,8枚胚胎由于单基因病结果异常,未继续进行染色体检测。在94枚胚胎中,染色体整倍性胚胎43枚(45.74%),染色体非整倍性胚胎51枚(54.26%)。PGT-A检测的胚胎350枚,染色体整倍性胚胎169枚(48.29%),染色体非整倍性胚胎181枚(51.71%)。
四、胚胎单基因病致病位点检测结果
本研究用于PGT-M检测的102枚胚胎,96枚胚胎进行了单基因病致病位点的检测,6枚由于已检测为染色体异常的胚胎而未继续单基因致病位点检测。在96枚胚胎中,完全正常胚胎28枚,携带胚胎29枚,致病胚胎37枚,无法判断胚胎2枚。完全正常胚胎占29.17%,表型正常胚胎占59.38%。根据孟德尔遗传规律,本研究所涉及的不同类型单基因病周期,96枚胚胎中,理论完全正常胚胎40.5枚,占42.19%,理论表型正常胚胎66.75枚,占69.53%。
统计分析结果显示,完全正常胚胎,实际占比显著小于理论占比(P<0.05);表型正常胚胎,实际占比较理论占比低,但无显著性差异(P>0.05)(表2)。

表2 PGT-M患者胚胎单基因病诊断结果及孟德尔理论预测结果[n(%)]
注:与理论完全正常相比,*P<0.05
五、PGT-M患者检测后的有效胚胎占比情况
31个促排周期所获得的102枚胚胎中,染色体整倍性胚胎43枚,其中有效胚胎(即表型正常胚胎,包含正常胚胎及携带胚胎)28枚,占27.45%,其中完全正常胚胎(不含携带胚胎)13枚,占12.75%。
讨 论
染色体非整倍性与女性年龄、复发性流产、染色体结构异常等密切相关[4-7]。随着女性年龄的增长,染色体非整倍性比率增加,流产率增加[5-6,8]。遗传因素在复发性流产的诱因中占70%,染色体非整倍性异常是遗传因素中的最主要原因[7,9]。
PGT-A主要适用于存在高度胚胎非整倍性风险的夫妇,以提高胚胎着床率及活产率,降低流产率[10];PGT-M主要针对存在单基因病致病风险的夫妇,以减少出生缺陷,实现优生。我们的检测结果显示,PGT-A患者囊胚染色体非整倍性占比51.71%。这与文献报道基本一致[11-12]。PGT-M患者,均是以排除单基因病致病位点为目的,并不属于不孕不育人群。有最新的研究报道显示,在非不孕不育人群中,胚胎染色体非整倍性显著低于不孕不育人群[13]。
本研究的数据显示:PGT-M患者在平均年龄与PGT-A患者无显著差异的条件下,PGT-M患者的整倍性胚胎(45.74%),与PGT-A(48.29%)相比并无显著性差异,也就是说,PGT-M患者所获得的染色体整倍性胚胎与染色体非整倍性高发的不孕不育人群(PGT-A)水平相当,从占比上看,甚至整倍性胚胎占比更少。仅通过染色体检测这一项,就已经淘汰掉了54.26%的胚胎,导致后续可用胚胎数骤减。分析原因,可能与Gn用量有一定关系。研究指出胚胎非整倍体形成与排卵药物剂量相关[14-15]。发生机制可能是,在促排卵过程中,生理条件下的激素节律和稳态发生急剧变化,增加卵母细胞形成过程中染色体的分离错误,最终导致受精胚胎发生染色体异常,造成流产率增高[16]。本研究显示,虽然Gn用量在PGT-M与PGT-A之间无显著差异,但PGT-M患者促排卵状态已属于非自然状态,很可能胚胎染色体非整倍性会随之增加,因此,这可能是PGT-M患者累积妊娠率低的可能原因之一。
在单基因病致病位点检测中,实际检测完全正常胚胎占比(29.17%)显著低于孟德尔遗传规律预测的完全无致病突变胚胎占比(42.19%),而实际表型正常胚胎占比(59.38%)与预测值(69.53%)相比虽然无统计学差异,但也较预测值低大约10个百分点,这一结果并未见相关文献报道。这意味着单基因病致病位点检测可能会淘汰掉40%~70%的胚胎,笔者猜测这是PGT-M患者累积妊娠率低的可能原因之二。
目前,临床医生在PGT-M患者辅助生殖助孕之前行遗传咨询时,往往是以孟德尔遗传规律为参考,估算最终可用胚胎数,对患者的临床结局预期过高。而患者在最终选择胚胎植入时,由于家庭压力或心理焦虑等原因,往往又倾向于选择完全正常的胚胎而不是表型正常的携带胚胎,这无疑更是雪上加霜,导致可用胚胎数再次减少。
PGT-M患者胚胎遗传学诊断后,临床可以使用的有效胚胎,需满足染色体非整倍性正常且至少单基因病诊断表型正常。综合本研究中31个周期的PGT-M胚胎检测结果,能够供患者选择的染色体正常且表型正常的有效胚胎28枚,只占遗传学检测囊胚的27.45%,而染色体及单基因病致病位点完全正常的胚胎13枚,仅占12.75%。目前还不能准确统计出PGT-M患者31个促排卵周期的累积临床妊娠率,但通过检测结果可判断出理论值:表型正常的胚胎存在于11个促排卵周期中,也就是说如果移植这些胚胎,最多能够使11个周期获得临床妊娠,PGT累积临床妊娠率最高为35.48%(11/31);完全正常胚胎存在于9个促排周期中,同理推算,PGT累积临床妊娠率最高为29.03%(9/31)。而在90个PGT-A周期中,有可用胚胎的周期81个,PGT累积临床妊娠率最高可达90%(81/90)。根据我中心2015年至2016年数据显示,PGT-A患者,累积临床妊娠率为70.75%。由此可见,PGT-M患者累积临床妊娠率远低于PGT-A患者。
综上所述,PGT-M患者要经历胚胎染色体非整倍性筛查及单基因病诊断双重筛选,使得可用胚胎骤减,最终导致累积临床妊娠率降低。随着检测患者增多,统计数据量的增大,我们将继续关注此类患者的累积临床妊娠率,验证并进一步寻找可能的形成原因,为临床遗传咨询提供理论参考。
