磺胺甲噁唑与吉富罗非鱼血浆蛋白结合率的测定方法研究
2018-11-12王赛赛
王赛赛,宋 怿,程 波
(1.上海海洋大学水产与生命学院,上海 201306;2.中国水产科学研究院农业部水产品质量安全控制重点实验室,北京 100141)
药物-血浆蛋白结合率是一个重要的药代动力学参数。大部分药物经吸收进入血液循环后,会不同程度地与血浆蛋白结合而丧失药理活性,只有游离的药物才能自由透过细胞膜最终到达作用部位[1]。药物血浆蛋白结合率通过制约游离药物浓度,来影响药物在动物体内的分布、代谢和消除规律[2,3]。因此,药物-血浆蛋白结合率的测定无论是对于药物代谢动力学、药效学还是药物残留预测模型的构建均具有重要意义。目前测定药物-血浆蛋白结合率最常用的方法为体外平衡透析法和体内超滤法,在以往的研究中,体外平衡透析法涉及的因素主要为平衡时间[4-5]、血浆含量[4]、透析温度[1,4-5]和药物浓度[4-5],透析时间的确定试验大多以空白透析液取代空白血浆为主,忽略了实际试验中结合率达到稳定的时间;不同药物血浆蛋白结合率受温度的影响存在差异;不同药物浓度对结合率的影响也因药物与物种的差异而有所不同。体内超滤法[6]大多采用解冻后的血浆进行超滤,忽略了血浆储存过程中pH的改变以及其对结合率造成的影响[7,8]。因此,本研究在前人的基础上,将平衡时间、温度、pH、药物浓度列入结合率测定的影响因素,以磺胺甲噁唑(SMZ)为研究对象,通过采用体外平衡透析法,研究不同温度(4、25、37 ℃)、不同pH(7.4、7.8、8.2)对结合率的影响,来确定体外平衡透析法和体内超滤法的最佳测定条件,从而得出不同药物浓度下体内外SMZ罗非鱼血浆蛋白结合率。最后,通过对体内外测定结果进行对比分析,确定SMZ血浆蛋白结合率的最佳测定方法,为SMZ药物代谢理论研究和药物残留预测模型的构建提供了理论依据。
1 材料与方法
1.1 药品与试剂
SMZ标准品(≥99.0%),氘代磺胺邻二甲氧嘧啶(99.8%±0.2%)购于德国Dr.Ehrenstorfer公司;SMZ(≥99.0%)购于艾览(上海)化工科技有限公司;肝素钠(H8060,≥99.0%),购于北京索莱宝科技有限公司;磷酸氢二钠、磷酸二氢钠、氯化钠、碳酸氢钠、高氯酸均为分析纯,购于国药集团化学试剂有限公司;甲醇、乙腈购于飞世尔实验器材(上海)有限公司;甲酸购于上海安谱科学仪器有限公司;醋酸铵购于美国Fluka公司;超纯水由MilliQ纯水系统制备而成。
1.2 仪器与设备
高效液相色谱仪、TQU03530型质谱仪,均购自赛默飞世尔科技(中国)有限公司;HCB 1002型电子天平,购自艾德姆衡器(武汉)有限公司;H-2050R型离心机、H/T16MM型离心机均购自湖南湘仪实验室开发有限公司;MIR-154-PC恒温培养箱,购自日本三洋电机公司;N-EVAP1/2型氮吹仪,购自美国Organomation公司;MS3bsic型涡旋振荡器,购自IKA公司;SB-5200DTN型超声波清洗仪,购自新芝有限公司;美国MilliQ纯水系统;透析袋MD-10(8-14 kD)购自北京索莱宝科技有限公司;超滤管(Millipore,10 kD)购自北京兰博利德商贸有限公司。
1.3 实验动物
健康的罗非鱼购买于北京市岳各庄批发市场,体重为(650±50)g,暂养于消毒后的水箱中,使用加热棒将水温控制在(22±2)℃,自然光照,24 h不间断充气;每天更换1/3水,投饵并及时清除残饵和排泄物,暂养1周后,80尾用于取空白血浆及空白超滤液,从而进行体外药物-血浆蛋白结合率的测定,20尾用于体内药物-血浆蛋白结合率的测定。采取尾静脉取血方式,离心管(加入50 μL)和注射器用1%的肝素钠溶液润洗,全血于4 ℃、4 000 r/min下离心5 min,分离后的空白血浆合并,均匀混合后,用10 mL离心管分装,置4 ℃保存备用,若不能及时处理,需转至-20 ℃保存。
1.4 体外平衡透析法-测定药物血浆蛋白结合率
采用体外平衡透析法测定血浆蛋白结合率,首先将透析袋(约12 cm)进行预处理[9],使用前用蒸馏水将透析袋里外冲洗干净。用棉线扎紧透析袋的一端使不漏液,用移液枪取1 mL空白血浆于透析袋内,并将透析袋置于盛有10 mL含药透析液的15 mL离心管中,用棉线和透析袋上端调节透析袋,使袋内液面稍低于袋外液面(液面高度差为(0.5±0.1)cm),注意透析袋不能紧贴管壁,以免影响透析效果。透析达到平衡后,吸出1 mL透析外液,加等量的高氯酸溶液(质量分数为10%),涡旋,检查有无白色絮状物析出。若透析外液显阳性,说明有蛋白漏出,则该样本作废。若显阴性,则取出透析袋,分别取透析内外液,分别测定透析內液药物浓度(总浓度Ct)和透析外液药物浓度(游离浓度Cf),计算药物血浆蛋白结合率Fb=(Ct-Cf)/Ct×100%。
1.4.1 平衡透析时间的确定
向透析袋内加入1 mL空白透析液(0.1 mol/L磷酸盐缓冲液),将透析袋置于10 mL含药浓度为 30 μg/mL的磷酸盐缓冲液中,分别透析4、8、12、24、36、48、60 h,每组做5个平行。透析结束后,分别取透析内液与透析外液进行检测,考察因素为透析内外液中药物浓度的比值,若比值接近于1并保持稳定,则透析达到平衡。
将上述空白透析液改为空白血浆,其他操作同上。透析结束后,分别取透析内液(血浆)与透析外液进行检测,考察因素为结合率,若结合率趋于稳定,则透析达到平衡。
1.4.2 透析袋对药物的吸附作用
在透析袋中加入空白透析液1 mL(设体积为V1),将透析袋置于10 mL (V2) SMZ质量浓度为10、30、60 μg/mL(C1)的透析液中,于4 ℃恒温培养箱中透析48 h,每组5个平行,测定透析外液的药物浓度(C2),计算透析袋吸附率X。
1.4.3 温度对结合率的影响
向透析袋内加入1 mL空白血浆,并将透析袋置于10 mL含药浓度为10、30和60 μg/mL的磷酸盐缓冲液,分别置于4、25、37 ℃恒温培养箱中透析,每组5个平行,达到平衡后,分别取透析内外液进行检测。
1.4.4 pH对结合率的影响
向透析袋内加入1 mL空白血浆,将透析袋置于10 mL含药浓度为10、30和60 μg/mL,pH分别为7.4、7.8、8.2的磷酸盐缓冲液(用1 mol/L的NaOH溶液调节pH),每组5个平行,达到平衡后,分别取透析内外液进行检测。
1.4.5 药物浓度对结合率的影响
向透析袋内加入1 mL空白血浆,将透析袋置于10 mL含药浓度为0.5、1、5、10、30和60 μg/mL的磷酸盐缓冲液中进行透析,每组5个平行。透析结束后,分别取透析内外液进行检测。
1.5 体内超滤法-测定血浆蛋白结合率
混饲药物(浓度为150 mg/mL)的配制:6.06 g磺胺甲噁唑原料药与6 g饲料(已过筛)混合,加水定容至40 mL。按200 mg/kg鱼体重用1 mL注射器和3 cm输液管对罗非鱼进行单次口灌给药,出现回吐现象的舍弃。给药后用1 mL的注射器分别于0.5、1、2、4 h进行尾部静脉取血,每个时间点三个平行,每条鱼取4 mL血,分四次置于含有50 μL 1%肝素钠的2 mL离心管中,于4 ℃、4 000 r/min下离心5 min,4次分离的血浆合并置于5 mL离心管中,混匀后取0.5 mL血浆(总药物浓度Ct)于预处理过的超滤管(加入0.5 mL超纯水置于4 ℃冰箱中保存,使用前,于14 000 g下离心15 min),于4 ℃、14 000 g下离心30 min,收集超滤液(游离药物浓度Cf)于2 mL离心管中,血浆与超滤液置于-20 ℃下保存,待测。结合率Fb=(Ct-Cf)/Ct×100%。
按上述方法收集空白超滤液,分别向5 mL的空白超滤液中加入一定量的标准工作液,使其浓度分别为10、30和60 μg/mL(C0),按上述方法进行超滤离心,收集超滤液(药物浓度为Ct),测定膜吸附率Y。
Y=(C0-Ct)/C0×100%
1.6 样品前处理
含药血浆:取血浆0.2 mL,加入浓度为1 μg/mL的内标氘代磺胺邻二甲氧嘧啶50 μL,涡旋,加入5 mL酸化乙腈(含1%甲酸),涡旋混匀1 min,超声提取10 min,加1.0 g无水硫酸钠,涡旋混匀1 min,4 000 r/min离心5 min,取上清液于10 mL离心管中,残渣用3 mL酸化乙腈重复上述步骤再次提取,合并提取液,于40 ℃下氮吹至干,用1 mL 20%甲醇溶液复溶,加入2 mL正己烷除脂,过0.22 μm滤膜,供液相色谱-质谱检测[10]。
透析外液和超滤液:取透析外液(超滤液)0.5 mL,加入浓度为1 μg/mL的内标液50 μL,涡旋混匀,加入5 mL乙酸乙酯,涡旋混匀1 min,4 000 r/min离心5 min,取有机相于另一支10 mL离心管中,加入3 mL乙酸乙酯重复上述步骤,合并有机相,于40 ℃下氮吹至干,1 mL 20%的甲醇溶液复溶,过0.22 μm滤膜,供液相色谱-质谱检测[10]。
1.7 数据处理及分析
采用EXCEL进行数据处理,采用SPSS 20进行最小显著性差异检验(P>0.05)。
2 结果与分析
2.1 方法确证
用甲醇溶液对SMZ储备液(1 000 μg/mL,甲醇溶解)进行稀释,制备0.01、0.1、1、10、100 μg/mL等5个浓度梯度的标准工作液。由此制得标曲:0.05、0.1、0.2、0.5、1.0、2.0、5.0 μg/mL的SMZ溶液(含内标:0.05 μg/mL),以SMZ峰面积与内标峰面积比值(y)对药物浓度(x)作线性回归,得SMZ在0.05~5 μg/mL的范围内,线性方程为y=2.852 8x+0.462 1,r2=0.995 8,样品(血浆、缓冲液和超滤液)中SMZ的最低检出限(S/N≥3)为0.002 μg/mL。低、中、高浓度(0.05、0.5、5.0 μg/mL)SMZ在血浆、缓冲液和超滤液中的绝对回收率均在82%~112%之间,说明本方法具有较高的可靠性。日内精密度(n=5)均低于11.2%、9.94%和11.79,日间精密度(n=5)均低于13.9%、8.13%和11.0%。
2.2 膜对药物的吸附作用
透析袋与超滤膜对SMZ的吸附作用见表1。高中低三种浓度条件下,透析袋(超滤膜)对SMZ的吸附率不超过3.8%(8.6%)。表明试验中使用的透析袋(超滤膜)对SMZ仅起到微量吸附作用,对结合率的测定影响不显著。因此,可采用该透析袋和超滤膜进行SMZ血浆蛋白结合率的测定。

表1 膜对SMZ的吸附作用Tab.1 The adsorbtion of SMZ for dialysis tubing
2.3 体外平衡透析法测定SMZ血浆蛋白结合率
2.3.1 稳定性
三种(10、30、60 μg/mL)含药浓度的血浆、透析液在37 ℃避光条件下放置72 h,分别于0、12、24、36、48、60、72 h取样检测,结果见图1、2。低中高三种含药浓度的血浆样品在0~48 h内,SMZ的浓度较为稳定,RSD值分别为6.68%、5.99%和3.85%,均低于15%。60、72 h内,RSD值均高于15%。低中高三种含药浓度的磷酸盐缓冲液在0~72 h内,SMZ的浓度较为稳定,RSD值分别为2.64%、6.24%和4.27%,均低于15%。以上结果表明,SMZ在37 ℃避光条件下48 h内基本稳定。
2.3.2 透析时间的确定
透析內液为空白透析液时,考察结果如图3所示,透析内外液药物浓度比值于8 h后达到稳定状态,比值维持在1左右。透析內液为空白血浆时,考察结果如图4所示,药物血浆蛋白结合率于24 h后达到稳定状态,维持在13.26%~14.24%。综合图1~4分析结果,确定平衡透析时间为48 h。

图1 血浆中SMZ的稳定性Fig.1 Stability of SMZ in plasma

图2 磷酸盐缓冲液中SMZ的稳定性Fig.2 Stability of SMZ in phosphate buffer

图3 平衡透析时间-透析液Fig.3 Equilibrum dialysis time-dialysate
2.3.3 温度对结合率的影响
温度对结合率的影响结果见图5,相同药物浓度下,不同温度对药物血浆蛋白结合率的影响不显著。在同一温度下,不同的药物浓度对血浆蛋白结合率的影响差异不显著。其中,药物浓度30 μg/mL时,各温度下的结合率平均值分别(14.89±0.75)%、(15.71±2.04)%、(13.94±2.7)%。
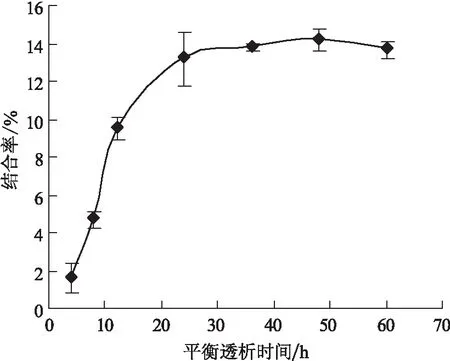
图4 平衡透析时间-血浆Fig.4 Equilibrum dialysis time-plasma

图5 不同温度下磺胺甲噁唑与罗非鱼血浆蛋白的结合率Fig.5 Binding rates of SMZ to plasma protein at different temperature
2.3.4 pH对结合率的影响
4 ℃条件下,不同pH对血浆蛋白结合率的影响结果见图6,相同药物浓度下,不同pH对血浆蛋白结合率的影响较为显著,其中低浓度下影响最为显著。在同一pH条件下,不同的药物浓度对血浆蛋白结合率的影响差异不显著。其中,药物浓度为30 μg/mL时,各pH条件下的结合率平均值分别(15.50±2.55)%、(13.66±0.73)%、(10.91±1.49)%。
2.3.5 药物浓度对药物-血浆蛋白结合率的影响
4 ℃条件下SMZ血浆蛋白结合率随药物浓度的变化结果见图7,在透析外液药物浓度为0.5~60.0 μg/mL时,SMZ血浆蛋白结合率为14.65%~25.12%,其中,在0.5~10 μg/mL时,药物血浆蛋白结合率随药物浓度的升高而依次递减,表明在该范围内,血浆蛋白结合率具有浓度依赖性;在10~60 μg/mL时,药物血浆蛋白结合率趋于平衡,维持在14.65%~15.48%。
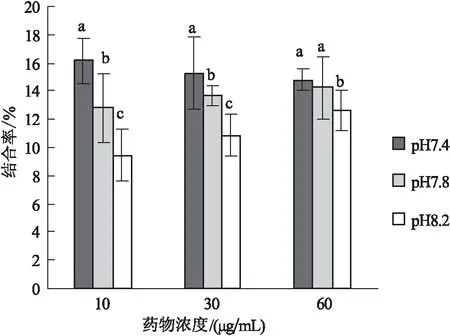
不同柱上字母表示不同pH组间差异显著(P<0.05).

图7 不同药物浓度下SMZ的血浆蛋白结合率Fig.7 Plasma protein binding rates of SMZ in different concentration in dialysate
2.4 体内超滤法SMZ血浆蛋白结合率
灌药结束后,罗非鱼血浆中SMZ浓度及SMZ血浆蛋白结合率随时间的变化结果见表2。为更加清晰地描述结合率随药物浓度的变化规律,特将12条鱼血浆中SMZ的浓度进行排序,以浓度为横坐标、结合率为纵坐标作图,详见图8。由图8可知,在血浆含药浓度为1~5 μg/mL时,SMZ血浆蛋白结合率为15.34%~20.1%,结合率随药物浓度的升高而减小;在10~20 μg/mL时,结合率趋于稳定,维持在12.7%~14.9%。

表2 SMZ血浆蛋白结合率在罗非鱼体内的变化Tab.2 The changes of protein binding rates in O.niloticus
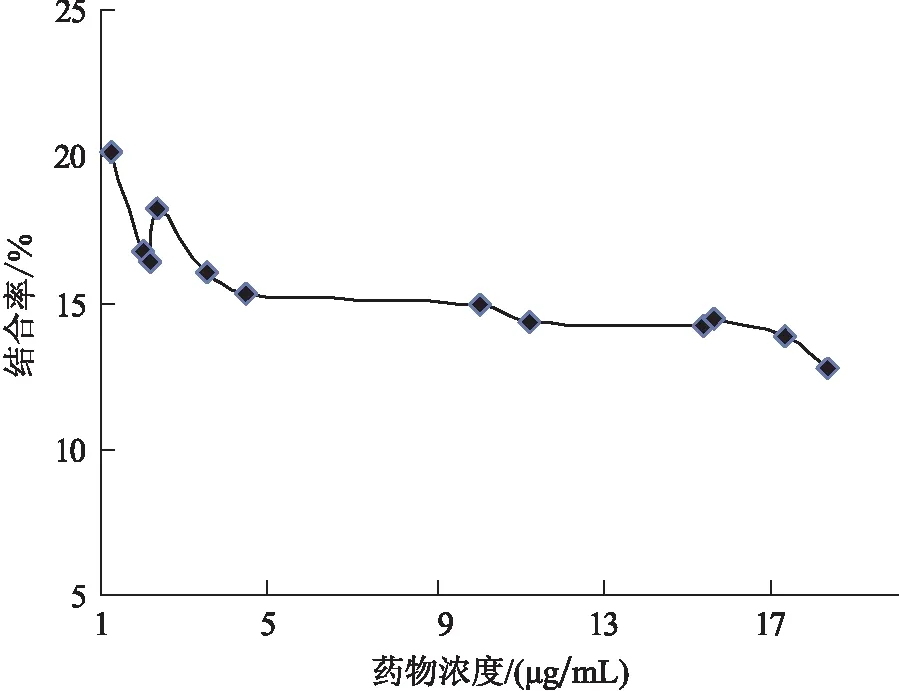
图8 不同药物浓度下SMZ的血浆蛋白结合率Fig.8 Protein binding rates of SMZ in different concentration in plasma
3 讨论
3.1 温度对SMZ血浆蛋白结合率的影响
关于温度对血浆蛋白结合率影响的研究已有很多,章海鑫等[4]和赵凤等[5]研究发现双氟沙星、喹烯酮分别与异育银鲫、草鱼血浆蛋白结合率不同温度条件(4~37 ℃)下变化差异不显著;Lee等[11]、Trnavská等[12]、Dorn等[13]发现,达托霉素、吡罗昔康、替加环素与人血浆蛋白的结合率不受温度(5、22、25、37 ℃)的影响。本实验中,SMZ与吉富罗非鱼血浆蛋白结合率在4、25、37 ℃条件下差异不显著,该试验结果与章海鑫等[4]、赵凤等[5]、Lee等[11]的结果一致,然而与肖超[1]、Munsey等[14]的研究结果刚好相反。肖超等[1]通过体外模拟试验研究发现,平衡温度从4 ℃上升到37 ℃,磺胺二甲基嘧啶与家兔血浆蛋白结合率下降近了20%;Munsey等[14]同样发现,平衡温度从4 ℃上升到45 ℃,磺胺二甲基嘧啶与猪血浆蛋白的亲和力降低86%。综合上述比较研究,可推测出温度对药物血浆蛋白结合率的影响主要与药物的结构、性质以及药物与血浆蛋白的亲和力有关。
3.2 pH对SMZ血浆蛋白结合率的影响
血浆中的结合蛋白以白蛋白和α1-酸性糖蛋白为主,与α1-酸性糖蛋白不同,白蛋白的结构具有pH依赖性,中性药物(pH 5~7)和碱性药物(pH>8)与白蛋白的结合位点至少有6个,其中结合位点Ⅰ和结合位点Ⅱ结合量最多[3,15-16],有研究表明,药物与白蛋白结合位点Ⅰ的结合具有pH依赖性[17],Munsey等[14]和操继跃等[8]的研究验证了这一观点。Munsey等[14]研究发现,在37 ℃下,pH由6.0调至8.0,磺胺二甲基嘧啶与猪血浆蛋白的亲和力可增强10倍。与之相反的是,操继跃等[8]研究发现,在pH为6.8、7.4、7.8条件下,磺胺甲氧嘧啶和磺胺二甲基嘧啶与黄牛血浆蛋白结合的程度随pH的增大而减小,在低浓度时这一变化最为明显,这可能源于不同物种间血浆蛋白结构的特异性[18]。SMZ是一种酸性药物[19],易与白蛋白结合。本实验中,SMZ与吉富罗非鱼血浆蛋白结合率在不同pH(7.4、7.8、8.2)条件下为差异显著,SMZ血浆蛋白结合率随pH的增大而减小,其中低浓度时尤为显著,这与操继跃等[8]的研究相一致。因含药血浆经长期冷冻贮藏后,血浆的pH将会因过程中CO2的损失由7.4上升为7.8甚至到8.0[7]。为了防止因储存期间pH的改变而影响超滤法测定结果,建议取血后直接进行超滤离心。
3.3 药物浓度与结合率的关系
药物与血浆蛋白的结合具有浓度依赖和饱和结合的特点,这些特点主要与药物的理化性质及血浆蛋白的结合性质有关[1,20]。余建鑫等[20]、陈培荣等[21]分别在各自的研究中发现血啉甲醚小鼠血浆蛋白结合率和河豚毒素血浆蛋白结合率在一定的药物浓度范围内随药物浓度的升高而降低;Matsumoto[22,23]、肖超等[1]研究发现在一定浓度范围内,河豚毒素、磺胺二甲基嘧啶及其乙酰化代谢产物的浓度对血浆蛋白结合率无影响。实验中,体外平衡透析法和体内超滤法的测定结果(详见图7、8)均综合以上两种结果,在低浓度(0.5~10.0 μg SMZ/mL透析液或1~5 μg SMZ/mL血浆)范围内,结合率随药物浓度的升高而减小;在高浓度(10.0~60.0 μg SMZ/mL透析液或10~20 SMZ/mL血浆)范围内,结合率保持不变。由此可知,SMZ与罗非鱼血浆蛋白结合率与药物的浓度有关,从而推断出SMZ是一种浓度依赖性药物。
3.4 体外平衡透析法与体内超滤法的比较研究
目前已有大量学者对体外平衡透析法和体内超滤法进行了对比研究[24,25],体外平衡透析法操作方便,条件易于控制,结果可靠,然而该方法耗时长,需要模拟体内环境,透析过程中透析内外液体积易发生变化,易产生Gibbs-Donnan效应;体内超滤法周期短,可进行实时监测,然而含药血浆储存期间pH易发生变化,在超滤期间蛋白质逸漏现象频发。针对两种方法存在的一些缺点,有关学者作了相应改进,平衡透析液选择高强度的浓度为0.1 mol/L的磷酸盐缓冲液[26](内含0.15 mol/L NaCl),可维持透析期间pH恒定不变、以防血浆稀释;体内超滤法选择新鲜血浆,或预先向1 mL解冻血浆加入10 μL 2 mol/L磷酸盐缓冲液(pH7.45)[13],使血浆的pH维持在正常生理范围[27]内;为了防止超滤离心期间,结合率因温度而发生改变,离心温度通常设为4 ℃;在不同离心力和离心时间的研究中发现,在4 ℃、14 000g下离心30 min,超滤液经高氯酸检测,无蛋白逸出,规避了蛋白逸漏的缺点。在此基础上,进行平衡透析法与体内超滤法的比较研究,获得一致的结论:磺胺甲噁唑与血浆蛋白的结合具有浓度依赖性。然而,不同的是:在1~20 μg SMZ/mL血浆浓度范围内,结合率达到稳定状态时,平衡透析法与体内超滤法的测定结果分别为(15.48±1.49)%、(14.07±0.76)%,体内超滤法测定结果低于体外平衡透析法,这可能与超滤离心造成的滤液浓缩和体内磺胺甲噁唑代谢物竞争性结合血浆蛋白有关;另外,在实验期间发现,与上次试验间隔两周后重复测定SMZ血浆蛋白结合率,体外平衡透析法测定结果重现性较差(RSD>15%),体内超滤法测定结果较为稳定(RSD<15%),因此,优先推荐体内超滤法作为测定SMZ血浆蛋白结合率的最佳选择。
4 结语
本研究采用体外平衡透析法研究了温度、pH对SMZ罗非鱼血浆蛋白结合率的影响,结果表明结合率不受温度影响,但具有pH依赖性,由此确定体外平衡透析法的测定条件:空白血浆于4 ℃条件下在含药透析液(内含0.15 mol/L NaCl 、pH为7.4、浓度为0.1 mol/L的磷酸盐缓冲液)中透析48 h;并推断出体内超滤法的最佳测定条件:口灌给药后,采用新鲜血浆于4 ℃条件下进行超滤。在最佳测定条件下,采用以上两种方法测定体内外SMZ血浆蛋白结合率,测定结果分别为14.65%~25.12%(体外平衡透析法)和12.7%~20.1%(体内超滤法)。两种方法测定结果一致表明,在1~20 μg SMZ/mL血浆浓度范围内,结合率随血浆中SMZ浓度的升高先减小而后保持稳定,即 SMZ血浆蛋白结合率具有浓度依赖性。通过对两种方法进行比较研究发现,在高浓度血药范围(≥10 μg SMZ/mL)内,结合率达到稳定状态时,体内超滤法测定结果低于体外平衡透析法,又因体外平衡透析法重现性较差,故推荐使用体内超滤法进行磺胺甲噁唑罗非鱼血浆蛋白结合率的测定,该方法周期短、重现性好,可作为体内药物血浆蛋白结合率测定的最佳选择。
