载尼群地平壳聚糖/明胶微球的制备及药物缓释性能研究
2018-11-07李鸣明侯维敏宫蕾詹世平
李鸣明,侯维敏,宫蕾,詹世平
(大连大学环境与化工学院,辽宁大连 116002)
尼群地平作为一种二氢吡啶类钙通道阻滞剂,是具有良好持久降压能力和血管扩张作用的药物之一[1]。在物理性质方面,尼群地平最显著的特征是不溶于水,该性质导致其在医学市场上的利用率不高,并且还伴有血药浓度波动大、服用较频繁等缺点。制备尼群地平载药微球,利用对特定器官、组织的靶向性和药物的缓释性来降低毒副作用,提高尼群地平的生物利用度,可使药物的释放达到较为理想的效果[2-3]。
壳聚糖作为药物载体,除了无毒和优良的生物相容性外,还具有很多优点:(1)壳聚糖分子链上聚集很多功能丰富的基团,可用吸附或包裹的方式运载不同药物;(2)壳聚糖是天然多糖中唯一的碱性多糖,来源丰富;(3)壳聚糖分子链上含有丰富的多糖链,能被特异组织或器官所识别,达到靶向定位释放的效果[4-5]。明胶是由18种氨基酸组成的蛋白质大分子,兼具蛋白质和高分子材料的双重特性。明胶由于具有大量不同种类的活性官能团,具备了各种交联及目标配位改性的可能,在生物医学领域得到了广泛的应用[6]。明胶与壳聚糖分子间相互作用力强,易于成球。两者共混后化合物的物理及化学特性可以实现协同增效的目的,使壳聚糖的分子链排列规则整齐,明胶刚性强度增大;同时微球成球性能突出,表面光滑无皱褶,且力学性能得到很好的提升,使药物的保存及缓释得到整体的改善。
本文以尼群地平为模型药物,以壳聚糖及明胶为载体材料,采用乳化交联及丙酮浸泡载药制备载尼群地平壳聚糖/明胶微球,并对其载药量和缓释性能进行了研究,为研制尼群地平微球提供参考。
1 药品与仪器
尼群地平(医药级,西安瑞林生物科技有限公司);壳聚糖(Mw=20w,分析纯,天津市凯信化学工业有限公司);明胶(分析纯,天津市科密欧化学试剂有限公司);二氯甲烷(分析纯,天津市科密欧化学试剂有限公司);液体石蜡(分析纯,天津市科密欧化学试剂有限公司);丙酮(分析纯,天津市凯信化学工业有限公司);戊二醛(分析纯,天津市科密欧化学试剂有限公司);Span-80(分析纯,天津市科密欧化学试剂有限公司);数字恒温水浴锅DF-101D(巩义市予华仪器有限责任公司);扫描电镜(SU3500,日立高科技有限公司);紫外分光光度计(UV2100,美国UNICO)。
2 实验方法
2.1 壳聚糖/明胶空白微球的制备
将0.45 g壳聚糖溶于10 mL醋酸溶液中(体积分数3%),称取1.00 g明胶溶于10 mL 70 ℃蒸馏水中,待壳聚糖和明胶充分溶解后,室温下用磁力搅拌器将两者混合均匀。量取80 mL液体石蜡并加入2 mL乳化剂span-80,55 ℃下恒温搅拌15 min中后加入壳聚糖明胶混合溶液,继续搅拌15 min形成稳定的混合溶液。在室温下继续搅拌45 min后分两次加入12.5%(体积分数)的交联剂戊二醛,每次间隔10 min,使微球固化。加入90 mL丙酮搅拌10 min,使微球脱水。2 000 r/min下离心15 min后,用丙酮润洗两次,再用异丙醇润洗,离心后于干燥箱中干燥得到空白微球。
2.2 载尼群地平壳聚糖/明胶微球的制备
采用丙酮浸泡载药法制备载药微球,尼群地平溶于90 mL丙酮中搅拌30 min后,将制备好的壳聚糖/明胶空白微球浸泡在溶有药物的介质溶液中,离心后经干燥得到载药微球。
2.3 正交试验设计
在考察单因素试验的基础上,选取对微球质量与载药量影响较为显著的四个因素作为考察对象,即乳化时间(A)、乳化剂span-80用量(B)、尼群地平用量(C)及壳聚糖与明胶浓度比(D),采用L9(43)正交试验,试验设计见表1,以尼群地平吸附量作为评价指标,优化制备条件,乳化温度55 ℃。

表1 因素设计表
2.4 载药量的测定
准确称取定量(20 mg)载药微球,用适量二氯甲烷(DCM)溶解,加入pH为6.86的磷酸盐缓冲溶液(PBS),将溶液置于水浴中45℃加热并搅拌,等待二氯甲烷完全挥发,将溶液经0.22 μm微孔滤膜过滤后,于236 nm处测滤液的吸光值。通过尼群地平的标准曲线计算浓度。载药量按式(1)计算。

2.5 扫描电镜
将扫描样品进行喷金处理后进行电镜扫描,观察样品的形貌及粒径。
2.6 药物释放性能的测定
药物缓释微粒的体外释放性能由其在磷酸缓冲液(PBS,pH6.86)中的药物溶出量表征[7]。精确称量20 mg载药微球后置于透析袋中,放在10 mL磷酸缓冲液中,在37.0 ℃水平恒温振荡器中振荡,设3组平行样,每次测量取1 mL并补充相同体积缓冲液,所取的溶液用紫外分光光度计于236 nm处测定吸光度,重复取样测定,绘制时间-累积释放率的药物释放曲线。
3 结果与讨论
3.1 尼群地平的标准曲线
用紫外吸收法测定尼群地平,制作标准曲线。用测得的吸光度对浓度回归,作标准曲线和计算回归方程。结果如图1所示。由图1可以看出,标准曲线的方程为C=1.00037+14.05365A,其中C为尼群地平的质量浓度(μg/mL),A为吸光度,R=0.9997,尼群地平在3~25 μg有良好的线性关系。
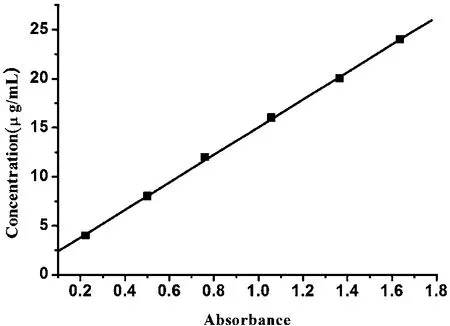
图1 尼群地平的标准曲线
3.2 正交试验优化制备条件
对载药微粒的制备工艺条件进行正交试验优化。正交试验结果如表2所示。以吸附药量为评判标准,由表2正交试验结果可知,乳化时间(A)、乳化剂span-80用量(B)、尼群地平用量(C)及壳聚糖与明胶浓度比(D)四个因素对载药量的影响RB>RC>RA>RD,因此在微粒的制备过程中,影响因素最大的是乳化剂用量,其他影响因素排序依次为尼群地平用量、乳化时间和壳聚糖明胶浓度比。试验最佳组合为第8组,即A3B2C1D3,制备条件为乳化时间18 min、乳化剂用量4 mL、尼群地平0.025 g、壳聚糖明胶浓度比为1∶4,乳化温度55 ℃,交联剂戊二醛用量12.5%(体积分数,在此条件下,尼群地平吸附量为6.404 mg,载药微粒载药量为32.02%。
3.3 载药微粒的形貌分析
用扫描电镜对壳聚糖/明胶空白微球及载尼群地平壳聚糖/明胶微球(第8组)进行形貌表征观察,结果如图2a、2b所示。图2a可以看出,微球表面光滑圆润,成球性良好,粒径多分布在1~10μm。图2b可以看出,载药微粒成球状,形态比较均匀,表面光滑无褶皱,粒径分布在4~28 μm。
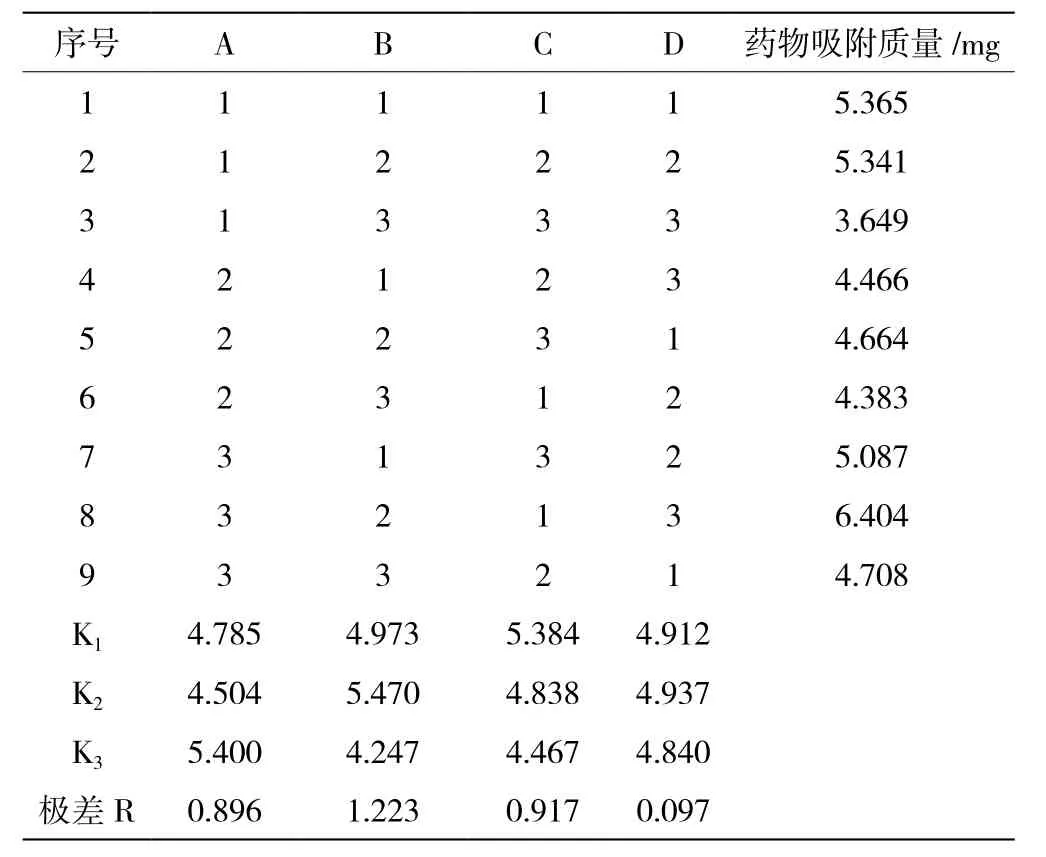
表2 载药微球制备最佳工艺条件正交试验结果

图2 SEM表征
3.4 载药微粒释放性能研究
载药微粒在PBS溶液中的累积释放曲线如图3所示。由图3可知,载药微粒的释药前期出现了一定程度的突释现象。在5 h时,累积释药量达到80%,后阶段释放很缓慢,趋于平缓,10 h基本释放完全,由此可见载尼群地平壳聚糖/明胶微球具备明显的缓释性能。
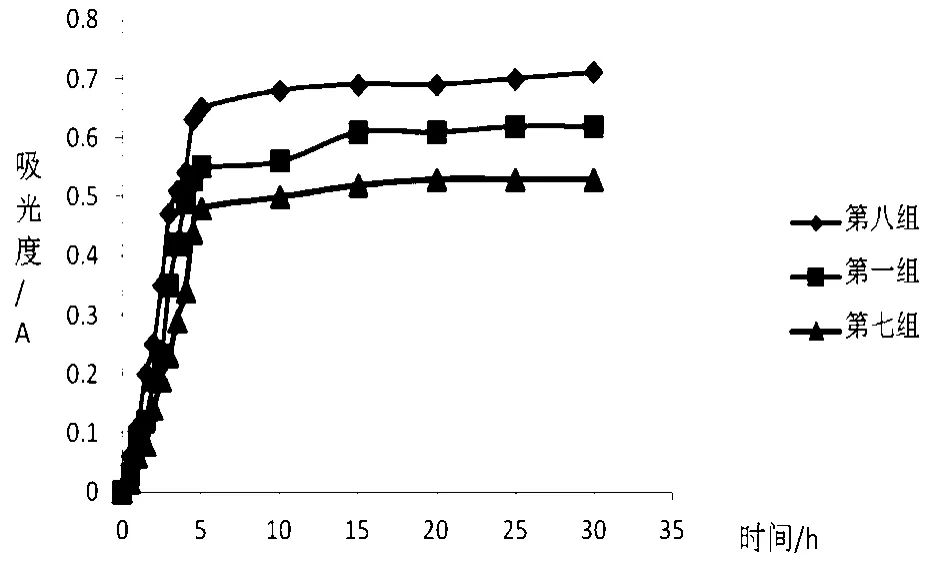
图3 载药微粒在PBS溶液中的释放曲线
4 结论
采用乳化交联法制备壳聚糖/明胶空白微球,并用丙酮浸泡载药/常温干燥法制备载尼群地平壳聚糖/明胶微球。通过正交试验确定了最佳制备工艺条件:乳化时间为18 min、乳化剂用量为4 mL、尼群地平为0.025 g、壳聚糖明胶浓度比为1∶4、乳化温度 55 ℃、交联剂戊二醛用量12.5%(体积分数),在此条件下,尼群地平吸附量为6.404 mg,载药微粒载药量为32.02%。空白微球及载药微球均为完整球形,光滑,均匀。载药微粒在PBS缓冲溶液中5h累积释药量为80%,体外释药性能表明微粒具有明显的缓释作用。
